HLP合并DKA的临床特征及危险因素分析
瞿伊晨 吴婵妮 王霖 王志勇 赵承满
高甘油三酯血症(hypertriglyceridemia,HTG)是急性胰腺炎(acute pancreatitis,AP)的重要病因之一,近年来随着国民生活水平的提高和饮食结构的改变,高脂血症性胰腺炎(hyperlipidemic pancreatitis,HLP)已成为AP的第二大常见原因[1]。糖尿病酮症酸中毒(diabetic ketoacidosis,DKA)是以高血糖、酮症及代谢性酸中毒为特征的急性代谢并发症。两者均是临床工作中需早期识别及治疗的严重疾病。研究显示,DKA可增加HTG患者发生AP的风险,约36.4%的DKA患者同时存在HLP[2-3],合并DKA将加重HLP患者的低血容量性休克和代谢障碍,导致临床治疗复杂化[4]。因此,早期识别至关重要。本文分析HLP合并DKA患者的临床特征及其危险因素,为临床工作提供帮助。
1 资料与方法
1.1 临床资料 收集2021年1月至 2023年2月本院81例HLP患者的临床资料,其中HLP合并DKA患者24例(HLP+DKA组),HLP患者57例(HLP组)。纳入标准:①符合AP诊断标准:至少符合以下3项中的2项:a.急性发作的持续性、剧烈的上腹痛;b.血清脂肪酶或淀粉酶至少大于正常值上限 3倍;c.增强 CT或磁共振成像(MRI)检查中提示AP的特征性变化[5];②符合HLP诊断标准:血清甘油三酯(TG)>11.3 mmol/L或TG 为5.65~11.30 mmol/L,但血清呈乳糜状,且除外其他病因诱发的AP[1]。③符合酮症酸中毒诊断标准[6]:a.酮血症(血酮体≥3 mmol/L)或尿糖和尿酮体阳性(++以上);b.高血糖(血糖>13.9 mmol/L);c.静脉血pH<7.3和(或)血清碳酸氢盐<18 mmol/L;④临床资料完整。排除标准:①年龄<18 岁;②慢性胰腺炎;③胆源性、酒精性等其他病因导致的胰腺炎;④胰腺癌或合并其他恶性肿瘤;⑤妊娠及哺乳期女性。回顾性收集并记录患者一般临床资料及实验室资料。本研究经本院伦理委员会批准。
1.2 方法 收集两组患者入院时一般资料,包括性别、年龄、既往史(吸烟史、饮酒史、糖尿病史、高血压病史、脂肪肝病史)、入院时血压、心率、随机血糖;入院后48 h根据《中国AP诊治指南》对HLP患者进行严重程度分级:轻型:无器官功能衰竭及局部或全身并发症;中度重型:伴有一过性的器官衰竭(48 h内恢复),或伴有局部或全身并发症;重型:伴有持续(>48 h)的器官功能衰竭。采用BISAP评分及MCTSI评分系统评估患者严重程度。在治疗过程中记录患者腹痛持续时间、禁食时间。收集患者入院后48 h内实验室检查指标最差值,包括白细胞计数、红细胞计数、血红蛋白、红细胞压积、血淀粉酶、血脂肪酶、白蛋白、丙氨酸氨基转移酶、天冬氨酸氨基转移酶、总胆红素、空腹血糖、糖化血红蛋白、血肌酐、血尿素氮、TG、总胆固醇、高密度脂蛋白胆固醇、低密度脂蛋白胆固醇、血钙、凝血酶原时间、国际标准化比值、活化部分凝血活酶时间、凝血酶时间、D-D二聚体、血pH值、乳酸。统计住院时间及住院费用。
1.3 统计学方法 采用SPSS 25.0 统计软件。符合正态分布计量资料以(±s)表示,两组间比较采用t 检验;偏态分布计量资料以M(Q1,Q3)表示,两组间比较采用秩和检验。计数资料采用n(%)表示,两组间比较采用卡方检验或Fisher确切概率法。将单因素P<0.05的变量带入多因素Logistic回归分析,得出HLP合并DKA的独立危险因素的比值比,并绘制受试者工作特征(ROC)曲线,评估预测性能。以P<0.05为差异有统计学意义。
2 结果
2.1 一般资料比较 见表1。
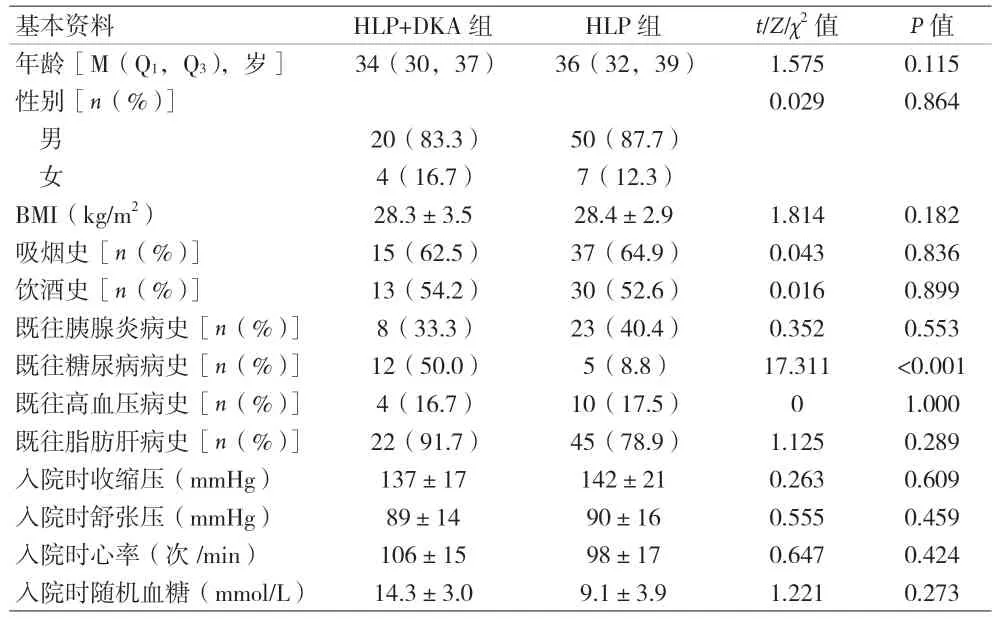
表1 两组基本资料
2.2 两组临床特征比较 见表2。
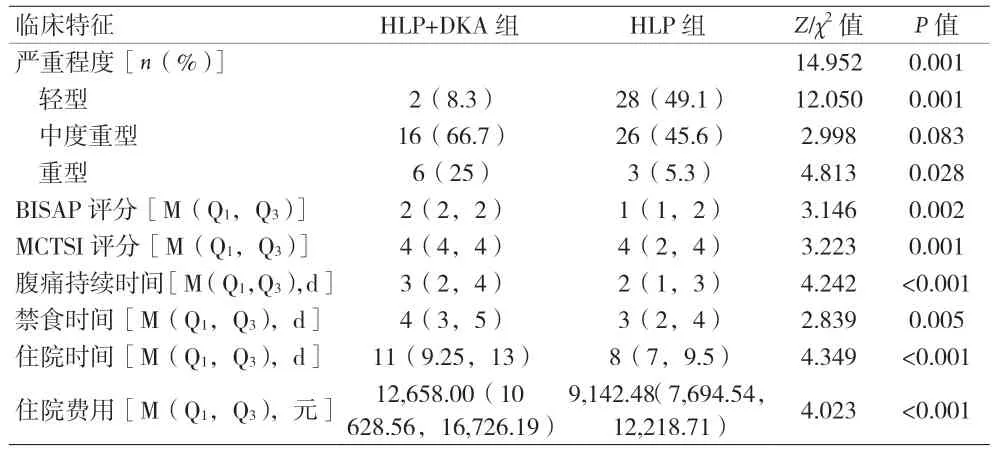
表2 两组临床特征比较
2.3 实验室资料比较 见表3。
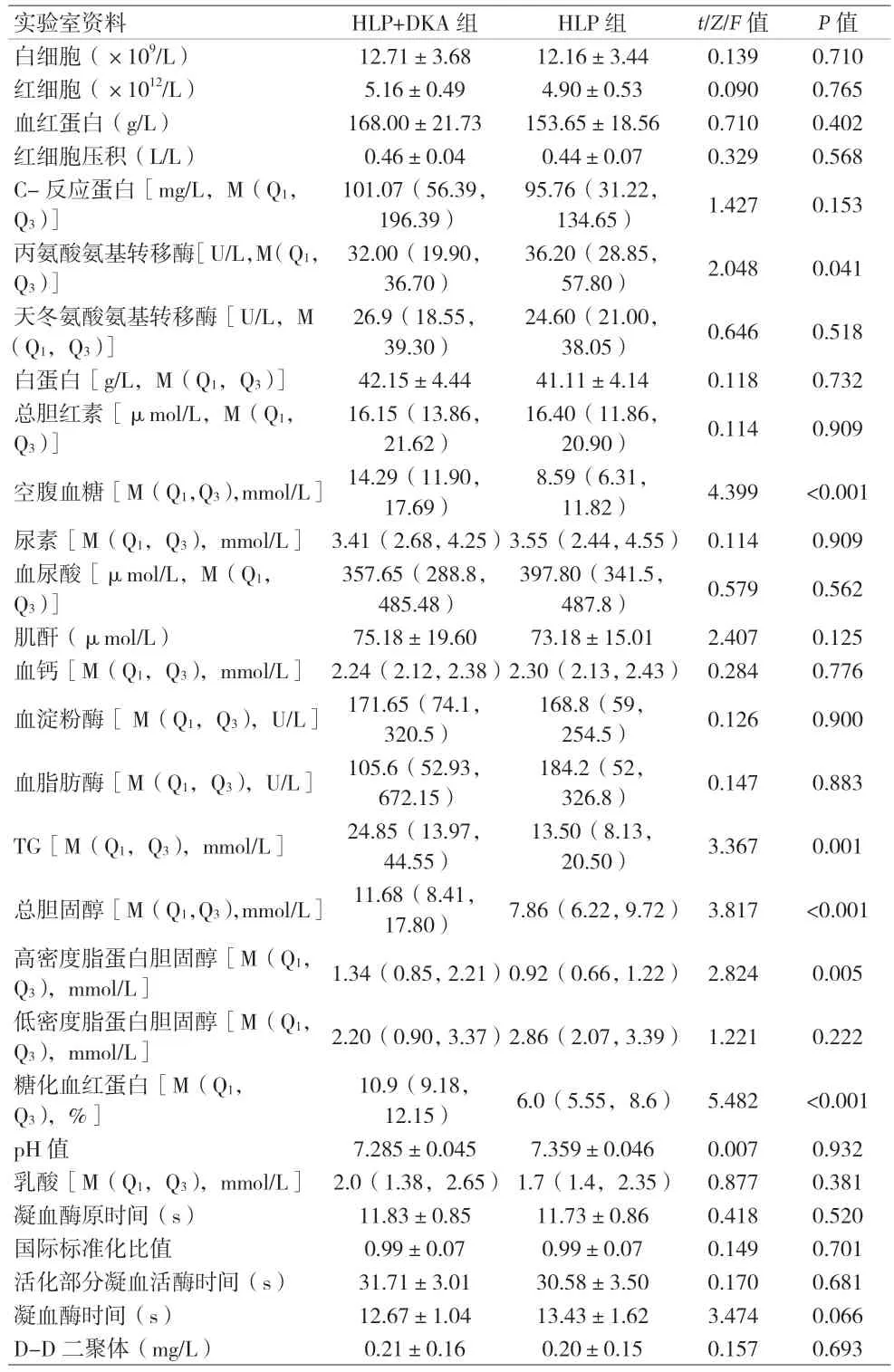
表3 两组实验室资料比较
2.4 多因素Logistic回归分析 既往糖尿病病史(P=0.032)、糖化血红蛋白升高(P=0.013)是HLP合并DKA的独立危险因素(见表4)。ROC曲线分析显示,既往糖尿病病史预测HLP+DKA的AUC为0.695,糖化血红蛋白预测HLP+DKA的AUC为0.893,临界值为8.85%时,预测HLP+DKA的敏感度91.3%,特异度78.9%(见图1、表5)。

图1 HLP+DKA的ROC曲线
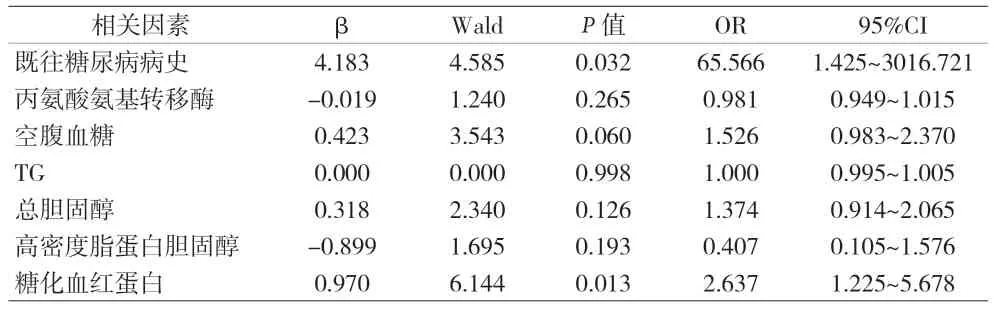
表4 多因素Logistic回归分析
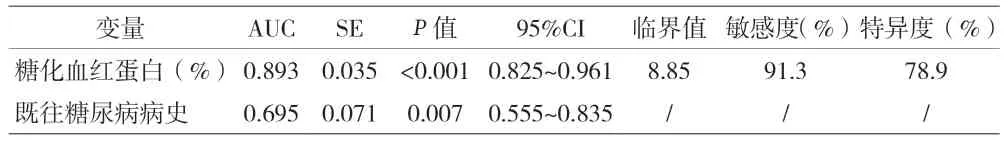
表5 糖化血红蛋白对于HLP+DKA的临界值及预测价值
3 讨论
重症HLP与DKA均为临床中常见的危重疾病,早期识别及治疗对患者具有重要临床意义。本研究中,24例HLP患者同时存在DKA,这与以往研究相似[7-8]。据报道,DKA可引起 40%患者腹痛[9],16%~25% DKA患者同时存在淀粉酶及脂肪酶非特异性升高[10],而AP也同样具有腹痛、血淀粉酶及脂肪酶升高的特点。这种重叠现象使得AP与DKA的诊断存在困难。但两者的及时诊断在临床中具有重要意义。因AP可增加血管内容量消耗,加重DKA的严重程度;其次,AP可影响葡萄糖稳态,导致血糖控制更加困难。一项队列研究结果表明,AP+TG+DKA组比AP组具有更高的住院死亡率、多器官衰竭率以及更长的住院时间。在该研究中,AP+TG组未表现出更高的死亡率及器官衰竭率,故研究者认为三联征患者死亡率增加的驱动力可能是DKA[3]。然而,近期也有研究表明合并DKA的AP患者虽然严重程度更高,但死亡率并未显著增加[11]。本研究并未统计死亡率,但HLP+DKA组中重症患者占比更高,住院时间更长,间接表明合并DKA可加重患者病情,为临床治疗带来挑战。
既往研究显示,糖尿病患者发生AP的风险显著增加[12-13]。LIAO等[8]分析了糖尿病合并HLP患者的临床特征,结果表明糖尿病是HLP的重要危险因素,同时可影响HLP的发展及预后。近期研究表明糖尿病合并 AP患者发生DKA的风险也显著增加,且发生DKA患者的血糖及甘油三酯水平较高[14]。糖尿病作为HLP合并DKA的独立危险因素,需更加引起临床重视。糖化血红蛋白是临床中常用指标,反映近2~3个月平均血糖浓度。付燕等[15]回顾性研究指出2型糖尿病合并HLP患者的血糖及糖化血红蛋白明显升高,以血糖13.650 mmol/L和糖化血红蛋白8.150%为临界值时,预测2型糖尿病合并HLP诊断的敏感度为88.3%和77.3%,特异度为75.7%和71.4%。MA等[9]认为DKA合并AP患者的糖化血红蛋白明显升高,同时伴有HTG。本研究中HLP+DKA组空腹血糖及糖化血红蛋白均高于HLP组(P<0.001),且多因素分析显示,糖化血红蛋白是HLP+DKA的独立危险因素。表明血糖控制不佳时,可引起TG显著升高,最终诱发DKA及HLP,这可能与患者内源性胰岛素分泌不足,脂蛋白酶活性降低相关[4,16]。因此,加强糖尿病患者的血糖管理,可以有效减少DKA及HLP的发生,改善预后[8]。
近年来,HTG、AP、DKA三联征因其复杂性而被广泛报道[2-3,9],但三者的内在联系尚不明确。其可能机制是:(1)AP影响胰岛素分泌并引起全身炎症反应,触发交感神经反应,导致皮质醇、肾上腺素、胰高血糖素和生长激素的释放增加,加重胰岛素抵抗。上述改变同时可促进脂肪分解,游离脂肪酸释放及肝酮形成,导致高血糖、酮症酸中毒、脱水和高渗性昏迷[17]。另一方面,HLP可能导致急性β细胞功能障碍,引起短暂胰岛素缺乏,诱发DKA,尤其是在血糖控制不佳的患者中[7]。(2)DKA是一种严重的胰岛素缺乏状态,该状态下脂肪组织加速分解,游离脂肪酸大量释放并转移至肝脏,导致肝脏产生的极低密度脂蛋白增加,再加上外周组织中脂蛋白脂肪酶被抑制,致使低密度脂蛋白清除及代谢减少,引起HTG[2]。(3)HTG引起AP的机制中最被普遍接受的是Havel理论,即血浆中乳糜微粒阻塞胰腺毛细血管,导致经TG脂蛋白代谢分解的游离脂肪酸在胰腺中聚集,进一步引起胰腺内皮细胞和腺泡细胞损伤、胰腺微循环障碍及钙超载,最终诱发HLP[18]。本研究中,HLP+DKA组患者血清TG及总胆固醇均显著升高,提示高脂血症是这类患者的重要诱发因素。PASCUAL等[19]对1,457例AP 患者进行回顾性分析发现,TG水平升高与AP 的严重程度独立相关,且器官衰竭、胰腺坏死的严重程度均随TG增加而显著增加。近期研究也表明,TG水平与HLP的严重程度、复发及预后密切相关,长期降甘油三酯治疗可有效降低HLP复发[20]。
综上所述,有糖尿病病史及糖化血红蛋白升高是HLP合并DKA独立危险因素。DKA的共存使得HLP患者严重程度更高,临床需早期识别,精准治疗。

