生物质基吸附剂在糖汁脱色中的应用研究进展
陈静 张霞 熊艳舒 贾冉 陆海勤 李文
摘要:近年来,生物质材料在糖汁脱色中的应用引起了广泛的关注。生物质具有成本效益高、环境友好和去除效率高等特性,这使其成为一种很有前途的吸附剂。糖汁中含有的大分子还原糖碱性降解色素(HISADPs)、类黑素(ME)、酚类物质严重影响了食糖的品质。文章综述了改性的生物质吸附剂(包括纤维素、壳聚糖、淀粉)在糖汁脱色中的最新研究进展,并提出未来生物质基吸附剂如何扩大在糖厂中的应用性。
关键词:生物质材料;吸附;色素;脱色
中图分类号:TS244 文献标志码:A 文章編号:1000-9973(2024)02-0203-06
Research Progress on Application of Biomass-Based Adsorbents in Decolorization of Sugar Juice
Abstract: In recent years, biomass materials have attracted widespread attention in the application of decolorization of sugar juice. Biomass has the characteristics of high cost effectiveness, environmental friendliness and high removal efficiency, making it a promising adsorbent. The high-molecular-weight invert sugar alkaline degradation pigments (HISADPs), melanoids (ME) and phenolic substances in sugar juice seriously affect the quality of sugar. In this paper, the latest research progress of modified biomass adsorbents (including cellulose, chitosan and starch) in the decolorization of sugar juice is reviewed, and how to expand the application of biomass-based adsorbents in sugar factories in the future is proposed.
Key words: biomass materials; adsorption; pigment; decolorization
社会经济的发展以及国民生活水平的提高使人们越来越关注食糖的品质问题[1]。糖汁中含有的大分子还原糖碱性降解色素(HISADPs)、类黑素(ME)和酚类物质是白砂糖晶体色素的主要成分。因此,糖汁脱色是食糖生产过程中的关键操作。糖厂采取的传统的澄清方法主要是亚硫酸法和碳酸法。这两种方法生产的白砂糖色值为80~150 IU,已不能满足人们对高品质食糖的要求[2]。因此,应开发先进有效的替代方法进一步解决这一问题。
近年来,各种方法已被用于糖汁的脱色,包括化学沉淀[3]、絮凝[4]、膜分离[5]、离子交换[6]、电沉积[7]。然而,离子交换树脂的热稳定性较差[8]。膜过滤可以有效去除污染物,但维护成本较高[9]。化学沉淀会产生大量的污泥,可能会导致二次污染[10]。电沉积消耗大量电力,对低浓度物质的处理性能较差[11]。吸附因其操作简单、成本低、效率高,被认为是糖汁脱色中最有前途的方法[12]。
早期,有研究者将活性炭用于糖汁的脱色,但难以再生,限制了其在工业中的应用。强碱性大孔阴离子交换树脂(SBMAR)具有很好的再生和吸附性能,且成本较低,因此在糖厂中SBMAR逐渐取代活性炭用于糖汁脱色[13]。但SBMAR结构中的苯乙烯和二乙烯基苯这两种物质被列为2B级致癌物[14],将其用于糖汁脱色后生产的食糖可能会对人体健康造成威胁。之后,Li[15]用松香基阴离子交换树脂吸附ME,但平衡时的吸附量只有0.83 mg/g,限制了其在糖厂中的大规模应用。许多研究表明,壳聚糖、纤维素、淀粉及其衍生物等天然物质可被用作吸附剂[16]。这些物质具有无毒、可生物降解和低成本的特性,使它们成为一种很有前途的吸附剂[17]。因此,将生物质基吸附剂用于糖汁的脱色具有重要意义。
1 改性生物质基吸附剂
1.1 纤维素基吸附剂
纤维素是自然界中来源最丰富的天然高分子材料,含有丰富的羟基,具有良好的生物相容性、可降解性、可再生性等,被广泛应用于环境、食品、化工等领域[18]。Dolphen等[19]采用虾壳废料制备甲壳素纳米纤维吸附ME。随着温度的升高,甲壳素纳米纤维对ME的吸附量增加,在131,331,353 ℃时分别达到20,40,60 mg/g,在pH分别为3.83,5.93,3.92,3.87时,甲壳素纳米纤维对ME的吸附量高于甲壳素、改性甲壳素和壳聚糖,最大吸附量分别为242,99,61,8 mg/g。红外光谱和洗脱实验结果证实,ME与甲壳素纳米纤维之间的相互作用包括静电吸附和化学吸附,-NH3+基团影响了ME的吸附。但是最佳吸附条件是在酸性条件下,影响了最终成品糖的产量。
Chai等[20]将乙二胺改性的甘蔗渣作为吸附剂,研究了不同吸附剂用量、pH值和吸附时间对糖汁中有色物质吸附的影响,结果显示吸附剂用量为0.05 g/mL、pH为5.0、吸附时间为30 min时脱色率可达59.18%。但是该吸附剂的脱色率较低,无法满足工业生产的要求。
Zhou等[21]制备了3-氯-2-羟丙基三甲氯化铵和聚乙烯亚胺共改性柚子皮纤维素气凝胶(CP-PPA),并以合成的ME作为重熔糖浆的模型着色剂,在柚子皮气凝胶中含有丰富的胺官能团(季铵和质子化胺),通过静电相互作用定向吸附带负电荷的ME。采用新型的液膜-颗粒内扩散混合(LFIDM)模型和活性位点吸附(AAS)模型研究传质动力学,在CP-PPA吸附ME的初始阶段,CP-PPA内部孔隙吸附类黑素的能力(YED)急剧增加,直至达到最大值。初始的ME浓度梯度是吸附的主要驱动力,决定了CP-PPA吸附ME的平衡时间为60~120 min。在描述相同条件下吸附行为方面,AAS模型明显优于LFIDM模型。CP-PPA具有良好的平衡吸附能力,对ME的吸附量为749.51 mg/g,去除率为93.69%。但柚子皮纤维素气凝胶的开发还处于起步阶段,在ME的去除过程中仍需考虑成本效益问题。
Zhou等[22]制备了聚乙烯亚胺(PEI)功能化柚子皮(PP)衍生气凝胶(PEI-PPA),用于去除ME,带正电荷的 PEI-PPA有效吸附带负电荷的ME。采用新型的 EDR-IDR混合模型和AAS研究传质动力学,在相同条件下,AAS模型比EDR-IDR混合模型更能描述PEI-PPA对ME的吸附行为,控制了整个过程的传质阻力,化学吸附是绝对主导的控制机制。静电相互作用是吸附的主要驱动因素,弱相互作用是次要驱动因素。PEI-PPA对ME的最大吸附量为615.70 mg/g,ME去除率达92.36%。
Verma等[23]制备了胺修饰的余甘子叶粉(PELP)吸附ME,但是该吸附剂需要在酸性条件才能获得最佳的糖汁脱色效果。酸性条件对实际生产过程并不理想,因为蔗糖可能会转化为葡萄糖和果糖,从而减少精制糖的产量。
1.2 壳聚糖基吸附剂
壳聚糖作为一种天然的生物质材料,含有大量的-NH2和-OH等活性基团,溶于酸性溶液中会形成阳离子型聚合物电解质,吸附糖汁中带负电荷的色素。但壳聚糖易受到分子间和分子内相互作用,只能溶于某些特定的有机酸以及少数的无机酸中,限制了其应用[24]。因此,通常对壳聚糖的活性基团进行化学修饰和改性,提高其吸附性能。
1.2.1 磁性壳聚糖复合物
吸附剂在回收过程中因效率低、环境友好性差限制了其使用,用磁性材料对壳聚糖进行修饰,制备磁性壳聚糖复合材料,在外加磁场作用下很容易将吸附剂从溶液中分离[25]。磁性壳聚糖具有比表面积较大、尺寸小、吸附能力强、环保、可再生、易于分离和回收等性能,已广泛用于糖汁脱色中。
Chai等[26]采用离子交换技术制备磁性壳聚糖(MCS),然后用精氨酸改性制备精氨酸改性磁性壳聚糖(AMCS),用其吸附糖汁中酚类色素(没食子酸),最大吸附量为48.38 mg/g。同时,AMCS具有良好的再生能力,实现了蔗汁的无硫澄清,与传统脱色方法相比更显著地提高了白糖的食用安全性。
Liang等[27]采用简单的一步共沉淀法制备新型壳聚糖/Fe3O4复合微粒(MCTS),用于吸附糖汁中的没食子酸(GA)和咖啡酸(CA)。该微粒具有蜂窝状的多孔骨架,具有超顺磁性。平衡时的吸附量仅为0.055 mg/g,吸附量低,限制了其在工业中的大规模应用。
Song等[28]采用沉淀法和交联法相结合的方法制备了新型吸附材料磁性壳聚糖改性硅藻土(MCMD),将Fe3O4加载到硅藻土中,实现固液分离循环,用于去除糖汁中的没食子酸(GA)和咖啡酸(CA)。MCMD的比表面积比未改性前增加了4倍,表明其不仅含有壳聚糖的氨基,而且含有大量的Fe3O4晶体结构。MCMD对GA和CA的最大吸附量分别为31.949 mg/g和27.640 mg/g,对GA的吸附效果优于CA。吸附符合PSO和Langmuir模型,为自发吸热过程,吸附机理可能涉及静电相互作用和微孔填充。MCMD具有良好的可再生性,可以更好地实现甘蔗汁的无硫澄清,保证食品安全。
Fan等[29]通过原位合成法在磁性壳聚糖微球(MCM)上原位生长羟基磷灰石(HA),制备了具有较大比表面积的新型吸附材料——磁性壳聚糖羟基磷灰石微球(MCHAM)。磁性高分子微球具有体积小、比表面积大、吸附量大、磁响应性强(易于分离和回收)等特点,MCHAM的比表面积比MCM增加了45.63 m2/g,可以有效地吸附并去除蔗汁中的酚类物质(没食子酸),在pH为6时,最大吸附量为40.77 mg/g,吸附过程符合PSO动力学模型和Langmuir等溫线模型,主要为非均质单层的化学吸附。但是,这两种吸附剂的最佳吸附条件是在pH为6的酸性条件下,而在食糖生产过程中,应避免在酸性条件下进行,否则会使食糖产量降低。
1.2.2 季铵化改性壳聚糖
将壳聚糖进行季铵化改性,可以使吸附材料表面带有更多的正电荷,通过与带负电荷的色素之间的静电相互作用提高吸附量。Guo等[14]以戊二醛为交联剂,采用反相乳液交联法制备了磁性壳聚糖微球,用三甲基氯化铵(CTA)进行季铵化改性,合成了季铵功能化磁性壳聚糖微球(QAMCM),作为大分子还原糖碱性降解色素(HISADPs)的脱色剂表现出良好的吸附性能。通过进一步表征,表明QAMCM具有磁响应性、无毒性和热稳定性。采用新型的PFO-PSO组合模型和膜孔传质(FPMT)模型研究吸附行为和传质机理,PFO-PSO组合模型能够准确地计算出吸附过程的物理和化学吸附速率,物理和化学吸附共同参与了吸附过程,但化学吸附是绝对的主导吸附机制。FPMT模型能够很好地描述内部和外部传质过程,控制各个步骤任意时刻的传质速率,结果表明,依据HISADPs的初始浓度,应将接触时间控制在100~200 min。QAMCM对大分子还原糖碱性降解色素(HISADPs)的最大吸附量为98.03 mg/g,去除率达到98%,且具有良好的再生性能。但是,由于该吸附剂孔隙较小,吸附平衡时间太长(24 h),只在实验室模拟,不利于大规模工业化应用,后续应继续优化。
Xiao等[30]以戊二醛为交联剂,采用化学交联法和冷冻干燥法相结合的方法,用三甲基氯化铵(CTA)作为改性剂对壳聚糖进行定向改性,制备接枝季铵化壳聚糖,再与无机材料氧化石墨烯复合,制备季铵功能化壳聚糖-氧化石墨烯复合气凝胶(GO-QACSA),用于吸附大分子还原糖碱性降解色素(HISADPs)。该吸附剂含有丰富的多孔网状结构,孔隙率高,比表面积大,暴露出大量吸附HISADPs的活性位点。采用新型MLA模型拟合吸附过程,并研究吸附机理,进一步证明HISADPs在GO-QACSA上的吸附是双层的,平均一个HISADPs可以被GO-QACSA的2~3个官能团共享,方向是平行的。采用外部传质阻力(EMTR)模型、内部传质阻力(IMTR)模型、EMTR-IMTR组合模型和活性位点吸附(AAS)模型研究传质机理。结果表明,AAS模型能更好地描述吸附行为,是GO-QACSA吸附HISADPs的限速步骤,化学吸附是绝对的主导机制,但同样也受到EMTR-IMTR模型的影响,组合模型可以很好地描述GO-QACSA 周围的液膜和内部的孔隙所实现的HISADPs吸附过程的动态特性。结果表明,HISADPs的去除率达90%左右,30 min即可达到动态平衡,克服了吸附平衡时间长的弊端,平衡时的最大吸附量为364.09 mg/g。但其制备工艺复杂,成本高,经济效益低于活性炭、大孔树脂,限制了其在制糖行业的大规模应用。
Tang等[31]制备了超支化聚乙烯亚胺功能化壳聚糖气凝胶(HPCA),用于电负性的类黑素(ME)的吸附,该吸附剂具有较大的比表面积、丰富的氨基官能团和较高的亲水性。基于密度泛函理论(DFT),定量分析了分子表面的静电势(EP),EP表面电位越高,越有利于吸附带负电荷的ME,HPCA吸附ME的主要官能团是伯胺,表明-RNH2是HPCA结构中质子化程度最高的基团。采用新的MA模型研究吸附机理,该模型表明吸附过程符合双层吸附模型,1个ME分子可以被HPCA的2个官能团共享。采用两种新型的外扩散阻力-内扩散阻力(EDR-IDR)混合模型和活性位点吸附(AAS)模型研究传质机理,AAS模型拟合效果优于EDR-IDR,是主要的传质阻力,表明ME能迅速扩散到吸附剂表面,以化学吸附为主。HPCA对ME的吸附量为765.19 mg/g,去除率为94.95%,5次循环后仍保持在91.45%,具有较好的再生性能。但HPCA在吸附ME方面存在一定的缺陷,其成本效益远不如目前常用的商业吸附剂(活性炭)。
1.3 淀粉基吸附剂
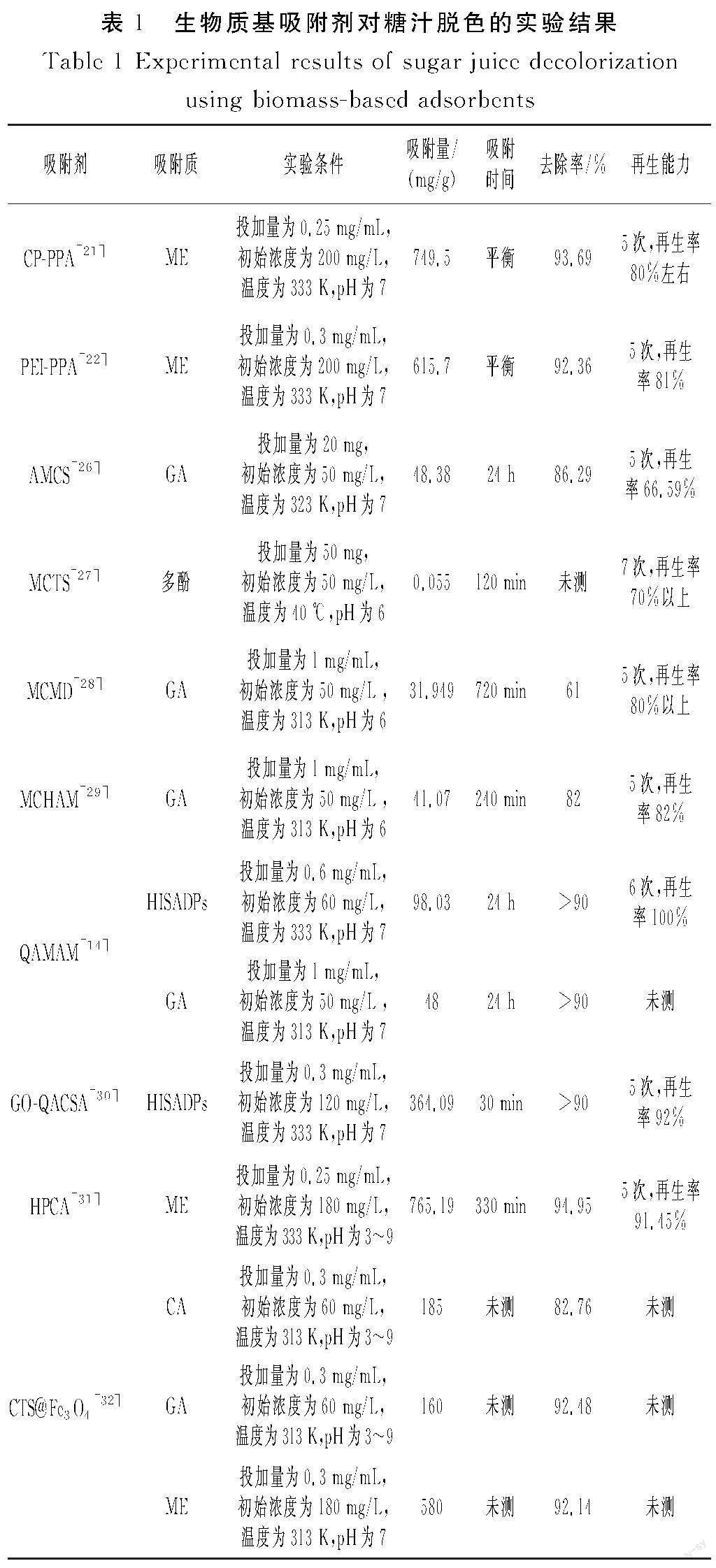
淀粉(starch)是一种来源广泛的天然有机高分子化合物,对环境友好、无毒、生物降解性能良好,是一种绿色环保材料[17]。Yin等[32]合成了新型的阳离子木薯淀粉(CTS)功能化磁性纳米颗粒(CTS@Fe3O4)并用于去除糖汁中的咖啡酸(CA)、没食子酸(GA)和ME。吸附过程符合二级动力学模型和Langmuir等温线模型,拟合系数接近1,在吸附剂表面形成了均匀分布的单分子层,以化学吸附为主。热力学研究表明其属于自发的吸热过程。在最佳条件下由于淀粉表面存在季铵基团,吸附剂表面具有稳定的正电荷,其对糖汁中的色素表现出优异的吸附性能。CTS@Fe3O4对CA、GA和ME的平衡吸附量分别为185,160,580 mg/g。在二元体系中,色素间的吸附主要是拮抗吸附,吸附量低于单一体系,共存色素浓度越高,拮抗作用越明显。吸附速度是影响竞争吸附的主要因素,吸附机理主要是强的静电相互作用和弱的氢键作用。糖汁中含有多种色素,制备的吸附剂只在单一体系中效果好,但是多种色素共存时吸附量降低,在糖厂中的应用受到了限制。如果能制备出一种可以同时应用于共存体系的吸附剂,效果更好。具体吸附结果见表1。
2 影响吸附效果的因素
吸附过程容易受到多种因素的影响,如pH、吸附剂投加量、接触时间。
2.1 pH的影响
溶液的pH值对吸附剂的吸附性能影响较大。在不同的pH环境中,吸附剂和溶剂之间经常存在质子化和脱质子化过程,这会改变吸附剂表面电荷的性质,进一步影响吸附剂与吸附质之间的相互作用。因此,吸附剂在不同pH环境下糖汁溶液中的吸附能力不同[33]。pH
2.2 吸附剂用量的影响
吸附剂的用量是影响吸附效率的重要因素。合适的吸附剂用量可以使吸附剂达到最大利用率[34]。通常情况下,生物质基吸附剂对糖汁色素的去除率随着吸附剂用量的增加而增加,主要是由于随着吸附剂用量的增加,吸附位点增加。但是,当吸附剂的用量超过一定值时,吸附量反而会下降,主要是由于过量的吸附剂导致活性位点过剩,不仅降低了吸附量,而且造成了资源浪费,在实际应用中增加了制糖的经济成本。因此,需通过实验确定最佳投加量。
2.3 接触时间的影响
接触时间也会对吸附过程产生影响。在初始阶段,由于吸附剂有大量可用的吸附活性位点和初始吸附阶段的高驱动力,吸附能力急剧增加。随后,随着接触时间的延长,吸附能力缓慢增加,吸附达到平衡,表明吸附剂的可用吸附位点基本被大量色素占据[35]。
3 吸附机制
糖汁中色素的吸附机理主要有静电相互作用、氢键、范德华力。其中,静电相互作用是主要的吸附机制,而氢键和范德华力是弱的相互作用。
3.1 静电相互作用
吸附剂表面的正电荷与吸附物中带负电荷的羧基/羧酸基团通过静电相互作用,使吸附量提高。Tang等[31]通过FTIR/XPS/DFT研究了超支化聚乙烯亚胺功能化壳聚糖气凝胶(HPCA)对ME的吸附机制。AAS模型表明化学吸附是主要的吸附机理。质子化氨基是促成HPCA吸附ME的主要基团。Zhou等[22]通过DFT定量分析了PPCE、PPCE-DA、PEI-PPA、质子化PEI-PPA和ME的静电势(EP)分布,质子化PEI-PPA显示出更强的正电荷,ME携带强的负电荷,因此很容易通过静电相互作用定向吸附。
3.2 氢键和范德华力
Zhou等[22]采用独立梯度模型(IGM)和Hirshfeld表面分析,在sign(λ2)ρ=-0.05 a.u.附近,对应的δginter峰高度为0.08 a.u.,表明存在氢键相互作用。ME羧基/羧酸基团上的氧原子与CP-PPA的季铵盐基团上的甲基氢之间出现大面积绿色平板,表明弱相互作用的范德华力也参与了吸附过程。
Tang等[31]采用独立梯度模型(IGM)对HPCA与ME的弱相互作用进行了可视化和定量分析,在sign(λ2)ρ=-0.04 a.u.附近出现了一个高度约为0.08 a.u.的峰,表明存在氢键作用。在HPCA的质子化胺基团上的H原子和ME羧酸基团间出现深蓝色的椭圆板,这也表明存在氢键作用[36]。出现绿色区域,表明HPCA和类黑素之间存在范德华力[37]。
4 结论和展望
本文综述和讨论了生物质基吸附剂对糖汁中主要色素的吸附,通过对吸附剂进行改性提高其吸附性能,总结了吸附剂用量、pH和接触时间对吸附量的影响。讨论了生物质基吸附剂对色素的吸附机理,主要包括强的静电相互作用和弱的氢键和范德华力。然而,通过生物质基吸附剂去除糖汁中的色素仍面临着许多挑战。下面进行以下几点的总结:
第一,目前糖厂仍采用亚硫酸法和碳酸法用于糖汁澄清,制备的改性吸附剂未能实现工业化应用。
第二,关于糖汁中酚类物质的吸附,最适pH为酸性条件,而酸性条件对食糖的生产不利,因为在酸性条件下,蔗糖会转化为葡萄糖和果糖,影响蔗糖产量。
第三,改性吸附剂的开发仍处于实验室阶段,产生的经济效益仍不如商用活性炭,未能进行大规模的工业化应用。
綜上,未来的研究中应简化吸附剂的合成方法、提高吸附剂对多种色素的适用性,并实现大规模的工业化应用。
参考文献:
[1]李辉尚,刘芷妍,宋建堂,等.国际食糖出口限制政策对我国食糖市场影响与启示[J].中国食物与营养,2023,29(1):42-46.
[2]许文婷,王周,陈国强,等.澄清脱色技术在甘蔗制糖中的应用[J].食品与机械,2022,38(9):234-238.
[3]ABDELRAHMANE A, HEGAZEY R M. Exploitation of Egyptian insecticide cans in the fabrication of Si/Fe nanostructures and their chitosan polymer composites for the removal of Ni(Ⅱ), Cu(Ⅱ), and Zn(Ⅱ) ions from aqueous solutions[J].Composites Part B,2019,166:382-400.
[4]MUNIRASUS, HAIJA M A, BANAT F. Use of membrane technology for oil field and refinery produced water treatment — a review[J].Process Safety and Environmental Protection,2016,100:183-202.
[5]EFOMEJ E, RANA D, MATSUURA T, et al. Effects of operating parameters and coexisting ions on the efficiency of heavy metal ions removal by nano-fibrous metal-organic framework membrane filtration process[J].Science of the Total Environment,2019,674:355-362.
[6]BEZZINA J P, ROBSHAW T, DAWSON R, et al. Single metal isotherm study of the ion exchange removal of Cu(Ⅱ), Fe(Ⅱ), Pb(Ⅱ) and Zn(Ⅱ) from synthetic acetic acid leachate[J].Chemical Engineering Journal,2020,394:124862.
[7]USSIPBEKOVA Y Z, SEILKHANOVA G A, JEYABHARATHI C, et al. Electrochemical deposition and dissolution of thallium from sulfate solutions[J].International Journal of Analytical Chemistry,2015(2):1-7.
[8]HOSSEINIS M, ALIBAKHSHI H, JASHNI E, et al. A novel layer-by-layer heterogeneous cation exchange membrane for heavy metal ions removal from water[J].Journal of Hazardous Materials,2020,381:120884.
[9]FOONG C Y, WIRZAL M D H, BUSTAM M A. A review on nanofibers membrane with amino-based ionic liquid for heavy metal removal[J].Journal of Molecular Liquids,2019,297:111793.
[10]WU H Y, WANG W J, HUANG Y F, et al. Comprehensive evaluation on a prospective precipitation-flotation process for metal-ions removal from wastewater simulants[J].Journal of Hazardous Materials,2019,371:592-602.
[11]ALLIOUXF M, KAPRUWAN P, MILNE N, et al. Electro-capture of heavy metal ions with carbon cloth integrated microfluidic devices[J].Separation and Purification Technology,2018,194:26-32.
[12]YU Y, YU L, KOH K Y, et al. Rare-earth metal based adsorbents for effective removal of arsenic from water: a critical review[J].Critical Reviews in Environmental Science and Technology,2018,48(22-24):1127-1164.
[13]COCA M, GARCA M T, MATO M, et al. Evolution of colorants in sugarbeet juices during decolorization using styrenic resins[J].Journal of Food Engineering,2008,89(4):429-434.
[14]GUO L Y, LU H Q, RACKEMANN D, et al. Quaternary ammonium-functionalized magnetic chitosan microspheres as an effective green adsorbent to remove high-molecular-weight invert sugar alkaline degradation products (HISADPs)[J].Chemical Engineering Journal,2021,416:129084.
[15]LI W. Rosin-based polymer@silica core-shell adsorbent: preparation, characterization, and application to melanoidin adsorption[J].LWT-Food Science and Technology,2020,132(1):109937.
[16]KUMAR S, WANI M Y, KOH J, et al. Carbon dioxide adsorption and cycloaddition reaction of epoxides using chitosan-graphene oxide nanocomposite as a catalyst[J].Journal of Environmental Sciences,2018,69:77-84.
[17]侯俊,尹雪雪,楊梓俊,等.生物质基吸附剂对水中磷酸盐的去除和回收研究进展[J/OL].水资源保护:1-17[2023-03-15].https://kns.cnki.net/kcms/detail/32.1356.TV.20230302.1604.002.html.
[18]MAHJOUB J, NOUHA S, YASSINE E, et al. Chemical modification of microcrystalline cellulose with polyethyleneimine and hydrazine: characterization and evaluation of its adsorption power toward anionic dyes[J].International Journal of Biological Macromolecules,2022,229:210-223.
[19]DOLPHEN R, THIRAVETYAN P. Adsorption of melanoidins by chitin nanofibers[J].Chemical Engineering Journal,2010,166(3):890-895.
[20]CHAI B H, MENG H C, ZHAO Z G, et al. Removal of color compounds from sugarcane juice by modified sugarcane bagasse: equilibrium and kinetic study[J].Sugar Technology,2016,18(3):317-324.
[21]ZHOU L S, XIONG Y S, JIA R, et al.(3-Chloro-2-hydroxypropyl) trimethylammonium chloride and polyethyleneimine co-modified pomelo peel cellulose-derived aerogel for remelt syrup decolorization in sugar refining[J].International Journal of Biological Macromolecules,2023,229:1054-1068.
[22]ZHOU L S, LU H Q, JIA R,et al. Insights into mass transfer mechanism and micro-interaction of melanoidin adsorption on polyethyleneimine-functionalised pomelo-peel-derived aerogel[J].Separation and Purification Technology,2023,310:123079.
[23]VERMA R, KUNDU L M, PANDEY L M. Enhanced melanoidin removal by amine-modified Phyllanthus emblica leaf powder[J].Bioresource Technology,2021,339:125572.
[24]CHEN B W, DING L, WANG Y, et al. High efficient adsorption for thorium in aqueous solution using a novel tentacle-type chitosan-based aerogel: adsorption behavior and mechanism[J].International Journal of Biological Macromolecules,2022,222:1747-1757.
[25]ZHANG Y Z, CAI T T, ZHAO Z W, et al. Poly(amidoxime)-graft-magnetic chitosan for highly efficient and selective uranium extraction from seawater[J].Carbohydrate Polymers,2023,301:120367.
[26]CHAI Z H, LI C L, ZHU Y, et al. Arginine-modified magnetic chitosan: preparation, characterization and adsorption of gallic acid in sugar solution[J].International Journal of Biological Macromolecules,2020,165:506-516.
[27]LIANG X Q, FAN S L, ZHANG J X, et al. Polyphenol removal from sugarcane juice by using magnetic chitosan composite microparticles[J].Sugar Technology,2019,21(1):104-112.
[28]SONG X R, CHAI Z H, ZHU Y, et al. Preparation and characterization of magnetic chitosan-modified diatomite for the removal of gallic acid and caffeic acid from sugar solution[J].Carbohydrate Polymers,2019,219:316-327.
[29]FAN S L, HUANG Z Q, ZHANG Y J, et al.Magnetic chitosan-hydroxyapatite composite microspheres: preparation, characterization, and application for the adsorption of phenolic substances[J].Bioresource Technology,2019,274:48-55.
[30]XIAO Y, LU H Q, SHI C R, et al. High-performance quaternary ammonium-functionalized chitosan/graphene oxide composite aerogel for remelt syrup decolorization in sugar refining[J].Chemical Engineering Journal,2022,428:132575.
[31]TANG J Y, XIONG Y S, LI M X, et al. Hyperbranched polyethyleneimine-functionalised chitosan aerogel for highly efficient removal of melanoidins from wastewater[J].Journal of Hazardous Materials,2023,447:130731.
[32]YIN J Y, FANG K, LI J B, et al. Competitive adsorption mechanisms of pigments in sugarcane juice on starch-based magnetic nanocomposites[J].International Journal of Biological Macromolecules,2023,231:123134.
[33]XUE H J, GAO X, SELIEM M K, et al. Efficient adsorption of anionic azo dyes on porous heterostructured MXene/biomass activated carbon composites: experiments, characterization, and theoretical analysis via advanced statistical physics models[J].Chemical Engineering Journal,2023,451:138735.
[34]LI H J, MIAO L, ZHAO G Q, et al. Preparation of high-performance chitosan adsorbent by cross-linking for adsorption of Reactive Red 2 (RR2) dye wastewater[J].Journal of Environmental Chemical Engineering,2022,10(6):108872.
[35]WEN Y P, XIE Z F, XUE S S, et al. Preparation of novel polymethacryloyl hydrazone modified sodium alginate porous adsorbent with good stability and selective adsorption capacity towards metal ions[J].Separation and Purification Technology,2022,303:122184.
[36]CORNETIN L, RUBEZ G, HASSAN K, et al. Accurately extracting the signature of intermolecular interactions present in the NCI plot of the reduced density gradient versus electron density[J].Physical Chemistry Chemical Physics:PCCP,2017,19(27):17928-17936.
[37]LU T, CHEN Q X. Independent gradient model based on Hirshfeld partition: a new method for visual study of interactions in chemical systems[J].Journal of Computational Chemistry,2022,43(8):539-555.

