蒙药额尔敦-乌日勒组方特点及治疗动脉粥样硬化研究概述
刘倩倩,赵舒婷,王昕蓉,胡志耕,陈进成
(1.山西中医药大学第一临床学院,太原 030024;2.山西中医药大学附属医院心内科,太原 030024)
动脉粥样硬化(atherosclerosis,AS)是最常见的心血管疾病(cardiovascular disorders,CVD)之一,其主要机制是大动脉的脂质堆积和炎症反应,并最终可能导致严重的临床结局:心肌梗死(myocardial infarction,MI)或卒中[1]。现在临床常用的抗AS药物[2-3]有调脂药(如贝特类、他汀类)和抗血小板药(如阿司匹林)等,这些药物对AS的发生发展具有降血脂、抗炎作用,但是存在肝功能损伤、胃肠道不适等副作用。
我国民族医药在长期发展中形成了自己独特的治疗理念和显著临床效果。其中额尔敦-乌日勒作为蒙药中具有代表性的方剂,被寓意为“珍贵神奇的药丸”,又被称为索布德乌日勒、桑丕勒诺尔布、如意珍宝丸等[4],最初记载于13世纪仁钦扎拉桑撰写的“满阿格·穆迪格坡仍瓦”(秘诀佛珠)中。近几年的研究中发现额尔敦-乌日勒在改善心血管供血方面具有一定疗效,在治疗冠心病、稳定心绞痛、缺血性脑卒中等疾病中取得了一定的临床效果。因此笔者在本文总结额尔敦-乌日勒的传统药性和现代药理研究,以及此方治疗AS的临床疗效,为今后抗AS的研究和防治提供思路。
1 蒙医学对AS的认识与治疗理念
蒙医学中并没有AS这个病名,其在蒙医学中归属于“精华消化不良”病范畴。蒙医学认为人体是由三根(赫依、希拉、巴达干)和七素(食之精华、面、肉、脂、骨、髓、精)组成,三根异常会导致七素的改变,从而引发疾病。蒙医认为AS的形成与肝胃二脏有着密切关系,在蒙医理论中胃可分清食物之精浊,肝可分清血之清浊,当胃对油腻湿重不能完全消化吸收,肝不能完全分清血之清浊,导致三根中巴达干偏盛,血脉中的油腻湿重逐渐增多,形成高脂血症,若日久凝滞于脉络中,沉附于血管壁形成脂质斑块,而出现AS的表现[5]。
《四部经典》中记载:“治心、主肠、大肠之病,应以抑赫依为主。”赫依在三根中居于首位,属性平和,属于五元(土、水、火、气、空)中气与空元,主宰生命活动,其中普兴赫依存在于心脏与四肢,支撑身体,推动血液循环;调节赫依存在于胃和腹部消化道,调节胃火,增强胃肠运动[6]。赫依为各种生理功能提供动力,楚斯(血液)为身体提供营养物质,因此心血管疾病的内因与赫依和楚斯有着密切关系。
蒙医在AS防治上提出温中健胃、化脂破坚、活血化瘀的原则,从而调理三根,促进赫依的运行,减少楚斯停留而形成瘀血,健胃改善消化,减少心脉中巴达干,从而防治血脂堆积[5],临床代表方剂有额尔敦-乌日勒、沉香-21味散、广枣-7味散等。其中额尔敦-乌日勒具有清热安神、行气活血、舒经活络的功效,可有效分别血之清浊,通过抑制赫依,调理三根七素,从而改善血液中血脂代谢问题,有效缓解血液循环。
2 额尔敦-乌日勒组方演变
随着时代发展,额尔敦-乌日勒的组方不断发生变化,现将1829—1998年有关记载额尔敦-乌日勒组成的文献进行比较,在1829年的《蒙医金匮》中额尔敦-乌日勒由紫檀、珍珠(制)、肉豆蔻、牛黄、犀角(制)、诃子、甘草、地锦草、白云香、决明子、苘麻子、红花、丁香、豆蔻、白苣胜、黑苣胜、荜茇、海金沙、螃蟹、川楝子、栀子、麝香、檀香、沉香、肉桂、广木香、土木香、石膏以及银朱30味药物组成;1984年内蒙古卫生厅编写的《内蒙古蒙成药标准》中将其分为珍宝丸方和珍珠丸方,珍宝丸将红花改为藏红花,珍珠丸在此又将犀角(制)改为水牛角粉,主要是将水牛角、人工牛黄代替犀牛角和天然牛黄,并减少麝香用量;1986年《中国医学百科全书·蒙医学》(蒙文版)和1992年的《中国医学百科全书·蒙医学》(汉文版)中均将石膏改为天竺黄。
目前以1998年版《中华人民共和国卫生部药品标准·蒙药分册》第128页的药物组成为临床标准[8],此方组成为珍珠(制)20 g,栀子15 g,沉香15 g,檀香15 g,地锦草10 g,海金沙15 g,方海10 g,石膏15 g,决明子10 g,土木香10 g,丁香10 g,降香15 g,白巨胜10 g,肉桂10 g,黑种草子10 g,荜茇10 g,白豆蔻15 g,红花15 g,木香10 g,诃子15 g,肉豆蔻10 g,苘麻子10 g,草果仁15 g,甘草10 g,牛黄5 g,牛角浓缩粉30 g,川楝子15 g,枫香脂15 g,水调为丸,银朱为包衣。
3 额尔敦-乌日勒治疗AS的传统药学阐释与现代药理学研究
额尔敦-乌日勒方中以珍珠为君药,具有安神益脑,扶正固本[4]的作用,但是珍珠入胃后在巴达干、协日、赫依的相互作用,其药由苦、涩、甘消化后效凉,可起到解毒镇静,养脑愈脉的功效;牛角味涩、咸,性温,可清肝热;牛黄味苦、甘,性凉,效重、钝、柔、燥,清热解毒、镇静安神;栀子味酸,消化后味甘,性凉,效钝、糙,清血脉之热;沉香味辛、苦,性凉,效重、软、腻、柔、燥、钝、柔,可抑制赫依,清心中赫依之热;地锦草味苦,性平、钝、浮,主治止血,燥黄水,愈合伤口,在方中起到清脉热之功效。檀香味涩,性寒,效柔钝燥,清心肺燥热;降香味辛,性凉,效腻,可抑制赫依、清热止痛;海金沙和方海(螃蟹)味甘,性寒凉以利尿清肾热;土木香味甘、苦、辛,性平,效腻、锐、燥、重,《无误蒙药鉴》中记载此药消化后味甘、苦、辛,转化味甘、酸,主治赫依,血瘀,巴达干热,止刺痛,在方中可平气血紊乱、止痛;丁香、白巨胜、肉桂性温,可祛赫依之寒,挟胃火;黑种草子味辛、甘,效轻、糙、燥,可健胃调理胃火、驱肝寒、疏肝;荜茇味辛,性温。效腻、锐、轻、燥。可调理胃火,祛“巴达干·赫依”,在方中护养胃火;白豆蔻味辛、苦性温,效轻、燥、腻、锐,可祛肾寒,镇赫依;诃子、肉豆蔻、苘麻子、红花、草果仁等可作为脏腑病及调理体素的辅药[8]。诸药合用起到清热安神、行气活血、舒经活络的功效。
额尔敦-乌日勒中药物按照三根-八性-药性进行分析,在圆环图中,中心为三根第二圈为药物的八性最外层为药性(图1)。图中清晰可见32%的药物为温性,药效以轻、糙、热、锐为主,可以有效制约巴达干,更好起到温中健胃的作用。其次占比较大的为平性和凉性,从总体上决定此方偏于凉性,而且药效显示重、腻、钝的药物偏多,重和腻可以有效的抑制赫依,起到调理血脉作用。还有19%的钝性药,可有效抑制阳性的希拉,起到额尔敦-乌日勒治疗的根本在于赫依的紊乱,其希拉和巴达干也均有相应的不适,导致三根偏盛异常,因此治疗上注重温胃火,调理三素。
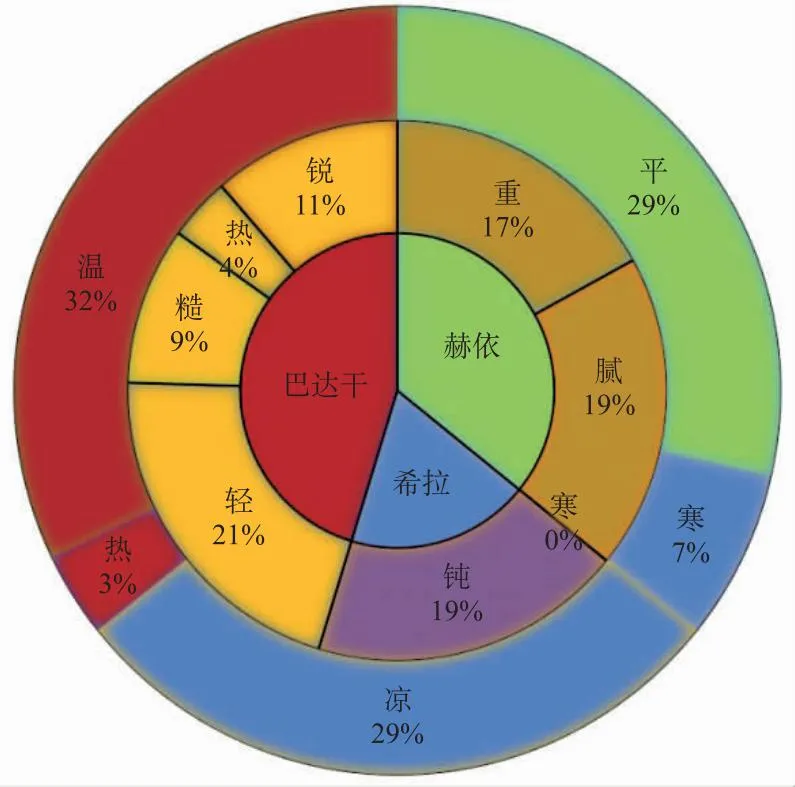
图1 额尔敦-乌日勒“三根-八性-药性”关系
现代药理研究表明,额尔敦-乌日勒中的栀子、决明子、诃子、荜茇具有调节血脂代谢作用;栀子、丁香、降香、肉桂等具有抗血小板凝聚,减少血栓形成;土木香、牛黄、川楝子通过激活不同通路,预防AS发以及和改善斑块(表1)。在额尔敦-乌日勒30味药物中,虽然只有一部分药物现代药理可以明确其对AS具有防治作用,但是整体运用此方在动物实验过程中发现其对AS具有显著效果。
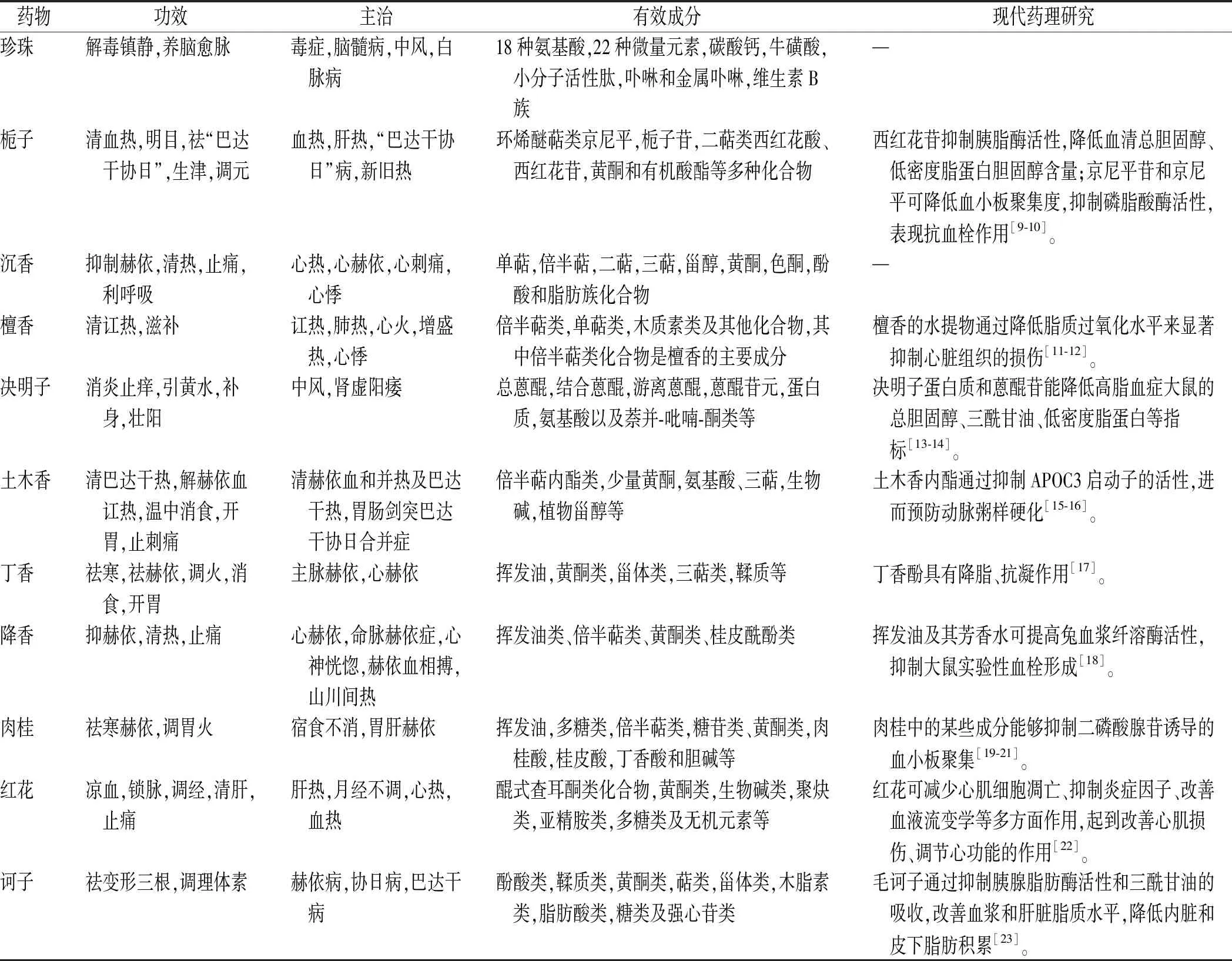
表1 额尔敦-乌日勒药物组成及现代药理

续表1 额尔敦-乌日勒药物组成及现代药理
基础实验研究表明额尔敦-乌日勒在治疗心血管疾病、神经系统疾病、风湿类疾病等方面均有疗效。额尔敦-乌日勒可通过调节血脂、改善血流变起到抑制AS斑块作用,其中给予家兔额尔敦-乌日勒药量与全血黏度和血浆黏度成正比,且中剂量以上的额尔敦-乌日勒显著抑制兔主动脉内膜加厚,减轻内膜损伤[28]。额尔敦-乌日勒能够减少AS家兔血清中炎性标志物超敏C反应蛋白(hypersensitive C-reactive protein,hs-CRP)含量,降低血管细胞粘附分子-1(vascular cell adhesion molecule-1,VCAM-1)水平,以及主动脉VCAM-1的表达,表明其可通过减轻炎症反应,阻抑单核细胞的迁移和聚集,干扰巨噬细胞来源的泡沫细胞的形成,从而起到阻抑粥样病变的形成、发展和消退斑块的作用[29]。董平等[30]通过以家兔主动脉平滑肌细胞(smooth muscle cells,SMC)增殖细胞核抗原(proliferating cell nuclear antig,PCNA)和血小板源性生长因子(platelet-derived growth factor A,PDGF-A)表达为靶点,研究发现额尔敦-乌日勒可能通过抑制家兔PCNA表达减少SMC吞噬脂质形成泡沫细胞,以及减少PDGF的释放与相应细胞膜PDGF受体结合,从而减少对平滑肌细胞的刺激,抑制血管平滑肌细胞(vascular smooth muscle cells,VSMC)迁移、增殖而起到抗AS的作用。
都格尔等[31]通过与辛伐他汀作对照,证明额尔敦-乌日勒可以预防AS斑块的形成,以及通过调节血脂,降低红细胞聚集指数、升高红细胞变性指数、降低全血黏度来对高脂血症的AS斑块起到拮抗作用,与辛伐他汀对比,额尔敦-乌日勒对于家兔的肝肾功能未产生副作用。研究发现额尔敦-乌日勒化裁出来的以珍珠为主的7味优化方,在治疗AS斑块上也具有显著疗效,并且在调节低密度脂蛋白、总胆固醇、三酰甘油作用上优于额尔敦-乌日勒和辛伐他汀;在稳定AS斑块方面,额尔敦-乌日勒可能是通过降低MMPs(MMP-1、MMP-2、MMP-9)活性和基因表达而起作用,但是7味优化方不具备降低MMPs活性和基因表达的作用[32-33]。乌兰其其格等[34-35]通过家兔实验发现该方可抑制AS血管壁NF-κB活性、下调MCP-1表达,起到抗AS作用,同时发现额尔敦-乌日勒可以通过促进动脉壁中一氧化氮合酶(endothelial nitric oxide synthase,eNOS)基因表达,增加其活性,升高血清中一氧化氮(nitric oxide,NO)水平,起到抑制AS斑块形成、发展和稳定易损斑块的作用。
研究发现,额尔敦-乌日勒可能是通过对血管内皮凝血纤溶物质的影响,降低PAI-1和Fbg的上升,增加主动脉组织t-PA的表达,恢复纤溶系统的平衡状态,从而稳定AS易损斑块,并且进一步研究表明,此方也可以通过降低血管内皮因子内皮素、血小板活化因子的上升,从而降低主动脉组织血管内皮因子内皮素的表达,恢复内皮功能的平衡状态,从而发挥稳定AS易损斑块的作用[36-37]。
4 额尔敦-乌日勒治疗AS的临床研究
本研究通过中国知网、维普数据库、万方数据库搜索额尔敦-乌日勒治疗和(或)联合治疗缺血性心血管病的随机对照研究文献,检索结果表明该方目前以治疗缺血性脑卒中为主,主要表现在:应用西药实行降低颅内压、扩张血管、保护神经、抵抗血小板聚集等治疗基础上加用额尔敦-乌日勒可以取得很好的临床效果;其中吉木斯[38]选取缺血性脑卒中患者60例,对照组温水服用拜阿司匹林肠溶片和瑞舒伐他汀钙片,观察组在对照组基础上晚饭后温水送服额尔敦-乌日勒,4周为1个疗程,共6个疗程,观察组治疗总有效率明显高于对照组,且神经功能改善与生活自理能力均优于对照组。胡玉荣等[39]收取120例缺血性脑卒中恢复期的患者,试验组给予阿司匹林肠溶片和额尔敦-乌日勒,对照组服用阿司匹林肠溶片和银杏叶片,其中两组神经功能缺损和两组日常生活活动能力得到明显改善,而且额尔敦-乌日勒可以有效改善血液黏度及降低低密度脂蛋白,并且在治疗期间心电图、血常规、尿常规、肝肾功能、凝血四项、血脂、血液流变学指标未出现异常改变。莲花等[40]临床研究发现额尔敦-乌日勒联合血栓通治疗脑梗死,不仅有效降低低密度脂蛋白,而且对于同型半胱氨酸和超敏 C 反应蛋白均起到显著作用。通拉嘎[41]收治100例AS患者作为研究对象,试验组和对照组血压控制<140/90 mmHg(1 mmHg=0.133 kPa),试验组给予额尔敦-乌日勒15粒,对照组口服阿司匹林肠溶片1~2片,试验组治疗后NIHSS评分(3.45±0.09)显著高于对照组(2.15±0.12),表明对照组神经功能修复能力强于试验组,两组总有效率分别为96.00%和84.00%,说明虽然试验组在神经修复能力上相对较弱,但总有效率明显优于对照组;此外当肾功能不全或妊娠期时,阿司匹林结合率相对较低,并且存在一定出血和胃肠道不适的风险,目前额尔敦-乌日勒的临床研究中没有发现不良反应,安全指标均未见异常。见表2。
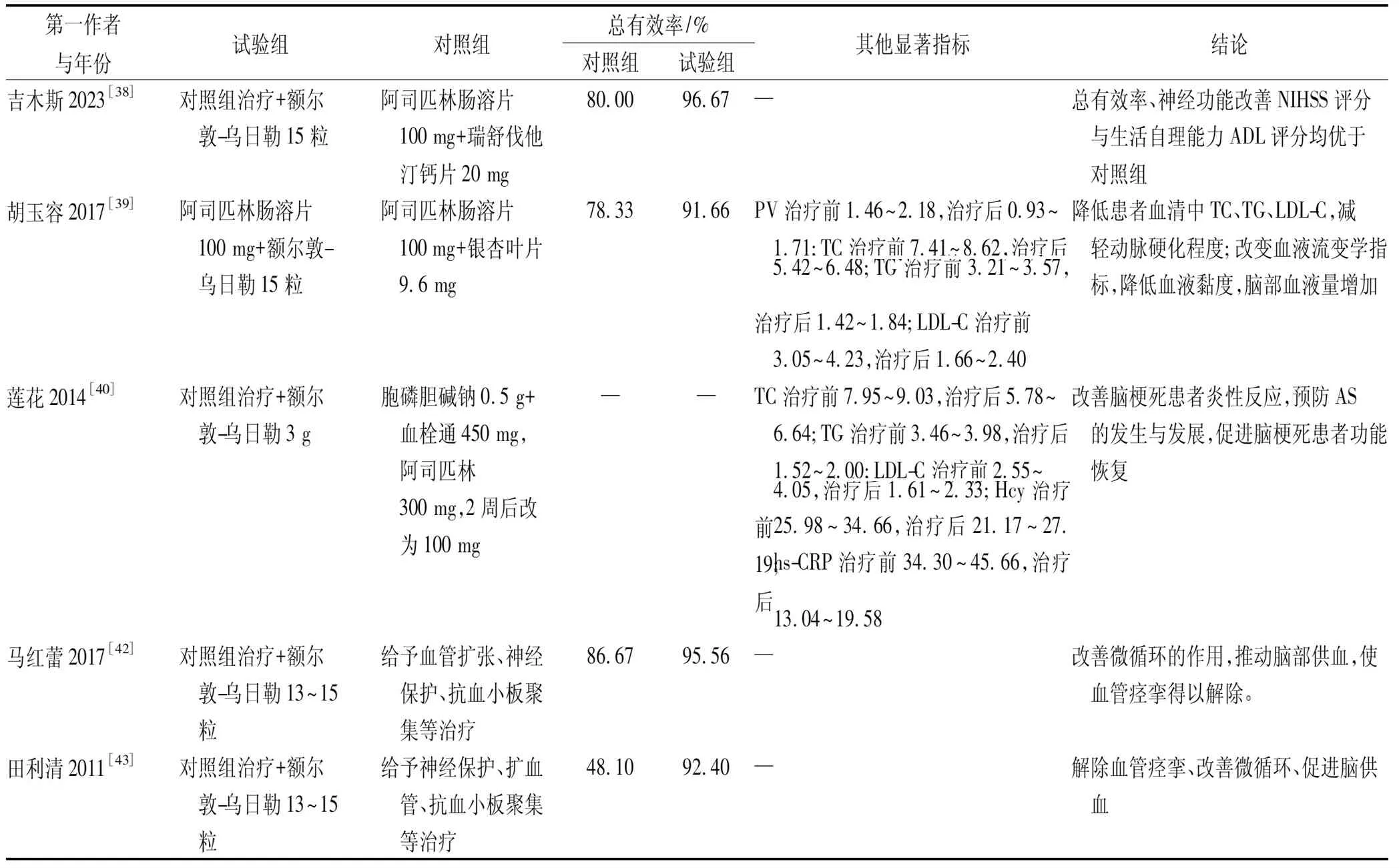
表2 额尔敦-乌日勒缺血性脑卒中文献
AS是冠心病、脑梗死等缺血性心血管疾病的主要病理学基础,额尔敦-乌日勒可有效缓解脑部缺血性疾病,并且具有五步同治绝病根特点:第一步:修复血管,软化血管;第二步:调节经络,镇静安神;第三步:强心健脑、激心活酶;第四步:清洗血毒,益气和血;第五:打通血管,裂解斑块[5],特别是修复损伤的血管,益气和血祛血毒,裂解斑块、疏通血管符合AS的病理学特点,是对AS治疗的强有力证据,因此该方对于AS的治疗会起到较好的临床效果。
5 研究展望
随着人们对蒙药疗效的认可和对传统医学的回归,越来越多的人开始关注和研究蒙药,以探索和发挥其巨大的潜力。这不仅促进蒙医民族医药的发展,还将为我国医疗事业注入新的活力和可能性。深入研究和理解藏药方剂配伍理论的变化规律,对推动蒙药的发展和应用具有重要意义。
我国现存在数量巨大的心血管病危险因素人群,负担持续加重,从“已病”和“未病”双重着手,既要做好心血管病的二级预防治疗,还应进一步强化高血压、高血糖、高血脂等可调节危险因素的上游治疗[44],这也是当前我们面临的形势与挑战。
本文通过大量的文献总结分析,研究表明额尔敦-乌日勒在调理血脂水平,降低红细胞聚集指数、升高红细胞变性指数、降低全血黏度等方面有着明显的作用,从而能抑制AS斑块的形成;通过降低MMPs活性和基因表达来稳定AS斑块,对动脉内斑块的发生发展起到干预和稳定作用,并且通过活血通脉,改善血液循环,对于缺血性心血管病的治疗有显著的临床效果,且安全性高。
综上所述,蒙药额尔敦-乌日勒在改善缺血、疏通血管等方面作用突出,为今后研究该方在AS的治疗上具有较大的研究价值,在AS的临床治疗上有可能成为一个更具特色、更加稳定,更安全的方药,为未来AS的防治提供新的治疗理念和方法。

