高血压合并脑小血管病患者情感淡漠危险因素及其与认知功能的相关性
曹佳丽,王天然,刘 洋,张 舵,徐金娥,刘 冲*,王淑梅,韩永昌,杨露露
(1.承德医学院研究生学院,河北 承德 067000;2.保定市第一中心医院医学影像一科,河北 保定 071000;3.河北医科大学研究生学院,河北 石家庄 050017;4.河北大学附属医院放射科,河北 保定 071000)
脑小血管病(cerebral small vessel disease,CSVD)是老年人常见疾病,长期发展可致卒中、认知障碍、步态障碍及情感障碍等,高血压为其主要危险因素[1]。近年来,情感淡漠逐渐被视为独立综合征,其在我国老年CSVD 患者中的患病率高达37.33%[2-3];有学者[4]由此提出血管淡漠假说,即CSVD 通过损伤投射至前额叶、基底节、顶叶和前扣带回的额叶区纤维束而引发淡漠。本研究观察高血压合并CSVD 患者情感淡漠危险因素及其与认知功能的相关性。
1 资料与方法
1.1 研究对象 前瞻性纳入2023 年5 月—12 月保定市第一中心医院收治的141 例高血压合并CSVD 患者,男77 例、女64 例,年龄44~86 岁、平均(65.8±9.4)岁;均符合2013 年CSVD 国际影像学标准[5],并接受神经精神问卷-淡漠量表(neuropsychiatric inventory-apathy scale,NPI-Apathy)[3]、简易精神状态检查(mini-mental state examination,MMSE)及蒙特利尔认知评估(Montreal cognitive assessment,MoCA)测评;将NPI-Apathy 评分≥4 分者纳入淡漠组(n=43)、<4 分者归为非淡漠组(n=98)。排除标准:①伴急性脑梗死、炎性脱髓鞘疾病、颅内占位及感染性脑病等颅脑异常改变;②MR 检查禁忌证;③临床及影像学资料不完整。本研究经医院伦理委员会批准[(2023)044 号],检查前患者均签署知情同意书。
1.2 仪器与方法 采用Philips Ingenia 1.5T MR 仪、头部16 通道线圈采集头颅MRI;参数:①轴位T1WI,TR 475 ms,TE 15 ms,FOV 230 mm×181 mm,层厚6 mm,层间距1 mm;②轴位T2WI,TR 2 500 ms,TE 115 ms,FOV 230 mm×230 mm,层厚6 mm,层间距1 mm;③T2-液体衰减反转恢复(fluid attenuated inversion recovery,FLAIR)序列成像,TR 9 000 ms,TE 130 ms,FOV 220 mm×183 mm,层厚6 mm,层间距1 mm;④磁敏感加权成像(susceptibility weighted imaging,SWI),TR 51 ms,TE 11 ms,FOV 230 mm×184 mm,层间距-1 mm。
1.3 评分 由2 名具有15 年及以上工作经验的影像科医师共同阅片,意见不一致时经协商决定。
1.3.1 影像学标志物 血管源性腔隙:T1WI、T2WI及T2-FLAIR 所见病灶信号均与脑脊液信号一致时计1 分[6]。脑白质高信号(white matter hyper-intensity,WMH):①侧脑室旁WMH Fazekas 评分,无病变计0分、帽状/铅笔样薄层信号计1 分、光滑“晕圈”样病变计2 分、不规则高信号延伸至深部白质计3 分;②深部WMH Fazekas 评分,无病变计0 分、斑点状病变计1分、小部分融合病变计2 分、大片融合病变计3 分[7]。血管周围间隙扩大(enlarged perivascular spaces,EPVS):以总分为4 分的半定量评分系统分别评估基底节(basal ganglia,BG)及半卵圆中心EPVS,依次将无EPVS、EPVS≤10 个、EPVS 11~20 个、EPVS 21~40 个 及EPVS>40 个计为0~4 分[8]。脑微出血(cerebral microbleed,CMB):分别评估幕下/深部CMB 及脑叶CMB,存在则计1 分[5]。见图1。
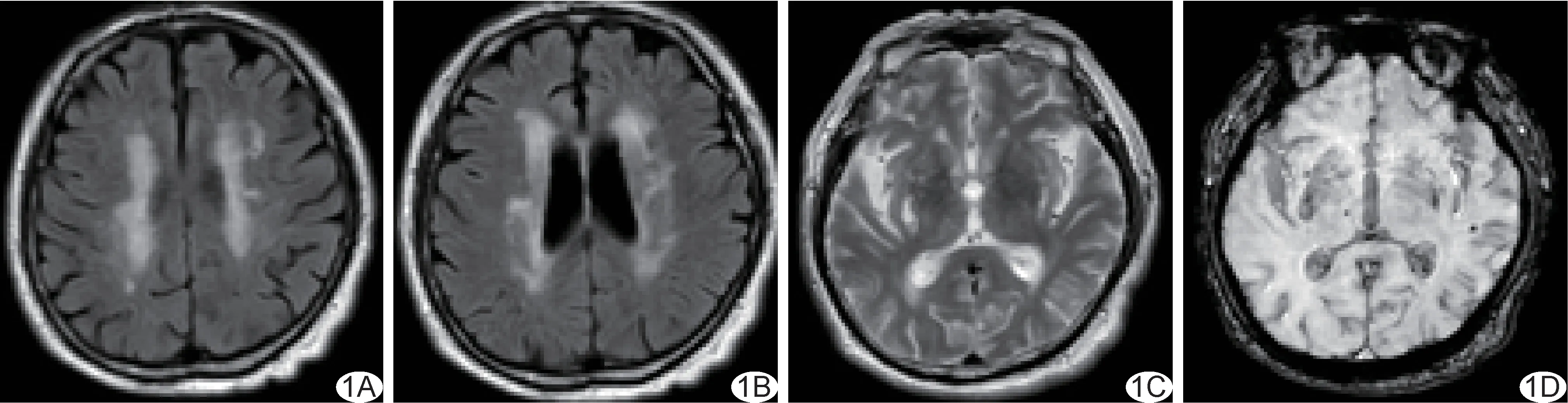
图1 患者男,80 岁,高血压合并CSVD,总负荷评分4 分 A、B.颅脑轴位MR T2-FLAIR 图示左侧放射冠区血管源性腔隙(A)、双侧侧脑室旁WMH(B);C.轴位MR T2WI 示双侧BG 多发EPVS,右侧为著;D.轴位MR SWI 示右侧BG、右侧丘脑及左侧颞叶CMB
1.3.2 总负荷评分 总负荷评分满分4 分,为以下各评分之和:血管源性腔隙≥1 个、侧脑室旁WMH Fazekas 评分为3 和/或深部WMH Fazekas 评分≥2、BG EPVS≥11 个及幕下/深部CMB≥1 个各计1 分[9]。见图1。
1.4 统计学分析 采用SPSS 26.0 统计分析软件。以表示正态分布计量资料,行t检验;以中位数(上下四分位数)表示不符合者,行Mann-WhitneyU检验。以χ2检验比较计数资料。采用多因素logistic 回归分析(向前逐步回归法)筛选高血压合并CSVD 患者情感淡漠的独立危险因素。以Spearman 相关性分析评价高血压合并CSVD 患者情感淡漠与认知功能的相关性:|r|≥0.8 为高度相关,0.5≤|r|<0.8 为中度相关,0.3≤|r|<0.5 为低度相关,0<|r|<0.3 为弱相关。P<0.05 为差异有统计学意义。
2 结果
2.1 组间比较 淡漠组患者年龄、高密度脂蛋白胆固醇(high density lipoprotein cholesterol,HDL-C)、侧脑室旁WMH Fazekas 评分、深部/幕下CMB 及总负荷评分均高于非淡漠组(P均<0.05);其MMSE 评分及MoCA 评分均低于非淡漠组(P均<0.05)。见表1。
2.2 多因素logistic 回归分析 将患者年龄、HDL-C、侧脑室旁WMH Fazekas 评分、深部/幕下CMB 及总负荷评分纳入多因素logistic 回归分析,结果显示HDL-C 及侧脑室旁WMH Fazekas 评分均为高血压合并CSVD 患者情感淡漠的独立危险因素(P均<0.05)。见表2。

表2 logistic 回归分析结果显示高血压合并CSVD 患者情感淡漠的危险因素
2.3 相关性分析 高血压合并CSVD 患者NPIApathy 评分与MMSE 评分及MoCA 评分均呈中度负相关(r=-0.543、-0.484,P均<0.001)。
3 讨论
长期高血压可致血管中膜脂质和透明质酸含量增多,管壁增厚、纤维化,进而发生血管硬化、脑血流量减少并诱发CSVD[10]。HDL-C 多被视为心血管疾病的保护因素,临床极易忽视其升高所带来的负面影响。既往研究[11-13]报道,男性抑郁症患者HDL-C 高于女性,且伴/不伴自杀意念女性抑郁症患者HDL-C 水平存在差异,考虑与HDL-C 升高使抗炎细胞因子水平降低有关。本研究发现HDL-C 为高血压合并CSVD 患者情感淡漠的独立危险因素,由于情感淡漠与抑郁表现存在重叠[3],推测淡漠组HDL-C 较高的机制与后者相似。
影像学总负荷评分对于脑小血管病颅脑MRI 特征,包括血管源性腔隙、WMH、EPVS 及CMB 具有重要临床意义[14];其中WMH 可反映颅内缺血性动脉硬化,为慢性低灌注及脑血管反应性受损引起受累组织及周围区域底层白质结构改变、而其近端白质各向异性值和N-乙酰天冬氨酸减少所致,可能与血脑屏障通透性升高、髓鞘重塑及皮层萎缩有关[10,15]。此外,本研究发现淡漠组侧脑室旁WMH Fazekas 评分、深部/幕下CMB 及总负荷评分均高于非淡漠组,且侧脑室旁WMH Fazekas 评分为高血压合并CSVD 患者情感淡漠的独立危险因素之一,与既往研究[16]相符。分析原因,WMH 相关神经网络损伤起源于低灌注脑白质并逐渐向下发展,跨神经元变性为其主要特征,而突触传递中断可致连接区域萎缩,累及情感淡漠相关脑区时表现为情感淡漠[15];或因WMH 引起白质纤维连接广泛性破坏,导致情感淡漠相关脑网络的关键节点效率下降或功能破坏而引起情感淡漠。临床应重视早期筛查、及早预防高血压合并CSVD、尤其影像学已存在WMH 特征患者发生情感淡漠。
情感淡漠可严重影响患者生活质量,其严重程度与认知功能下降、尤其执行功能障碍有关。本研究结果显示,高血压合并CSVD 患者NPI-Apathy 评分与反映认知功能的MMSE 及MoCA 评分均呈中度负相关,支持YEAGER 等[17]的观点。
综上所述,HDL-C 及侧脑室旁WMH Fazekas 评分均为高血压合并CSVD 患者情感淡漠的独立危险因素;情感淡漠越严重,则认知功能越差。但本研究为单中心分析,样本量有限,且NPI-Apathy 属于他评量表,可能因患者欲保护自身隐私而影响最终评分结果,有待后续扩大样本深入研究。
利益冲突:全体作者声明无利益冲突。
作者贡献:曹佳丽研究实施、数据分析、统计分析、撰写文章;王天然查阅文献;刘洋和徐金娥图像分析;张舵和王淑梅修改文章;刘冲指导、研究设计;韩永昌和杨露露研究实施。

