超声造影评估高强度聚焦超声联合化疗治疗结肠癌肝转移短期疗效的价值①
于红霞,吴海英
(洛阳市第六人民医院超声科,河南 洛阳 471003)
结肠癌是临床较为常见的消化系统恶性肿瘤类型,近年来,其患病率在全球范围内逐年上升[1]。结肠癌患者可能存在恶性进展,而最易发生转移的器官为肝脏[2],研究显示,肝转移在结肠癌患者中的发生率为50%,大部分患者预后差,病死率高[3]。此类患者无法进行根治性手术治疗,因此临床多采取高强度聚焦超声配合化疗治疗[4]。其中高强度聚焦超声是一种热源性消融治疗手段,其能精准消融肿瘤,且对周围组织破坏性小,且治疗过程中创伤小,因此被临床适用[5]。但因对部分存在远处转移的患者,可能存在消融不充分的现象,导致局部病灶复发,因此需在治疗后及时评估其消融疗效,以便调整治疗方式,提高治疗效果[6]。临床常通过肿瘤径线变化来评估疗效,但部分肝转移灶过小,影像学可能漏诊,导致癌细胞残留,肿瘤复发。而超声造影能将肿瘤内微循环血流灌注变化实时反映,有助于判定癌细胞恶性生物学行为,评估消融疗效[7]。本研究对超声造影评估高强度聚焦超声联合化疗治疗结肠癌肝转移短期疗效的价值进行探讨,观察其效果,现报道如下。
1 资料与方法
1.1 一般资料
选取2019年1月至2022年12月在洛阳市第六人民医院进行治疗的结肠癌肝转移患者79例,其中男42例,女37例;年龄39~78岁,平均(58.42±6.83)岁;原发部位:结肠肝曲28例,乙状结肠43例,横结肠8例。本研究经医院伦理委员会批准。(1)纳入标准:①符合结肠癌[8]的诊断标准,常规超声见肝转移征象;②所有患者均接受高强度聚焦超声及化疗治疗;③耐受超声造影检查的患者;④所有患者同意本次研究内容并签署知情同意书。(2)排除标准:①存在高强度聚焦超声及化疗治疗禁忌证者;②合并心、肺、肾等重大脏器病变者;③恶性肿瘤者;④伴随其他器官发生转移者;⑤合并精神、认知障碍;⑥对研究所用造影剂过敏者。
1.2 检查方法
对所有患者进行高强度聚焦超声联合化疗治疗,并在治疗前后进行超声造影检查。(1)高强度聚焦超声治疗方法:患者治疗前3d为清淡、少渣饮食,避免摄入豆类及粗纤维食物;治疗前2d为流食;治疗前1d为无渣饮食。术前1d午后禁食,于当日下午5点予以患者导泻药口服,后于晚9点为患者进行2次清洁灌肠。治疗当日早禁食,并于7点进行1次清洁灌肠,直至肠道清洁度合格为止。达到合格的肠道清洁度后,采取全身麻醉,采用聚焦超声治疗系统(型号JC200,上海聚慕医疗器械有限公司),在超声监测下确定病灶位置,然后行高强度聚焦超声治疗,设定频率为0.85MHz,功率为200~240W,采用单点治疗,超声能量发射时间0.12~0.15s,间隔时间0.26~0.3s,每个位置8~10次,声强80%~100%。(2)化疗治疗方法:予以患者奥沙利铂(江苏奥赛康药业有限公司,国药准字H20064296,规格:50mg/盒)85mg/m2或伊力替康(哈药集团生物工程有限公司,国药准字H20153210,规格:2mL:40mg)240mg/m2静脉注射,而后予以患者5-氟尿嘧啶(上海旭东海普药业有限公司,国药准字H31020593,规格:10mL:0.25g)400mg/静脉注射,期间予以患者亚叶酸钙(开封康诺药业有限公司,国药准字H41021710,规格:0.1g/10支)400mg/m2静脉注射,使用静脉化疗泵持续48h注入5-氟尿嘧啶2500mg/m2。化疗周期为3周,共治疗6个周期。(3)超声造影检查方法:在治疗前及治疗后1~7d内对患者进行超声造影检查,采用飞利浦Affiniti70彩色超声诊断系统,配合PureWave探头。检查前对患者采取12h禁食,检查时取仰卧位,对其肝脏整体进行扫描,观察肝脏内病灶的数量、位置、尺寸、形态等,并记录病灶内的血流情况,并确定感兴趣区:①病灶直径在1.5cm或以上,距患者体表4~10cm;②可连续观察病灶增强过程;③心肺对病灶显像干扰性不明显;④排除肝脏内大片无回声或回声较强且乱的病灶。确定病灶感兴趣区后,调整为超声造影模式对其进行检查,使用GE医疗公司的示卓安(Sonazoid)超声造影剂,使用5mL生理盐水与其配成5mg/mL的六氟化硫微泡悬浮液,使用2.4mL混悬液经患者上肢静脉注入,并注入5mL生理盐水进行冲洗。动态观察患者肝脏病灶在动脉期(0~40s)、门静脉期(40~120s)、延迟期(120s以上)的增强表现,并保存动态图像视频。记录信号强度的最高值,为峰值强度(PI);记录信号开始增强至达到PI的时间,为达峰时间(TTP);记录PI达到一半时对应的时间段,为平均渡越时间(MTT);记录曲线下面积(AUC)。
1.3 疗效判定标准
根据居伟等[9]制定的疗效标准对患者治疗后的效果进行判定,该标准分为完全缓解、部分缓解、疾病恶化、疾病稳定。完全缓解:肿瘤均被灭活;部分缓解:肿瘤直径减少30%以上;疾病恶化:肿瘤直径增加20%以上;疾病稳定:肿瘤直径较治疗前相比增加未达到20%,减少未达到30%,并以完全缓解、部分缓解及疾病稳定为有效组,疾病恶化为无效组。
1.4 统计学方法
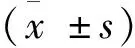
2 结果
2.1 疗效
治疗后,完全缓解患者8例(10.13%),部分缓解患者12例(15.19%),疾病恶化患者52例(65.82%),疾病稳定患者7例(8.86%)。无效组为52例(65.82%),有效组为27例(34.18%)。
2.2 有效组、无效组超声造影量化参数比较
治疗后,超声造影检查显示27例患者病灶内无血流信号或信号无增强现象,52例患者病灶内存在血流信号或信号有增强现象。治疗前,有效组、无效组患者PI、TTP、MTT、AUC对比无差异(P>0.05);治疗后,有效组患者PI、MTT较无效组低(P<0.05),有效组患者AUC、TTP较无效组高(P<0.05),见表1。

表1 两组患者超声造影量化参数比较
2.3 ROC曲线分析超声造影参数预测患者疗效的价值
当PI的截断值>77.59 dB时,其Youden指数为0.662,曲线下面积(AUC)为0.799,预测患者疗效敏感度为88.46%,特异度为77.78%;当TTP的截断值<12.76s时,其Youden指数为0.480,AUC为0.715,预测患者疗效敏感度为96.15%,特异度为51.85%;当MTT的截断值>94.44s时,其Youden指数为0.719,AUC为0.765,预测患者疗效敏感度为90.38%,特异度为81.48%;当AUC的截断值<453.29 dB·s时,其Youden指数为0.384,AUC为0.644,预测患者疗效敏感度为86.54%,特异度为51.85%,见图1、表2。
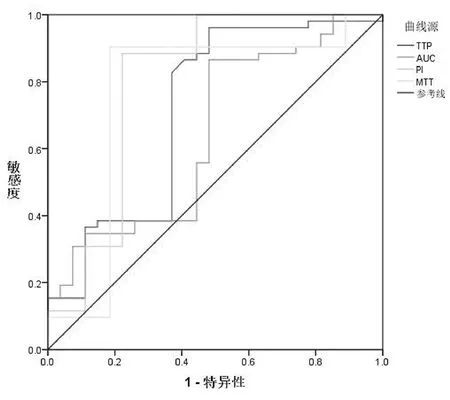
图1 超声造影参数预测患者疗效的ROC曲线
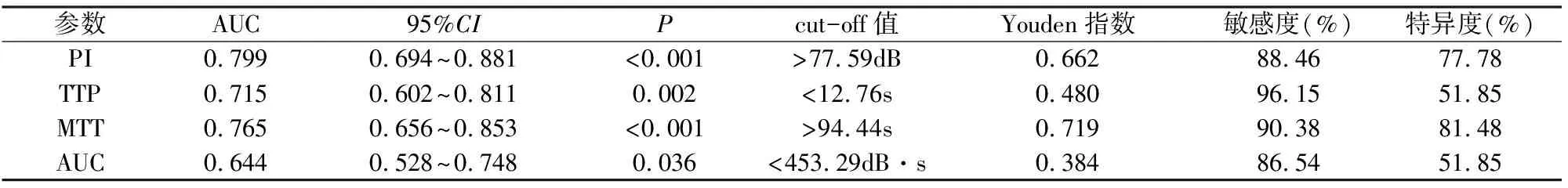
表2 超声造影参数预测患者疗效的ROC曲线
3 讨论
高强度聚焦超声通过聚集超声能量,在肝脏部位引发热效应,产生高温,使病灶处的组织凝固性坏死,达到消融肿瘤的目的,且在治疗过程中对肝脏周围组织不具有破坏性,具有无射线的特点,可有效减少周围组织受损,在治疗腹部肿瘤中有明确的效果。但结肠癌肝转移患者的病灶位置隐匿或病灶直径较小,可能定位不准,或部分深部病灶聚焦超声治疗能量减弱,导致消融不充分,且该类患者呼吸运动时可能对病灶部位有所改变,导致病灶残留,增加其复发风险。故尽早判断其疗效有助于指导临床诊疗方式的开展,以改善患者预后。
本研究超声造影结果显示,治疗后,有效组患者PI、MTT较无效组低(P<0.05),有效组患者AUC、TTP较无效组高(P<0.05),这说明经高强度聚焦超声配合化疗治疗结肠癌伴肝转移患者后,有效组患者其肿瘤内部微循环血流灌注发生改变,且血流信号减弱或消失,而无效患者上述微循环血流灌注依然维持活跃,血流信号较强。分析原因为高强度聚焦超声为一种高温治疗方式,其通过聚焦产生高温,对肿瘤产生消融作用,并减少肿瘤内部血流灌注,以达到肿瘤坏死的目的,提高治疗效果。但无效的患者肿瘤细胞增殖活跃,呈掠夺性生长,并生成新的肿瘤血管,导致肝脏内血流灌注高,促进血流信号的增强,从而使无效组PI、MTT提高。
本研究发现,超声造影可有效预测高强度聚焦超声配合化疗治疗结肠癌肝转移患者的疗效,其中以PI预测效能最高。考虑是超声造影作为一种实时检查方式,其能观察超声对比剂进入病灶内至消退的全部过程,准确显示患者肝脏内部血流信号变化,判断出残留的肿瘤组织,且有助于医生观测患者肿瘤内部微循环血流灌注状态,为后续开展治疗提供指导。而PI预测短期疗效效能最高,考虑是无效患者治疗后癌细胞保持活跃状态,造成肝脏内血流信号的增强,且超声显示高血流灌注状态,促进肿瘤持续进展;而PI为反映血流信号的重要参数,与癌灶微血管密度密切相关,便于指导患者新生肿瘤血管生成评估,预测效能更高。
综上所述,对于高强度聚焦超声配合化疗治疗结肠癌肝转移,超声造影技术可较为准确的显示肿瘤内血流灌注情况及信号强度,为后续治疗提供有效指导,为提高治疗效果奠定基础,是一种值得推广的检查方式。但本研究选取病例较少,得出的结论暂未得到大量数据证实,有待后续扩充样本量进行深入探讨。

