猫冠状病毒荧光定量PCR检测方法的建立
陈秋阳,梁瑞英,梁 琳,汤新明,秦 彤,丁家波
(中国农业科学院北京畜牧兽医研究所,北京 100193)
猫冠状病毒(Feline coronavirus,FCoV)是猫群中最常见感染的病原体之一。FCoVs根据生物类型分为猫肠道冠状病毒(FECV)和猫传染性腹膜炎病毒(FIPV),FECV感染引起轻度或亚临床消化道症状,持续排毒,导致猫群血清阳性率升高。FECV经基因突变演化为猫传染性腹膜炎病毒(FIPV),引起免疫介导的致命性猫传染性腹膜炎(FIP)[1-2]。猫传染性腹膜炎的临床症状多样,包括湿性腹膜炎,表现为胸膜腔或腹腔渗出性纤维蛋白浆膜炎;干性腹膜炎,在多个器官中出现弥散性血管周围脓肿,使得临床诊断变得困难。FCoV是一种有囊膜的单股正链 RNA病毒,基因组全长约30 kb,含有11个已确定的开放阅读框(ORF),与犬冠状病毒(CCoV)和猪传染性胃肠炎病毒(TEGV)同属于尼多病毒目、冠状病毒科、冠状病毒亚科、α-冠状病毒属的成员[3]。FCoV分为2种抗原性不同的血清型,Ⅰ型FCoV难以在细胞培养物中生长,Ⅱ型FCoV是Ⅰ型FCoV和CCoV重组的结果。2种FCoV血清型均可引起FIP,但血清学研究和最近的分子学研究证实,Ⅰ型FCoV迄今为止在全球猫种群中占主导地位[4]。
目前没有可以快速、准确地检测FCoV的方法,在幼龄猫发病的初期,出现轻微的腹泻症状是唯一的表征。在临床上,由于FIPV引起的症状和病理变化多样,无法通过临床症状和病理变化快速准确地诊断[5]。目前FIP的诊断一般采用临床诊断和实验室诊断相结合的方法做出综合判断[6],需要多种检测方法的联合[7]。传统上猫传染性腹膜炎诊断主要依赖组织病理学检查和免疫组化检测,目前腹腔积液检测和病原基因检测是FCoV检测的常用方法。常见的诊断流程需要综合考虑猫的品种、生活史、病史、体格检查、临床症状、影像学检查、血常规检查、间接免疫荧光试验(IFA)、酶联免疫吸附试验(ELISA)、免疫组化、RT-PCR检测以及组织病理学检查。但是,ELISA相较于TaqMan荧光定量PCR方法具有灵敏度较低、成本高等缺点[8];普通 RT-PCR 具有检测时间长、灵敏度相对较低的缺点;IFA、免疫组化及电镜等检测技术,对于仪器及人员的要求较高,且无法满足大批量的临床诊断[9]。相较于以上几种方法,荧光定量PCR不仅具有操作简便、成本低的优点,而且检测时间短,可适用于基层的临床检测。针对病毒棘突基因(S)和非翻译区基因(UTR)的逆转录聚合酶链式检测方法(RT-PCR)已有报道,而核衣壳蛋白(N)基因保守,且在感染细胞中的含量较高,因此是较好的检测基因。
FCoV是猫重要的致病性病原,临床诊断难度大。灵敏可靠的检测方法对该病的防控具有重要意义。本试验建立检测FCoV的TaqMan荧光定量PCR检测方法,为该病毒的检测提供特异、快速、准确的技术手段。
1 材料与方法
1.1 材料
1.1.1 病毒与病料 猫冠状病毒、猫细小病毒(FPV)、猫杯状病毒(FCV)、猫疱疹病毒(FHV)均由中国农业科学院北京畜牧兽医研究所动物生物安全与公共卫生防控科技创新团队保存;75份样本来源于全国多地宠物医院,所有样本于-80℃条件下保存。
1.1.2 主要试剂 FastPure®Viral DNA/RNA Mini Kit为诺唯赞产品,南京诺唯赞生物科技股份有限公司产品;Prime Star Max DNA Polymerase,TaKaRa公司产品;通用型DNA胶回收试剂盒、柱式质粒小量抽提试剂盒, OMEGA公司产品;反转录试剂盒,TIANGEN公司产品;EZ-Blunt Zero pTOPO II Cloning Kit、2×Real Star Fast Probe Mix,北京康润诚业生物科技有限公司产品;DH5α感受态细胞和琼脂糖,北京擎科生物科技有限公司产品;RNase-Free ddH2O ,北京索莱宝科技有限公司产品;Magpure病毒DNA/RNA纯化试剂盒(预分装板),杭州比格飞序生物科技有限公司产品。
1.1.3 主要仪器 凝胶成像系统,Tanon公司产品;-20℃冰箱,海尔股份有限公司产品;电泳仪、PCR仪,Bio-Rad公司产品;旋涡震荡仪,海门市麒麟医用仪器厂生产;细菌培养箱,上海一恒生物科技有限公司产品;超微量紫外可见分光光度计,Life Real公司产品;细菌超净工作台,北京亚泰科隆实验科技开发中心产品;4℃离心机、液氮罐、二氧化碳培养箱、小型台式离心机,生物安全柜、-80℃冰箱,Thermo公司产品;荧光定量PCR仪,西安天隆科技有限公司产品;全自动核酸提取纯化仪,杭州比格飞序生物科技有限公司产品。
1.2 方法
1.2.1 引物和探针的设计与合成 用SNAPGENE软件对NCBI上FCoV的N基因序列进行比对,选择保守区域设计引物及探针,由华大基因科技有限公司合成(表1)。
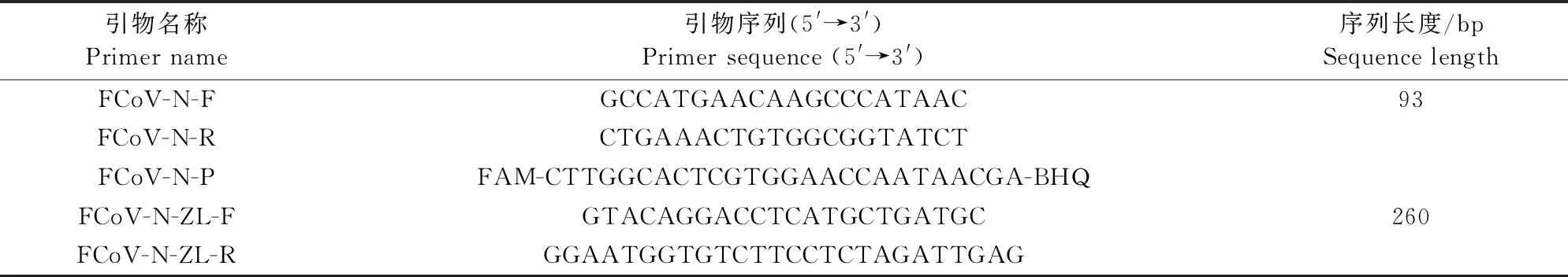
表1 Taqman荧光定量PCR引物及探针序列
1.2.2 质粒标准品的构建 按照诺唯赞FastPure®Viral DNA/RNA Mini Kit说明书提取病毒总RNA,参考TIANGEN反转录试剂盒说明书获取病毒的cDNA,20 μL反转录反应体系及程序如下:4 μL 5×FastKing-RT Super Mix,16 μL RNA;反转录程序:42℃ 15 min,95℃ 3 min。cDNA 置于-20℃保存备用。
以反转录产物cDNA为模板,用FCoV-N-ZL-F和FCoV-N-ZL-R引物进行扩增,扩增片段长260 bp。扩增产物经胶回收后连接至EZ-Blunt Zero pTOPO Ⅱ Cloning Kit载体,然后转化至DH5α感受态细胞,37℃培养12~16 h。挑取多个单菌落分别接入LB液体培养基37℃振荡培养6~8 h。通过菌液PCR筛选含有阳性重组质粒的细菌并进行测序,选择含有FCoV目的片段基因的菌落进行扩增,使用柱式质粒小量抽提试剂盒提取的质粒即为标准品。用分光光度计测定质粒浓度,计算其拷贝数,进行10倍梯度稀释,置-20℃保存备用。
计算公式:拷贝数=6.02×1023(copies/mol)×[标准品浓度(ng/μL)×10-9]/标准品长度(bp)×660(Dalton/bp)。
1.2.3 荧光定量PCR检测方法的建立
1.2.3.1 反应条件的优化 根据 2×Real Star Fast Probe Mix试剂说明书推荐的20 μL反应体系,分别对上、下游引物浓度(0.2~1.0 mol/L)、探针浓度(0.2~1.0 mol/L)、退火-延伸温度(58~62℃) 进行优化,设置阴性对照组,通过比较Ct值、荧光强度和扩增效率来选定优化结果。
1.2.3.2 标准曲线的绘制 以100~10-9倍梯度稀释的阳性质粒为模板,进行荧光定量PCR扩增,以标准品拷贝数的对数为X轴,Ct值为Y轴,绘制标准曲线。
1.2.3.3 特异性试验 利用已经建立的FCoV荧光定量PCR方法对实验室保存的FCV、FPV、FHV的核酸进行检测,同时设置阳性对照和阴性对照,验证该方法的特异性。
1.2.3.4 敏感性试验 将标准品质粒进行10倍梯度连续稀释作为模板,分别使用建立的荧光定量PCR方法和普通PCR方法进行扩增,比较二者的拷贝数检测下限。
1.2.3.5 重复性试验 取同一批次的3个稀释度的标准质粒为模板进行实时荧光定量PCR扩增,并设置阴性对照组,每组设置3个平行进行重复性试验,计算平均值,计算组内变异系数;以同样的反应条件再分别进行3次组间重复性试验,计算平均值,计算组间变异系数。根据变异系数判定该方法的组内及组间差异。
1.2.3.6 临床样品的检测 使用全自动核酸提取纯化仪提取75份临床样品核酸,应用已建立的FCoV荧光定量PCR方法和已发表的RT-PCR检测方法进行比对。
2 结果
2.1 质粒标准品的构建
以FCoV cDNA为模板,用FCoV-N-ZL-F和FCoV-N-ZL-R引物进行PCR扩增,得到与预期大小相符的片段(图1)。将胶回收产物连接至EZ-Blunt Zero pTOPO Ⅱ Cloning Kit,转化至DH5α感受态细胞筛选出阳性重组质粒菌落送测序鉴定。选择正确菌落扩增,用柱式质粒小量抽提试剂盒提取的质粒即为标准品。用分光光度仪测定重组质粒标准品浓度,通过计算得到拷贝数1.49×1011copies/μL,作为荧光定量PCR方法构建的质粒标准品。
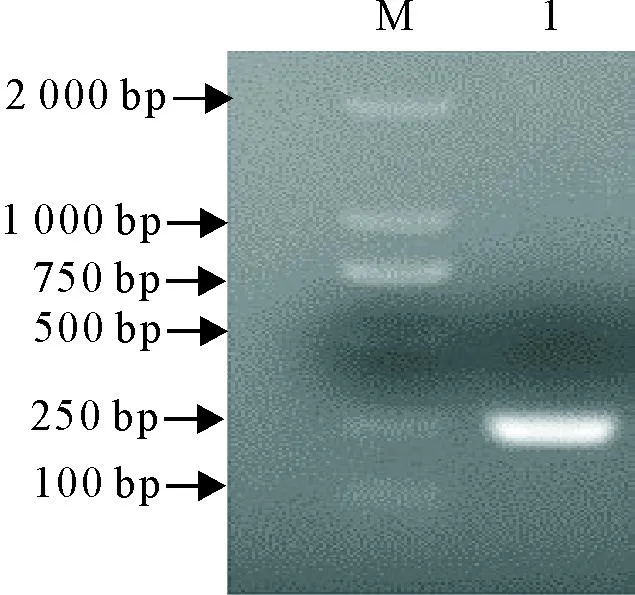
M.DNA标准DL 2 000;1.目的片段
2.2 实时荧光定量PCR反应条件的优化
通过对引物、探针浓度和退火温度的优化,以Ct值小、荧光值高为参考标准,结果表明该荧光定量PCR的最佳上、下游引物浓度为400 nmol/L,最佳探针浓度为200 nmol/L,最佳退火、延伸温度为60℃。20 μL的荧光定量PCR反应体系中含有10 μL 2×RealStar Fast Probe Mix、0.8 μL 上游引物 FCoV-N-F、0.8 μL下游引物 FCoV-N-R、0.4 μL探针 FCoV-N-P、0.4 μL cDNA、7.6 μL RNase free H2O。反应程序:95℃ 2 min;95℃ 15 s,60℃ 30 s,共40个循环。
2.3 标准曲线的建立
用优化得到的方法,以10倍稀释得到的浓度1.49×1011~1.49×102copies/μL的标准质粒作为模板进行荧光定量PCR扩增,绘制标准曲线(图2)。线性回归方程为:y=-3.137 4x+41.47,R2=0.998 1,扩增效率为108.3%,线性关系好。

图2 FCoV的荧光定量PCR测定的标准曲线
2.4 特异性试验
以FCV、FPV、FHV的基因组为模板,以FCoV质粒标准品为阳性对照,ddH2O为阴性对照,用优化得到的方法验证其特异性。只有FCoV有特异性扩增,其他病原及阴性对照均无扩增曲线,表明该方法特异性好(图3)。

1.FCoV; 2~5.FPV,FCV,FHV,RNase-free H2O作为阴性对照。
2.5 敏感性试验
将标准质粒进行10倍梯度连续稀释后作为模板,分别用建立的FCoV荧光定量PCR方法和普通PCR方法进行扩增。建立的荧光定量PCR方法的最低检测极限约为1.49×100copies/μL,常规 PCR方法的最低检测极限约为1.49×105copies/μL(图4和图5)。

1~12.1.49×1011~1.49×100copies/μL,13.RNase-free H2O作为阴性对照

1~12.1.49×1011~1.49×100copies/μL,13.RNase-free H2O作为阴性对照
2.6 重复性试验
取同一批次的1.49×107、1.49×106、1.49×105copies/μL 3个拷贝数的标准质粒为模板,3个稀释度分别设立3个重复孔进行组内重复性试验;同样的反应条件分别进行3次组间重复性试验。结果组内和组间试验Ct值的变异系数均小于3.0%,表明该方法重复性和稳定性良好(表2)。

表2 荧光定量PCR重复性试验
2.7 临床样品检测
用本试验优化后的反应体系及程序对75份临床样品进行检测,同时进行RT-PCR检测,分别设置阳性对照和阴性对照。普通RT-PCR方法只检出1份阳性病料,阳性率为1.33%,而本试验建立的荧光定量PCR方法则检出28份阳性病料,阳性率为37.33%,说明本试验建立的荧光定量PCR方法比普通RT-PCR方法敏感性更强(表3)。

表3 荧光定量PCR和RT-PCR临床样本检测结果
3 讨论
FCoV在世界各地猫群中流行。FECV传染性强,通过粪、口传播,感染大多无症状或仅引起轻度、一过性腹泻[10]。猫传染性腹膜炎病毒(FIPV)无法通过粪-口途径传播,但在一小部分感染猫中,FIPV由无毒力的FECV突变产生,然后引起致死性的FIP。近年来,FIP患病率逐年增加,病死率几乎为100%[11],目前正在继续努力寻找FIP的适当治疗方法,现在比较常见的方法是用抗病毒药物进行抑制[12],但是达到有效抑制剂量的药物可能会有严重的毒副作用[13]。而由于FCoV会产生抗体依赖增强作用(ADE),一直以来对于FCoV疫苗的研发始终不顺利。因此,有必要开发一种可以快速、准确地检测FCoV的方法,以尽早检出FCoV感染,并及时治疗。
病毒分离培养法是实验室检测病原的金标准,该方法可以为后期病原特性研究提供重要材料并奠定试验基础,目前常用猫肾细胞(CRFK)或猫巨噬细胞(Fcwf-4)培养FCoV。在分离临床样本中FCoV时,第1代或者盲传数代后,可观察到细胞皱缩、变圆、脱落等细胞病变效应(CPE),但初期CPE不明显、自然毒株对细胞系不适应、临床样本混合感染都会造成病毒的分离培养失败,而且该方法花费时间较久,往往需要1~2周才可完成。而通过电镜观察,可直接观察到表面有冠冕状突起的病毒粒子,但是做电镜要求样本有较多的病毒粒子,该方法虽然直观但敏感性不高,通常临床病料中病毒粒子数量达不到电镜观察的要求。酶联免疫吸附试验(ELISA)是常用的血清学诊断方法之一,有研究建立了用组氨酸标记的重组刺突蛋白检测FCoV抗体的间接ELISA方法[8],但ELISA方法存在重复性不好,受自身抗体、嗜异性抗体等干扰易出现假阳性,干扰因素较多等问题。反转录-聚合酶链反应(RT-PCR)也常被用于FCoV诊断和流行病学调查[9],很早就被用来检测猫粪便、组织中的FCoV 。不过RT-PCR比起荧光定量PCR方法敏感性较差。染料法荧光定量PCR方法可以较为高效的诊断FCoV[14-15],但比起探针法荧光定量PCR特异性较差,有人在开发FCoV荧光定量PCR方法并尝试应用于临床[16]。快速抗原免疫层析检测使用方便、快速,但是准确性较差[17]。一些新的检测方法如重组酶聚合酶扩增荧光方法(RT-RPA)[18]和重组酶介导等温核酸扩增(RT-RAA)[19]用于检测FCoV。
为了进一步提高FCoV检测灵敏度和诊断准确率,本研究选取FCoV N基因保守区片段进行引物与探针设计,在保证特异性的同时优化反应条件,构建重组质粒,建立了一种快速、灵敏、准确的TaqMan荧光定量PCR检测方法。该检测方法可用于检测FCoV,根据基因序列比对,本研究选择的FCoV序列与犬冠状病毒(CCoV) 、猪传染性胃肠炎病毒(TGEV)和猪流行性腹泻病毒(PEDV)等冠状病毒序列具有高度一致性,也可用于这些冠状病毒的检测。
本研究建立的方法可对微量病毒进行检测,对质粒DNA标准品的最低检测下限为1.49×100copies/μL。通过特异性试验,对猫常见病毒进行检测,证明了该方法具备很强的特异性。本试验通过重复性试验和批内重复性试验得到的变异系数均小于3.0%,显示了该方法具有较好的重复性。
本试验基于FCoV N基因保守区域成功建立了FCoV的TaqMan荧光定量PCR方法,为FCoV的早期检测和流行病学调查提供了有效的技术支撑,可实现在临床中对FCoV的全面筛查。

