瞬时弹性成像技术诊断自身免疫性肝炎的价值研究
陈津津,朱宏英,秦 菲
(江南大学附属无锡五院〈无锡市第五人民医院〉超声科 江苏 无锡 214001)
自身免疫性肝炎(autoimmune hepatitis,AIH)是由免疫系统攻击肝细胞导致的肝脏疾病,肝穿刺病理检查是诊断AIH 的金标准[1],但由于肝脏穿刺属于有创检查,可重复性差,不能在临床广泛开展。瞬时弹性成像技术(transient elastography,TE)是一门超声弹性影像学技术,操作简单且无创,该技术利用剪切波传播原理计算肝脏硬度,结果以肝硬度值(liver stiffness measurement,LSM)表示,单位kPa,以此定量评估肝脏的纤维化状态[2]。本研究通过对AIH 和乙肝患者的肝脏硬度测定,观察其在不同病理分期中的特点,并比较自AIH 和乙肝的肝脏硬度差异,从而研究TE 诊断AIH 的应用价值。
1 资料与方法
1.1 一般资料
回顾性收集2020 年11 月—2021 年12 月在江南大学附属无锡五院就诊的乙肝患者50 例及AIH 患者40 例。乙肝患者中男15 例,女35 例,年龄32~73 岁,平均年龄(53.24±10.76)岁;AIH 患者中男11 例,女29 例,年龄35~76 岁,平均年龄(54.95±9.56)岁。两组患者性别比例和年龄差异无统计学意义(P>0.05),有可比性。
纳入标准:(1)乙型肝炎:①符合《慢性乙型肝炎防治指南(2019 年版)》诊断标准患者[3];②肝功能异常患者;③HbsAg 阳性>6 个月,非急性起病患者[3]。(2)AIH:①符合《自身免疫性肝炎诊断和治疗共识(2015)》[4]诊断标准患者;②肝功能异常患者;③出现嗜睡、乏力、全身不适的患者;④非急性起病,病程>30 d[4]。排除标准:(1)酒精肝、脂肪肝、药物性肝病患者;(2)肝脏占位性病变患者;(3)胆红素异常患者;(4)腹水患者。
1.2 方法
1.2.1 肝脏硬度测定 使用FibroTouch 无创肝纤维化诊断系统进行检查,探头频率(1.0~6.0)MHz,患者取仰卧位,操作者将探头沿腋中线第9~11 肋间隙测量并采集图片,反复测量10 次,取中位数为最终值[5-6]。
1.2.2 病理检查 在超声引导下对入选患者进行肝穿刺,取两条肝脏组织送病理科。根据我国肝炎评分系统,将肝纤维化程度分为S0~S4 期[7],S0 为无肝纤维化,Sl~S2 为轻中度肝纤维化,S3~S4 为重度肝纤维化。
1.3 观察指标
(1)观察乙肝和AIH 的病理结果;(2)分析乙肝和AIH 患者的LSM,观察LSM 与病理分期的相关性;(3)对比相同病理肝纤维化分期中,乙肝和AIH 的LSM 差异。
1.4 统计学方法
应用GraphPad Prism 9 统计软件进行数据分析,符合正态分布的计量资料以均数±标准差(± s)表示,采用t检验,多组比较采用方差分析(ANOVA),并采用LSD 进行事后多重比较,非正态分布相关性分析采用Spearman 线性相关,P<0.05 表示差异有统计学意义。绘制受试者工作特征(ROC)曲线,计算曲线下面积(AUC),根据约登指数获得肝硬度值临界值。
2 结果
2.1 病理结果
病理结果显示,肝炎患者肝小叶汇管区周边呈炎症反应,肝硬化有“假小叶”形成,AIH 有“玫瑰花环”样改变,见图1。
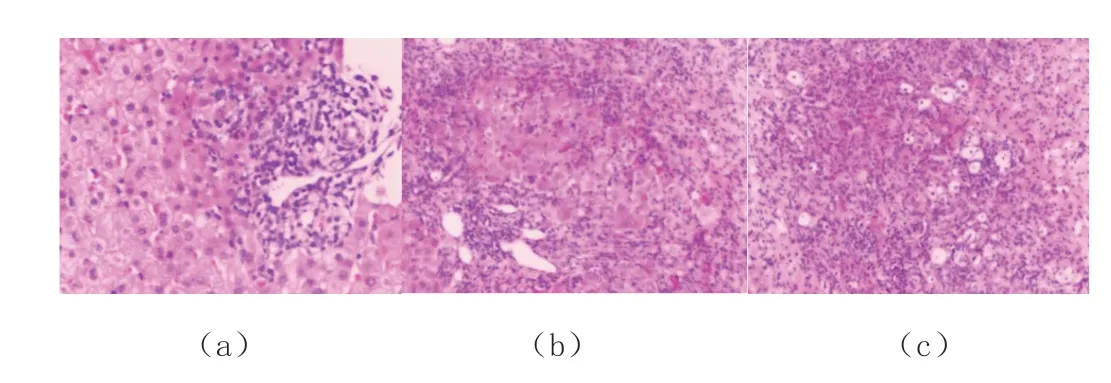
图1 病理结果图
2.2 超声肝脏硬度值与病理肝纤维化分期的分布比较
根据病理肝纤维化程度分期,分别将乙肝和AIH 患者分组,结果显示,无论乙肝还是AIH,肝纤维化程度越重,LSM 越大,差异有统计学意义(P<0.05),见表1~表3,表明肝纤维化程度和LSM 呈正相关,见图2、图3。
表1 乙肝和AIH 在不同病理分期中的肝硬度值分布情况(± s,kPa)
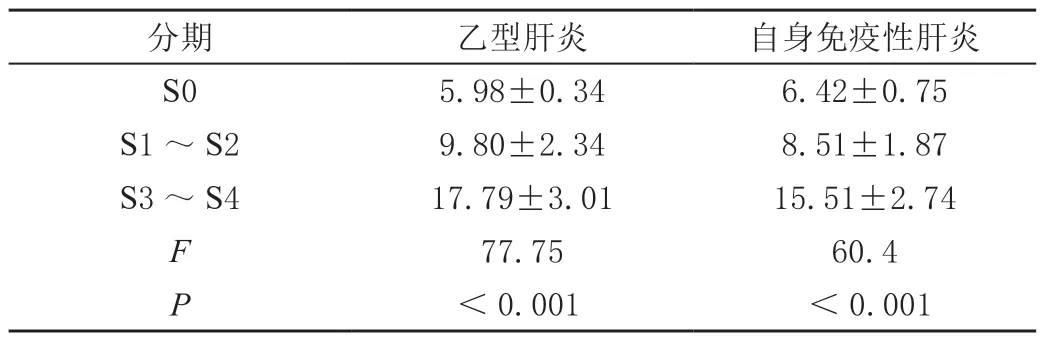
表1 乙肝和AIH 在不同病理分期中的肝硬度值分布情况(± s,kPa)
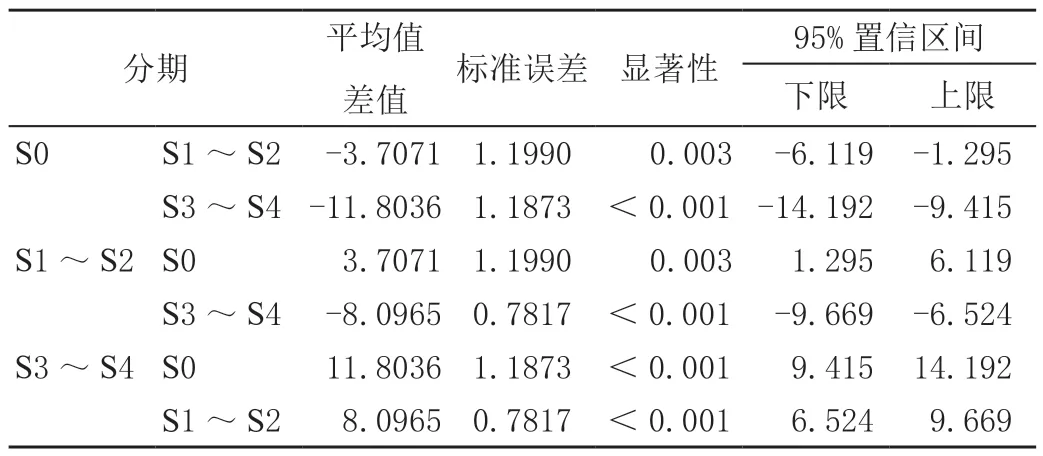
表2 乙肝肝硬度值组间多重比较
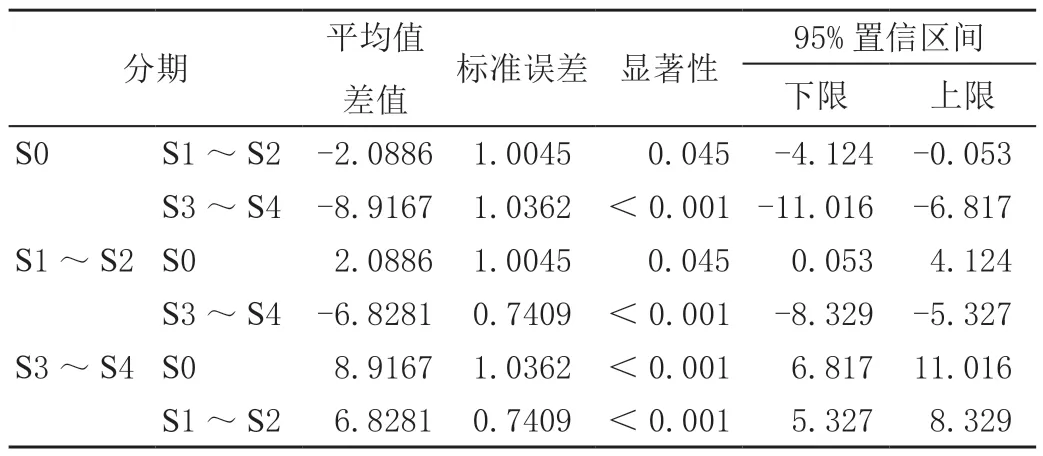
表3 AIH 肝硬度值组间多重比较
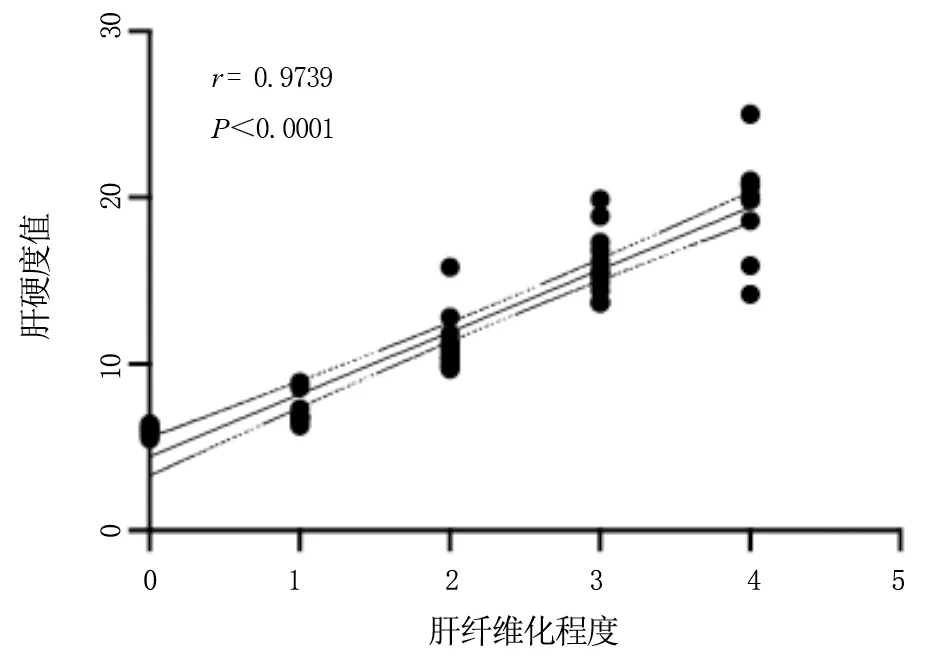
图2 乙肝肝纤维化程度和肝硬度值的相关性
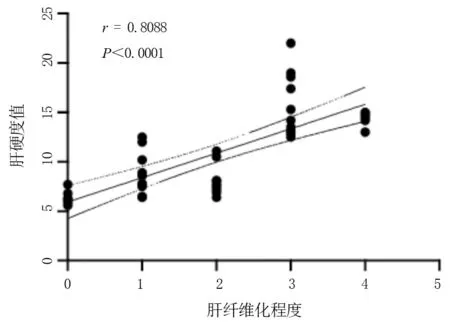
图3 AIH 肝纤维化程度和肝硬度值的相关性
2.3 相同病理肝纤维化分期中,乙肝和AIH 的LSM差异
分别将乙肝和AIH 患者的LSM 根据病理纤维化分期分组,结果显示肝脏无纤维化(S0)和肝脏轻中度纤维化(S1~S2)时,乙肝和AIH 的LSM 差异无统计学意义(P>0.05),病理分期提示重度纤维化(S3~S4)时,乙肝和AIH 的LSM 差异有统计学意义(P<0.05),见表4。
表4 相同病理分期乙肝和AIH 的肝硬度值对比(± s,kPa)
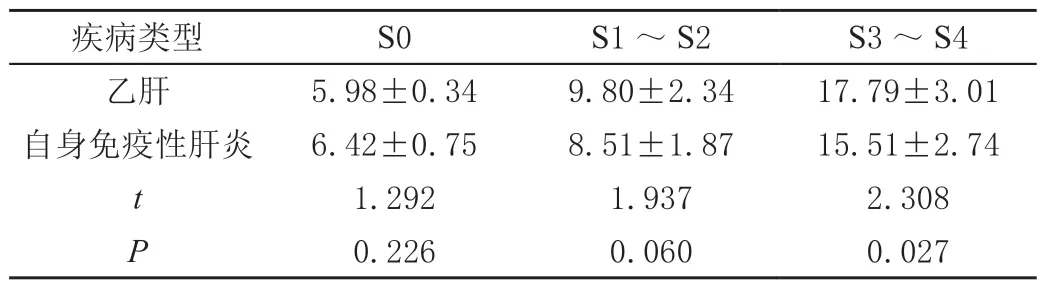
表4 相同病理分期乙肝和AIH 的肝硬度值对比(± s,kPa)
表4 结果显示,重度肝纤维化(S3~S4)时,乙肝和AIH 的LSM 对比差异有统计学意义(P=0.027),根据此结果,将重度肝纤维化期乙肝和AIH 的LSM 整理分析,并绘制ROC 曲线,AUC 为0.739,P=0.016,计算约登指数为0.453,得到LSM 的临界值为15.35 kPa,相对应的灵敏度和特异度分别为71.4%和73.9%,见图4。
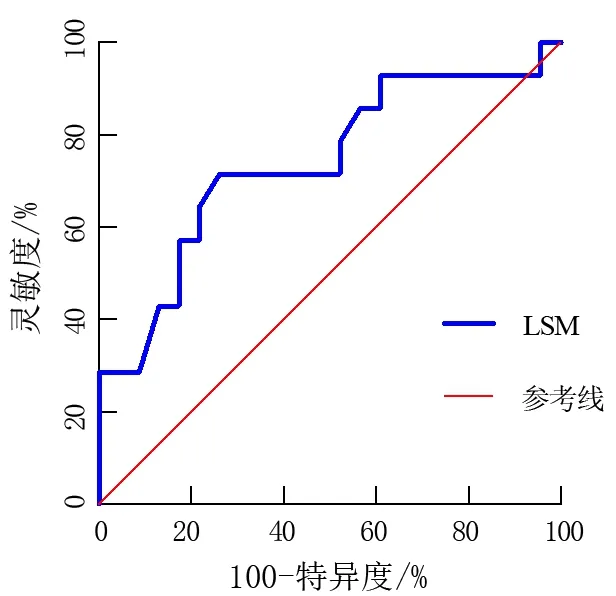
图4 重度肝纤维化期TE 诊断AIH 的ROC 曲线
3 讨论
TE 的原理是低频振动器发出的振动波通过超声换能器向肝脏组织传播,通过换能器记录回波信号,再计算出传播速度,肝脏硬度程度和剪切波的传播速度呈正相关,即肝脏质地越硬,剪切波传播速度越快,因此可以根据剪切波的传播速度进而判断肝脏组织纤维化程度[8-10]。
本研究数据显示:AIH 随着病理肝纤维化的加重,LSM 增大,提示肝纤维化程度和LSM 呈正相关,差异有统计学意义(P<0.05)。分析原因:AIH 主要的病理特征之一是界面性炎,汇管区浆细胞浸润侵入肝实质,根据破坏的程度分为轻、中、重度界面性炎,对于中重度界面性炎,肝细胞受到攻击发生变性坏死,其中心可见扩张的毛细血管,周围有假腺样结构形成,称之为“玫瑰花环”样改变,此病理表现诊断AIH 有一定的特异性,随着病情的进展,肝组织可见点状或碎片状坏死,病情较重可出现桥样坏死,进而出现肝硬化[11-13]。
有研究显示,不同病因所导致的肝硬化,其肝硬度界值也不相同[14]。本研究数据显示:当肝纤维化程度进展为重度(S3~S4)时,AIH 和乙肝的LSM 出现差异有统计学意义(P<0.05)。分析原因:有文献指出,利用TE 诊断肝纤维化,病理肝纤维化分期越高,TE 诊断价值越高[10]。AIH 患者随着纤维化程度的加重,病理特征愈发不典型,界面性炎渐不明显,但部分患者可能仍存在浆细胞浸润或“玫瑰花环”样改变,这也可能是病理显示重度肝纤维化(S3~S4)下AIH 和乙肝LSM出现差异的原因[15-16]。
本研究通过对TE 定量评估AIH 纤维化程度的讨论,为临床诊断AIH 提供更多依据,但是该技术也存在局限性,所以可以利用弹性成像,同时测量肝脏、脾脏二者纤维化程度,以此提高TE 评估AIH 的准确性[17-18]。

