阿糖胞苷致重度横纹肌溶解症继发多器官功能衰竭1例
杨钰华,刘月,黄晓娜(南京医科大学附属无锡人民医院药学部,江苏 无锡 214023)
横纹肌溶解症(rhabdomyolysis,RM)是骨骼肌肌肉破坏后,肌酸激酶(creatine kinase,CK)、肌红蛋白(myoglobin,Myo)等酶类以及离子和小分子毒性物质释放到循环中,引起的生化紊乱及脏器功能损伤的综合征。临床表现为肌痛、肌无力、深色尿、CK升高,严重者可能发展成急性肾衰竭(acute renal failure,ARF)[1]。目前,国际上尚未制订统一的RM诊断标准,常以下列几项指标[1-2]作出诊断:① 有引起横纹肌溶解的病因;② CK显著增高,≥正常峰值5倍或>1000 U·L-1;③ 血、尿肌红蛋白水平明显增高;④尿潜血试验阳性,但是镜下未见红细胞。临床上用CK的血浆浓度来判断RM的严重程度:CK在1000~5000 U·L-1时,为轻度RM;CK在5000~15 000 U·L-1时,为中度RM;CK≥15 000 U·L-1时,为重度RM[3]。引起RM的因素广泛而复杂,目前确定的导致RM的众多因素中,药物是最常见的诱因[4-5]。
RM是急性白血病罕见的并发症,偶有报道,多由感染或大剂量化疗药物引起[6-7]。标准剂量下,阿糖胞苷导致RM极为罕见。而急性白血病化疗后骨髓抑制期合并RM,极易漏诊,若不及时处理,易出现器官功能损伤,病死率近30%[6]。本文报道1例急性非淋巴细胞白血病患者在标准剂量阿糖胞苷治疗下引发的重度RM继发多器官功能衰竭,为识别及处理阿糖胞苷导致的RM提供参考。
1 病历资料
患者,女,50岁,身高 166 cm,体重59 kg,体质量指数21.41 kg·m-2。因“确诊急性非淋巴细胞白血病3 d” 于2022年10月11日入院。既往有剖宫产及子宫肌瘤切除术史,无基础疾病,无食物药物过敏史。入院查体:体温36.7℃,脉搏80次·min-1,呼吸16次·min-1,血压122/69 mmHg(1 mmHg=0.133 kPa),体格检查正常,心肺无特殊。入院诊断:急性非淋巴细胞性白血病。
患者入院后查肝肾功能、凝血功能正常,CK 80 U·L-1、肌酸激酶同工酶(CK-MB)3.2 U·L-1,均在正常范围内,血常规:白细胞计数(WBC)1.47×109·L-1↓,中性粒细胞计数(N)0.19×109·L-1↓,血红蛋白(Hb)103 g·L-1↓,血小板计数(PLT)102×109·L-1↓,C反应蛋白(CRP)<0.5 mg·L-1。10月12日起予标准IA方案诱导化疗,具体为:注射用盐酸伊达比星(瀚晖制药有限公司,规格:10 mg,批号:22002111)10 mg qd d1~4,注射用阿糖胞苷[辉瑞制药(无锡)有限公司,规格:0.1 g,批号:GA5500] 0.1 g q12h d1~7,辅以碳酸氢钠水化碱化、奥美拉唑抑酸护胃、托烷司琼止吐等治疗。化疗d1~5,患者有恶心、反酸,无其他不适。10月15日(化疗d4)复查血常规:WBC 0.99×109·L-1↓,N 0.17×109·L-1↓,PLT 102×109·L-1↓,Hb 96 g·L-1↓,CRP<0.5 mg·L-1。
10月17日,患者夜间出现低热,体温37.8℃,诉双下肢疼痛,以肌肉痛为主,急查血常规:WBC 0.20×109·L-1↓,N 0.06×109·L-1↓,PLT 74×109·L-1↓,Hb 96 g·L-1↓,CRP 15.2 mg·L-1↑;肝肾功能:谷丙转氨酶(ALT)20.8 U·L-1,谷草转氨酶(AST)54 U·L-1,肌酐(Scr)33.6 μmol·L-1;心肌酶谱:CK 745 U·L-1↑,CKMB 26 U·L-1↑,Myo 921.20 ng·mL-1↑。考虑化疗后RM,合并粒细胞缺乏,暂停阿糖胞苷,予碳酸氢钠水化碱化,曲马多、双氯芬酸钠止痛等对症治疗。
10月18日(暂停化疗d1),患者诉全身肌肉酸痛,疼痛剧烈,有低热(38.1℃),解深红色尿,大便正常。复查肾功能:Scr 32.2 μmol·L-1↓,钾3.38 mmol·L-1↓,总钙1.68 mmol·L-1↓,钠119.8 mmol·L-1↓。患者电解质紊乱,予补钾补钠补钙对症处理,加强利尿,同时加用拉氧头孢+莫西沙星预防感染。
10月19日1:13,患者再次出现双下肢剧烈疼痛,伴大汗淋漓。3:00左右患者血压66/47 mmHg,导出酱油色尿液,尿量少。查体:四肢湿冷,肢端、口唇青紫,右大腿外侧及膝关节以下、左侧膝关节以下痛触觉消失,伴胸闷气喘。肝功能:白蛋白21.8 g·L-1↓,ALT 714.1 U·L-1↑,AST 3668 U·L-1↑;心肌酶谱:CK 44 709 U·L-1↑,CK-MB 2966.4 U·L-1↑,Myo>2000 ng·mL-1↑。予升压、补液扩容、保肝、加强水化碱化等对症治疗,多学科综合治疗(MDT)讨论后调整抗菌药物为亚胺培南+替加环素+泊沙康唑广泛覆盖抗感染。
10月19日20:08,患者转入重症监护室,予呼吸机辅助呼吸,人粒细胞刺激因子升白,去甲肾上腺素升压,纠正酸中毒,连续性肾脏替代治疗(CRRT)等治疗。急查血培养(阴性),血常规:WBC 0.22×109·L-1↓,N 0.02×109·L-1↓,PLT 10×109·L-1↓,Hb 104 g·L-1↓,CRP 333.1 mg·L-1↑。
10月20日,复查肝功能:ALT 1349.9 U·L-1↑,AST 6417 U·L-1↑;CK、CK-MB无法检出。患者四肢湿冷伴花斑、肿胀较前明显加重,气喘明显,血压、指脉氧测不出,神志浅昏迷,并出现室颤、心搏骤停,病情危重,患者家属要求放弃治疗自动出院。
患者住院期间ALT、AST、CK、CK-MB变化趋势及相关用药情况见图 1。
2 讨论
2.1 阿糖胞苷致RM的关联性分析
患者入院后予阿糖胞苷联合伊达比星治疗急性非淋巴细胞性白血病,化疗第6日出现肌肉剧烈疼痛,解深红色尿等症状,CK值最高达44 709 U·L-1↑,可诊断为重度RM[3]。据文献报道,感染是急性白血病发生RM的主要诱因[6-7]。患者在化疗后粒细胞低下期出现发热,有感染可能,但患者血培养阴性,使用广谱抗菌药物治疗后症状改善不明显,且粒细胞缺乏伴发热出现在患者CK升高、肌肉酸痛症状之后,考虑感染引起该患者RM的可能性不大。虽然高热也有引起RM的报道,但多为近40℃的恶性高热[8]。患者发热与双下肢肌肉疼痛同时发生,且最高体温仅有38.1℃,考虑发热可能是RM的伴随症状,而非导致RM的原因。
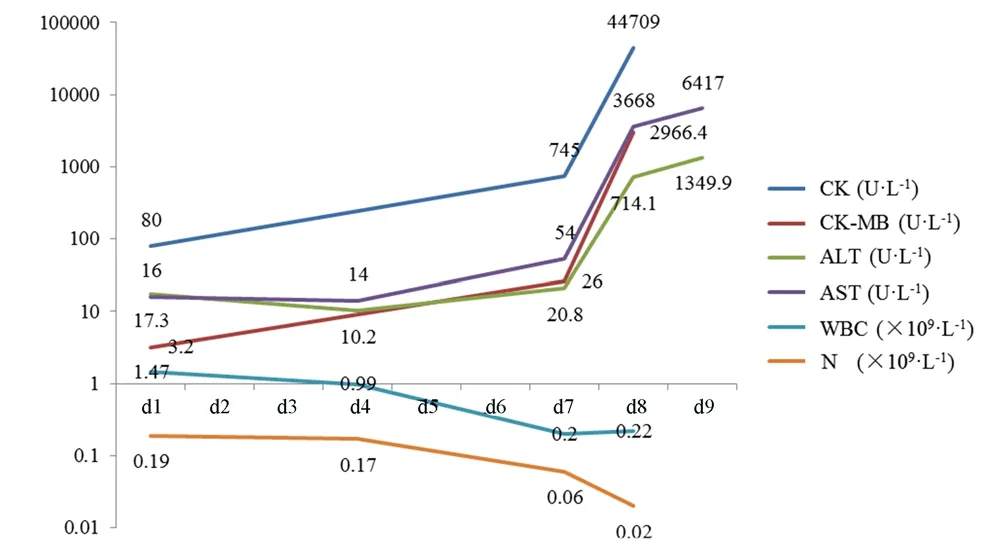
图1 住院期间实验室检查指标变化趋势
该患者在应用阿糖胞苷第6日发生RM,符合阿糖胞苷已知的药物不良反应类型,且用药与不良反应的发生有合理的时间关联性。其合并用药伊达比星目前无引起RM的报道,且在发生RM前2日已停用。虽然在发生RM后及时停用阿糖胞苷,但因疾病进展较快,RM未能缓解。此外,用药前患者体征正常,CK、CK-MB均在正常范围,多脏器功能衰竭是在RM之后发生,RM发生与其原发病也无明确的相关性。阿糖胞苷与RM的诺氏评估量表评分为5分,表明该患者发生RM继发多器官功能衰竭与阿糖胞苷“很可能”相关,属于极少见的药物严重不良反应。
2.2 阿糖胞苷致RM继发多器官功能衰竭原因分析
阿糖胞苷抑制DNA聚合酶,干扰体内DNA的生物合成,从而阻滞肿瘤细胞增殖,属于细胞周期特异性药物。有研究者认为肌肉损伤可能与已知的阿糖胞苷触发线粒体释放细胞色素C的能力有关,从而严重影响骨骼肌产生三磷酸腺苷(ATP)并导致横纹肌溶解,同时低钾血症、低磷血症和感染等因素可能增强阿糖胞苷对线粒体的作用[9]。
阿糖胞苷引发RM极为少见,通过检索CNKI、万方、PubMed等中外文数据库,仅收集到阿糖胞苷致RM的病例报道2例,均为使用大剂量阿糖胞苷后出现了RM,1例死亡,1例预后不详[9-10]。本例患者入院后使用标准剂量阿糖胞苷(100 mg q12 h),化疗第6日出现RM,之后继发电解质紊乱、急性肾功能不全、肝功能不全、代谢性酸中毒、低蛋白血症、感染等,虽然及时停药,液体治疗并启动CRRT等相关治疗,但是患者病情进一步恶化,最终发展成多器官功能衰竭。回顾该病例,患者处于化疗后骨髓抑制状态,并发感染,也是其疾病进展迅速,继发多器官功能衰竭的原因之一。电解质紊乱也会引起RM[11-12]。患者在RM发生后出现了严重的电解质紊乱,考虑这也是患者RM逐渐加重的原因之一。其次,CK>5000 U·L-1时即有肾脏替代治疗的指征,患者10月19日晚启动CRRT治疗时,CK已急剧升高至44 709 U·L-1,因此预后差。有研究指出,McMahon风险评分可以预测肾脏替代治疗或导致RM患者的死亡率,McMahon评分6分及以上与CK水平大于5000 U·L-1相比,在预测肾脏替代治疗风险方面具有更高的敏感性和特异性[13-14]。根据评分标准,该患者女性(1分),10月18日即出现电解质紊乱(总钙1.68 mmol·L-1)(2分),阿糖胞苷化疗后出现RM(3分),总评分6分,应尽早考虑CRRT肾脏保护治疗。
3 小结
目前的病例报道及药品说明书均仅提示在使用高剂量阿糖胞苷后可能发生RM,本例标准剂量下阿糖胞苷致重度RM继发多器官功能衰竭的病例报道极为罕见,具有一定的临床价值。结合患者诊疗经过,在临床使用标准剂量阿糖胞苷时也应充分意识到化疗后骨髓抑制期间RM的可能性,并警惕其引发严重的并发症,迅速停药并积极进行液体治疗,及时进行McMahon风险评分,保护肾功能,同时及时处理感染、电解质紊乱等潜在诱发因素。

