新型酰基磺酰亚胺类化合物的合成及生物活性
李瑞丽, 徐志红, 周 静, 杜晓英*,,2, 朱 祥*,,2
(1.长江大学 农学院,湖北 荆州 434025;2.长江大学 农药研究所,湖北 荆州 434025)
酰基磺酰亚胺类化合物具有良好的抗真菌[1]、除草[2-3]、抗肿瘤[4]、抗病毒[5]、抗糖尿病[6]等多种生物活性,是近年农药和医药研究的热点。1995年,Cloudsdale 等[7]研究发现,N-酰基磺酰亚胺类化合物图式1,1)对乙酰羟酸合成酶(AHAS)具有较强的抑制活性,其除草活性 (IC50= 0.3 mg/L) 高于对照药剂氯嘧磺隆 (IC50= 0.386 mg/L),具有开发为防除阔叶杂草除草剂的潜力;由巴斯夫公司开发的含苯甲酰基磺酰亚胺结构的脲嘧啶类除草剂苯嘧磺草胺[saflufenacil (图式1,2)][8],为原卟啉原氧化酶(PPO)类抑制剂,可快速铲除70 余种阔叶杂草,具有除草效果好、作用快的特点,是第一个作用于玉米田的PPO 类芽前除草剂;刘卓等[9]报道了14 种包含酰基磺酰亚胺结构的新型嘧啶磺酰脲化合物(图式1,3),其中有3 种新化合物对黄瓜灰霉病菌、油菜菌核病菌和水稻纹枯病菌表现出一定的抑菌效果;Avupati 等[10]合成了一系列新型二芳基酰基磺酰亚胺结构化合物(图式1,4),其中有 2 种化合物具有广谱抗真菌活性,对枯草芽孢杆菌(NCIM 2063)、短小芽孢杆菌(NCIM 2327)、金黄色葡萄球菌(NCIM 2079)和藤黄微球菌(NCIM 2155) 等 12 种病菌显示出一定的抗菌活性。由此可见,酰基磺酰亚胺类化合物在农用除草剂和杀菌剂开发方面表现出巨大潜力。

图式 1 N-酰基磺酰亚胺除草剂和抑菌剂Scheme 1 N-Acylsulfonimide herbicides and fungicides
磺草灵(asulox,图式1,5),1965 年由英国May&Baker 公司(现拜耳公司)[11-12]研发,是典型的含酰基磺酰亚胺结构的氨基甲酸酯类广谱性除草剂,也是目前唯一的二氢叶酸合酶抑制剂类除草剂。磺草灵因具有内吸传导性,很容易被植物茎叶吸收传导至地下根茎的生长点,从而抑制根茎呼吸,阻碍细胞分裂,影响叶酸合成,使植物枯死,是一种较好的除草剂品种。但由于磺草灵长期大量被使用,导致杂草对其抗性增加,田间除草效果下降。Rueb 等[13]发现,在苯环上引入N-取代四氢邻苯二甲酰胺可以提高该类化合物(图式1,6)的除草活性。为了进一步提高其除草活性,本研究通过在磺草灵苯环上引入邻苯二甲酸酐结构,设计合成了20 个未见文献报道的化合物 (合成路线见图式2 ),初步测定了其除草活性和抑菌活性,并对化合物的构效关系进行了初步探讨,以期望能够发现高活性的化合物,为磺草灵类似物的农用活性的开发和应用提供依据。

图式 2 目标化合物的合成路线Scheme 2 Synthetic route of target compounds
1 材料与方法
1.1 药剂与仪器
97.4% 磺草灵原药,南通泰禾化工股份有限公司;98%多菌灵原药,江苏龙灯化学有限公司;99.5% 对氨基苯磺酰胺和间氨基苯磺酰胺、99.7%邻苯二甲酸酐、98% 氯甲酸丁酯和98% 氯甲酸异丁酯,均为上海麦克林生化科技股份有限公司产品。
Bruker Avance DPX400 型核磁共振仪 (以TMS 作内标物,CDCl3作溶剂),德国-瑞士布鲁克光谱公司;WRR 熔点测定仪 (熔点未校正),上海精密科学仪器有限公司;Themo Scientific Q Exactive 型高分辨质谱仪 (ESI-MS),赛默飞世尔科技 (中国) 有限公司;Digital Water Bath SB1000旋转蒸发仪,日本 EYELA 公司。
1.2 供试植物病原真菌及杂草
油菜菌核病菌Sclerotinia sclerotiorum、茶叶炭疽病菌Colletotrichum camalliae、水稻恶苗病菌Fusarium moniliforme、白芨白绢病菌Sclerotium rolfii和辣椒疫霉Phytophthora capsici,均由长江大学农学院植物病理实验室提供。
稗草Echinochloa crus-galli,由长江大学农药研究所提供。
1.3 化合物的合成
1.3.1 中间体2a~2t 的合成 参考文献方法[14]合成。将对氨基苯磺酰胺或间氨基苯磺酰胺(1.17 mmol)、邻苯二甲酸酐(1 mmol) 和20 mL 的醋酸溶液,在氮气下于130 ℃回流搅拌过夜,薄层色谱(TLC,V(石油醚) :V(乙酸乙酯) = 14 : 1)检测至反应完全,反应液趁热过滤,滤饼用乙醇进行洗涤,粗产品用V(石油醚) :V(乙酸乙酯) = 1 : 8 重结晶,进行重结晶,分别得中间体4-(1,3-二氧代异吲哚啉-2-基)苯磺酰胺和3-(1,3-二氧代异吲哚啉-2-基)苯磺酰胺 (2a~2t)。
1.3.2 目标化合物3a~3t 的合成 参考文献方法[15]合成。在室温下,向100 mL 圆底烧瓶中加入中间体2 (3.96 mmol)和 4-二甲氨基吡啶 (7.90 mmol)溶于二氯甲烷 (12 mL)的溶液,缓慢滴加氯甲酸丁酯(4.76 mmol),室温反应约1 h,薄层色谱(TLC,V(石油醚) :V(乙酸乙酯) = 2 : 1) 监测至反应完全。用1 mmol/L 的稀盐酸(10 mL)酸洗,再用二氯甲烷(20 mL × 3)萃取,合并有机相,减压浓缩得到粗品,经V(二氯甲烷) :V(石油醚) = 1 : 6重结晶,得到目标化合物3a~3t。
(4-(4-氯-1,3-二氧代异吲哚啉-2-基) 苯基) 磺酰基) 氨基甲酸丁酯(3a): 白色固体, 收率89%, m.p.169.2-171.4 ℃;1H NMR (400 MHz, CDCl3)δ: 8.21 (d,J= 8.4 Hz, 2H), 7.95(t,J= 4.0 Hz, 1H), 7.85 - 7.73 (m, 4H), 4.14 (t,J= 6.8 Hz,2H), 1.67 - 1.56 (m, 2H), 1.42 - 1.26 (m, 2H), 0.93 (t,J= 7.2 Hz, 3H);13C NMR (100 MHz, CDCl3)δ: 165.18, 164.19,150.45, 137.59, 136.69, 136.43, 135.82, 133.47, 132.42,129.36, 127.06, 126.31, 122.67, 67.20, 30.42, 18.87, 13.63;HRMS-ESI(m/z) C19H17ClN2O6S (M-H)-435.0420 计算值435.0420, 测试值 435.0428.
(4-(5-溴-1,3-二氧代异吲哚啉-2-基) 苯基) 磺酰基) 氨基甲酸丁酯 (3b): 白色固体, 收率87% , m.p.161.2-163.2 ℃;1H NMR (400 MHz, CDCl3)δ: 8.20 (d,J=8.8 Hz, 2H), 8.14 (s,1H), 8.01 (dd,J= 7.6, 1.6 Hz, 1H), 7.88 (d,J= 8 Hz, 1H),7.75 (d,J= 8.8 Hz, 2H), 4.14 (t,J= 6.4 Hz, 2H), 1.67 - 1.54(m, 2H), 1.41 - 1.26 (m, 2H), 0.92 (t,J= 7.2 Hz, 3H);13C NMR (100 MHz, CDCl3)δ: 165.80, 165.28, 150.48, 138.05,137.55, 136.48, 132.96, 130.03, 129.87, 129.39, 127.48,126.18, 125.52, 67.20, 30.42, 18.87, 13.63; HRMS-ESI(m/z)C19H17BrN2O6S (M-H)-478.9920 计算值478.9920, 测试值478.9922.
(4-(5-硝基-1,3-二氧代异吲哚啉-2-基) 苯基) 磺酰基) 氨基甲酸丁酯(3c): 白色固体, 收率85% , m.p.176.8-179.1 ℃;1H NMR (400 MHz, CDCl3)δ: 8.83 (d,J= 2.0 Hz, 1H), 8.75(dd,J= 8.0, 2.0 Hz, 1H), 8.24 (d,J= 8.4 Hz, 3H), 7.82 - 7.74(m, 2H), 4.15 (t,J= 6.4 Hz, 2H), 1.67 - 1.56 (m, 2H), 1.42 -1.34 (m, 2H), 0.93 (t,J= 7.4 Hz, 3H);13C NMR (100 MHz,CDCl3)δ: 164.52, 164.29, 152.25, 150.36, 138.02, 136.04,135.68, 132.79, 130.11, 129.55, 126.19, 125.52, 119.58, 67.26,30.42, 18.87, 13.62; HRMS-ESI(m/z) C19H17N3O8S(M-H)-446.0660 计算值446.0660, 测试值 446.0667.
(4-(5-氯-1,3-二氧代异吲哚啉-2-基) 苯基) 磺酰基) 氨基甲酸丁酯(3d): 白色固体, 收率86% , m.p.167.8-169.6 ℃;1H NMR (400 MHz, CDCl3)δ: 8.21 (t,J= 2 Hz, 1H), 8.18 - 8.08(m, 2H), 8.00 (dd,J= 8, 1.6 Hz, 1H), 7.91 - 7.68 (m, 3H), 4.15(t,J= 6.4 Hz, 2H), 1.66 - 1.55 (m, 2H), 1.40 - 1.26 (m, 2H),0.91 (t,J= 7.6 Hz, 3H);13C NMR (100 MHz, CDCl3)δ:165.85, 165.33, 150.39, 139.63, 137.96, 132.99, 132.24,131.36, 129.92, 129.84, 127.81, 127.42, 125.92, 125.46, 67.25,30.42, 18.85, 13.63; HRMS-ESI(m/z) C19H17ClN2O6S (M-H)-435.0420 计算值435.0420, 测试值 435.0427.
(3-(4,5,6,7-四溴-1,3-二氧代异吲哚啉-2-基) 苯基) 磺酰基) 氨基甲酸丁酯(3e): 白色固体, 收率88% , m.p.169.7-172.5 ℃;1H NMR (400 MHz, CDCl3)δ: 8.22 - 8.13(m, 1H), 7.84 - 7.69 (m, 1H), 7.30 (d,J= 1.6 Hz, 3H), 4.16 (t,J= 6.8 Hz, 2H), 1.61 (d,J= 7.2, 2H), 1.32 (d,J= 7.6 Hz, 2H),0.92 (t,J= 7.2 Hz, 3H);13C NMR (100 MHz, CDCl3)δ:162.00, 150.27, 141.10, 139.75, 131.48, 130.54, 129.96,128.39, 126.93, 126.09, 67.32, 30.42, 18.85, 13.63; HRMSESI(m/z) C19H14Cl4N2O6S (M-H)-536.9250 计算值536.9250, 测试值 536.9260.
(4-(1,3-二氧代异吲哚啉-2-基) 苯基) 磺酰基) 氨基甲酸丁酯(3f): 白色固体, 收率91% , m.p.162.7-164.6 ℃;1H NMR(400 MHz, CDCl3)δ: 8.21 (d,J= 8.8 Hz, 2H), 8.03 (dd,J=5.6, 3.2 Hz, 2H), 7.88 (dd,J= 5.2, 2.8 Hz, 2H), 7.78 (d,J= 8.8 Hz, 2H), 4.14 (t,J= 6.8 Hz, 2H), 1.67 - 1.56 (m, 2H), 1.42 -1.26 (m, 2H), 0.93 (t,J= 7.2 Hz, 3H);13C NMR (100 MHz,CDCl3)δ: 166.59, 150.46, 137.31, 136.83, 134.99, 131.39,129.34, 126.22, 124.19, 67.16, 30.43, 18.88, 13.63; HRMSESI(m/z) C19H18N2O6S(M-H)-401.0810 计算值401.0810, 测试值 401.0816.
(4-(5-氯-1,3-二氧代异吲哚啉-2-基) 苯基) 磺酰基) 氨基甲酸异丁酯(3g): 白色固体, 收率90% , m.p.> 220 ℃;1H NMR(400MHz, DMSO-d6)δ: 8.09 (d,J= 2 Hz, 1H), 8.05 - 7.95(m, 2H), 7.86 (d,J= 8.4 Hz, 2H), 7.47 (d,J= 8.4 Hz, 2H),3.49 (d,J= 6.8 Hz, 2H), 1.80 - 1.65 (m, 1H), 0.83 (d,J= 6.4 Hz, 6H);13C NMR (100 MHz, DMSO-d6)δ: 166.53, 166.17,159.29, 146.34, 139.96, 135.00, 134.13, 133.09, 130.67,127.78, 126.85, 125.73, 124.05, 70.12, 28.10, 19.74; HRMSESI(m/z) C19H17ClN2O6S (M-H)-435.0420 计算值435.0420,测试值 435.0427.
(4-(4-硝基-1,3-二氧代异吲哚啉-2-基) 苯基) 磺酰基) 氨基甲酸丁酯(3h): 白色固体,76% , m.p.178.2-179.6 ℃;1H NMR (400 MHz, DMSO-d6)δ: 12.19 (s, 1H), 8.39 (d,J= 8.0 Hz, 1H), 8.32 (d,J= 7.2 Hz, 1H), 8.16 (t,J= 7.6 Hz, 1H), 8.13 -8.04 (m, 2H), 7.77 (d,J= 8.4 Hz, 2H), 4.03 (t,J= 6.4 Hz, 2H),1.56 - 1.44 (m, 2H), 1.32 - 1.18 (m, 2H), 0.85 (t,J= 7.2 Hz,3H);13C NMR (100 MHz, DMSO-d6)δ: 165.20, 162.65,151.76, 145.05, 139.09, 137.10, 136.34, 133.93, 129.08,128.76, 128.21, 127.72, 123.33, 66.22, 18.82, 13.93; HRMSESI(m/z) C19H17N3O8S(M-H)-446.0660 计算值446.0660,测试值 446.0672.
(4-(4,5,6,7-四溴-1,3-二氧代异吲哚啉-2-基) 苯基) 磺酰基) 氨基甲酸丁酯(3i): 白色固体, 收率83% , m.p.> 220 ℃;1H NMR (400 MHz, DMSO-d6)δ: 12.22 (s, 1H), 8.09 (d,J=8.8 Hz, 2H), 7.74 (d,J= 8.4 Hz, 2H), 4.03 (d,J= 6.4 Hz, 2H),1.55 - 1.44 (m, 2H), 1.34 - 1.18 (m, 2H), 0.85 (t,J= 7.6 Hz,3H);13C NMR (100 MHz, DMSO-d6)δ: 162.99, 151.77,139.23, 137.33, 136.33, 131.44, 128.77, 128.29, 121.46, 66.21,30.51, 18.82, 13.95.
(4-(1,3-二氧代-1,3,4,5,6,7-六氢-2H-异吲哚-2-基) 苯基) 磺酰基) 氨基甲酸丁酯(3j): 白色固体, 收率90% , m.p.189.5-190.9 ℃;1H NMR (400 MHz, CDCl3)δ: 8.13 (d,J= 9.2 Hz, 1H), 7.69 (d,J= 8.8 Hz, 2H), 4.12 (t,J= 6.4 Hz, 2H), 2.48(s, 4H), 1.87 (m,J= 3.2 Hz, 4H), 1.65 - 1.54 (m, 2H), 1.40 -1.26 (m, 2H), 0.92 (t,J= 7.2 Hz, 3H);13C NMR (100 MHz,CDCl3)δ: 169.13, 150.41, 142.41, 137.19, 136.27, 129.29,125.04, 77.39, 77.27, 77.07, 76.76, 67.12, 30.41, 21.27, 20.25,18.86, 13.62; HRMS-ESI(m/z) C19H22N2O6S (M-H)-405.1130 计算值405.1130, 测试值 405.1131.
(4-(5-甲基-1,3-二氧代异吲哚啉-2-基) 苯基) 磺酰基) 氨基甲酸丁酯(3k): 白色固体, 收率91% , m.p.156.7-158.8 ℃;1H NMR (400 MHz, CDCl3)δ: 8.20 (d,J= 8.8 Hz, 2H), 7.90(d,J= 7.6 Hz, 1H), 7.84 - 7.71 (m, 3H), 7.66 (d,J= 7.6 Hz,1H), 4.14 (t,J= 6.4 Hz, 2H), 2.60 (s, 3H), 1.64 - 1.54 (m, 2H), 1.42 -1.26 (m, 2H), 0.93 (t,J= 7.6 Hz, 3H);13C NMR (100 MHz,CDCl3)δ: 166.74, 166.59, 150.33, 146.50, 137.13, 137.05,135.56, 131.79, 129.29, 128.81, 126.13, 124.61, 124.07, 77.36,77.25, 77.04, 76.73, 67.16, 30.44, 22.15, 18.86, 13.59; HRMSESI(m/z) C20H20N2O6S (M-H)-415.0970 计算值415.0970,测试值, 415.0978.
(3- (4-氯-1,3-二氧代异吲哚啉-2-基) 苯基) 磺酰基) 氨基甲酸丁酯(3l): 白色固体, 收率87% , m.p.126.7-129.2 ℃;1H NMR (400 MHz, CDCl3)δ: 8.22 (t,J= 2.0 Hz, 1H), 8.17 -8.09 (m, 1H), 7.94 (t,J= 4.0Hz, 1H), 7.86 - 7.66 (m, 4H),4.15 (t,J= 6.4 Hz, 2H), 1.67 - 1.55 (m, 2H), 1.40 - 1.27 (m,2H), 0.91 (t,J= 7.6 Hz, 3H);13C NMR (100 MHz, CDCl3)δ:165.23, 164.26, 150.42, 139.63, 136.60, 135.75, 133.50,132.33, 132.18, 131.46, 129.81, 127.89, 127.09, 125.99,122.62, 67.24, 30.42, 18.85, 13.63; HRMS-ESI(m/z)C19H17ClN2O6S (M-H)-435.0420 计算值435.0420, 测试值435.0424.
(3-(4,5,6,7-四溴-1,3-二氧代异吲哚啉-2-基) 苯基) 磺酰基) 氨基甲酸丁酯(3m): 白色固体, 收率80% , m.p.> 220 ℃;1H NMR (400 MHz, DMSO-d6)δ: 12.22 (s, 1H), 8.08 (d,J=8.8 Hz, 2H), 7.72 (d,J= 8.4 Hz, 2H), 4.03 (d,J= 6.4 Hz, 2H),1.55 - 1.43 (m, 2H), 1.34 - 1.18 (m, 2H), 0.85 (t,J= 7.6 Hz,3H);13C NMR (100 MHz, DMSO-d6)δ: 162.99, 151.77,139.23, 137.33, 136.33, 131.44, 128.77, 128.29, 121.46, 66.21,30.51, 18.82, 13.95.
(3- (1,3-二氧代异吲哚啉-2-基) 苯基) 磺酰基) 氨基甲酸丁酯(3n): 白色固体, 收率91% , m.p.78.7-80.4 ℃;1H NMR(400 MHz, CDCl3)δ: 8.24 (d,J= 2.0 Hz, 1H), 8.12 (d,J= 7.6 Hz, 1H), 8.02 (dd,J= 5.2, 3.2 Hz, 2H), 7.92 - 7.81 (m, 3H),7.73 (t,J= 8.0 Hz, 1H), 4.16 (t,J= 6.8 Hz, 2H), 1.67 - 1.56(m, 2H), 1.35 (m,J= 7.2Hz, 2H), 0.91 (t,J= 7.2 Hz, 3H);13C NMR (100 MHz, CDCl3)δ: 166.60, 150.33, 139.60, 134.87,132.60, 131.44, 129.73, 127.59, 125.96, 124.10, 67.22, 30.43,18.83, 13.58; HRMS-ESI(m/z) C19H18N2O6S (M-H)-401.0810 计算值401.0810, 测试值, 401.0817.
(3- (4-硝基-1,3-二氧代异吲哚啉-2-基) 苯基) 磺酰基) 氨基甲酸丁酯(3o): 白色固体, 收率94% , m.p.148.3-150.7 ℃;1H NMR (400 MHz, CDCl3)δ: 8.29 (d,J= 7.2 Hz, 1H), 8.27 -8.20 (m, 2H), 8.16 (dd,J= 8, 1.6 Hz, 1H), 8.11 - 8.02 (m, 1H),7.86 - 7.70 (m, 2H), 4.16 (t,J= 6.4 Hz, 2H), 1.67 - 1.56 (m,2H), 1.41 - 1.27 (m, 2H), 0.92 (t,J= 7.2 Hz, 3H);13C NMR(100 MHz, CDCl3)δ: 164.21, 161.37, 150.33, 139.85, 136.20,133.45, 131.77, 131.49, 129.92, 129.30, 128.28, 127.74,126.12, 123.12, 77.36, 77.04, 76.72, 67.28, 30.42, 18.83,13.58; HRMS-ESI(m/z) C19H17N3O8S (M-H)-446.0660 计算值446.0660, 测试值, 446.0671.
(3-(4,5,6,7-四氯-1,3-二氧代异吲哚啉-2-基) 苯基) 磺酰基) 氨基甲酸丁酯(3p): 白色固体, 收率89% , m.p.176.4-177.9 ℃;1H NMR (400 MHz, CDCl3)δ: 8.22 - 8.12 (m, 2H),7.83 - 7.68 (m, 2H), 4.15 (t,J= 6.8 Hz, 2H), 1.67 - 1.55 (m,2H), 1.41 - 1.26 (m, 2H), 0.92 (t,J= 7.2 Hz, 3H);13C NMR(100 MHz, CDCl3)δ: 162.01, 150.37, 141.06, 139.76, 131.60,131.47, 130.51, 129.95, 128.37, 126.95, 126.08, 77.39, 77.27,77.07, 76.75, 67.30, 30.41, 18.84, 13.63; HRMS-ESI(m/z)C19H14Cl4N2O6S (M-H)-536.9250 计算值536.9250, 测试值536.9261.
(3-(5-甲基-1,3-二氧代异吲哚啉-2-基) 苯基) 磺酰基) 氨基甲酸丁酯(3q): 白色固体, 收率93% , m.p.101.9-104.1 ℃;1H NMR (400 MHz, CDCl3)δ: 8.22 (t,J= 2 Hz, 1H), 8.11 (dt,J= 8.0, 1.6 Hz, 1H), 7.92 - 7.78 (m, 4H), 7.76 - 7.61 (m, 2H),4.15 (t,J= 6.4Hz, 2H),2.60 (s, 3H), 1.70 - 1.52 (m, 2H), 1.40 -1.25 (m, 2H), 0.91 (t,J= 7.2 Hz, 3H);13C NMR (100 MHz,CDCl3)δ: 166.80, 166.66, 150.35, 146.37, 139.54, 135.46,132.74, 131.81, 131.38, 129.66, 128.83, 127.45, 125.88,124.55, 124.00, 67.20, 30.42, 22.14, 18.83, 13.58; HRMSESI(m/z) C20H20N2O6S (M-H)-415.0970 计算值415.0970,测试值, 415.0977.
2) 功率反映柴油机对外做功的能力,是柴油机的重要性能指标。但其功率输出大小主要由外界需要所决定,通过调整喷油量来满足功率需求。功率本身对柴油机故障诊断并没有实际参考价值,但据其计算所得单位功率油耗可为故障诊断提供有效地指导。
(3-(5-氯-1,3-二氧代异吲哚啉-2-基) 苯基) 磺酰基) 氨基甲酸丁酯(3r): 白色固体, 收率86% , m.p.114.9-116.3 ℃;1H NMR (400 MHz, CDCl3)δ: 8.22 (t,J= 2 Hz, 1H), 8.13 (d,J=8.0 Hz, 1H), 8.01 - 7.92 (m, 2H), 7.83 (dd,J= 8.0, 1.6 Hz,2H), 7.73 (t,J= 8.0 Hz, 1H), 4.16 (t,J= 6.4 Hz, 2H), 1.67 -1.55 (m, 2H), 1.35 (m, 2H), 0.91 (t,J= 7.6 Hz, 3H);13C NMR(100 MHz, CDCl3)δ: 165.65, 150.32, 141.69, 139.68, 134.98,133.08, 132.31, 131.32, 129.81, 129.46, 127.78, 125.91,125.34, 124.48, 77.36, 77.25, 77.04, 76.73, 67.25, 30.43,18.83, 13.59; HRMS-ESI(m/z) C19H17ClN2O6S (M-H)-435.0420 计算值435.0420, 测试值, 435.0433.
(3-(5-硝基-1,3-二氧代异吲哚啉-2-基) 苯基) 磺酰基) 氨基甲酸丁酯(3s): 白色固体, 收率88% , m.p.118.6-120.1 ℃;1H NMR (400 MHz, CDCl3)δ: 8.81 (s, 1H), 8.77 - 8.70 (m,1H), 8.22 (d,J= 8.4 Hz, 1H), 8.17 - 8.11 (m, 1H), 7.86 - 7.80(m, 1H), 7.76 (t,J= 8 Hz, 1H), 4.15 (t,J= 6.4 Hz, 2H), 1.66 -1.55 (m, 2H), 1.40 - 1.26 (m, 2H), 0.91 (t,J= 7.6Hz, 3H);13C NMR(100 MHz, CDCl3)δ:164.64, 164.41, 152.18, 150.44,139.79, 135.75, 132.81, 131.85, 131.32, 130.05, 130.01,128.15, 125.99, 125.45, 119.49, 77.28, 67.30, 30.40, 18.83,13.63; HRMS-ESI(m/z) C19H17N3O8S (M-H)-446.0660 计算值446.0660,测试值, 446.0676.
(3-(5-溴-1,3-二氧代异吲哚啉-2-基) 苯基) 磺酰基) 氨基甲酸丁酯(3t): 白色固体, 收率90% , m.p.116.2-118.3 ℃;1H NMR (400 MHz, CDCl3)δ: 8.20 (s, 1H), 8.11 (dd,J= 9.2,2 Hz, 2H), 7.99 (dd,J= 8.0, 2 Hz, 1H), 7.87 (d,J= 8.0 Hz,1H), 7.81 (d,J= 9.2 Hz, 1H), 7.72 (t,J= 8.0 Hz, 1H), 4.14 (t,J= 6.4 Hz, 2H), 1.65 - 1.53 (m, 2H), 1.39 - 1.25 (m, 2H), 0.90(t,J= 7.6 Hz, 3H);13C NMR (100 MHz, CDCl3)δ: 165.89,165.36, 150.53, 139.64, 137.95, 132.98, 132.22, 131.33,129.89, 129.83, 127.78, 127.39, 125.89, 125.47, 67.24, 30.40,18.83, 13.63; HRMS-ESI(m/z) C19H17BrN2O6S (M-H)-478.9920 计算值478.9920, 测试值, 478.9934.
1.4 生物活性测定
1.4.1 抑菌活性的测定 采用菌丝生长速率法[16]测定目标化合物3a~3t 对5 种植物病原真菌的抑菌活性。将50 mg 待测化合物用1 mL 二甲基亚砜(DMSO)溶解,用含体积分数为0.1%吐温80 的灭菌去离子水定容至100 mL,得到500 mg/L 的药液。取5 mL 药液加到45 mL PDA 培养基中均匀混合,待其冷却凝固。在供试菌种菌落边缘打取直径7 mm 的菌饼,接种至上述含药培养基平板中央。将培养基置于28 ℃培养箱中培养。每处理重复3 次。以含1 mL DMSO 的0.1%吐温80 灭菌去离子水为空白对照,以磺草灵、多菌灵原药为阳性对照。待空白对照处理组的菌丝长至培养皿的三分之二处时,用十字交叉法测量各处理组菌落直径,按 (1) 式计算菌丝生长抑制率。
式中:I为抑制率;Dc为对照菌落直径,mm;Dt为处理菌落直径,mm;D0为菌饼直径,mm。
1.4.2 除草活性的测定 采用盆栽法[17]测定目标化合物对稗草的除草活性。在直径11 cm、高9 cm的花钵装上育苗基质,将催芽至露白的草种均匀地撒在上面,覆浅土,盆底渗透吸水。播种后移入温室培养,温度25~30 ℃,湿度60%~80%,光照/黑暗 = 14 h/10 h,待稗草生长至二叶一心备用。
供试药剂初筛质量浓度为150 mg/L,采用HCL-500 智能生测喷雾塔进行茎叶喷雾处理(压力2.5 kPa),以磺草灵为对照药剂,清水为空白对照,自然晾干后移至温室进行培养,培养条件同上。处理15d 后观察中毒症状并按 (2) 式计算鲜重抑制率。
式中:IFw为鲜重抑制率,%;mc为对照杂草地上部分鲜重;mt为处理杂草地上部分鲜重。
2 结果与讨论
2.1 化合物的合成
以不同取代基的苯甲酸酐与间位或者对位苯磺酰胺进行缩合,以较高收率 (75%~95%) 获得了4-(1,3-二氧代异吲哚啉-2-基)苯磺酰胺和3-(1,3-二氧代异吲哚啉-2-基)苯磺酰胺中间体2a~2t ,化合物2 再与氯甲酸丁酯或氯甲酸异丁酯发生缩合反应,得到目标化合物3a~3t,部分化合物可用二氯甲烷和石油醚重结晶获得,其余化合物需要通过柱层析纯化。
2.2 目标化合物的生物活性
2.2.1 离体抑菌活性 测试结果 (表1) 表明:在50 mg/L 时,部分化合物对油菜菌核病菌、茶叶炭疽病菌、白芨白绢病菌和辣椒疫霉均具有良好的抑制作用,在 50 mg/L 下,化合物 3n 对白芨白绢病菌抑菌率为63.70%,化合物3f、3n 和3q 对油菜菌核病菌的抑制率分别为63.98%、79.56%和77.83%,其中化合3n、3q 的抑菌活性优于磺草灵,化合物3q 对茶叶炭疽病菌的抑菌率为68.75%,部分化合物对辣椒疫霉的抑菌率高于50% 以上,抑菌活性优于或相当于多菌灵。
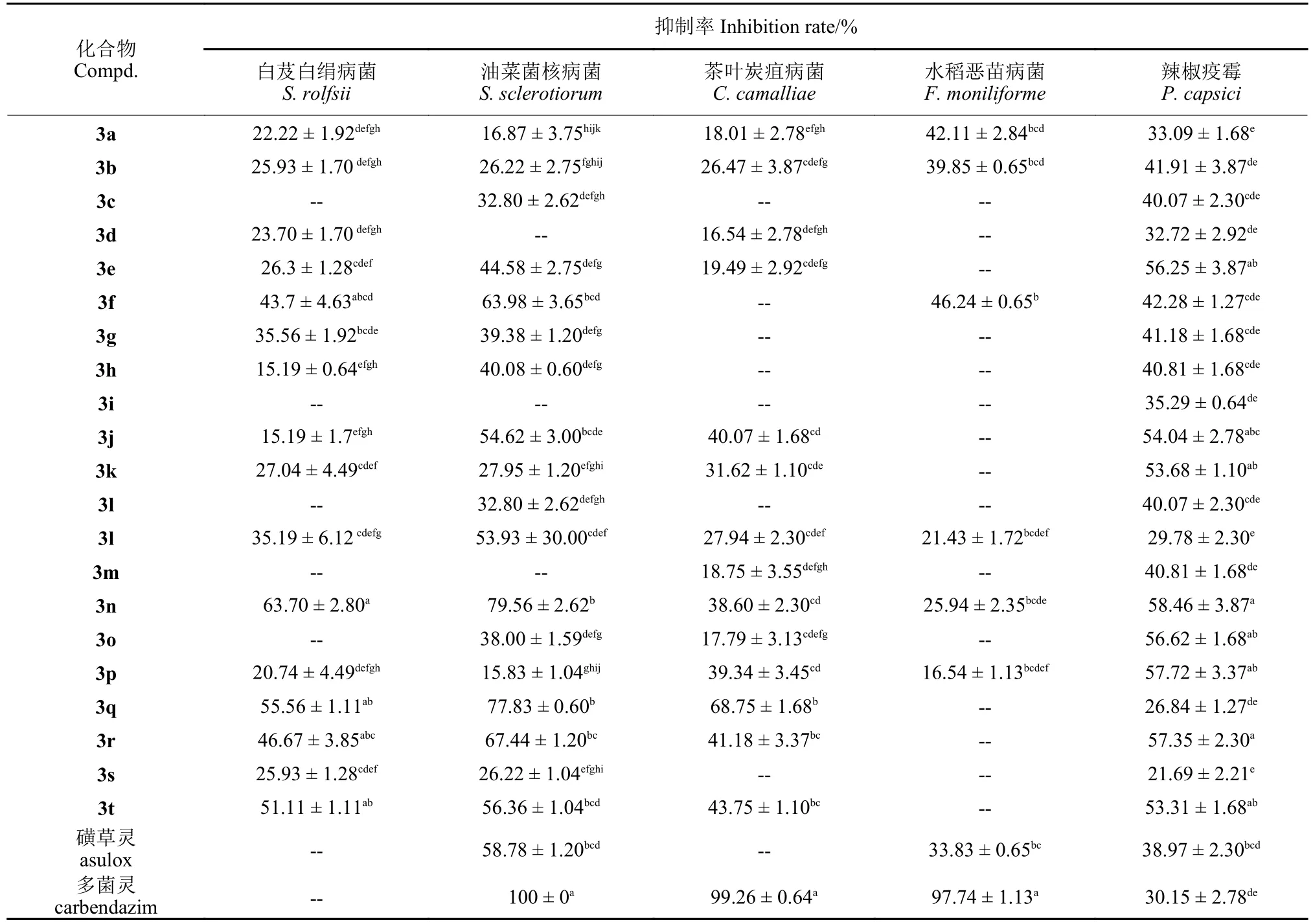
表1 目标化合物对 5 种植物病原菌菌丝生长的抑制作用Table 1 Inhibitory of target compounds against five pathogenic fungi in vitro
根据初筛结果,测定了部分化合物对油菜菌核、茶叶炭疽病菌和白芨白绢病菌的EC50值。结果 (表2) 表明,化合物 3q 对油菜菌核病菌和茶叶炭疽病菌的EC50值分别为10.49 mg/L 和21.57 mg/L,抑菌活性均高于对照药剂磺草灵。化合物 3n 对白芨白绢病菌的EC50值为28.26 mg/L,抑菌活性优于磺草灵。
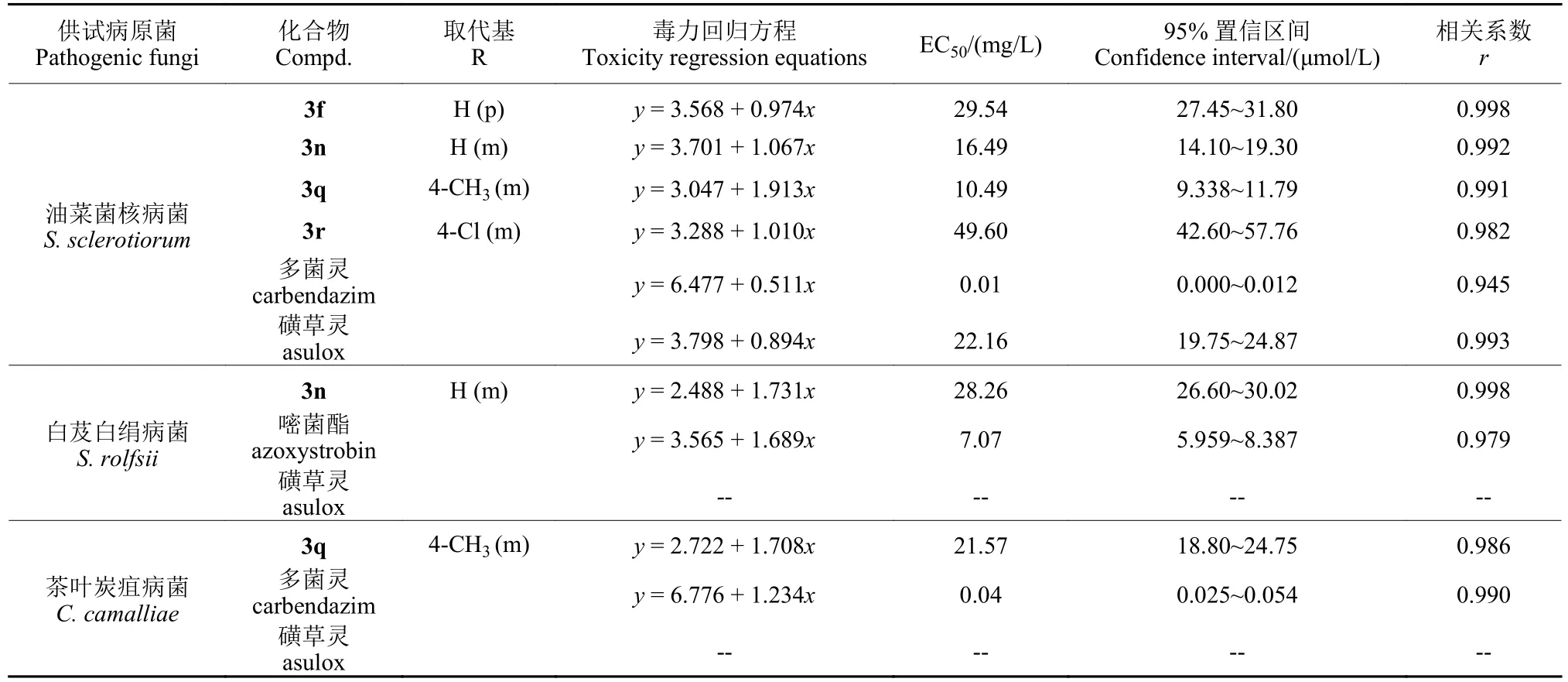
表2 部分目标化合物对供试植物病原菌的EC50 值Table 2 The EC50 values of some target compounds against pathogenic fungi
初步构效关系分析结果表明,在目标化合物的苯环上引入不同取代基 (R),会对化合物的抑菌活性产生影响。从3f和3n对油菜菌核病菌的抑制活性可以看出:当 R 为无取代时,间位的酰基磺酰亚胺结构活性优于对位的。从3n、3q和3r对油菜菌核病菌的抑制活性可以看出:间位结构供电子基的抑菌活性优于吸电子基的。总之,当磺草灵类似物苯环上是无取代或者有甲基这样的供电子基时抑菌活性增强。
2.2.2 除草活性 除草活性测定结果 (表3) 显示:经150 mg/L 的化合物处理后,大部分处理组的稗草叶片经过先变细、发白的中毒症状后返青,表明目标化合物的除草活性较差,只有化合物3a除草效果较好,平均鲜重防效为52.48%,但低于对照药剂磺草灵(71.68%)。
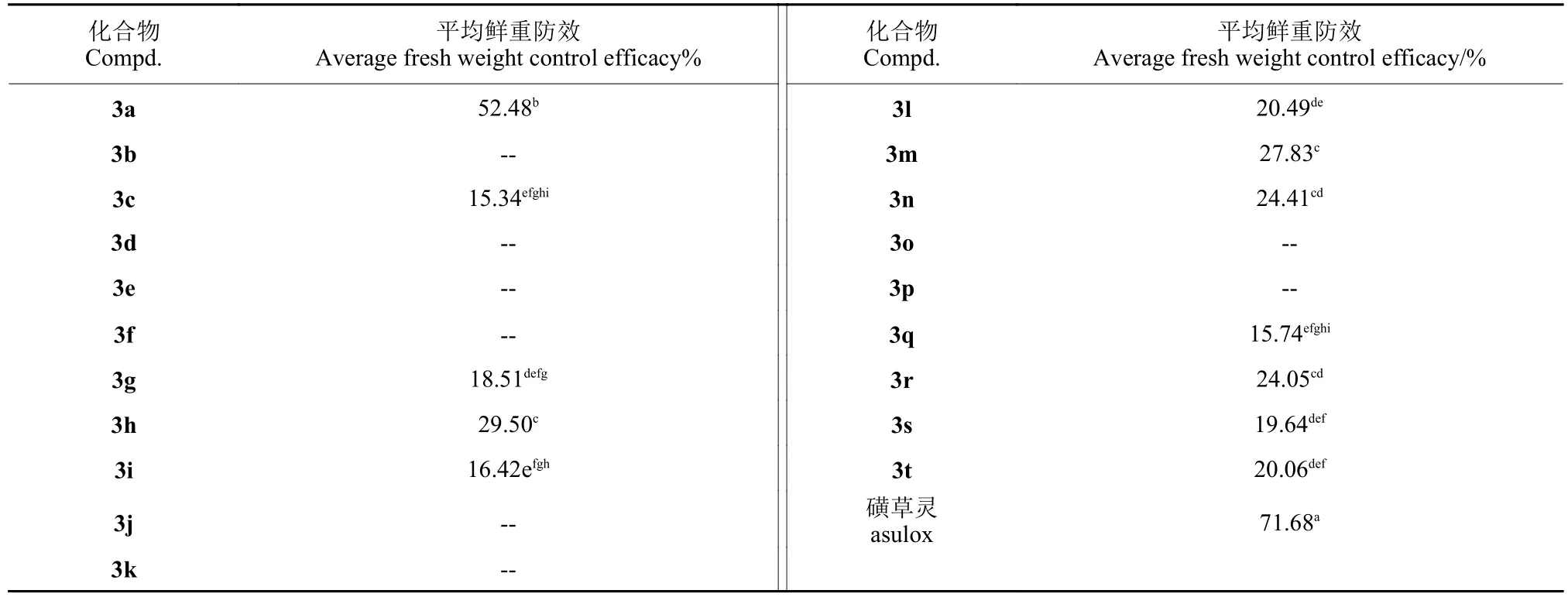
表3 目标化合物对稗草的除草活性Table 3 Herbicidal activity of target compounds on Echinochloa crus-galli
初步的构效关系分析表明,与磺草灵相比,目标化合物的除草谱减少,除草活性降低,说明引入大体积的酸酐对化合物的除草活性无益,进一步研究表明,当酸酐的3 号位是卤素氯时具有一定的除草活性,其活性优于3 位供电子基取代的化合物。
3 结论
本研究通过活性亚结构拼接的方式,设计合成了20 个未见文献报道的新型酰基磺酰亚胺类化合物,其结构均通过1H NMR、13C NMR 和高分辨质谱表征确认。抑菌活性结果表明:在50 mg/L时,大部分目标化合物对油菜菌核病菌、茶叶炭疽病菌、白芨白绢病菌和辣椒疫霉具有一定的抑制作用。化合物3f、3n和3q对油菜菌核病菌的抑菌活性较好,其中化合物3q对油菜菌核病菌的抑菌活性最好,优于磺草灵;化合物3n对白芨白绢病菌也有具有较好的抑菌活性,其余大部分化合物的杀菌活性并未达到预期。除草活性结果表明,在150 mg/L 时,化合物3a对稗草表现出一定的除草活性,但低于对照药剂磺草灵,除草活性并不理想。说明酸酐基团的引入没有提高酰基磺酰亚胺类化合物的除草活性,但能显著提高其抑菌活性。本研究经过试验证明引入酸酐,部分化合物在母体磺草灵的基础上提高了抑菌活性。可以通过进一步结构修饰作为抗真菌剂的候选物质,这为进一步寻求新的具有生物活性的物质提供了有价值的先导化合物。

