N-苯基八元氧桥环新烟碱化合物的合成及其增效活性
谭 都, 须志平, 邵旭升, 李 忠
(华东理工大学 药学院,上海市化学生物学 (芳香杂环) 重点实验室,上海 200237)
以吡虫啉为代表的新烟碱类杀虫剂,是一类具有触杀、胃毒及内吸活性的高效低毒杀虫剂,广泛应用于害虫防治、种子处理及动物健康等方面[1-2]。然而,随着该类杀虫剂的频繁使用,害虫抗药性迅速发展[3-5],加之其对蜜蜂和其他非靶标生物的安全性低[6-8],导致许多国家或组织重新评估了该类杀虫剂的风险,部分品种已被限制使用或禁止使用。目前,只有少数几个新开发的品种安全性较好或无交互抗性,如氟啶虫胺腈[9-10]、氟吡呋喃酮[11-12]和flupyrimin[13-14]等,新烟碱类杀虫剂的发展处于低迷期。
本课题组前期以NTN32692 为先导结构,基于顺硝烯的设计思路发现了一系列高活性结构[15],其中哌虫啶[15-16]和环氧虫啶[17-18](图式1) 已取得中国农药登记证。在研究环氧虫啶的同系物八元氧桥环结构化合物IPPA08 时,发现其在低浓度下化合物本身无活性,但和吡虫啉、噻虫嗪、啶虫脒、烯啶虫胺等传统新烟碱类杀虫剂联合使用时,能显著提高这些杀虫剂对害虫的防治效果[19],可作为一种新烟碱类杀虫剂的特异性增效剂,这为解决传统新烟碱类杀虫剂存在的问题提供了潜在方法。然而,IPPA08 与吡虫啉等杀虫剂联用时对蜜蜂的毒性也升高,不具有选择性。后续研究时,将吡啶环替换成苯环,发现苯环对位为叔丁基取代的化合物IPP217D25 增效活性更好且不会增加吡虫啉对蜜蜂的毒性,具有选择性[20],并且在苯环对位上引入芳基的部分化合物[21]增效活性优于IPP217D25,表明该类结构增效活性的构效关系不同于具有杀虫活性的新烟碱类化合物,将吡啶环替换成苯环是可行的。
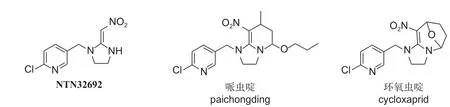
图式 1 NTN32692、哌虫啶和环氧虫啶的结构式Scheme 1 Structural fomulas of NTN32692, paichongding and cycloxaprid
基于上述研究,本文继续对八元氧桥环结构进行改造,将苯环直接和咪唑环相连,设计合成了15 个N-苯基八元氧桥环新烟碱化合物,探索该类结构衍生物对吡虫啉的增效活性。目标化合物的设计如图式2,合成路线如图式3。
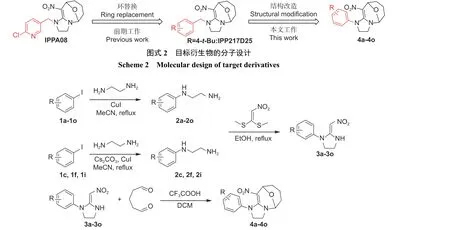
图式 3 目标衍生物4a~4o 的合成路线Scheme 3 Synthetic procedure for the target derivatives 4a-4o
1 实验部分
1.1 仪器与试剂
Buchi Melting Point B-450 熔点仪(未校正);Bruker AM-400 MHz 核磁共振分析仪 (以CDCl3或DMSO-d6为溶剂,TMS 为内标); MicroMass GCT CA055 质谱仪 (ESI 源)。所有的试剂和溶剂均为市售分析纯并直接使用。对照药剂IPP217D25 参照文献合成及纯化,99% 吡虫啉 (imidacloprid) 原药,购自Sigma-Aldrich 公司。
1.2 化合物的合成
1.2.1 中间体3 的合成 参考文献方法[22]合成。
(E)-2-(硝基亚甲基)-1-苯基咪唑烷 (3a) 的合成:室温下,将碘苯1a (5 mmol) 和无水乙二胺 (1.5 g, 25 mmol) 溶于15 mL 乙腈中,加入碘化亚铜 (0.1 g, 0.5 mmol),加热回流8 h,薄层层析 (V(二氯甲烷) :V(甲醇) = 20 : 1) 监测反应。反应完成后,冷却至室温,加入水 (20 mL) 并用二氯甲烷 (30 mL × 3) 萃取,合并有机相,干燥后浓缩得N-苯基乙二胺的粗产物2a,直接用于下一步反应。将粗产物2a 溶于25 mL 无水乙醇中,加入1,1-二硫甲基-2-亚硝基乙烯 (0.495 g, 3 mmol),加热至回流2 h;反应结束后,减压下除去溶剂,将残留物溶于10 mL 乙酸乙酯中,超声后大量固体析出,抽滤,滤饼用少量乙酸乙酯洗涤,烘干后得白色固体3a,收率65.1%;1H NMR (400 MHz, CDCl3)δ8.94 (s, 1H), 7.44-7.40 (m, 2H), 7.35-7.29 (m, 1H), 7.24-7.20(m, 2H), 6.46 (s, 1H), 4.08-4.03 (m, 2H), 3.95-3.90 (m, 2H).13C NMR (100 MHz, CDCl3)δ158.70, 137.72, 130.03, 127.99,125.07, 97.94, 51.49, 42.63.
(E)-1-(4-叔丁基苯基)-2-(硝基亚甲基) 咪唑烷 (3b) 合成方法同3a,白色固体,收率70.1%;1H NMR (400 MHz,CDCl3)δ8.89 (s, 1H), 7.47-7.37 (m, 2H), 7.17-7.11 (m, 2H),6.44 (s, 1H), 4.06-4.01 (m, 2H), 3.95-3.89 (m, 2H), 1.32 (s,9H).13C NMR (100 MHz, CDCl3)δ159.05, 151.54, 134.96,127.03, 124.95, 98.07, 51.64, 42.75, 34.86, 31.37.
(E)-1-(3-氯苯基)-2-(硝基亚甲基) 咪唑烷 (3d) 合成方法同3a,白色固体,收率69.8%;1H NMR (400 MHz, CDCl3)δ8.97 (s, 1H), 7.37 (t,J= 8.0 Hz, 1H), 7.31 (ddd,J= 8.0, 2.0,1.2 Hz, 1H), 7.24 (t,J= 2.0 Hz, 1H), 7.16-7.13 (m, 1H), 6.50(s, 1H), 4.07-4.03 (m, 2H), 3.96-3.91 (m, 2H).13C NMR (100 MHz, CDCl3)δ158.32, 139.06, 135.69, 131.02, 128.06,125.06, 123.06, 97.98, 51.32, 42.57.
(E)-1-(4-氯苯基)-2-(硝基亚甲基) 咪唑烷 (3e) 合成方法同3a,黄色固体,收率62.7%;1H NMR (400 MHz, CDCl3)δ8.93 (s, 1H), 7.43-7.37 (m, 2H), 7.21-7.15 (m, 2H), 6.43 (s,1H), 4.05-4.00 (m, 2H), 3.95-3.91 (m, 2H).13C NMR (100 MHz, CDCl3)δ158.49, 136.34, 133.64, 130.25, 126.33, 97.86,51.44, 42.60.
(E)-1-(3-氟苯基)-2-(硝基亚甲基) 咪唑烷 (3g) 合成方法同3a,淡黄色固体,收率76.9%;1H NMR (400 MHz, CDCl3)δ8.96 (s, 1H), 7.39 (td,J= 8.2, 6.4 Hz, 1H), 7.09-6.91 (m,3H), 6.51 (s, 1H), 4.04 (dd,J= 9.6, 7.0 Hz, 2H), 3.93 (dd,J=9.6, 7.0 Hz, 2H).13C NMR (100 MHz, CDCl3)δ163.15 (d,J=248.0 Hz), 158.22, 139.34 (d,J= 9.7 Hz), 131.30 (d,J= 9.3 Hz), 120.42 (d,J= 3.3 Hz), 114.79 (d,J= 21.0 Hz), 112.15 (d,J= 23.5 Hz), 97.93, 51.27, 42.57.
(E)-1-(4-氟苯基)-2-(硝基亚甲基) 咪唑烷 (3h) 合成方法同3a,白色固体,收率80.7%;1H NMR (400 MHz, CDCl3)δ8.88 (br, 1H), 7.24-7.19 (m, 2H), 7.14-7.09 (m, 2H), 6.32 (s,1H), 4.04-3.89 (m, 4H).13C NMR (100 MHz, CDCl3)δ161.76(d,J= 248.0 Hz), 158.97, 133.68 (d,J= 3.2 Hz), 127.49 (d,J=8.8 Hz), 117.07 (d,J= 22.8 Hz), 97.73, 51.83, 42.72.
(E)-1-(3-甲基苯基)-2-(硝基亚甲基) 咪唑烷 (3j) 合成方法同3a,黄色固体,收率76.1%;1H NMR (400 MHz, CDCl3)δ8.93 (s, 1H), 7.31 (t,J= 7.8 Hz, 1H), 7.14 (d,J= 7.6 Hz,1H), 7.03-6.99 (m, 2H), 6.47 (s, 1H), 4.06-4.00 (m, 2H), 3.94-3.90 (m, 2H), 2.37 (s, 3H).13C NMR (100 MHz, CDCl3)δ158.97, 140.44, 137.19, 129.99, 129.02, 125.83, 122.24, 98.21,51.71, 42.77, 21.54.
(E)-1-(4-甲基苯基)-2-(硝基亚甲基) 咪唑烷 (3k) 合成方法同3a,黄色固体,收率67.1%;1H NMR (400 MHz, CDCl3)δ8.91 (s, 1H), 7.23 (d,J= 8.0 Hz, 2H), 7.13-7.09 (m, 2H),6.43 (s, 1H), 4.05-4.00 (m, 2H), 3.95-3.88 (m, 2H), 2.37 (s,3H).13C NMR (101 MHz, CDCl3)δ158.96, 138.29, 134.98,130.61, 125.09, 97.95, 51.66, 42.64, 21.12.
(E)-1-(3-三氟甲基苯基)-2-(硝基亚甲基) 咪唑烷 (3l) 合成方法同3a,白色固体,收率61.5%;1H NMR (400 MHz,CDCl3)δ8.98 (s, 1H), 7.60-7.56 (m, 2H), 7.50-7.45 (m, 2H),6.43 (s, 1H), 4.11-4.07 (m, 2H), 3.99-3.93 (m, 2H).13C NMR(100 MHz, CDCl3)δ158.33, 138.62, 132.84 (q,J= 32.7 Hz),130.79, 128.44, 124.67 (q,J= 271.0 Hz), 124.55 (q,J= 3.8 Hz), 121.69 (q,J= 3.8 Hz), 97.80, 51.37, 42.64.
(E)-1-(4-三氟甲基苯基)-2-(硝基亚甲基) 咪唑烷 (3m) 合成方法同3a,白色固体,收率58.6%;1H NMR (400 MHz,CDCl3)δ9.03 (s, 1H), 7.70 (d,J= 8.2 Hz, 2H), 7.37 (d,J= 8.2 Hz, 2H), 6.56 (s, 1H), 4.13-4.08 (m, 2H), 3.98-3.94 (m, 2H).13C NMR (100 MHz, CDCl3)δ157.92, 141.25, 129.59 (q,J=33.0 Hz), 127.25 (q,J= 3.7 Hz), 124.46, 122.25 (q,J= 270.7 Hz), 98.09, 51.05, 42.55.
(E)-3-(2-(硝基亚甲基) 咪唑烷-1-基)苯甲腈 (3n) 合成方法同3a,白色固体,收率63.7%;1H NMR (400 MHz, CDCl3)δ9.00 (s, 1H), 7.64-7.50 (m, 4H), 6.48 (s, 1H), 4.10-4.06 (m,2H), 3.99-3.94 (m, 2H).
(E)-4-(2-(硝基亚甲基) 咪唑烷-1-基)苯甲腈 (3o) 合成方法同3a,淡黄色固体,收率80.4%;1H NMR (400 MHz,CDCl3)δ9.09 (s, 1H), 7.78-7.69 (m, 2H), 7.39-7.32 (m, 2H),6.66 (s, 1H), 4.16-4.08 (m, 2H), 3.98-3.94 (m, 2H).
(E)-1-(2-氯苯基)-2-(硝基亚甲基) 咪唑烷 (3c) 的合成:室温条件下,将2-氯碘苯1c (5 mmol) 和无水乙二胺 (1.5 g,25 mmol) 溶于15 mL 乙腈中,加入碘化亚铜 (0.1 g, 0.5 mmol)和碳酸铯 (1.63 g, 5 mmol),加热回流8 h,薄层色谱 (V(二氯甲烷) :V(甲醇) = 20:1) 监测至反应完成。冷却到室温,加入水 (20 mL) 并用二氯甲烷 (30 mL × 3) 萃取,合并有机相,干燥浓缩得N-2-氯-苯基乙二胺粗产物2c,直接用于下一步反应。将1,1-二硫甲基-2-硝基乙烯 (0.495 g, 3 mmol)溶于15 mL 无水乙醇中,回流15 min, 然后缓慢滴加化合物2c 的20 mL无水乙醇溶液,继续反应;反应结束后,减压除去溶剂,残余物溶于10 mL 乙酸乙酯中,超声后大量固体析出,抽滤,滤饼用少量乙酸乙酯洗涤,烘干后得淡黄色固体3c,收率52.3%;1H NMR (400 MHz, CDCl3)δ8.81 (s, 1H), 7.54-7.50 (m, 1H), 7.40-7.30 (m, 3H), 6.07 (s,1H), 4.18 (q,J= 8.8 Hz, 1H), 4.04-3.94 (m, 2H), 3.83 (q,J=9.0 Hz, 1H).13C NMR (100 MHz, CDCl3)δ159.48, 134.43,133.23, 131.22, 130.77, 130.02, 128.59, 97.76, 50.44, 43.17.
(E)-1-(2-氟苯基)-2-(硝基亚甲基) 咪唑烷 (3f) 合成方法同3c,淡黄色固体,收率59.7%;1H NMR (400 MHz,CDCl3)δ8.87 (s, 1H), 7.40-7.35 (m, 1H), 7.30 (td,J= 8.0, 2.0 Hz, 1H), 7.24-7.17 (m, 2H), 6.24 (s, 1H), 4.03-3.95 (m, 4H).13C NMR (100 MHz, CDCl3)δ159.52 (d,J= 251.3 Hz),159.35, 130.68 (d,J= 7.9 Hz), 129.05, 125.41 (d,J= 4.0 Hz),124.89 (d,J= 12.0 Hz), 117.54 (d,J= 19.3 Hz), 97.70, 50.90,43.08.
(E)-1-(2-甲基苯基)-2-(硝基亚甲基) 咪唑烷 (3i) 合成方法同3c,淡黄色固体,收率59.3%;1H NMR (400 MHz,CDCl3)δ8.75 (s, 1H), 7.33-7.28 (m, 3H), 7.15 (d,J= 7.6 Hz,1H), 6.03 (s, 1H), 4.07-3.84 (m, 4H), 2.25 (s, 3H).13C NMR(100 MHz, CDCl3)δ159.56, 136.40, 135.58, 131.85, 129.60,127.88, 127.75, 97.62, 51.15, 43.03, 17.45.
1.2.2 目标化合物的合成 将中间体3 (1.5 mmol)溶于15 mL 二氯甲烷中,加入三氟乙酸 (4.5 mmol)搅拌使固体完全溶解,然后缓慢滴加质量分数为50%的戊二醛(2mmol)水溶液,室温下反应2 h,薄层色谱 (V(二氯甲烷) :V(甲醇) = 20 : 1) 监测反应完成后,用饱和NaHCO3水溶液调节pH 到中性,二氯甲烷 (15 mL × 2) 萃取,合并有机相,干燥浓缩,残余物用乙酸乙酯重结晶,干燥后得到目标产物4。目标化合物的性质及相关谱图数据如下。
10-硝基-1-苯基-1,2,3,5,6,7,8,9-八氢-5,9-环氧咪唑并[1,2-a] 氮杂环辛烯 (4a):黄色固体,收率81.4%;m.p.164.8-165.6 ℃;1H NMR (400 MHz, CDCl3)δ7.36-7.29 (m,2H), 7.19-7.13 (m, 1H), 7.13-7.09 (m, 2H), 5.40 (d,J= 4.2 Hz,1H), 5.06 (s, 1H), 4.33 (q,J= 9.8 Hz, 1H), 4.09-4.03 (m, 1H),3.76-3.62 (m, 2H), 2.11 (d,J= 13.8 Hz, 1H), 2.00-1.88 (m,2H), 1.80-1.76 (m, 1H), 1.72-1.65 (m, 2H).13C NMR (100 MHz, CDCl3)δ151.94, 142.88, 128.94, 125.64, 121.10,107.17, 82.84, 69.39, 52.88, 45.95, 29.91, 27.15, 15.07.HRMS(ESI) C15H17N3O3(M + H)+计算值288.1343, 测试值288.1334。
1-(4-叔丁基苯基)-10-硝基-1,2,3,5,6,7,8,9-八氢-5,9-环氧咪唑并[1,2-a]氮杂环辛烯 (4b):黄色固体,收率81.6%;m.p.187.5-188.2 ℃;1H NMR (400 MHz, CDCl3)δ7.33-7.29(m, 2H), 7.04-7.00 (m, 2H), 5.40 (dd,J= 4.0, 1.8 Hz, 1H),5.05 (t,J= 2.4 Hz, 1H), 4.30 (q,J= 9.8 Hz, 1H), 4.13-4.01 (m,1H), 3.72-3.61 (m, 2H), 2.13-2.10 (d,J= 13.8 Hz, 1H), 1.98-1.90 (m, 2H), 1.80-1.74 (m, 1H), 1.72-1.66 (m, 2H), 1.29 (s,9H).13C NMR (100 MHz, CDCl3)δ152.02, 148.30, 140.27,125.76, 120.58, 107.08, 82.83, 69.41, 52.94, 45.94, 34.51,31.38, 29.87, 27.22, 15.07.HRMS (ESI):C19H25N3O3(M +H)+计算值344.1969, 测试值344.1958。
1-(2-氯苯基)-10-硝基-1,2,3,5,6,7,8,9-八氢-5,9-环氧咪唑并[1,2-a] 氮杂环辛烯 (4c):淡黄色固体,收率68.5%;m.p.173.5-174.5 ℃;1H NMR (400 MHz, CDCl3)δ7.47-7.39(m, 1H), 7.25-7.16 (m, 3H), 5.37-5.31 (m, 1H), 5.08 (q,J=2.4, 1.8 Hz, 1H), 4.47-4.45 (m, 0.7H), 4.21-4.18 (m, 0.3H),3.90-3.86 (m, 0.3H), 3.80-3.68 (m, 2.7H), 2.06-1.88 (m, 3H),1.84-1.63 (m, 3H).13C NMR (100 MHz, CDCl3)δ153.78,141.19, 140.93, 130.40, 130.29, 129.97, 128.18, 128.06,127.60, 127.56, 126.08, 124.73, 106.95, 82.71, 82.24, 69.07,68.89, 52.34, 52.12, 46.53, 46.31, 29.98, 29.35, 27.87, 27.04,15.08, 14.98.HRMS (ESI):C15H16N3O335Cl (M + H)+计算值322.0953, 测试值322.0944; C15H16N3O337Cl (M + H)+计算值324.0923, 测试值324.0912。
1-(3-氯苯基)-10-硝基-1,2,3,5,6,7,8,9-八氢-5,9-环氧咪唑并[1,2-a]氮杂环辛烯 (4d):淡黄色固体,收率68.8%;m.p.173.9-174.7 ℃;1H NMR (400 MHz, CDCl3)δ7.24-7.20 (m,1H), 7.15-7.11 (m, 1H), 7.09 (t,J= 2.0 Hz, 1H), 6.99 (ddd,J=8.0, 2.2, 1.0 Hz, 1H), 5.39 (dd,J= 4.4, 1.8 Hz, 1H), 5.06 (d,J=2.8 Hz, 1H), 4.31 (q,J= 9.8 Hz, 1H), 4.12-3.96 (m, 1H), 3.79-3.62 (m, 2H), 2.13-2.06 (m, 1H), 2.01-1.90 (m, 2H), 1.80-1.75(m, 1H), 1.72-1.62 (m, 2H).13C NMR (100 MHz, CDCl3)δ151.66, 144.07, 134.60, 129.80, 125.73, 121.52, 119.47,107.45, 82.77, 69.27, 52.86, 45.84, 29.90, 27.11, 15.03.HRMS(ESI):C15H16N3O335Cl (M + H)+计算值322.0953, 测试值322.0945; C15H16N3O337Cl (M + H)+计算值324.0923, 测试值324.0913。
1-(4-氯苯基)-10-硝基-1,2,3,5,6,7,8,9-八氢-5,9-环氧咪唑并[1,2-a] 氮杂环辛烯 (4e):淡黄色固体,收率62.3%;m.p.181.5-182.3 ℃;1H NMR (400 MHz, CDCl3)δ7.30-7.26(m, 2H), 7.08-6.97 (m, 2H), 5.38 (d,J= 4.4 Hz, 1H), 5.06 (s,1H), 4.31 (q,J= 9.8 Hz, 1H), 4.05-3.98 (m, 1H), 3.79-3.60 (m,2H), 2.11-2.07 (m, 1H), 1.99-1.87 (m, 2H), 1.80-1.75 (m, 1H),1.72-1.63 (m, 2H).13C NMR (100 MHz, CDCl3)δ151.84,141.46, 130.89, 129.03, 122.40, 107.29, 82.83, 69.31, 52.84,45.90, 29.88, 27.09, 15.05.HRMS (ESI):C15H16N3O335Cl(M + H)+计算值322.0953, 测试值322.0945; C15H16N3O337Cl(M + H)+计算值324.0923, 测试值324.0913。
1-(2-氟苯基)-10-硝基-1,2,3,5,6,7,8,9-八氢-5,9-环氧咪唑并[1,2-a]氮杂环辛烯 (4f):黄色固体,收率68.8%;m.p.167.6-168.0 ℃;1H NMR (400 MHz, CDCl3)δ7.22-7.05 (m,4H), 5.35 (dd,J= 4.0, 2.0 Hz, 1H), 5.07 (t,J= 2.4 Hz, 1H),4.27 (br, 1H), 3.93 (br, 1H), 3.78-3.66 (m, 2H), 2.09-2.01 (m,1H), 2.00-1.88 (m, 2H), 1.82-1.76 (m, 1H), 1.72-1.63 (m, 2H).13C NMR (100 MHz, CDCl3)δ157.37 (d,J= 246.4 Hz),153.05, 131.10, 130.98 (d,J= 11.7 Hz), 127.76 (d,J= 7.8 Hz), 124.33 (d,J= 3.6 Hz), 116.28 (d,J= 19.4 Hz), 107.03,82.57, 69.10, 52.53, 46.19, 29.74, 27.31, 14.91.HRMS(ESI):C15H16N3O3F (M + H)+计算值306.1248, 测试值306.1239.
1-(3-氟苯基)-10-硝基-1,2,3,5,6,7,8,9-八氢-5,9-环氧咪唑并[1,2-a]氮杂环辛烯 (4g):淡黄色固体,收率72.1%;m.p.166.1-166.7 ℃;1H NMR (400 MHz, CDCl3)δ7.30-7.22 (m,1H), 6.92-6.78 (m, 3H), 5.38 (dd,J= 4.2, 1.8 Hz, 1H), 5.06 (d,J= 2.6 Hz, 1H), 4.29 (q,J= 9.8 Hz, 1H), 4.03 (td,J= 9.6, 5.8 Hz, 1H), 3.76-3.63 (m, 2H), 2.11-2.06 (m, 1H), 2.01-1.88 (m,2H), 1.80-1.75 (m, 1H), 1.71-1.63 (m, 2H).13C NMR (100 MHz, CDCl3)δ164.08 (d,J= 245.0 Hz), 151.75, 144.48 (d,J= 10.1 Hz), 130.02 (d,J= 9.4 Hz), 116.95 (d,J= 3.1 Hz),112.57 (d,J= 21.0 Hz), 108.91 (d,J= 24.0 Hz), 107.41,82.73, 69.27, 52.84, 45.83, 29.82, 27.16, 15.01.HRMS(ESI):C15H16N3O3F (M + H)+计算值306.1248, 测试值306.1239。
1-(4-氟苯基)-10-硝基-1,2,3,5,6,7,8,9-八氢-5,9-环氧咪唑并[1,2-a]氮杂环辛烯 (4h):淡黄色固体,收率88.4%;m.p.185.7-186.4 ℃;1H NMR (400 MHz, CDCl3)δ7.09-7.05 (m,2H), 7.02-6.97 (m, 2H), 5.39-5.34 (m, 1H), 5.05 (t,J= 2.4 Hz,1H), 4.27 (q,J= 9.8 Hz, 1H), 3.99 (td,J= 9.8, 6.0 Hz, 1H),3.77-3.62 (m, 2H), 2.10-2.05 (m, 1H), 1.99-1.87 (m, 2H), 1.80-1.74 (m, 1H), 1.71-1.64 (m, 2H).13C NMR (100 MHz, CDCl3)δ161.39 (d,J= 243.9 Hz), 152.34, 139.18 (d,J= 3.2 Hz),123.00 (d,J= 8.3 Hz), 115.90 (d,J= 22.9 Hz), 106.91, 82.77,69.29, 53.10, 45.93, 29.80, 27.11, 15.03.HRMS (ESI):C15H16N3O3F (M + H)+计算值306.1248, 测试值306.1239。
1-(2-甲基苯基)-10-硝基-1,2,3,5,6,7,8,9-八氢-5,9-环氧咪唑并[1,2-a] 氮杂环辛烯 (4i):白色固体,收率66.4%;m.p.163.0-163.9 ℃;1H NMR (400 MHz, CDCl3)δ7.26-7.21(m, 1H), 7.18-7.03 (m, 3H), 5.40-5.28 (m, 1H), 5.10-5.07 (m,1H), 4.31-4.23 (m, 0.6H), 4.10-4.08 (m, 0.4H), 3.88-3.62 (m,3H), 2.41 (s, 1.8H), 2.31 (s, 1.2H), 2.11-1.62 (m, 6H).13C NMR (100 MHz, CDCl3)δ155.12, 143.10, 133.87, 131.23,127.35, 127.28, 126.81, 123.61, 122.87, 82.79, 82.20, 69.17,69.07, 52.55, 52.46, 46.71, 46.15, 30.13, 29.27, 28.10, 26.83,18.60, 18.45, 15.16, 15.05.HRMS (ESI):C16H19N3O3(M +H)+计算值302.1499, 测试值302.1491。
1-(3-甲基苯基)-10-硝基-1,2,3,5,6,7,8,9-八氢-5,9-环氧咪唑并[1,2-a]氮杂环辛烯 (4j):淡黄色固体,收率70.9%;m.p.175.8-176.5 ℃;1H NMR (400 MHz, CDCl3)δ7.20 (dd,J= 8.6, 7.6 Hz, 1H), 6.97 (d,J= 7.6 Hz, 1H), 6.92 (dd,J= 4.2, 2.0 Hz, 2H), 5.40 (dd,J= 4.2, 1.8 Hz, 1H), 5.06 (t,J=2.6 Hz, 1H), 4.32 (q,J= 9.8 Hz, 1H), 4.07-3.98 (m, 1H), 3.76-3.60 (m, 2H), 2.33 (s, 3H), 2.13-2.10 (m, 1H), 1.97-1.91 (m,2H), 1.81-1.74 (m, 1H), 1.71-1.66 (m, 2H).13C NMR (100 MHz, CDCl3)δ152.06, 142.88, 138.88, 128.72, 126.60,121.82, 118.29, 107.08, 82.83, 69.40, 52.98, 45.94, 29.93,27.12, 21.54, 15.07.HRMS (ESI):C16H19N3O3(M + H)+计算值302.1499, 测试值302.1490。
1-(4-甲基苯基)-10-硝基-1,2,3,5,6,7,8,9-八氢-5,9-环氧咪唑并[1,2-a] 氮杂环辛烯 (4k):黄色固体,收率54.2%;m.p.172.7-173.5 ℃;1H NMR (400 MHz, CDCl3)δ7.12 (d,J= 8.2 Hz, 2H), 7.00 (d,J= 8.2 Hz, 2H), 5.39 (d,J= 4.2 Hz,1H), 5.05 (s, 1H), 4.29 (q,J= 9.8 Hz, 1H), 4.05-3.99 (m, 1H),3.75-3.62 (m, 2H), 2.31 (s, 3H), 2.12-2.09 (m, 1H), 1.96-1.90(m, 2H), 1.79-1.75 (m, 1H), 1.71-1.65 (m, 2H).13C NMR (100 MHz, CDCl3)δ152.18, 140.40, 135.42, 129.55, 120.99,106.94, 82.86, 69.41, 52.96, 45.99, 29.89, 27.10, 21.05, 15.07.HRMS (ESI) C16H19N3O3(M + H)+计算值302.1499, 测试值302.1490。
10-硝基-1-(3-(三氟甲基)苯基)-1,2,3,5,6,7,8,9-八氢-5,9-环氧咪唑并[1,2-a] 氮杂环辛烯 (4l):白色固体,收率56.3%;m.p.172.4-173.4 ℃;1H NMR (400 MHz, CDCl3)δ7.45-7.38 (m, 2H), 7.32 (d,J= 2.4 Hz, 1H), 7.25-7.23 (m, 1H),5.39 (dd,J= 4.2, 1.8 Hz, 1H), 5.08 (t,J= 2.4 Hz, 1H), 4.36 (q,J= 9.8 Hz, 1H), 4.06 (td,J= 9.6, 5.6 Hz, 1H), 3.80-3.65 (m,2H), 2.12-2.05 (m, 1H), 2.02-1.89 (m, 2H), 1.82-1.76 (m, 1H),1.73-1.63 (m, 2H).13C NMR (100 MHz, CDCl3)δ151.57,143.44, 131.01 (q,J= 32.3 Hz), 129.36, 125.11 (q,J= 270.9 Hz), 124.35, 122.07 (q,J= 3.8 Hz), 117.89 (q,J= 3.8 Hz),107.57, 82.78, 69.24, 52.81, 45.81, 29.87, 27.10, 15.01.HRMS(ESI):C16H16N3O3F3(M + H)+计算值356.1217, 测试值356.1205。
10-硝基-1-(4-(三氟甲基)苯基)-1,2,3,5,6,7,8,9-八氢-5,9-环氧咪唑并[1,2-a] 氮杂环辛烯 (4m):黄色固体,收率73.2%;m.p.187.4-188.1 ℃;1H NMR (400 MHz, CDCl3)δ7.55 (d,J= 8.4 Hz, 2H), 7.14 (d,J= 8.4 Hz, 2H), 5.38 (d,J= 4.4 Hz, 1H), 5.08 (s, 1H), 4.34 (q,J= 9.8 Hz, 1H), 4.10-4.03 (m, 1H), 3.77-3.64 (m, 2H), 2.13-2.04 (m, 1H), 2.00-1.88(m, 2H), 1.81-1.76 (m, 1H), 1.71-1.60 (m, 2H).13C NMR (100 MHz, CDCl3)δ151.34, 145.71, 127.23 (q,J= 32.6 Hz),126.01 (q,J= 3.8 Hz), 124.00 (q,J= 270.3 Hz), 120.93,107.82, 82.77, 69.26, 52.60, 45.79, 29.80, 27.15, 15.00.HRMS(ESI):C16H16N3O3F3(M + H)+计算值356.1217, 测试值356.1204。
1-(3-氰基苯基)-10-硝基-1,2,3,5,6,7,8,9-八氢-5,9-环氧咪唑并[1,2-a]氮杂环辛烯 (4n):黄色固体,收率80.1%;m.p.179.8-180.7 ℃;1H NMR (400 MHz, CDCl3)δ7.45-7.39 (m,2H), 7.35-7.33 (m, 1H), 7.30-7.28 (m, 1H), 5.42-5.36 (m, 1H),5.09 (d,J= 2.4 Hz, 1H), 4.35 (q,J= 9.8 Hz, 1H), 4.05 (td,J=9.6, 5.6 Hz, 1H), 3.82-3.67 (m, 2H), 2.13-2.06 (m, 1H), 2.03-1.89 (m, 2H), 1.82-1.77 (m, 1H), 1.74-1.62 (m, 2H).13C NMR(100 MHz, CDCl3)δ151.31, 143.74, 129.72, 128.82, 125.60,124.32, 118.27, 113.00, 107.76, 82.77, 69.19, 52.71, 45.77,29.87, 27.09, 15.01.HRMS (ESI):C16H16N4O3(M + H)+计算值313.1295, 测试值313.1285。
1-(4-氰基苯基)-10-硝基-1,2,3,5,6,7,8,9-八氢-5,9-环氧咪唑并[1,2-a]氮杂环辛烯 (4o):淡黄色固体,收率70.5%;m.p.185.1-186.1 ℃;1H NMR (400 MHz, CDCl3)δ7.64-7.55(m, 2H), 7.14-7.08 (m, 2H), 5.40-5.37 (m, 1H), 5.10 (s, 1H),4.37 (q,J= 9.8 Hz, 1H), 4.13-4.07 (m, 1H), 3.81-3.67 (m, 2H),2.12-1.90 (m, 3H), 1.83-1.63 (m, 3H).13C NMR (100 MHz,CDCl3)δ150.78, 146.34, 132.81, 121.17, 118.62, 108.20,82.80, 69.23, 52.37, 45.74, 29.87, 27.11, 15.00.HRMS(ESI):C16H16N4O3(M + H)+计算值313.1295, 测试值313.1284。
1.3 目标化合物增效活性测试
以上海晓明检测技术服务有限公司生测药效实验室提供的苜蓿蚜Aphis craccivora为测试对象,采用叶片浸渍法[23]测定。准确称取适量的目标化合物和吡虫啉原药,分别溶于1 mL 二甲基亚砜中,加入含有体积分数0.1% Triton X-100 的蒸馏水,制备成质量浓度为100 mg/L 的目标化合物和吡虫啉母液。然后根据测试要求用含有0.1%Triton X-100 的蒸馏水稀释,制备一系列浓度药液。将苜蓿蚜成虫饥饿1 h 后接入新鲜蚕豆苗上,控制每颗蚕豆苗上15~25 只成虫,然后将带虫豆苗在上述配制的药液中浸泡5 s。重复3 次。浸药完成后吸去多余药液,转移到海绵上。每个浓度平行测定3 次,空白对照用含有1 mL 二甲基亚砜和0.1% Triton X-100 的水溶液处理。将试虫置于(24 ± 1) ℃、相对湿度50%~60% 条件下,48 h后检查并统计成虫的死亡率。
2 结果与分析
2.1 目标化合物的合成
目标化合物以取代碘苯1 和乙二胺为起始原料,首先在碘化亚铜的催化下在乙腈中进行回流反应,以较高收率得到中间体2,其中邻位取代的碘苯1c、1f 和1i 由于位阻较大,反应发生较慢,即使延长反应时间后原料仍有大量剩余,需要加入碳酸铯作为碱促进反应从而提高收率。该中间体纯度较高,即便含有少量乙二胺,由于副反应生成的硝基咪唑水溶性好,能通过萃取除去,故可直接用于下一步反应。随后中间体2 和1,1-二硫甲基-2-硝基乙烯在乙醇中回流,合成关键中间体3,中间体3 与戊二醛水溶液在三氟乙酸催化下,以二氯甲烷为溶剂,经过双曼尼希缩合反应生成八元氧桥环目标化合物4,该步反应收率较高,部分底物反应收率偏低的原因是产物在乙酸乙酯中重结晶过程中发生了损耗。
2.2 目标化合物的增效活性
首先测试了目标化合物4a~4o 在100 mg/L 下单独使用时对苜蓿蚜的致死率,结果(表S1)表明其对苜蓿蚜无活性。随后测试了吡虫啉对苜蓿蚜的活性,根据毒力标准曲线计算出LC30值为0.49 mg/L,LC50值为0.86 mg/L。为了比较化合物4a~4o 的增效活性,测试了不同质量浓度下的目标化合物与0.5 mg/L (接近LC30值的浓度)的吡虫啉联用对苜蓿蚜的致死率,以IPP217D25 作为对照药剂,测定结果见表1。

表1 不同质量浓度目标化合物4a~4o 与0.5 mg/L 吡虫啉联用对苜蓿蚜的杀虫活性aTable 1 Insecticidal activities of different concentrations of target compounds 4a-4o combined with 0.5 mg/L imidacloprid against A. craccivoraa
通过比较发现,无取代的化合物4a 在1、0.5和0.25 mg/L 时对吡虫啉表现出跟IPP217D25 相当的增效作用,而4 位叔丁基取代的化合物4b 在上述浓度下基本没有增效作用。对比化合物4c~4o与吡虫啉联用时对苜蓿蚜的致死率,发现在苯环上引入取代基的化合物增效活性会减弱,部分化合物在低浓度下没有增效作用,仅4-三氟甲基取代的化合物4m 表现出跟IPP217D25 相当的增效作用。在我们前期研究中,苯环和咪唑环由亚甲基连接的八元氧桥环结构的构效关系表明,苯环4 位有较大空间位阻基团取代的化合物增效活性较好 (如4-叔丁基取代的化合物IPP217D25),苯环上无取代和4-三氟甲基取代的化合物活性低于IPP217D25,而将苯环和咪唑环直接连接后的八元氧桥环结构化合物,苯环上无取代4a 和4-三氟甲基取代的化合物4m 的增效活性与IPP217D25相当,而引入其他取代基的大部分化合物增效活性降低,且4-叔丁基取代的化合物4b 在测试浓度下无增效作用,表明两类结构的构效关系不一致。
进一步测试了化合物4a、4m 和IPP217D25与吡虫啉联用时对苜蓿蚜的相对应LC50值,与单独使用吡虫啉的LC50值 (0.86 mg/L) 比较,并计算联用后的增效倍数。结果见表2。当化合物4a 和4m 的联用质量浓度为1 mg/L 时,可将吡虫啉的LC50值分别降低至0.25 mg/L 和0.24 mg/L,增效倍数分别为3.44 和3.58,稍弱于IPP217D25(使吡虫啉的LC50值降低至0.21 mg/L,增效倍数为4.09);当化合物4a 和4m 的联用质量浓度为0.5 mg/L 时,增效倍数与IPP217D25 相当。
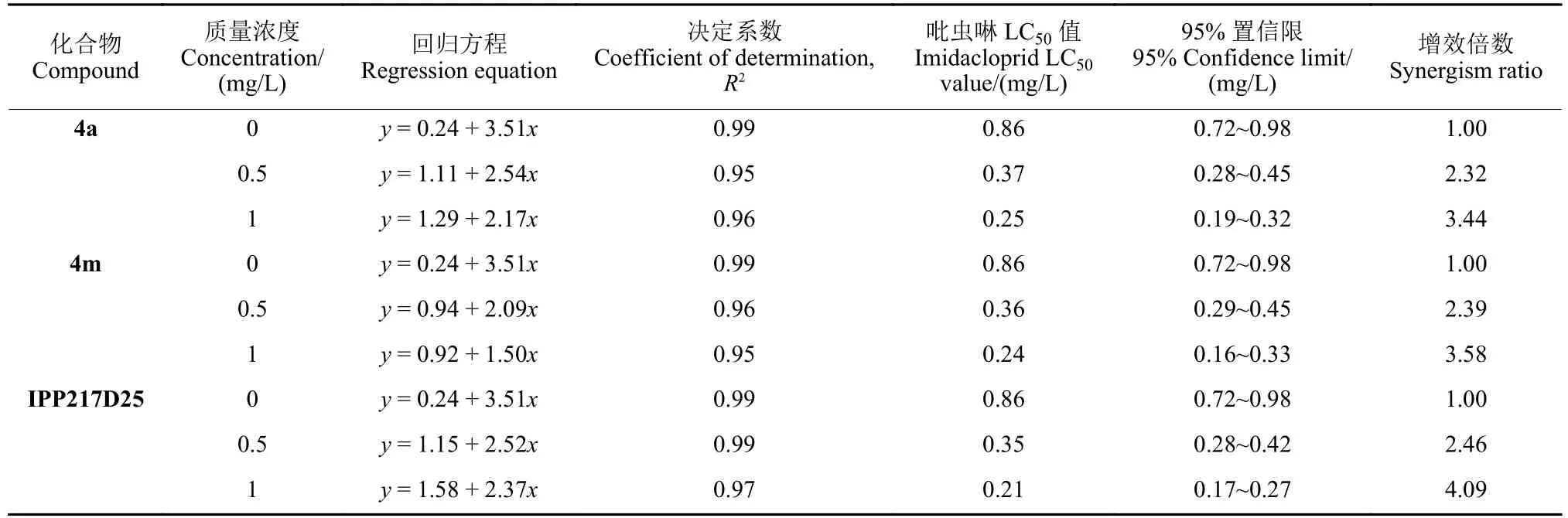
表2 化合物4a、4m 和IPP217D25 对吡虫啉对苜蓿蚜毒力的增效作用aTable 2 Synergistic effects of compound 4a, 4m and IPP217D25 on imidacloprid toxicity against A. craccivoraa
3 结论
本研究对前期发现的对新烟碱类杀虫剂具有特异性增效活性的八元氧桥环结构进行衍生,将苯环和咪唑环直接相连,设计合成了15 个N-苯基八元氧桥环新烟碱衍生物,并测试了其和吡虫啉联用时对苜蓿蚜的致死率,以此评估化合物的增效活性。测试结果表明:大部分目标化合物在1 mg/L质量浓度下与吡虫啉联用时表现出较好的增效活性,部分化合物的增效活性与IPP217D25相当;苯环上无取代的化合物4a和苯环4-三氟甲基取代的4m增效活性最好,在苯环上引入其他取代基的化合物增效活性降低;当化合物4a和4m的联用质量浓度为1 mg/L 时,可使吡虫啉对苜蓿蚜的LC50值分别降低为0.25 mg/L 和0.24 mg/L,增效倍数分别为3.44 和3.58。4a和4m可作为候选化合物进一步研究其增效活性。

