大豆蛋白强化羧甲基纤维素钠复合油凝胶的性能
崔梦琦,单冠程,孙若涵,田 波,隋晓楠
(东北农业大学食品学院,黑龙江 哈尔滨 150030)
油凝胶是一种半固态油,它是通过将液态油固定在由凝胶剂和稳定剂形成的三维网络中形成,能够降低脂肪迁移率、消除饱和及反式脂肪酸的危害。因此,油凝胶被视为传统固体脂肪的理想替代物,受到各领域研究人员的青睐。最常用的油凝胶化方法是将胶凝剂在高于熔点的温度下分散在油中,然后冷却使胶凝剂结晶或自组装形成三维网络结构固定油,常用的胶凝剂有结晶颗粒网络(脂肪醇[1]、植物蜡[2]等)、自组装体系(12-羟基硬脂酸[3]、卵磷脂[4]等)和聚合物网络(乙基纤维素[5])。然而,制备过程中的高温处理不仅对油中的热敏性成分降解,而且还会导致油的进一步氧化。此外,较高含量胶凝剂的添加也不利于其在食品中的应用[6]。
气凝胶模板法是制备油凝胶的一种间接方法,它是将聚合物预先水合以形成水凝胶,然后将其干燥获得聚合物网络骨架并将其作为吸油的多孔材料。以气凝胶为模板制备油凝胶只需要经过简单的物理吸附,这意味着它避免了剧烈的理化处理,可以更安全地负载油脂及营养物质。同时,气凝胶骨架具有较高的机械强度和高孔隙率等优异的结构性能,能够获得高吸油率和高强度的油凝胶。近年来,基于生物相容性的天然大分子如多糖、蛋白质等已被广泛研究用于构建气凝胶模板,而后通过物理吸附以得到固化油凝胶。Manzocco等[7]以κ-角叉菜胶气凝胶为模板,得到最大吸油量为80%的高强度油凝胶。Chen Kailun等[8]通过美拉德反应制备了海藻酸盐/大豆蛋白复合物气凝胶,然后将其浸入玉米油以获得具有优秀乳化能力和乳液稳定性的油凝胶。
羧甲基纤维素(carboxyl methyl cellulose,CMC)是一种阴离子长链多糖,其具有良好的凝胶性、生物相容性和稳定的内部网络结构。Tang Shuaishuai等[9]通过干热处理得到羧甲基纤维素钠(carboxy methyl cellulose-Na,CMC-Na)/卵清蛋白(egg white protein,EWP)共聚物,并研究了不同接枝率对EWP/CMC-Na气凝胶机械性能和载油性能的影响。Jaberi等[10]使用卵清蛋白和黄原胶复合物制备了高机械强度和高持油率的油凝胶。Le等[11]研究了黄原胶和β-乳球蛋白在静电吸引作用下诱导形成网络的凝胶化机制,发现黄原胶能提供凝胶组织框架,而β-乳球蛋白则作为交联剂参与网络的形成。综上,蛋白质和多糖可以通过相互作用聚合形成稳定的复合物,从而提高凝胶的力学性能。
本研究通过添加大豆蛋白球状颗粒包裹纤维素形成稳定的复合物以制备高弹性、高强度的脂肪模拟物,并探究不同蛋白添加量对CMC-Na油凝胶性能的影响。使用平均粒径、宏观和微观形态、红外光谱、吸油能力、持油能力和质构特性评价油凝胶,此外还对油凝胶的抑菌能力和氧化稳定性进行分析测定。本研究提出基于球状蛋白-长链纤维静电吸附结合制备油凝胶的方法,用以改善油凝胶性质,提高其强度和弹性,旨在为多糖-蛋白聚合物强化油凝胶及其进一步的应用提供有效的参考。
1 材料与方法
1.1 材料与试剂
大豆分离蛋白(soybean protein isolate,SPI)由实验室自制;CMC-Na(黏度1500~3100 mPa·s)上海麦克林公司;无水柠檬酸 上海阿拉丁生化科技股份有限公司;葵花籽油购自当地超市。
1.2 仪器与设备
SCIENTZ-18N/A冷冻干燥机 宁波新芝生物科技股份有限公司;TA.XT Plus C质构仪 英国Stable Micro Systems公司;Nicolet is50傅里叶变换红外光谱(Fourier transform infrared,FTIR)仪 赛默飞世尔科技(中国)有限公司;TM 4000台式扫描电子显微镜日本日立公司。
1.3 方法
1.3.1 CMC-Na/SPI复合溶液的制备
将CMC-Na溶解在去离子水中,质量分数为1.5%,1000 r/min磁力搅拌1 h,得到均匀的溶液,向溶液中加入SPI粉末制备不同质量比的CMC-Na/SPI溶液(1∶1、1∶2、1∶3、1∶4),然后向混合溶液中加入质量分数0.15%的柠檬酸,继续搅拌至完全溶解,得到复合溶液。
1.3.2 气凝胶制备
将样品溶液倒入内径13 mm、高15 mm的中空圆柱体中,在-20 ℃预冻5 h。在真空条件下(<5 Pa)于-58 ℃在冻干机中冷冻干燥24 h,制备气凝胶,将获得的气凝胶于150 ℃加热5 min以使CMC-Na气凝胶在柠檬酸的作用下交联,放置在干燥器中备用。
1.3.3 气凝胶密度测定
准确称量气凝胶样品的质量,并测定体积。根据式(1)计算其密度:
式中:m为气凝胶的质量/g;V为气凝胶的体积/cm3。
1.3.4 复合物平均粒径的测定
参考董亚博等[12]的方法,并稍作修改。测定前用溶液等pH值的去离子水将CMC-Na溶液和不同比例的CMC-Na/SPI溶液(1∶1、1∶2、1∶3、1∶4)稀释100 倍,以避免聚集。
1.3.5 气凝胶的微观形态
为了分析气凝胶的内部结构,将样品切成薄片,并将其由双面胶黏附在观察台上,将样品表面喷金后,使用扫描电子显微镜观察样品的微观形态。
1.3.6 FTIR测定
参考Huang Guo等[13]的方法,将SPI、CMC-Na和CMC-Na/SPI复合物的溶液冷冻干燥后充分研磨成粉末。在4000~500 cm-1的频率范围内进行扫描,扫描32 次,分辨率为4 cm-1。
1.3.7 吸油动力学分析
参考Khosravi等[14]方法,气凝胶底面接触葵花籽油开始计时,每隔2.5 s取出一次气凝胶,待表面葵花籽油滴完全滴落后,称质量,直至质量恒定。通过记录吸油过程中每个时刻油的质量,确定吸油量与时间的相关性。
1.3.8 吸油能力分析
准确称量气凝胶,然后浸入葵花籽油中。通常,在浸入30 s内,吸收过程达到平衡以形成油凝胶。吸收过程完成后,取出油凝胶,自然滴落30 s,去除表面多余的油,立即对油凝胶称质量。吸油量通过式(2)计算:
式中:m0为气凝胶的质量/g;m1为油凝胶的质量/g。
1.3.9 持油能力分析
参考Manzocco等[7]的方法,测定油凝胶的持油能力。将1.5 g油凝胶样品置于两块滤纸之间,然后放入50 mL离心管中,8000 r/min离心20 min。根据式(3)计算持油率:
式中:m1为离心前油凝胶的质量/g;m2为离心后油凝胶的质量/g。
1.3.10 质构测试
参考Wang Yihui等[15]的方法,并稍作修改。使用直径为36 mm的圆柱探头(P 36R)进行质构分析。使用全质构分析模式对样品进行压缩测试,测试前速率为2.0 mm/s,测试中速率为1.0 mm/s,测试后速率为2.0 mm/s,触发力为5.0 g,压缩程度设定为80%。
1.3.11 抑菌物质释放能力评估
参考Liu Yuyu等[16]的方法,使用圆盘扩散法统计含有质量分数5%肉桂醛的葵花籽油凝胶对革兰氏阳性菌金黄色葡萄球菌ATCC 25922和革兰氏阴性菌大肠杆菌CMCC 26003的抑制区,以评估抑菌物质的释放能力。将直径10 mm的油凝胶置于接种了105CFU/mL微生物的琼脂平板钻孔中,并在37 ℃孵育过夜。使用纳米测量器1.2软件对样品周围形成的抑菌圈直径进行测量。
1.3.12 贮藏稳定性
将液态油和新鲜制备的油凝胶在黑暗中于50 ℃贮藏14 d。每隔1 d测量一次样品,以评估油凝胶和液态油的氧化稳定性变化。
1.3.1 2.1 过氧化物值(peroxide value,PV)的测定
参考Pan Haibo等[17]的方法,将200 mg油凝胶溶解在1.5 mL异辛烷和异丙醇(异辛烷和异丙醇的混合比例为3∶1,V/V)的混合物中,充分振荡以提取油,5000 r/min离心2 min,取上层清液0.2 mL,加入到2.8 mL甲醇-丁醇混合液(2∶1,V/V)中,随后分别加入20 μL 3.94 mol/L的硫氰酸铵溶液和20 μL Fe2+溶液(等体积的0.132 mol/L BaCl2溶液和0.144 mol/L FeSO4溶液混合制备),混合后避光20 min,于510 nm波长处测定吸光度,根据Fe3+标准曲线计算样品中过氧化物的浓度。
1.3.1 2.2 硫代巴比妥酸反应物(thiobarbituric acid reactive substances,TBARS)值的测定
参考Du Chenxing等[18]的方法,并稍作修改。在离心管中加入200 mg油凝胶,然后加入4 mL TBARS测试液(包含0.375%的硫代巴比妥酸、15%三氯乙酸和0.25 mol/L盐酸溶液),将混合液在沸水中加热60 min后取出,冷却至室温,8000 r/min离心15 min,在532 nm波长处测定上清液吸光度。通过1,1,3,3-四乙氧基丙烷标准曲线计算样品中TBARS的浓度。
1.4 数据统计与分析
2 结果与分析
2.1 CMC-Na/SPI复合溶液的平均粒径分析
粒径是反映聚合物在水溶液中相互作用的重要指标之一[19]。由表1可知,CMC-Na溶液平均粒径为(317.47±11.86)nm,随着蛋白添加量的增加,CMC-Na∶SPI=1∶4溶液的平均粒径增长到(1561.33±10.70)nm,表明蛋白与多糖成功复合。此时溶液pH值为5.5左右,高于大豆分离蛋白的等电点(isoelectric point,pI)4.5。Souza等[20]认为当系统的pH值略高于蛋白质等电点pI时,蛋白质与多糖会形成以静电相互作用为特征的可溶性复合物。这表明大豆分离蛋白上带有正电荷的区域或分子片段可与CMC-Na的阴离子基团发生静电相互作用[21]。蛋白质颗粒吸附于CMC-Na长链表面形成复合物,提高长链强度的同时形成均一、稳定的复合物溶液。

表1 不同多糖蛋白比例溶液的平均粒径与气凝胶密度Table 1 Average particle size and aerogel density of CMC-Na/SPI mixed solutions at different ratios
2.2 气凝胶微观结构分析
气孔的形态与分布会显著影响油凝胶吸油、持油、机械强度等性能。由图1可知,添加蛋白后,蛋白质作为结构强化剂,吸附在纤维丝表面,逐渐将其包裹。随着蛋白比例的增加,蛋白沿纤维丝表面不断沉积形成片层结构。在低蛋白含量下,可以观察到纤维丝被一些蛋白颗粒黏附,在CMC-Na∶SPI=1∶2时,纤维素开始被大豆蛋白完全包覆,蛋白含量的进一步增加导致了吸附蛋白厚度的逐渐增加[22]。由扫描电镜图可以看出,随着大豆蛋白的不断加入,气凝胶结构变得更加致密,孔径大小和孔隙度随着蛋白含量的增加而降低,CMC-Na∶SPI=1∶4时气凝胶呈现出最致密的结构。这佐证了粒径分析中SPI与CMC-Na之间发生静电吸附形成蛋白质-多糖复合物,这些结果表明,CMC-Na为气凝胶提供了弹性网络骨架,而SPI作为一种结构强化剂沿着CMC-Na链聚集。

图1 不同蛋白含量气凝胶的微观结构Fig.1 Microstructure of aerogels with different protein contents
2.3 FTIR分析
为进一步分析聚合物形成过程中CMC-Na和SPI之间的相互作用,测定了CMC-Na溶液在不同SPI添加量下的FTIR光谱。由图2可知,聚合物气凝胶的光谱表现出SPI和CMC-Na的特征峰。SPI的主要谱带有酰胺A带(3285 cm-1,O—H或N—H伸缩振动)、酰胺I带(1655 cm-1,C=O伸缩振动)、酰胺II带(1537 cm-1,N—H弯曲变形和C—N伸缩振动)。酰胺I带和酰胺II带被认为是蛋白质二级结构的敏感区域[23]。1061 cm-1附近是多糖分子中C—O—C伸缩振动的典型特征峰,SPI在此处无吸收峰。聚合物在1655 cm-1和1537 cm-1处的吸收峰随着蛋白含量的增加而增大,说明CMC-Na和SPI成功结合。在1061 cm-1左右的吸收峰随着大豆蛋白含量的增加而减小,表明CMC-Na的羧基与SPI的氨基之间可能存在静电相互作用,同时静电相互作用的形成也促进了酰胺I带的弱位移[20]。1712 cm-1处的尖峰为酯基的C=O拉伸,表明纤维素的羟基与柠檬酸的羧基发生了交联。一般认为此时多元羧酸先脱水形成环酐,然后与纤维素分子链上的羟基发生酯化交联反应[24]。波数3600~3000 cm-1处的吸收峰是多糖分子内或分子间—OH的伸缩振动所引起。相较于SPI,所有聚合物在3600~3000 cm-1处吸收峰的最高点向高波数方向发生位移,这说明SPI和CMC-Na间可能存在氢键相互作用[25]。
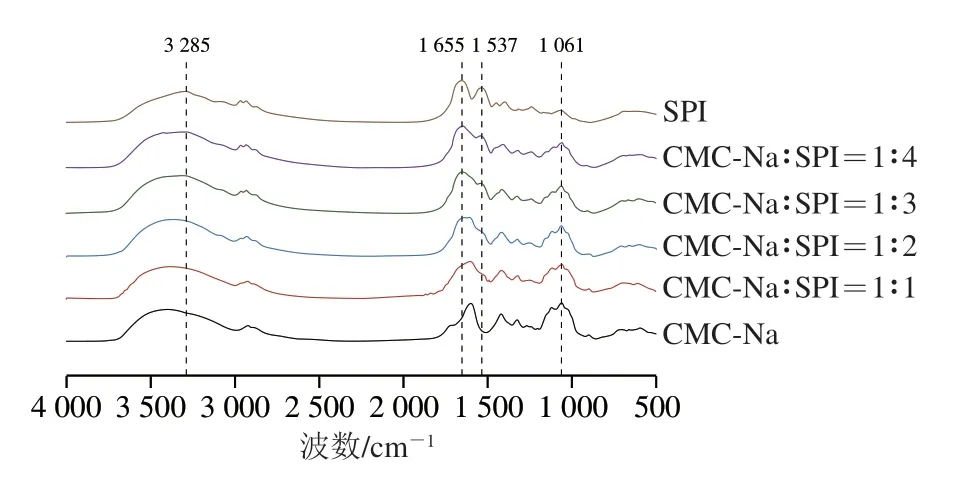
图2 CMC-Na/SPI气凝胶和SPI的FTIRFig.2 FTIR spectra of CMC-Na/SPI aerogels and SPI
2.4 表观形貌分析
在本研究中,使用直径13 mm、高15 mm的中空圆柱体制备冻干气凝胶,气凝胶样品均为白色不透明圆柱体。将气凝胶吸满油后得到油凝胶,从图3可以看出,吸油后凝胶体积没有明显变化,形状完好。CMC-Na油凝胶由于其规则的孔隙结构具有良好的透光性而呈现半透明的状态,随着大豆蛋白添加量的增加,固形物含量升高,密度增加,孔隙度下降,透光性变差。所有油凝胶都具有均匀、半透明的外观,这表明液态油在气凝胶中均匀分布,证明两者具有良好的相容性。

图3 不同蛋白含量的气凝胶和油凝胶外观图Fig.3 Appearance of aerogel and oleogel samples with different protein contents
2.5 吸油能力和持油能力
图4A表示油凝胶吸油量随时间变化的关系,曲线初始斜率表示吸油速率。随着蛋白含量的增加,曲线斜率变小,表示吸油速率减慢。吸收速率的降低可能在很大程度上归因于CMC-Na/SPI气凝胶密度的升高和孔隙率的降低[26]。对于所有样品,液态油在前5 s时吸附速率较快,在10 s时吸附达到平衡状态,体现出气凝胶模板良好的吸油能力。由图4B可以看出,不同蛋白含量气凝胶模板吸油量在13.58~56.48 g/g之间。较高蛋白质含量的溶液含有更少的水,因此冻干后获得的气凝胶有较少的空间负载油[27]。并且随着蛋白质含量的增加,气凝胶自身质量显著增加,吸附的油与气凝胶的相对质量比降低,因此,吸油率下降。通过高速离心模拟油释放评估油凝胶持油能力,所有样品的持油率均高于60%,最高可达80%,油凝胶的油损失随着大豆蛋白含量的增加而降低。结合扫描电镜结果可知,气凝胶中更高的大豆蛋白含量形成了更致密和均匀的网络,虽然一定程度上降低了相对的吸油率,但提供了更高的离心稳定性,减少了油的泄漏。

图4 油凝胶吸油量随时间变化的关系(A)和不同蛋白含量油凝胶的吸油及持油能力(B)分析Fig.4 Oil absorption as a function of time (A),OAC and OHC (B) of CMC-Na/SPI oleogels with different protein contents
2.6 质构分析
良好的抗压能力对于防止油凝胶产品被外力损坏非常重要。图5A呈现了不同比例SPI与CMC-Na的样品在80%应变范围内的应力-应变曲线。所有应力-应变曲线都显示出凝胶结构特征的3 个阶段,包括在屈服点之前在低应变值(小于10%)下的线性弹性区域,在中等应变值(10%~70%)下具有相对平坦曲线的塑性区域,以及在高应变值(超过70%)下应力急剧增加的最后致密化阶段[28]。所有油凝胶在被压缩至80%的整个过程中表现出优异的柔韧性和弹性。随着大豆蛋白含量的增加,油凝胶密度同时逐渐增加,可以观察到更明确的屈服点和曲线平台期更高的压缩强度,表明在更高的密度下油凝胶由高弹性向高硬度发生转变。如图5B~D所示,CMC-Na∶SPI=1∶4 显示出最高的压缩强度(0.39 MPa)、杨氏模量(0.36 MPa)和屈服强度(0.09 MPa),而CMC-Na油凝胶显示出最低的压缩强度(0.10 MPa)、杨氏模量(0.09 MPa)和屈服强度(0.01 MPa),表明SPI的加入显著增强了油凝胶强度,使油凝胶获得更优异的力学性能[29]。与扫描电镜的结果对比,SPI与CMC-Na吸附结合对油凝胶的机械强度有显著的积极影响。由此可知,在CMC-Na弹性支架的基础上通过静电吸附SPI可以获得高弹性、高强度的油凝胶。

图5 油凝胶(CMC-Na/SPI)的机械性能Fig.5 Mechanical properties of CMC-Na/SPI oleogels
2.7 抑菌物质释放能力评估
采用圆盘扩散法对油凝胶对抑菌物质的释放能力进行初步评估。图6显示了负载有5%肉桂醛的油凝胶对金黄色葡萄球菌和大肠杆菌的抑制效果,对抑菌圈直径的统计结果如表2所示。结果表明,不同蛋白比例的油凝胶对大肠杆菌和金黄色葡萄球菌均有明显的抑制作用,而且抑菌圈的直径与SPI含量明显相关[30]。样品中SPI含量越多,抑菌圈直径越小,这表明相同培养时间下释放到外界的抑菌物质更少,抑菌物质在油凝胶内留存含量更高,进而提高了样品的抑菌能力。这说明蛋白含量高的油凝胶通过减少外源抑菌物质的释放,以维持油凝胶内较高的抑菌物质浓度,避免细菌繁殖,以实现产品的高效贮藏。此外,油凝胶对大肠杆菌的抑菌活性比金黄色葡萄球菌弱,这是因为革兰氏阴性菌的外部有一层亲水膜,肉桂醛作为疏水物质会降低其渗透能力[31],因此,同一油凝胶对大肠杆菌的抑菌圈直径比金黄色葡萄球菌更小。

图6 负载5%肉桂醛油凝胶对大肠杆菌和金黄色葡萄球菌的抑制区Fig.6 Inhibition zones of oleogels loaded with 5% cinnamaldehyde against E.coli and S.aureus

表2 负载5%肉桂醛油凝胶的抑菌圈直径Table 2 Diameters of inhibition zones of oleogels loaded with 5% cinnamaldehyde mm
2.8 贮藏稳定性分析
油凝胶在55 ℃贮藏14 d的氧化稳定性变化如图7所示。在加速氧化期间,使用液态油作为对照,同时监测油的初级和次级反应产物的生成量以确定油凝胶的氧化稳定性。在所有的样品中,初级和次级脂质氧化产物含量在整个贮藏过程中逐渐增加,表明脂质被氧化。新鲜制备的油凝胶PV与液态油的PV没有显著差异,这是因为本实验油凝胶的制备只需经过简单快速的物理吸油过程,油凝胶未受到剧烈的理化处理或长时间暴露在空气中。在贮藏前期,油凝胶的PV增长趋势慢于液态油。这表明油凝胶内部结构通过限制油的流动和迁移减缓油的氧化[32];在贮藏后期,油凝胶的PV曲线依然低于液态油,可以推断,在加速氧化过程中,油凝胶的网络结构依然保持完好,可以阻挡氧气与油脂的接触。就次级反应产物而言,油凝胶和液态油的TBARS值在贮藏期内趋于增加。与液态油相比,油凝胶的增长慢得多。Abdollahi等[33]的研究表明,由明胶和黄原胶组成的网络结构在延缓油的氧化方面发挥重要作用,本实验结果与其相似。综上所述,油凝胶形成的网络结构可以显著提高油脂氧化稳定性。

图7 液态油和油凝胶的贮藏稳定性分析Fig.7 Storage stability of oil and oleogels
3 结论
采用气凝胶模板法制备CMC-Na油凝胶,大豆蛋白与CMC-Na通过静电吸附作用形成稳定的复合物结构,从而增强油凝胶弹性和强度。随着大豆蛋白含量的增加,油凝胶网络结构更加致密,持油率更高,最终形成高弹性、高强度的凝胶。蛋白质的加入明显减少了抑菌物质向外界的释放,进而降低了抑菌物质的损失,并延缓了油脂氧化速度,这提高了油凝胶的抑菌能力和抗氧化性能。综上所述,CMC-Na/大豆蛋白结合可形成稳定的油凝胶,有望替代食品加工中饱和反式脂肪酸的使用,本研究可为多糖蛋白聚合物在食品加工中的应用提供参考。

