射血分数保留的心力衰竭患者心房利钠肽前体A 基因多态性与5 年全因死亡的关系
马江云 陈金焕 徐胜华
心力衰竭是各种原因引起心肌病变发展至终末阶段的共同表现,5 年病死率约50%,10 年病死率超90%,严重危害人类生命健康[1]。射血分数保留的心力衰竭(heart failure with preserved ejection fraction,HFpEF)是指左心室射血分数(left ventricular ejection fraction,LVEF)>50%的心力衰竭,主要表现为心脏舒张功能及顺应性降低而非收缩功能降低[2]。研究指出,心房利钠肽前体A(natriuretic peptide precursor A,NPPA)基因多态性与心血管疾病的发生、发展密切相关,但其与HFpEF 患者5 年全因死亡的关系研究较少[3]。此外,氨基末端脑钠肽前体(Nterminal pro-brain natriuretic peptide,NT-proBNP)被证实在各种临床收缩性心力衰竭的诊治、病情和预后评估方面具有较好的参考价值[4-5]。本研究探讨NPPA 基因多态性与HFpEF 患者5 年全因死亡的相关性及对NT-proBNP 水平的影响,现将结果报道如下。
1 对象和方法
1.1 对象 选择2013 年1 月至2016 年1 月杭州市第九人民医收治的HFpEF 患者233 例,男133例,女100 例,年龄39~88(65.93±11.43)岁,体重指数(body mass index,BMI)19.8~27.6(23.82±1.81)kg/m2。根据5 年全因死亡(包括心血管死亡和非心血管死亡)情况分为死亡组31 例和存活组202 例。纳入标准:符合心力衰竭诊断标准[6];LVEF≥50%。排除标准:血液系统疾病;严重肝肾功能障碍;严重呼吸系统疾病、脑血管疾病;恶性肿瘤;精神疾病;妊娠或哺乳期;存在其他可引起检测指标异常的疾病(如感染、应激、发热等)。本研究经本院医学伦理委员会审查通过(批准文号:WH8675),患者或家属均知情同意。
1.2 方法
1.2.1 一般资料收集 收集并比较两组患者一般资料,包括性别、年龄、民族、BMI、饮酒史、吸烟史、纽约心脏病协会(New York Heart Association,NYHA)心功能分级、既往病史[糖尿病、冠心病、高血压、慢性阻塞性肺疾病(chronic obstructive pulmonary disease,COPD)、心房颤动、慢性肾功能不全、贫血]、既往用药。
1.2.2 血脂、NT-proBNP、心功能指标检测 采集两组患者入院时(治疗前)外周静脉血6 mL,抗凝处理后保存于-80 ℃冷藏室,由专业检测人员统一检测。两组患者均取2 mL 血液标本,采用杭州艾康生物技术有限公司CCM-101 型血脂分析仪测定血脂指标,包括总胆固醇(total cholesterol,TC)、甘油三酯(triglyceride,TG)、低密度脂蛋白胆固醇(low density lipoprotein cholesterol,LDL-C)、高密度脂蛋白胆固醇(high density lipoprotein cholesterol,HDL-C)。另取2 mL 血液标本,3 500 r/min 离心5 min,取上清液,采用苏州光景生物科技有限公司的试剂盒、时间分辨荧光免疫层析法检测血清NT-proBNP 水平,比较不同基因型患者血清NT-proBNP 水平。采用苏州飞依诺科技有限公司VINNO M50 型数字化彩色超声诊断仪测定心功能指标,包括LVEF、左心室输出量、左心室舒张末容积、左心室收缩期横径、A 峰、E 峰。
1.2.3 NPPA 基因检测 两组患者均取入院2 mL血液标本,解冻后提取DNA,采用徐州赛恩生物试剂有限公司全血基因组DNA 快速提取试剂盒,以荧光PCR 技术进行NPPA 基因扩增及基因型测序,共检测NPPA 基因的2 个单核苷酸基因多态性位点,即rs5063 位点、rs5065 位点。rs5063 位点正引物为5'-GACCAGAGCTAATCCCATGTACA-3',负引物为5'-GCTTTCCTGGCCCTACCTT-3';rs5065 位点正引物为5'-AAGTGTTGACAGGAAGCTGC-3',负引物为5'-AAGTTCAGAGGATGGGCACA-3',材料均购自广州锐博生物科技有限公司。采用美国Invitrogen 公司Taq DNA Poly-merase High Fidelity 试剂进行电泳鉴定。采用美国ABI 公司ABI3730 XL 全自动DNA 测序仪进行基因型测序,分析rs5063、rs5065 位点基因是否存在多态性,并比较两组患者NPPA 基因rs5063、rs5065 位点基因型、等位基因分布情况。
1.2.4 治疗和随访方法 两组患者出院后5 年均严格按照《心力衰竭合理用药指南》给予利尿剂、血管扩张剂、血管紧张素转换酶抑制剂或血管紧张素Ⅱ受体拮抗剂、β 受体阻滞剂、洋地黄类正性肌力药物及醛固酮受体拮抗剂等联合治疗[7]。通过门诊或电话随访,出院后第1 年每3 个月随访1 次,第2~5年每6 个月随访1 次,随访截至2021 年1 月,统计随访期间两组患者存活情况。
1.3 统计学处理 采用SPSS 22.0 统计软件。符合正态分布的计量资料以表示,多组间比较采用单因素方差分析,两两比较采用SNK-q检验,组间比较采用两独立样本t检验。计数资料组间比较采用χ2检验。通过Cox 回归模型进行多因素回归分析,运用R 语言随机森林模型对5 年全因死亡影响因素进行重要性排序。P<0.05 为差异有统计学意义。
2 结果
2.1 两组患者一般资料比较 死亡组患者的NYHA 心功能分级Ⅳ级、COPD、心房颤动、慢性肾功能不全患者占比高于对照组,差异均有统计学意义(均P<0.05)。两组患者其他指标比较,差异均无统计学意义(均P>0.05),见表1。
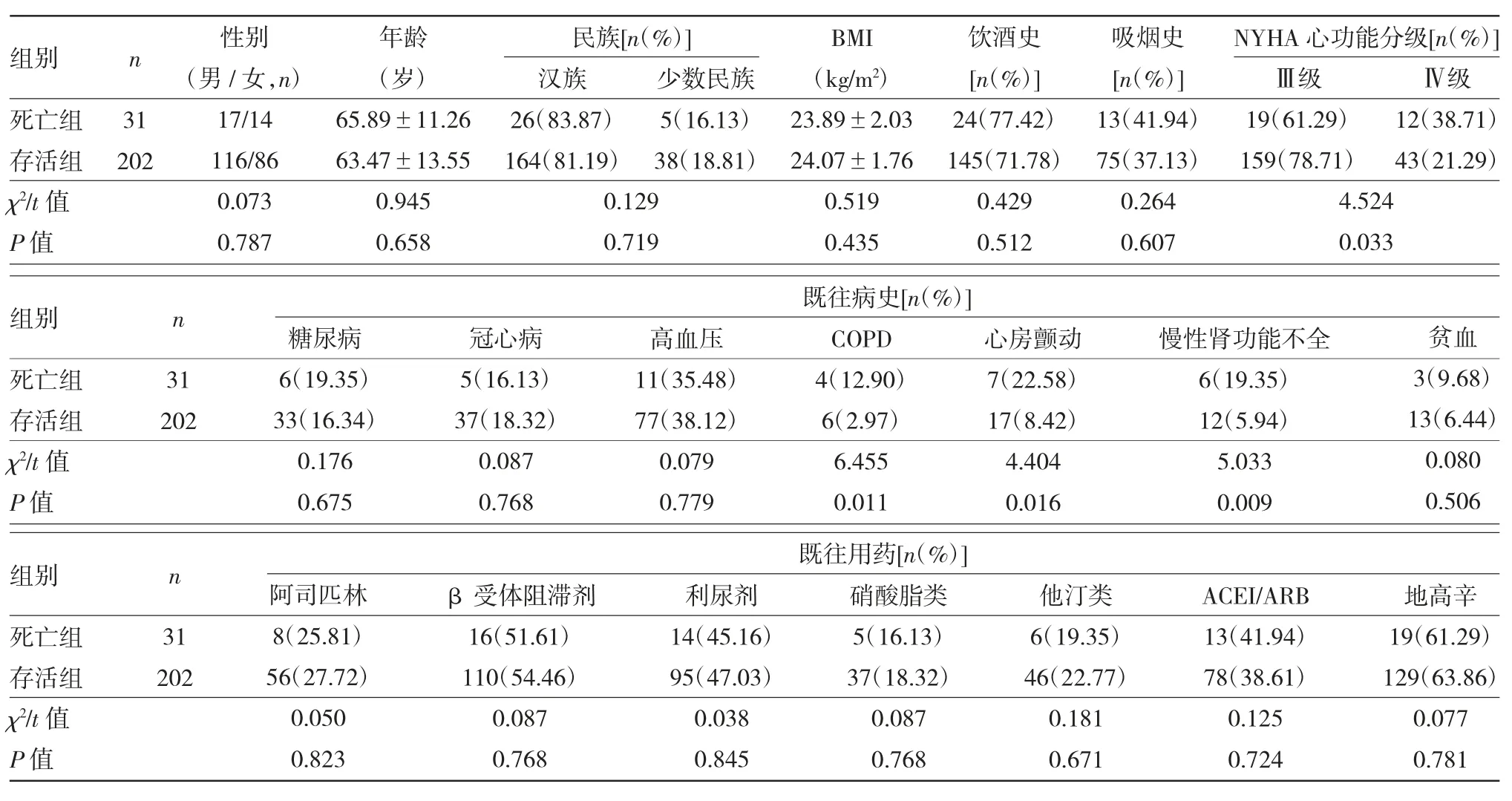
表1 两组患者一般资料比较
2.2 两组患者血脂、NT-proBNP、心功能指标比较死亡组患者的NT-proBNP 水平高于存活组,差异有统计学意义(P<0.05);两组患者血脂及其他心功能指标比较,差异均无统计学意义(均P>0.05),见表2。
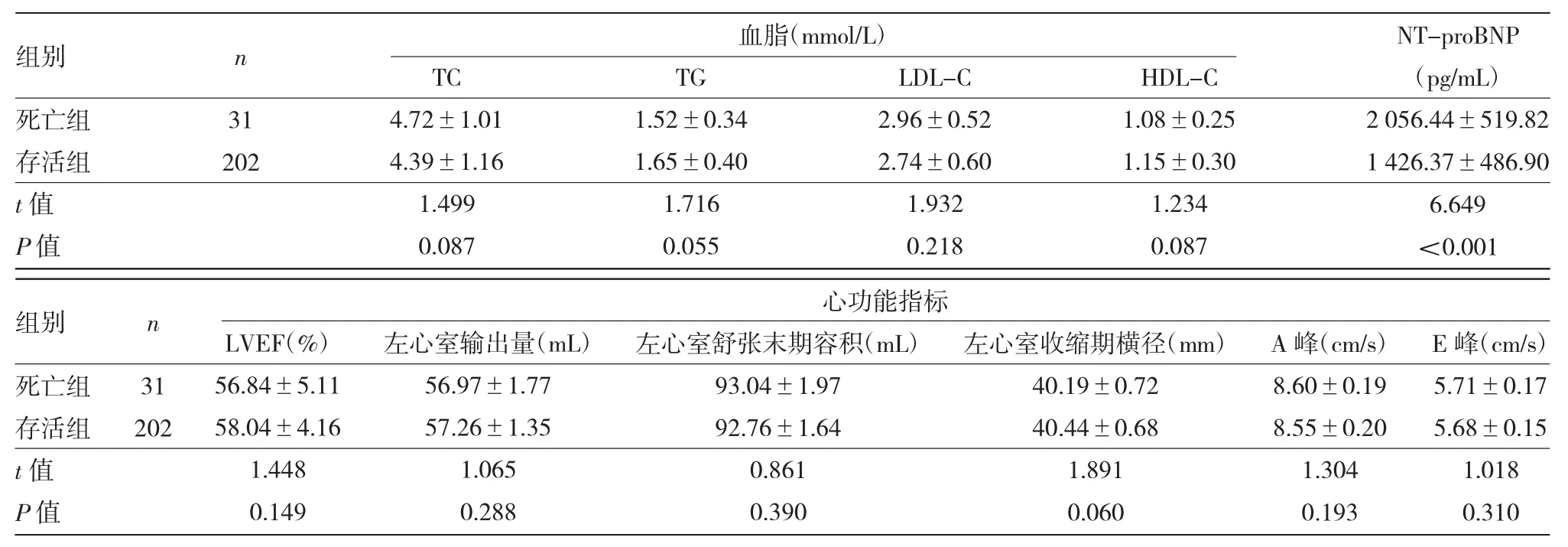
表2 两组患者血脂、NT-proBNP、心功能指标比较
2.3 NPPA 基因扩增结果 基因分型检测结果显示,rs5063 位点基因型包括AA、AG、GG;rs5065 位点基因型包括AA、AG、GG,rs5063、rs5065 均存在多态性。见图1。
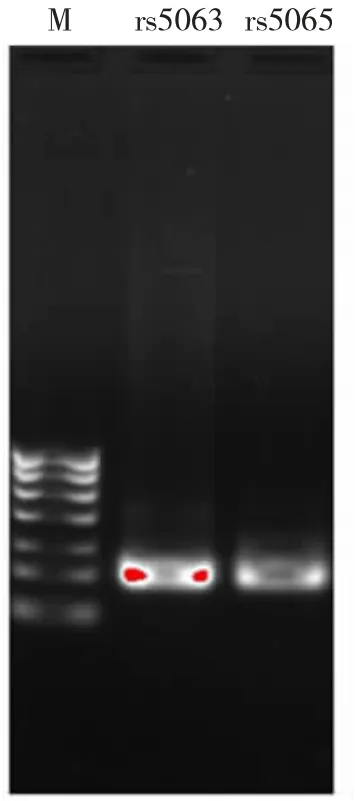
图1 NPPA 基因扩增电泳图
2.4 两组患者NPPA 基因多态性比较 死亡组NPPA 基因rs5063 位点AA 基因型、A 等位基因占比高于存活组,差异均有统计学意义(均P<0.05)。两组患者rs5065 位点基因型、等位基因分布比较,差异均无统计学意义(均P>0.05),见表3。
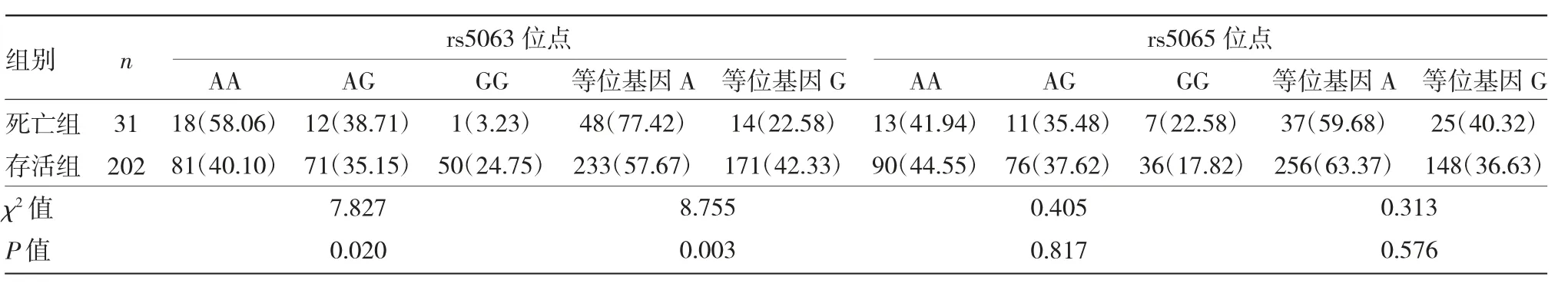
表3 两组患者NPPA 基因多态性比较[例(%)]
2.5 HFpEF 患者5 年全因死亡的影响因素分析NYHA 分级、COPD、心房颤动、慢性肾功能不全、NT-proBNP、rs5063 位点AA 基因型均为HFpEF 患者5 年全因死亡的影响因素(均P<0.05),见表4。影响因素从高到底依次为NT-proBNP、慢性肾功能不全、rs5063 基因型、COPD、NYHA 心功能分级、心房颤动,见图2。
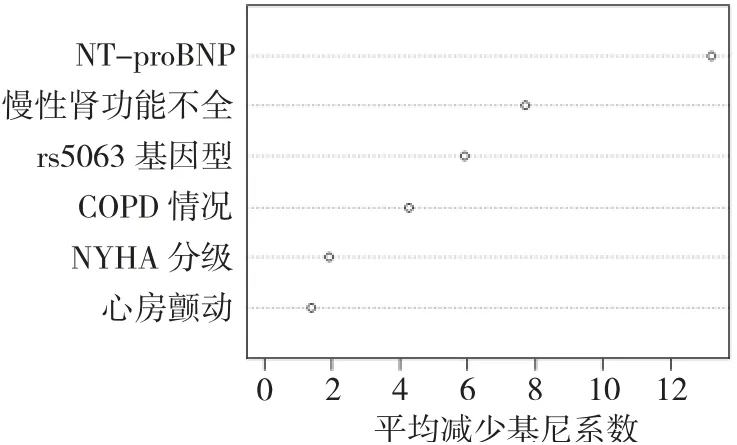
图2 各影响因素的排序图
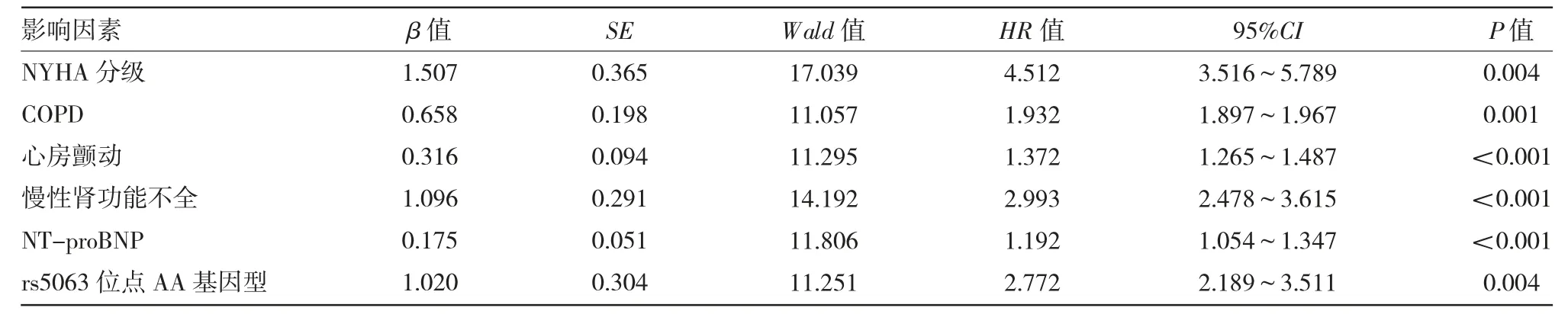
表4 5 年全因死亡的Cox 回归分析
2.6 NPPA 基因多态性对NT-proBNP 水平的影响NPPA 基因rs5063 与rs5065 位点AA、AG、GG 患者NT-proBNP 水平比较,差异均有统计学意义(均P<0.01)。NPPA 基因rs5063 与rs5065 位点AG、GG 基因型患者NT-proBNP 水平低于AA 型患者,差异均有统计学意义(均P<0.05),见表5。
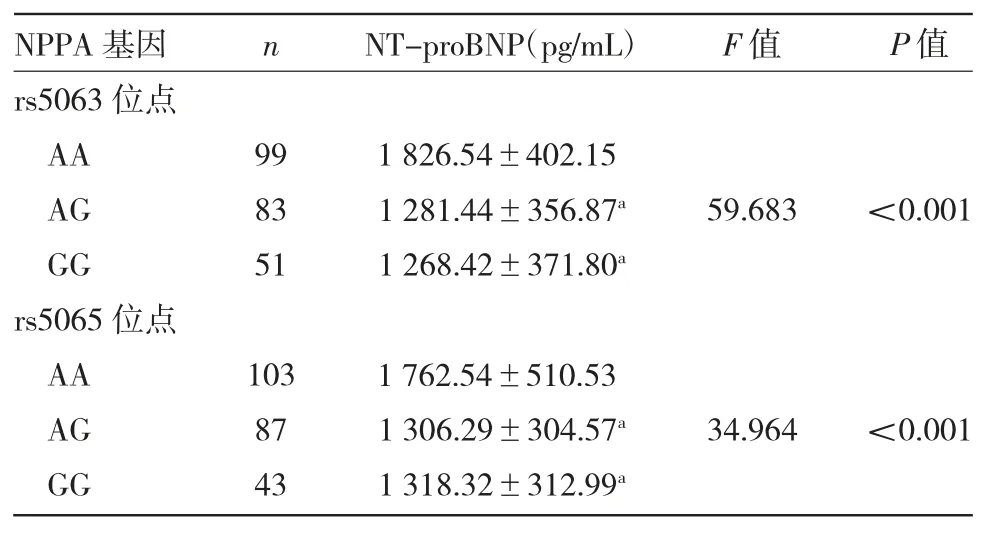
表5 NPPA 基因多态性对NT-proBNP 水平的影响
3 讨论
近年来,HFpEF 的患病率呈逐渐升高趋势,进一步了解与研究HFpEF 发病机制对指导临床治疗意义重大[9-10]。NPPA 基因作为研究疾病遗传易感性的候选基因受到人们的关注,NPPA 基因多态性与急性左心衰患者的易感性显著相关[11]。
本研究NPPA 基因扩增结果显示,rs5063 位点基因型包括AA、AG、GG;rs5065 位点基因型包括AA、AG、GG,rs5063、rs5065 均存在多态性。笔者推测NPPA 基因rs5063、rs5065 位点的基因多态性可能与HFpEF 的发生、发展有关。NPPA 基因定位于染色体1P36,编码心房钠尿肽(atrial natriuretic peptide,ANP),而ANP 作为一种利尿剂控制细胞外液量和电解质的平衡[12-13]。相关动物学研究显示,通过有效措施下调ANP 表达水平,有助于改善心功能,发挥防治慢性心力衰竭的作用[14]。研究发现,ANP 参与调节电解质平衡和血压,其调控基因NPPA 基因突变可通过引起ANP 的水平变化,进而激活炎症和心肌纤维化引起心房颤动[15]。本研究结果显示,死亡组患者NPPA 基因rs5063 位点等位基因A 的分布比例高于存活组患者,等位基因G 的分布比例低于存活组患者,提示NPPA 基因rs5063 位点等位基因A、等位基因G 可增加患者5 年全因死亡率。李文安等[16]通过对急性左心衰患者研究发现,NPPA 基因rs5063、rs5065 位点的基因多态性均为急性左心衰的独立危险因子,与本研究结果存在一定差异。造成此项差异的原因可能与两项研究的对象不同有关。本研究通过Cox 回归分析发现NPPA 基因rs5063位点AA 基因型为HFpEF 患者5 年全因死亡的独立危险因素,进一步证实了NPPA 基因rs5063 位点基因突变可增加HFpEF 患者5 年全因死亡发生风险。笔者认为突变型ANP 较野生型ANP 具有更强和更持续的利钠、利尿作用,激活炎症和心肌纤维化,从而促进HFpEF 患者心功能损伤,增加死亡率。
研究证实,血清NT-proBNP 水平变化与HFpEF 患者心功能指标存在显著相关性,与HFpEF 的发生、发展密切相关[17]。本研究发现,NPPA 基因rs5063 与rs5065 位点AG、GG 基因型患者NT-pro-BNP 水平低于AA 型患者。NPPA 基因使ANP 活性增强,导致钠负荷增加、心房扩张或血容量增加,从而引起BNP 的合成、释放增多,引起NT-proBNP 水平升高。李文安等[16]的研究也证实急性左心衰患者NPPA 基因多态性与NT-proBNP 有较强的关联性。而NT-proBNP 被证实具有扩血管、利尿、抗心肌纤维化和抑制交感神经的作用,其血清水平越高,慢性心力衰竭患者5 年全因死亡率越高[18-19]。据此笔者认为NPPA 基因rs5063 与rs5065 位点基因突变可通过上调血清NT-proBNP 水平,促进HFpEF 的疾病进展,增加患者5 年全因死亡风险。
此外,本研究还发现,NYHA 心功能分级、COPD、心房颤动、慢性肾功能不全均为HFpEF 患者5 年全因死亡的影响因素,因此对于NYHA 心功能分级较高及合并COPD、心房颤动、慢性肾功能不全的HFpEF 患者,应加强关注及进行相关治疗,或可降低5年全因死亡风险。
综上所述,NPPA 基因多态性可能通过上调NT-proBNP 水平增加HFpEF 患者5 年全因死亡风险,成为HFpEF 的独立危险因素。但本研究存在样本量较少的不足,研究结果可能存在一定误差,仍需扩大样本量进一步验证。