华蟾素联合替莫唑胺治疗脑恶性胶质瘤的疗效及安全性
杨易,陈晓英,喻国峰,顾文,刘学政
脑恶性肿瘤的治疗方式主要包括手术、放疗等[1],替莫唑胺现已被广泛使用,其具有分子量小、脂溶性高等特点,且人体吸收快速,能够直接作用于肿瘤组织。有研究表明,脑恶性胶质瘤患者化疗时使用替莫唑胺可降低疾病恶化风险,提高患者的存活率[2]。因此,替莫唑胺联合化疗目前已成为临床治疗脑恶性胶质瘤的主要方法,但也存在一定不足。华蟾素是一种中成药,具有抗肿瘤效用,能够抑制肿瘤细胞生长,增强患者免疫力[3],且具有镇痛、抗炎消肿等作用[4]。现观察华蟾素联合替莫唑胺治疗脑恶性胶质瘤的疗效及安全性,报道如下。
1 资料与方法
1.1 临床资料 回顾性分析2020年4月—2022年4月上海市东方医院吉安医院收治的116例脑恶性胶质瘤患者的临床资料,患者符合《中国中枢神经系统胶质瘤诊断与治疗指南(2015)》[5]中的脑恶性胶质瘤诊断标准。排除标准:(1)合并脑梗死、肝肾功能严重不全者;(2)其他恶性肿瘤者;(3)严重精神疾病者;(4)临床资料不完整者。根据治疗方式的不同将患者分为单一组(n=48)和联合组(n=68)。2组患者性别、年龄、TNM分期比较,差异无统计学意义(P>0.05),见表1。本研究符合《赫尔辛基宣言》相关伦理准则。

表1 单一组与联合组临床资料比较
1.2 治疗方法 根据《实体瘤疗效评价标准简介》[6]制定常规的基础性化疗方案,化疗结束后,单一组采取替莫唑胺胶囊(北京双鹭药业股份有限公司生产)空腹口服,第1周初始用药剂量为150 mg/m2,连续用药5 d;第2周,对于血小板计数≥100×109/L、中性粒细胞计数≥30×109/L者增加用药剂量为200 mg/m2;对于中性粒细胞计数<30×109/L者,将用药剂量降低50 mg/m2,但最低用药剂量不得<100 mg/m2。患者治疗4周。联合组在单一组基础上加用华蟾素注射液(安徽金蟾生化股份有限公司生产)20 ml加入5%葡萄糖溶液500 ml,缓慢静脉滴注(40~50滴/min),每天1次,患者治疗4周。
1.3 观察指标与方法 (1)实验室指标:于治疗前、治疗4周后,用K3EDTA抗凝真空管收集患者静脉血2~3 ml,室温下放置,12 h内使用流式细胞仪检测CD3+、CD4+、CD8+、CD4+/CD8+;另采集患者清晨空腹静脉血5 ml,静置25~30 min,室温下以4 000 r/min离心10 min,取上清液;采用酶联免疫吸附法测定血清炎性因子,包括白介素-6(IL-6)、白介素-1β(IL-1β)和肿瘤坏死因子-α(TNF-α)。(2)生活质量:于治疗前及治疗4周后采用生活质量评定量表评估患者的生活质量,量表包含身体功能、情感功能及其他领域,每项计100分,评分越高表明患者的生活质量越高。(3)不良反应:包括肝功能异常、呕吐、恶心、发热等。
1.4 疗效判定标准 采用《实体瘤疗效评价标准简介》[6]判定患者的临床疗效,即完全缓解:患者病灶完全消失;部分缓解:患者病灶直径之和缩小≥30%;疾病进展:患者病灶最小直径之和增加≥20%,或出现新病灶;疾病稳定:患者病情介于疾病进展和部分缓解间。疾病控制率=(完全缓解+部分缓解+疾病稳定)/总例数×100%。
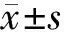
2 结 果
2.1 临床疗效比较 联合组疾病控制率为57.35%,高于单一组的37.50%(χ2=4.437,P=0.035),见表2。
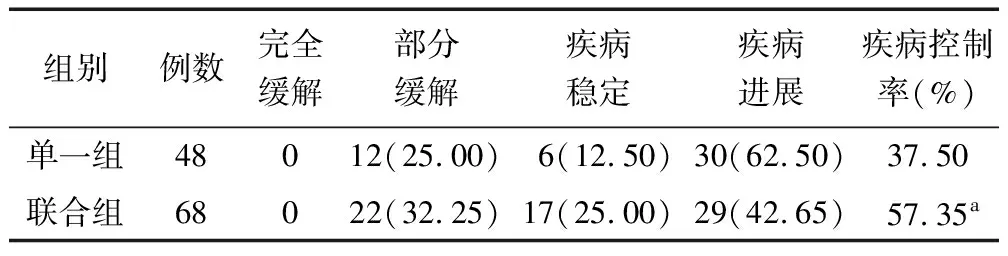
表2 单一组与联合组临床疗效比较 [例(%)]
2.2 T淋巴细胞亚群比较 2组治疗前CD3+、CD4+、CD8+、CD4+/CD8+及治疗4周后CD8+、CD4+/CD8+比较,差异无统计学意义(P>0.05);治疗4周后,2组CD3+、CD4+、CD4+/CD8+高于治疗前,且联合组CD3+、CD4+高于单一组(P<0.01),见表3。

表3 单一组与联合组治疗前后T淋巴细胞亚群比较
2.3 血清炎性因子比较 治疗前,2组血清IL-6、IL-1β、TNF-α水平比较,差异无统计学意义(P>0.05);治疗4周后,2组血清IL-6、IL-1β、TNF-α水平低于治疗前,且联合组低于单一组(P<0.01),见表4。
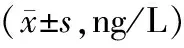
表4 单一组与联合组治疗前后血清炎性因子比较
2.4 生活质量评分比较 治疗前,2组身体功能、情感功能及其他领域评分比较,差异无统计学意义(P>0.05);治疗4周后,2组身体功能、情感功能及其他领域评分高于治疗前,且联合组高于单一组(P<0.05或P<0.01),见表5。
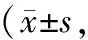
表5 单一组与联合组治疗前后生活质量评分比较分)
2.5 不良反应比较 联合组不良反应总发生率为29.41%,与单一组的31.25%比较,差异无统计学意义(χ2=0.042,P=0.832),见表6。

表6 单一组与联合组不良反应比较 [例(%)]
3 讨 论
脑部恶性肿瘤以脑胶质瘤、脑膜瘤较常见,临床以手术、化疗等方法为主,患者若实施手术治疗易损伤其脑组织,使其神经突触功能及形态发生变化且损伤难以逆转,且疾病复发风险和并发症发生率均较高[7-9]。脑恶性胶质瘤患者病情发展较快,且病死率较高[10]。华蟾素具有抗炎镇痛的作用,常用于治疗骨癌痛[11]。替莫唑胺作为新型化疗药物,对人脑瘤的生长具有一定的抑制作用[12-13]。脑恶性胶质瘤患者的肿瘤组织会释放多种递质来抑制机体免疫功能,使机体进入免疫抑制状态[14],而患者口服替莫唑胺胶囊后,药物可进入脑脊液,在肿瘤部位形成有效浓度,阻止细胞增殖并使其凋亡,控制局部肿瘤进展,提高患者的免疫功能,且可降低患者不良反应发生率。
本研究结果显示,联合组疾病控制率高于单一组,表明华蟾素联合替莫唑胺治疗脑恶性胶质瘤可增强疗效。此外,联合组治疗4周后CD3+、CD4+高于单一组,且2组患者不良反应总发生率比较差异无统计学意义,表明华蟾素联合替莫唑胺治疗脑恶性胶质瘤患者可显著改善机体免疫功能,且安全性较高。华蟾素是从蟾蜍中提取出来的生物活性成分,可通过抑制信号传导表达来降低癌细胞的增殖能力,从而达到抗肿瘤的效果。癌细胞转移是晚期恶性肿瘤最主要的死因,抑制肿瘤新生血管形成对控制肿瘤细胞转移具有重要意义,华蟾素可明显降低癌细胞表达水平,抑制肿瘤血管新生及肿瘤细胞的生长、远处转移;此外,华蟾素能增强LAK细胞的杀伤活性,增强巨噬细胞功能,增强机体免疫力。本研究结果显示,联合组治疗4周后身体功能,情感功能及其他领域评分高于单一组,表明华蟾素联合替莫唑胺治疗脑恶性胶质瘤可明显提升患者的生活质量,促进患者病情恢复。IL-6、IL-1β、TNF-α可反映机体炎症状态,脑恶性胶质瘤患者体内的IL-6、IL-1β、TNF-α水平会显著升高。IL-6会使B细胞前体产生抗体从而发生炎症,IL-1β对疼痛和炎症过程具有较大影响;TNF-α在病理状态下会异常升高,机体炎症状态下升高较明显,上述炎性因子可相互作用,导致组织和细胞损伤。本研究结果显示,治疗4周后联合组血清IL-6、IL-1β、TNF-α水平低于单一组,表明华蟾素联合替莫唑胺治疗脑恶性胶质瘤可更好地缓解机体炎症状态。
综上所述,华蟾素联合替莫唑胺治疗脑恶性胶质瘤患者具有较好疗效,可有效提高患者的免疫功能,减轻机体炎性反应,提高患者的生活质量,且安全性较高。
利益冲突所有作者声明无利益冲突

