过表达CASP1诱导人急性髓系白血病细胞THP-1的G0/G1细胞周期阻滞和NLRP3炎性小体介导的焦亡
艾克拜尔·阿布都热衣木, 徐 丽, 阿孜古丽·麦麦提,阿依姆妮萨·阿卜杜热合曼, 帕提古力·苏力坦
(新疆维吾尔自治区喀什地区第一人民医院血液内科, 新疆 喀什 844000)
人急性髓系白血病(acute myeloid leukemia,AML)细胞的增殖被异常激活且细胞凋亡被抑制,在体内呈现生长不受控制的爆发性生长[1]。目前,化疗、放疗、免疫治疗和造血干细胞移植是治疗AML的主要手段[2],但是AML患者的总体生存率仍然不令人满意,迫切需要新的治疗策略[3-4],然而,对于AML发生机制的研究仍处于初步阶段。炎性小体是参与先天免疫反应的胞质多蛋白复合物。含有半胱天冬酶1(Caspase1,CASP1)、NOD样受体热蛋白结构域相关蛋白3(Nod-like receptor heat protein domain associated protein 3,NLRP3)、凋亡相关斑点样蛋白((apoptosis-associated speck-like protein,ASC)的NLRP3炎性小体是表征最好的炎性小体之一。尽管NLRP3炎性小体激活的确切机制仍在研究中,然而,目前认为NLRP3炎性小体的形成导致CASP1激活形成cleaved-CASP1,随后将促炎细胞因子IL-1β或IL-18转化为成熟的生物活性形式[5]。成熟的IL-1β或IL-18随后被释放到细胞外[5]。另外,CASP1的抑制剂VX765被证明可以促进癌细胞的增殖并抑制细胞CASP1/Gasdermin D介导的细胞焦亡(pyroptosis)。这些特征均指向CASP1激活可能促进了细胞焦亡。然而,目前尚不清楚CASP1是否调控AML细胞的焦亡。本文研究过表达CASP1对AML THP-1细胞焦亡和细胞周期阻滞的影响,并探讨过表达CASP1诱导AML THP-1细胞焦亡的潜在机制。
1 材料与方法
1.1试剂与耗材:人急性髓系白血病原代细胞THP-1购于于中国科学院上海生物科学研究所。RPMI-1640培养基和胎牛血清均购于美国Gibco公司。CASP1过表达载体(pcDNA3.1-CASP1)和阴性对照(pcDNA3.1-null)构建于美国Invitrogen公司。Annexin V-FITC/PI细胞凋亡检测试剂盒购于上海碧云天生物科技有限公司。细胞周期检测试剂盒购于美国伯乐公司。TRIzol蛋白提取试剂、BCA蛋白测定试剂、超级信号PLUS化学发光底物均购于北京天根生物科技有限公司。细胞活性氧检测试剂盒和兔抗人增殖相关蛋白Ki67、兔抗人增殖细胞核抗原(proliferating cell nuclear antigen,PCNA),兔抗人细胞周期蛋白D1(cyclin D1)、兔抗人NOD样受体热蛋白结构域相关蛋白3(Nod-like receptor heat protein domain associated protein 3,NLRP3)、兔抗人凋亡相关斑点样蛋白((apoptosis-associated speck-like protein,ASC)、兔抗人CASP1、兔抗人切割半胱天冬酶1(cleaved-caspase 1,cleaved-CASP1)、兔抗人白细胞介素(interleukin,IL)-1β,兔抗人IL-18、兔抗人cleaved-Gasdermin D,兔抗人磷酸甘油醛脱氢酶(Glyceraldehyde-phosphate dehydrogenase,GAPDH)的一抗购于英国Abcam公司。聚偏二氟乙烯膜购于上海碧云天生物科技有限公司。ABI7900快速实时PCR系统(美国卡尔斯巴德应用生物系统公司)SYBR Green PCR主混合物(上海碧云天生物科技有限公司)
1.2方 法
1.2.1细胞培养:THP-1在添加了10% (v/v)胎牛血清和1% (v/v)青霉素/链霉素的RPMI-1640中培养,培养箱环境为37℃和5% (v/v) CO2。待细胞生长到对数生长期用于细胞转染和后续检测实验。
1.2.2细胞转染和分组 用24孔板接种对数生长期的细胞(2×105个/孔),待细胞生长到融合度达到90%时,根据Invitrogen公司转染试剂盒的说明方法,更换为500μL的无血清RPMI-1640培养基,培养基中含10μL Lipofectamine 3000和0.8μg的pcDNA3.1-CASP1,孵育细胞24h,将该处理命名为pcDNA3.1-CASP1组。使用含10μL Lipofectamine 3000和0.8μg的pcDNA3.1-null的RPMI-1640培养基孵育细胞24h作为pcDNA3.1-null组。另外,用24孔板接种对数生长期的细胞(2×105个/孔),待细胞生长到融合度达到90%时更换为500μL的无血清培养基培养24h作为对照组。最后收集对照组、pcDNA3.1-null组、pcDNA3.1-CASP1组的细胞用于后续实验。
1.2.3细胞增殖实验:各组细胞转染THP-1细胞用磷酸盐缓冲盐水洗涤两次,1000 rpm离心10min。细胞浓度通过血球计计数检测。细胞在96孔板中以5×104细胞/孔立即接种,根据CCK-8试剂盒提供的说明加入10μL CCK-8试剂孵育4h,在490nm处读取吸光度。
1.2.4细胞凋亡实验:细胞凋亡实验中各组细胞以每孔1×106个细胞接种在24孔板中。根据试剂盒提供的说明用Annexin V对细胞进行染色,孵育10min后,并在PI缓冲液中重悬。然后用流式细胞术(FACSCantoTMⅡ)对其进行分析,并检测其荧光强度。数据分析使用FlowJo软件分析凋亡细胞的比例。
1.2.5细胞周期分析:各组细胞以1×106的密度接种于24孔板中过夜。在2000rpm下离心5min,在冷PBS中洗涤2次,在75% (v/v)的冷液中重悬。按照碘化丙啶细胞周期染色方案进行细胞周期分析。采用FACSCantoTMⅡ检测DNA含量。使用FCS Express 7 Flow软件程序分析数据。
1.2.6Western blot收集各组细胞,使用TRIzol提取试剂分离细胞中全蛋白裂解物。使用BCA蛋白测定试剂检测蛋白浓度。用十二烷基硫酸钠-聚丙烯酰胺凝胶电泳分离50μg的细胞总蛋白,并转移到聚偏二氟乙烯膜。在4℃下孵育封闭液封闭聚偏二氟乙烯膜,随后用针对Ki67(1∶500)、PCNA(1∶1000)、cyclin D1(1∶1000)、NLRP3(1∶800)、ASC(1∶800)、cleaved-CASP1(1∶500)、IL-1β(1∶600),IL-18(1∶800)、cleaved-Gasdermin D(1∶1200)的一抗在4℃下孵育过夜,然后加入辣根过氧化酶偶联的二抗(1∶5000)。内参蛋白为GAPDH(1∶10000),使用SuperSignal West Pico PLUS化学发光底物,检测感兴趣的蛋白,并使用Invitrogen iBright FL1000成像系统进行观察。
1.2.7实时定量PCR (qRT-PCR):使用Trizol试剂(美国Invitrogen公司)从各组细胞中提取总RNA。并将mRNA逆转录为互补DNA,并在ABI 7900快速实时PCR系统上使用SYBR Green PCR试剂进行qRT-PCR。使用U6作为内参基因。然后用2-ΔΔCT方法计算相对表达水平。引物(5′~ 3′)序列如下:caspase-1正向ATCCGTTCCATGGGTGAAGGTACA,caspase-1反向CAAATGCCTCCAGCTCTGTAATCA;IL-18正向GCTTGAATCTAAATTATCAGTC;IL-18反向GAAGATTCAAATTGCATCTTAT;IL-1β正向TGCAGTTCACAGAGCAGACC,IL-1β反向GACCGGAAACCTCATGGAG;GAPDH正向GACATTGTTGCCATCAACGACC,GAPDH反向CCCGTTGATGACCAGCTTCC。

2 结 果
2.1过表达CASP1对THP-1细胞增殖的影响:与对照组比,pcDNA3.1-null组的细胞增殖活力变化无统计学意义(P>0.05),而且Ki67和PCNA的相对表达水平变化无统计学意义(均P>0.05)。与对照组比,pcDNA3.1-CASP1组的细胞的增殖活力减少,差异有统计学意义(均P<0.05),Ki67和PCNA的相对表达水平减少,差异有统计学意义(均P<0.05)。与pcDNA3.1-null组比,pcDNA3.1-CASP1组细胞的增殖活力减少,Ki67和PCNA的相对表达水平减少,差异有统计学意义(P<0.05)。见图1A~1D。

图1 过表达CASP1对THP-1细胞增殖的影响
2.2过表达CASP1对THP-1细胞凋亡的影响:与对照组比,pcDNA3.1-null组的细胞凋亡率变化无统计学意义(P>0.05)。与对照组比,pcDNA3.1-CASP1组的细胞凋亡率增加,差异有统计学意义(P<0.05)。与pcDNA3.1-null组比,pcDNA3.1-CASP1组的细胞凋亡率增加,差异有统计学意义(P<0.05)。见图2。
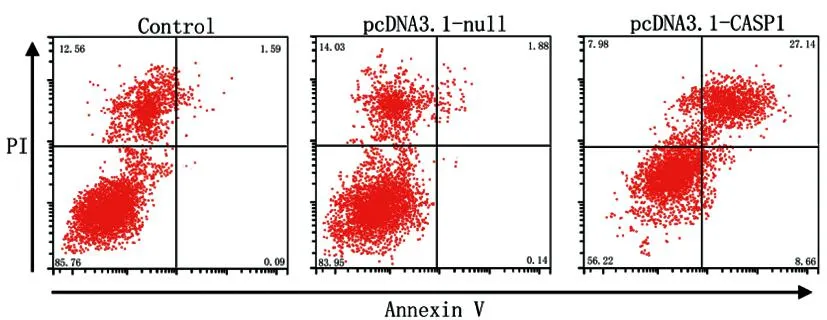
图2 用流式细胞术检测过表达CASP1对THP-1细胞凋亡的影响
2.3过表达CASP1对THP-1细胞周期的影响:与对照组比,pcDNA3.1-null组的细胞周期变化均无统计学意义,且cyclin D1的相对表达水平变化无统计学意义(P>0.05)。与对照组比,pcDNA3.1-CASP1组的G0/G1细胞周期被阻滞,cyclin D1的相对表达水平(对照组:1.00±0.12 vs.pcDNA3.1-CASP1组:0.52±0.08)减少,差异有统计学意义(均P<0.05)。与pcDNA3.1-null组比,pcDNA3.1-CASP1组的G0/G1细胞周期被阻滞,cyclin D1的相对表达水平减少(pcDNA3.1-null组:0.97±0.05 vs.pcDNA3.1-CASP1组:0.52±0.08),差异有统计学意义(P<0.05)。见图3和表1。

表1 cyclin D1的相对表达水平

图3 用流式细胞术检测过表达CASP1对THP-1细胞周期进程的影响
2.4过表达CASP1对THP-1细胞中炎症小体的影响:与对照组比,pcDNA3.1-null组的NLRP3、ASC、cleaved-CASP1的相对表达水平差异无统计学意义(均P>0.05)。与对照组比,pcDNA3.1-CASP1组的NLRP3、ASC、cleaved-CASP1的相对表达水平均增加,差异有统计学意义(均P<0.05)。与pcDNA3.1-null组比,pcDNA3.1-CASP1组的NLRP3、ASC、cleaved-CASP1的相对表达水平均增加,差异有统计学意义(均P<0.05)。见图4和表2。

表2 NLRP3 ASC cleaved-CASP1 CASP1的相对表达水平
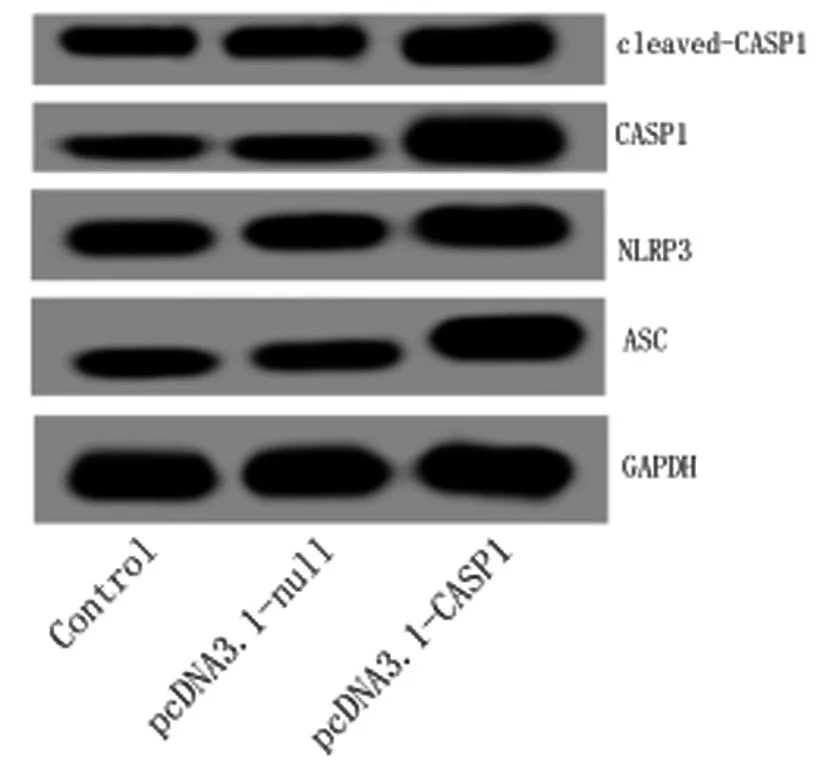
图4 Western blot法检测各组NLRP3、ASC、cleaved-CASP1、CASP1表达所得到的条带图
2.5过表达CASP1对THP-1细胞中CASP1、IL-1β,IL-18 mRNA水平的影响:与对照组比,pcDNA3.1-null组的CASP1、IL-1β,IL-18的相对mRNA水平差异无统计学意义(均P>0.05)。与对照组比,pcDNA3.1-CASP1组的CASP1、IL-1β,IL-18的相对mRNA水平均增加(均P<0.05)。与pcDNA3.1-null组比,pcDNA3.1-CASP1组的CASP1、IL-1β,IL-18的相对mRNA表达水平均增加(均P<0.05)。见表3。

表3 CASP1 IL-1β IL-18的相对mRNA
2.6过表达CASP1对THP-1细胞焦亡的影响:与对照组比,pcDNA3.1-null组的IL-1β,IL-18、cleaved-Gasdermin D(30 kDa)的相对表达水平差异无统计学意义(均P>0.05)。与对照组比,pcDNA3.1-CASP1组的IL-1β,IL-18、cleaved-Gasdermin D(30 kDa)的相对表达水平均增加(均P<0.05)。与pcDNA3.1-null组比,pcDNA3.1-CASP1组的IL-1β,IL-18、cleaved-Gasdermin D(30 kDa)的相对表达水平均增加(均P<0.05)。见图5和表4。
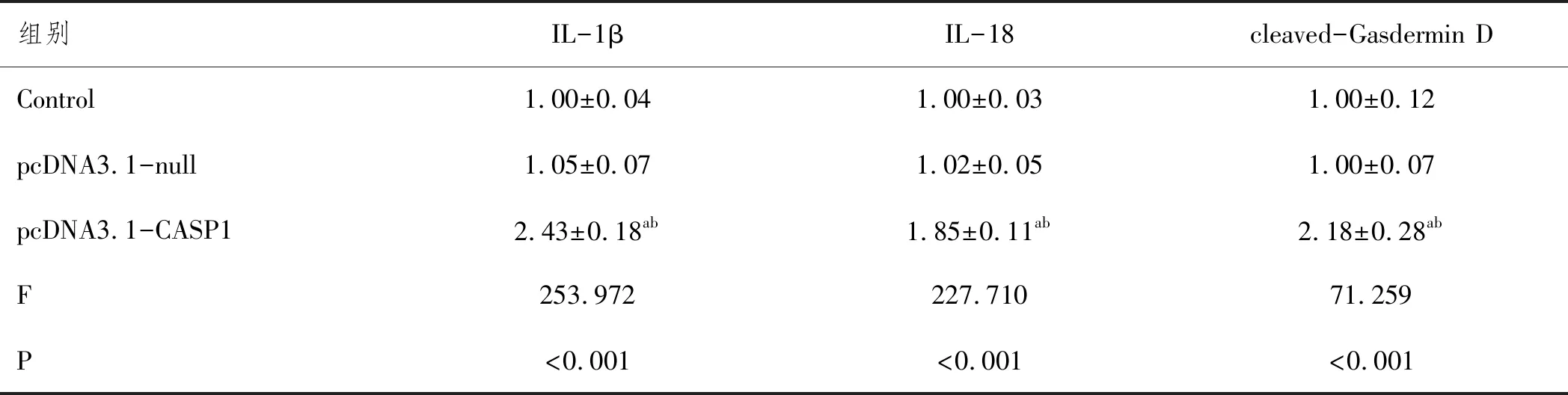
表4 IL-1β IL-18 cleaved-Gasdermin D的相对表达水平
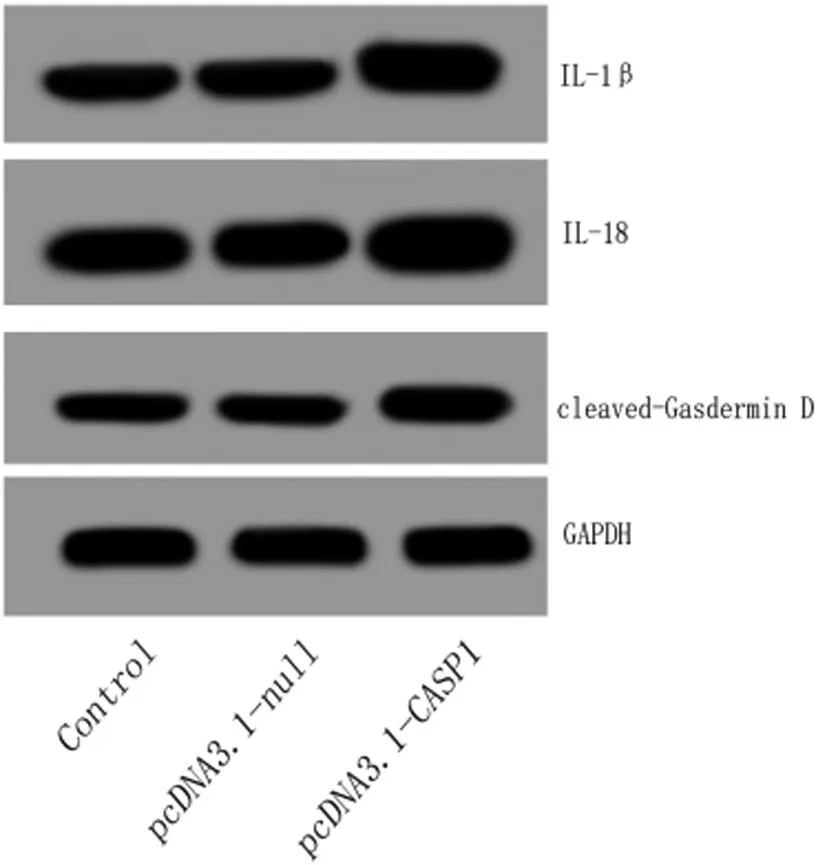
图5 Western blot法检测各组IL-1β,IL-18、cleaved-Gasdermin D表达所得到的条带图
3 讨 论
AML是人类最常见的恶性肿瘤,尤其是儿童和年轻人[6]。此外,在20岁以下人群中,白血病造成的死亡人数超过任何其他癌症。AML的特点是抑制细胞的凋亡和促进细胞的增殖,因此近年来,AML的治疗目标是促进白血病细胞凋亡和抗白血病细胞增殖[7]。先前的研究表明,炎性或病毒感染诱导的炎性小体会导致大多数阶段的癌症发展,并引起细胞焦亡。而最近的研究也表明,细胞焦亡同样在白血病中扮演重要角色[8]。然而,促进细胞焦亡以阻止AML细胞增殖或生长的研究报道仍然较少。CASP1是半胱氨酸-天冬氨酸蛋白酶家族的成员,与细胞凋亡过程密切相关。CASP1及其激活剂NLRP3是炎症小体的核心成分,CASP1能被NLRP3和ASC所招募从而激活NLRP3炎症小体,研究表明,CASP1在白血病中的过表达可导致糖皮质激素耐药[6]。此外,CASP1的遗传变异与慢性淋巴细胞白血病的风险相关。然而,到目前为止,CASP1对AML的调控作用和机制尚不清楚。因此,本研究探讨了CASP1对THP-1细胞行为的调控作用和潜在机制。通过在THP-1中过表达CASP1可明确观察CASP1对AML的调控作用并探讨可能存在的机制,特别是可以深入探讨NLRP3炎症小体激活后THP-1细胞的细胞行为学变化和潜在机制。本研究结果表明,过表达CASP1通过激活NLRP3炎症小体促进了THP-1细胞的周期阻滞和细胞焦亡。
细胞焦亡的典型途径中,炎性小体和前CASP1通过ASC与炎性复合体结合,然后激活CASP1。CASP1参与IL-1β与IL-18的激活和Gasdermin D的裂解。然后,GSDMD的N端片段易位到细胞膜上,引起细胞肿胀和孔形成,导致细胞质流出,导致细胞膜破裂。从而导致细胞焦亡。因此,肿瘤细胞的焦亡可以阻止肿瘤细胞增殖[9]。Liu等[6]发现CASP1的mRNA表达水平在白血病细胞系中升高,并且认为CASP1可能参与了AML的发病机制,该报道把CASP1作为预测AML预后的因素和AML患者的治疗靶点。在我们的研究中,过表达CASP1明显促进了细胞的凋亡活性并抑制了细胞的增殖活力,Xu等[9]也发现CASP1过表达可以通过激活细胞焦亡从而抑制前列腺癌细胞的增殖并促进细胞凋亡。这些结果提示了CASP1可能介导了细胞焦亡从而在AML细胞的恶性进展中扮演着重要作用。
研究表明,细胞焦亡发生时,Gasdermin D(53 kDa)被切割,产生30 kDa左右的片段cleaved-Gasdermin D[10]。另外,IL-1β和IL-18则会被大量释放到细胞中,参与Gasdermin D的切割和细胞肿胀和孔的形成[11]。为了进一步研究CASP1是否通过激活细胞焦亡从而扮演了抑制AML细胞增殖的作用,本研究检测CASP1过表达后THP-1细胞中CASP1、IL-1β、IL-18、cleaved-Gasdermin D的表达,结果显示,CASP1过表达可以明显促进CASP1、IL-1β、IL-18、cleaved-Gasdermin D的表达。因此表明,AML细胞过表达CASP1促进了细胞焦亡。
细胞周期的进展是由不同的细胞周期蛋白、细胞周期蛋白依赖性激酶及其抑制剂调控的,它们影响核苷酸代谢和DNA复制。cyclin D1通常有助于加速G1/S期的进展。本文数据显示,CASP1过表达抑制了近50%的cyclin D1表达,减少S期细胞数量,增加G0/G1期细胞数量,提示了THP-1中的CASP1过表达可以形成G0/G1阻滞,从而抑制THP-1细胞的增殖。
综上所述,本研究初步探讨了过表达CASP1诱导THP-1细胞中炎症小体并激活焦亡相关的信号通路。本研究数据表明,CASP1可以通过细胞周期阻滞和焦亡途径抑制THP-1细胞的细胞增殖。我们的研究为CASP1作为AML治疗靶点提供了新的见解。

