安菲博肽生物活性测定
戴向荣,梁杰,蒋涛,李刚,许雷鸣
[1.兆科药业(合肥)有限公司,合肥 230088;2.安徽省食品药品检验研究院,合肥 230051]
目前抗血小板药物根据不同的作用机制主要有环氧化酶(cyclooxygenase,COX)抑制剂,如阿司匹林;腺苷二磷酸(adenosine diphosphate,adp)受体拮抗剂,如氯吡格雷;磷酸二酯酶(phosphodiesterase,PDE)抑制剂,如双嘧达莫、西洛他唑;血小板膜糖蛋白Ⅱb/Ⅲa(platelet membrane glycoprotein Ⅱb/Ⅲa,GPⅡb/Ⅲa)受体拮抗剂,如替罗非班以及其他抗血小板药物,如奥扎格雷[1-4]。
GPⅡb/Ⅲa受体拮抗剂主要作用于血小板膜糖蛋白(glycoprotein,GP),通过阻断GPⅡb/Ⅲa与纤维蛋白原结合阻止血小板聚集[5-8]。GP是介导血小板聚集的关键成分,GPIb是血小板表面最主要的糖蛋白之一,与GPⅡb/Ⅲa介导的粘附机制不同,它通常只介导在高剪切力作用下的粘附[9-11]。GPIb与血管性血友病因子(von willebrand factor,vWF)特异性结合,使血小板粘附到血管壁上,导致血小板聚集,引起血栓[12-13]。因此,通过阻断GPIb与血浆vWF结合,可阻止血小板粘附在血管内皮细胞壁上,抑制血小板聚集。这种阻断作用不涉及凝血酶类及任何其他凝血因子,安全性高,将成为特异性更好的抗血栓药物的新方向。
安菲博肽(anfibatide,ANF)是从皖南尖吻蝮蛇毒中提取到的一种多肽药物,由α、β 链两条肽链组成,其比活力大于每毫克蛋白1 000个活力单位[14],是首创血小板GPIbα受体拮抗剂。在健康测试人中具有快速起效、有效及可逆的抗血栓作用,不损害凝血功能或延长出血时间。其作用机制为介导血小板聚集关键成分的GPIb 蛋白,阻断其与血浆vWF 结合,阻止血小板粘附在血管内皮细胞壁上,从而抑制血小板聚集[15]。抗血小板治疗是心血管病重要的治疗方法,由于其治疗后仍存在出血或再次血栓的问题,临床实验室可以通过检测血小板功能监测患者治疗情况。检测血小板功能有诸多方法,如光学比浊法、全血电阻法、连续血小板计数法等,其原理是通过观察诱聚剂引起血小板聚集前后血小板数量的改变来评估血小板功能[16-17]。本研究通过比较以上3种血小板功能检测方法,优选安菲博肽生物活性测定方法,并对该方法进行验证。
1 仪器与试药
1.1仪器 四通道光学聚集仪(CHRONO-LOG Corporation,型号:700),血小板聚集仪(CHRONO-LOG Corporation,型号:700),血小板功能分析仪(江苏英诺华医疗技术有限公司,型号:PL-12),真空采血管(Becton,Dickinson And Company,规格:0.109 M,3.2%枸橼酸钠),微量移液器[艾本德(上海)国际贸易有限公司,规格:10 μL,100 μL,1 000 μL];PL-12专用样品杯(江苏英诺华医疗技术有限公司)。
1.2试药 安菲博肽[兆科药业(合肥)有限公司,规格:每支10 U,批号:20180205、20180206、20190601];安菲博肽安慰剂[兆科药业(合肥)有限公司,批号:20190603];0.9%氯化钠溶液(华润双鹤利民药业有限公司,批号:21011301B);PLR-01血小板稀释液(江苏英诺华医疗技术有限公司,批号:22006022)、血小板分析仪专用清洗液(江苏英诺华医疗技术有限公司,批号:22001151);瑞斯托霉素(American Biochemical &Pharmaceuticals Ltd.,批号:880204)。
2 方法与结果
2.1溶液的制备
2.1.1诱聚剂的配制 取1支瑞斯托霉素(ristomycin,RIS)冻干粉,加0.9%氯化钠溶液配制成100 mg·mL-1RIS母液,分装,-20 ℃冰箱保存;检测前取出,室温溶解后混匀,0.9%氯化钠溶液稀释至250 mg·mL-1(光学比浊法、全血电阻法)和7.7 mg·mL-1(连续血小板计数法),备用。
2.1.2血样的制备
2.1.2.1富血小板血浆(platelet-rich plasma,PRP)的制备 抽取健康受试者血液,置含有1/10体积枸橼酸钠抗凝液(0.109 mol·L-1)的硅化玻璃管中混匀,1 000 r·min-1(r=8.2 cm)离心6 min,收集上清液。
2.1.2.2贫血小板血浆(platelet-poor plasma,PPP)的制备 将上述剩余血液4 000 r·min-1(r=8.2 cm)离心10 min,取上清液。
2.1.2.3全血取样 空腹或餐后2 h采用肘静脉取血法采取健康人血液于真空采血管中备用。本试验已获得蚌埠医学院第一附属医院临床医学研究伦理委员会审查通过批件。
2.1.3供试品溶液配制 取安菲博肽(每支10 U)3支,每支加入0.9%氯化钠溶液200 μL溶解,合并,混匀,备用。
2.1.4空白溶液的配制 取0.9%氯化钠溶液10 μL和全血290 μL,置PL-12专用样品杯,轻轻混匀样品,室温孵育5 min,备用。
2.1.5空白辅料溶液的配制 取安菲博肽安慰剂(批号:20190603)3支,每支加0.9%氯化钠溶液200 μL溶解,合并、混匀,取稀释空白辅料溶液10 μL和全血290 μL至PL-12专用样品杯,轻轻混匀样品,室温孵育5 min,备用。
2.2方法步骤
2.2.1光学比浊法 以PPP 350 μL进行透光率调节。比浊管中加入PRP 350 μL,37 ℃孵育3 min,加入125 mg·mL-1诱聚剂7.2 μL,记录对照管血小板聚集百分率。比浊管中加入PRP 350 μL,加入供试品溶液10 μL,37 ℃孵育3 min,加入125 mg·mL-1诱聚剂7.2 μL,记录样品管血小板聚集百分率。血小板聚集抑制百分率(%)=(对照管血小板聚集百分率-样品管血小板聚集百分率)/对照管血小板聚集百分率×100%。
2.2.2全血电阻法 取全血0.5 mL,加入0.9%氯化钠溶液0.5 mL,37 ℃孵育3 min,加入电极放入检测通道,然后加入诱聚剂20 μL(125 mg·mL-1),记录聚集曲线,测定电阻值,为对照电阻值。取全血0.5 mL,加入0.9%氯化钠溶液0.5 mL和供试品溶液10 μL,37 ℃孵育3 min,加入电极放入检测通道,再加入诱聚剂20 μL(125 mg·mL-1),记录聚集曲线,测定电阻值,为供试品电阻值。血小板聚集抑制百分率(%)=(对照管电阻值-供试品电阻值)/对照管电阻值×100%。
2.2.3连续血小板计数法 将含待测供试品溶液(或空白溶液)的PL-12样品杯,移至PL-12全自动血小板功能分析仪自动检测。检测开始后,首先进行2次血小板基础值计数(最终基础值为2次平均值),然后自动加入7.7 mg·mL-1RIS诱聚剂30 μL,当血小板计数达到最低时停止检测,计算最大聚集率(maximal aggregation ratio,MAR)。MAR(%)=(最终基础血小板数-最低血小板数)/最终基础血小板数×100%,血小板聚集抑制率(%)=(空白溶液聚集率-供试品溶液聚集率)/空白溶液聚集率×100%。
2.3数据分析方法 采用SPSS19.0版统计软件分析,多组样本间差异采用单因素方差(One-way ANOVA)分析方法,对数据进行分析。
2.4方法筛选 分别以光学比浊法、全血电阻法和连续血小板计数法对3批安菲博肽进行活性检测,结果见表1—3。3种不同方法检测3批安菲博肽活性,均差异无统计学意义,说明3种方法检测安菲博肽活性结果呈正相关。此前,也有通过光学比浊法与连续血小板计数法监测血小板聚集功能的比较,证实连续血小板计数法对全血标本检测与光学比浊法在检测血小板聚集功能时具有较好相关性[16-17]。综上,连续血小板计数法检测安菲博肽活性,RSD较小,检测数据较其他2种检测方法更稳定,故采用连续血小板计数法检测安菲博肽生物学活性。
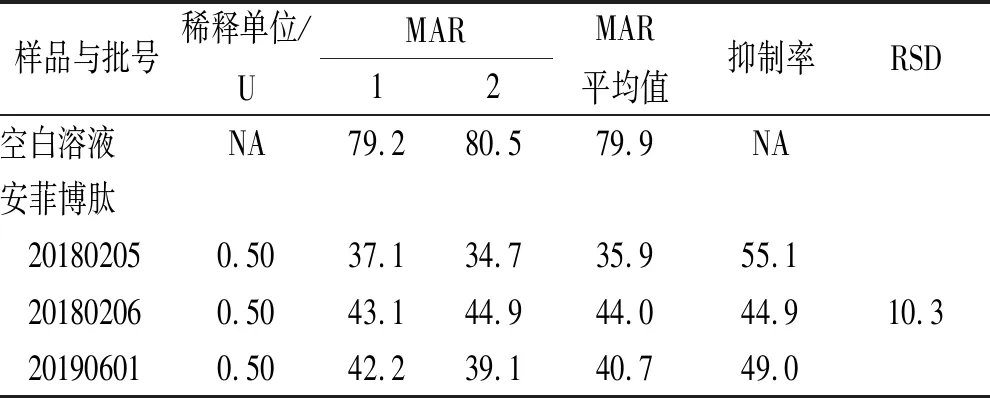
表1 安菲博肽活性检测结果(光学比浊法)
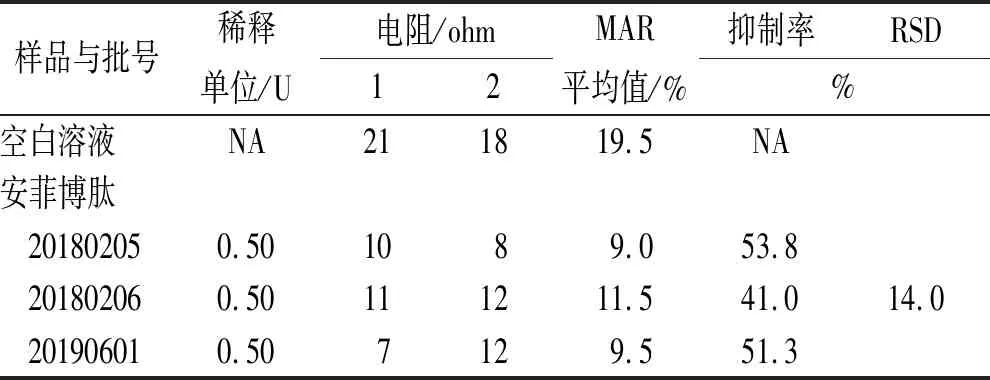
表2 安菲博肽活性检测结果(全血电阻法)
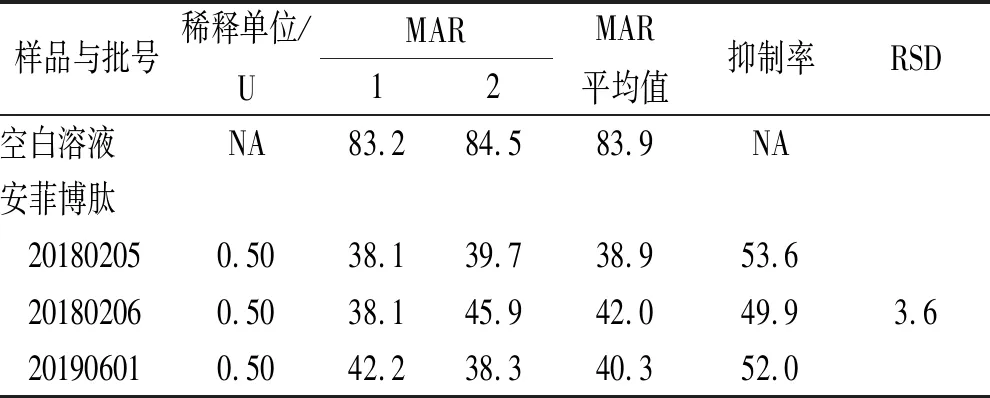
表3 安菲博肽活性检测结果(连续血小板计数法)
2.5方法学考察
2.5.1专属性考察 考察空白溶液(0.9%氯化钠溶液)、空白辅料溶液是否干扰安菲博肽活性检测结果,结果见表4。由表4可知,空白溶液、空白辅料溶液抑制率为0,不干扰安菲博肽活性检测。
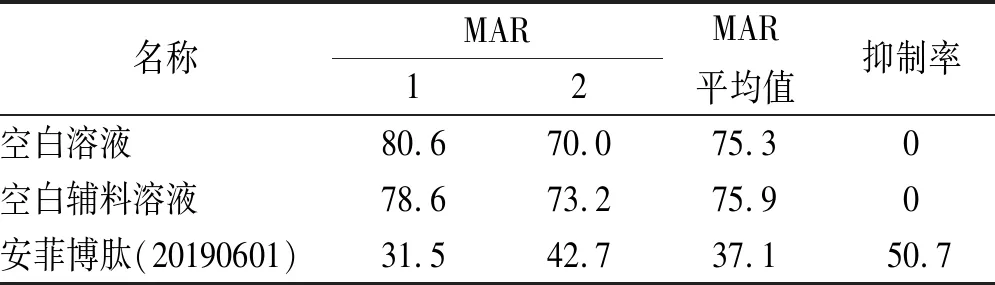
表4 专属性实验结果
2.5.2线性范围考察 配制0.30、0.35、0.40、0.45和0.50 U供试品溶液(批号:20190601),平行测定,结果见表5。以供试品活性单位(U)为横坐标,抑制率(%)为纵坐标,拟合标准曲线得Y=1.334X+0.062 4,相关系数r为0.994(>0.990)。安菲博肽活性检测在0.3~0.5 U范围内呈线性关系。
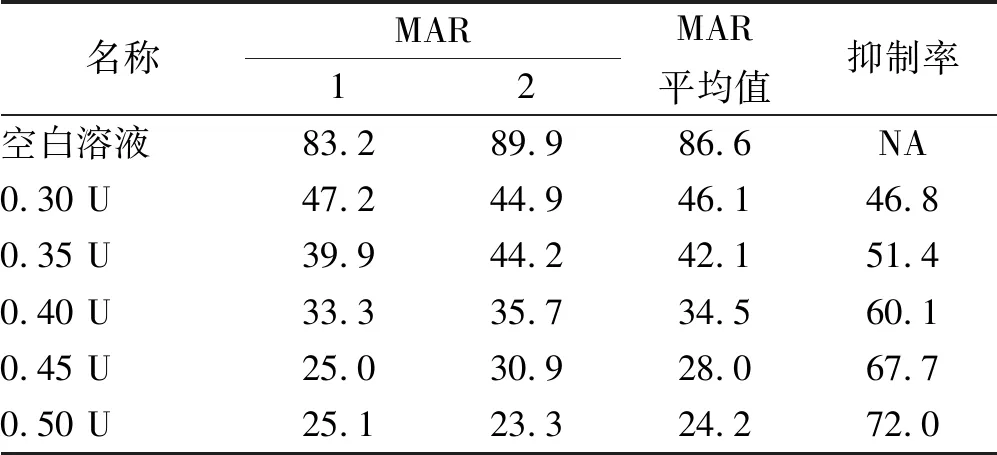
表5 线性范围考察结果
2.5.3精密度考察
2.5.3.1重复性 分别配制供试品溶液6组(批号:20190601),平行测定,结果见表6。由表6可知,6组样品抑制率RSD为11.0%(<20%)。
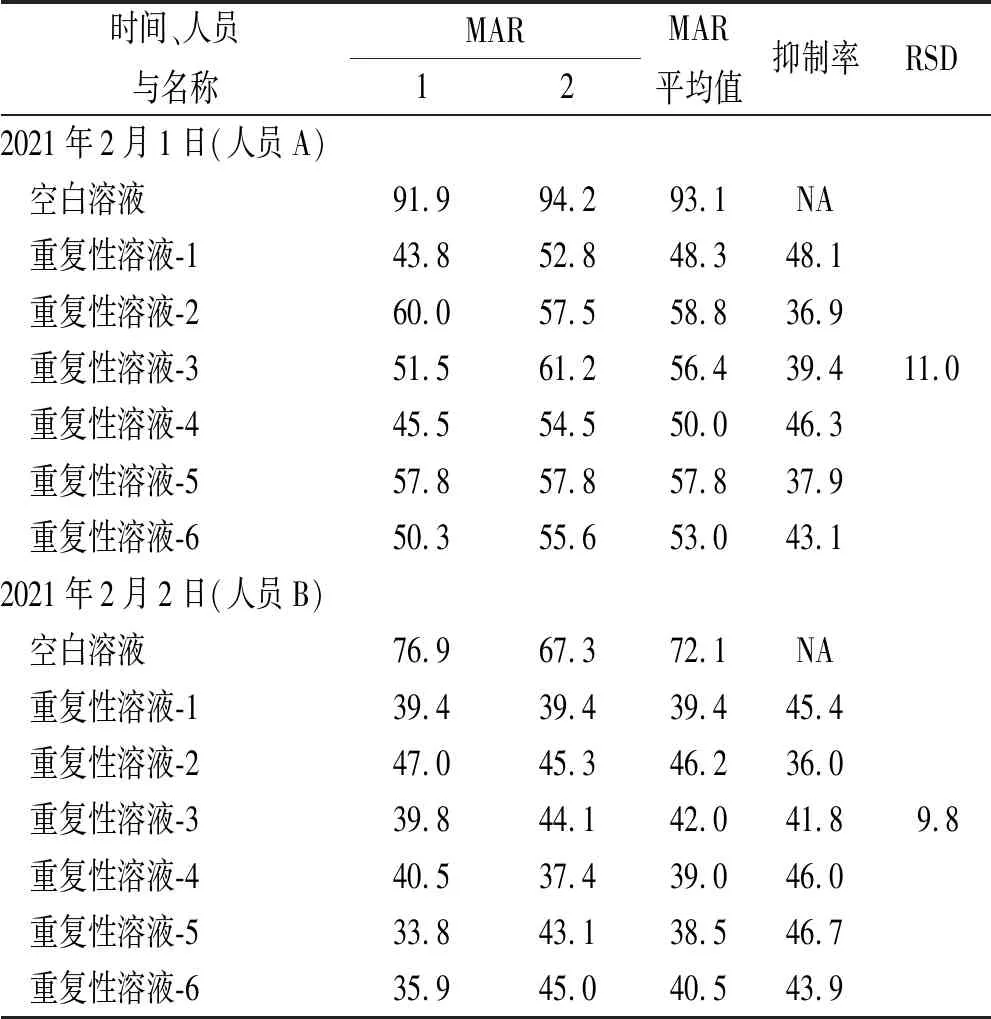
表6 精密度、重复性、中间精密度实验结果
2.5.3.2中间精密度 不同时间、不同人员分别配制供试品溶液6组(批号:20190601),平行测定,结果见表6。结合重复性检测结果,12组样品抑制率RSD为9.8%(<20%)。
2.5.4不同人血样对活性的影响 考察不同人血样对连续血小板计数法检测安菲博肽活性的影响,随机采用6份不同人的血样作为样本,另取2份处于血小板正常范围[(100~350)×109·L-1]上限和下限血样,作为样本7(85×109·L-1)、样本8(383×109·L-1);以上述空白溶液、安菲博肽(批号:20190601)于血小板功能分析仪检测样品溶液的抑制率。结果见表7,以6份随机不同人血样检测得安菲博肽(批号:20190601)抑制率为50.7%、48.1%、43.3%、45.4%、47.4%、43.7%,RSD为6.2%,以样本7、样本8血样检测得安菲博肽(批号:20190601)的抑制率为45.3%、42.8%,RSD为4.0%,可知不同人血样不影响连续血小板计数法检测安菲博肽的生物活性。
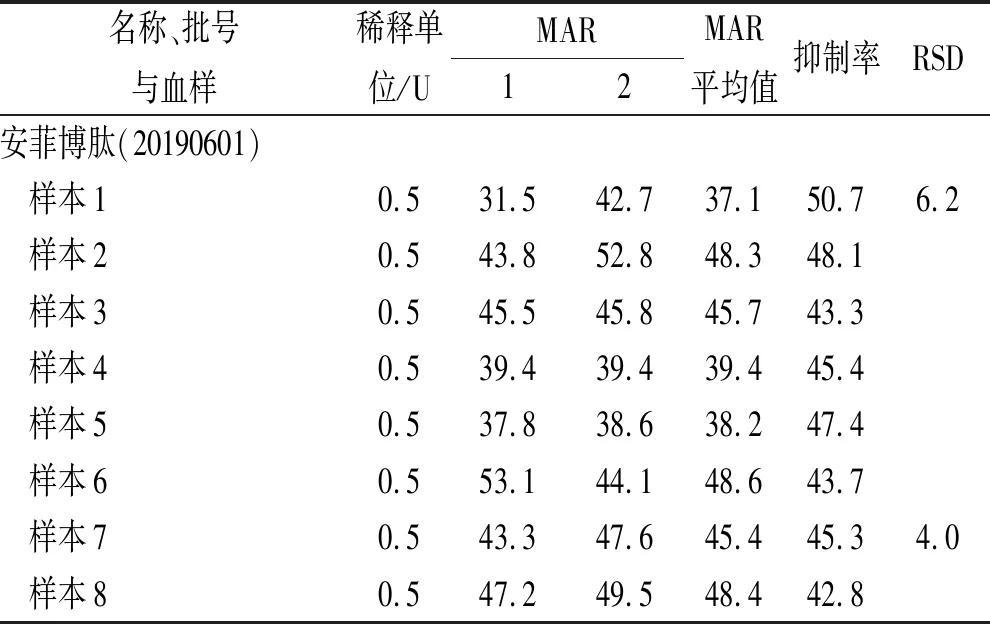
表7 不同人血样对安菲博肽活性测定的影响
3 讨论
光学比浊法应用于血小板功能检测比较广泛,甚至被认为是血小板功能检测方法的“金标准”,但该法存在操作繁杂、质量控制难等问题[18-19]。全血电阻法则通过加入诱导剂,诱导血小板聚集,因电极回路中电阻增加,电流减少,仪器通过检测电阻的变化来确定血小板聚集率[20]。连续血小板计数法是以库尔特原理为基础的新型血小板功能检测方法,通过观察诱聚剂引起血小板聚集前后全血中血小板数量的改变来评估血小板功能[16]。通过光学比浊法、全血电阻法、连续血小板计数法检测安菲博肽活性,3种方法检测安菲博肽活性结果呈正相关,且连续血小板计数法检测安菲博肽活性RSD较小,检测数据更稳定。因此,本实验确定以连续血小板计数法、以药物抑制率为评价指标检测安菲博肽的生物活性。
笔者在本实验建立了安菲博肽活性测定方法,并通过对方法专属性、精密度、准确度、线性范围进行验证,该方法操作简便,专属性、准确度和精密度符合生物制品活性测定要求。通过测定3批次安菲博肽活性,3批次结果一致,说明批次之间质量稳定和均一。所建立的方法可用于该产品的质量控制和一致性分析,同时可为其他类型蛋白药物的质量控制提供参考。

