中药及其天然产物通过靶向铁死亡治疗癌症研究进展*
焦泉慧,钟凌云,程子文,吕小斌,章常华
(1.江西中医药大学药学院,南昌 330004;2.南昌市第一医院中心实验室,南昌 330008)
铁死亡是调节细胞死亡的一种形式,主要依赖于铁介导的氧化损伤和细胞膜损伤,在形态、生化和遗传上不同于细胞凋亡、坏死和自噬[1]。其形态学特征包括线粒体变小,膜密度增加,线粒体嵴减少或消失,以及线粒体外膜破裂;生化特征包括细胞内铁积累,活性氧(reactive oxygen species,ROS)过量产生,谷胱甘肽(glutathione,GSH)水平降低和脂质过氧化[2]。铁死亡可通过外源性或内源性途径引起,外源性途径是通过调控转运蛋白,如抑制溶质载体家族7成员11(solute carrier family 7 member 11,SLC7A11),而内源性途径主要通过阻断细胞内抗氧化酶的表达或活性,如谷胱甘肽过氧化物酶4 (glutathione peroxidase 4,GPX4)[3]。自2012年提出铁死亡概念以来,许多研究表明,其在癌症治疗中发挥至关重要的作用[4-5],调控铁死亡可影响肿瘤对药物的敏感性,甚至逆转耐药[6]。因此,靶向铁死亡可能成为治疗癌症和逆转耐药性的可行治疗策略。中药在调节铁死亡方面有显著作用,并已有研究表明多种基于中药的天然成分可以诱导铁死亡的发生[7-9]。笔者在本文重点总结中药及其天然产物通过靶向铁死亡治疗癌症的机制及应用,为癌症治疗和逆转耐药性提供新思路。
1 中药及其天然产物通过靶向不同信号通路诱导铁死亡发挥抗癌作用
近年来的研究表明,中药及其天然产物可以通过靶向SLC7A11/ GPX4、P53、核因子E2相关因子2(nuclear factor erythroid 2-related factor 2,NRF2)/血红素加氧酶-1(heme oxygenase-1,HO-1)、铁蛋白重链(ferritin heavy chain 1,FTH1)等不同信号通路诱导癌细胞铁死亡,具有潜在的抗癌活性,为癌症治疗提供了新的研究思路(图1,图2)。
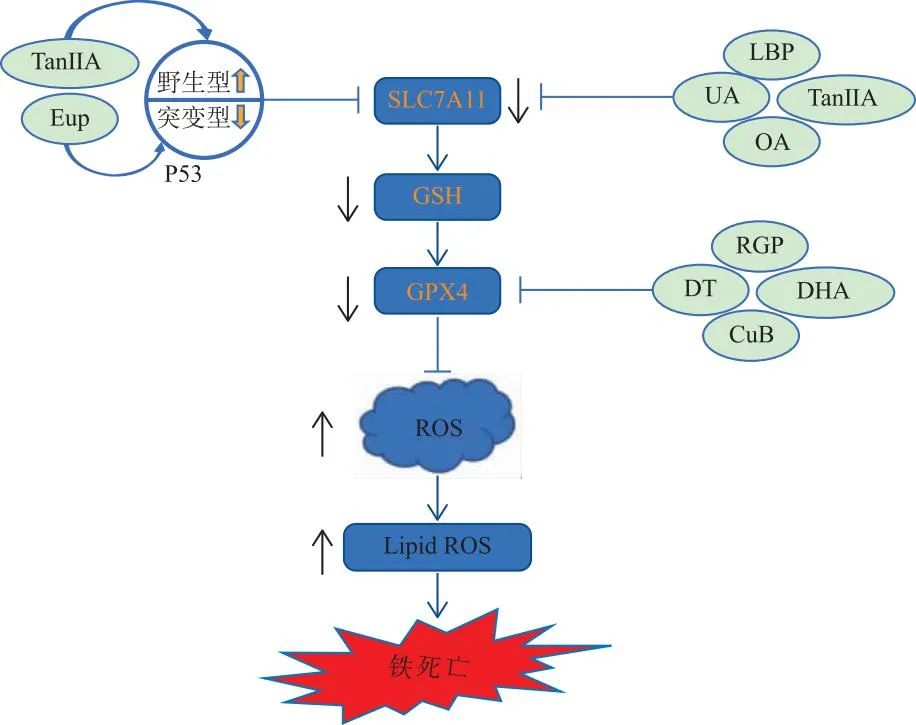
↑:增加;↓:减少。
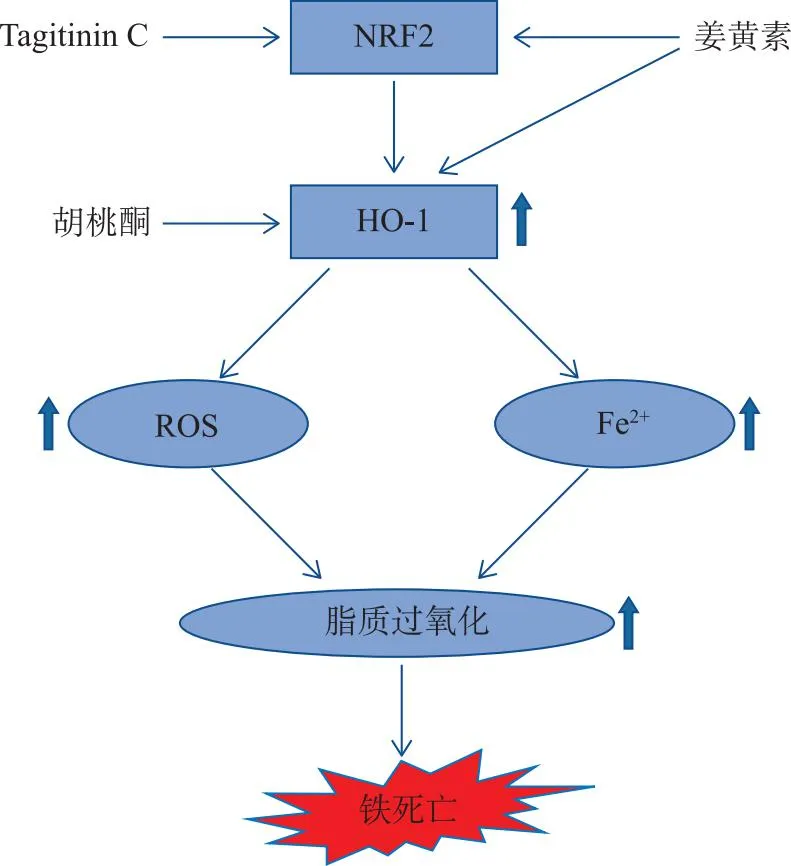
↑:增加;↓:减少。
1.1SLC7A11/GPX4 SLC7A11是一种胱氨酸/谷氨酸交换转运蛋白,介导细胞摄取胱氨酸,从而影响GSH的合成[10]。GSH是细胞内主要的抗氧化剂[11],其耗竭会降低GPX4的表达和活性,GPX4是一种抗氧化酶,其活性是抗过氧化防御的基石,研究表明GPX4失活是导致铁死亡的重要因素[12]。
枸杞多糖(lycium barbarum polysaccharide,LBP)是中草药枸杞果实的提取物,通过调节SLC7A11/GPX4通路,降低GSH合成,促使乳腺癌细胞发生铁死亡[13]。红参多糖(red ginseng polysaccharide,RGP)是人参的活性成分,可以剂量依赖方式显著降低肺癌和乳腺癌细胞中GPX4的表达,导致ROS积累,抑制细胞增殖,RGP通过下调GPX4诱导铁死亡而显示抗癌活性[14]。中华猕猴桃(actinidia chinensis planch,ACP)的提取物熊果酸(ursolic acid,UA)和齐墩果酸(oleanolic acid,OA)是两种主要的三萜类抗肿瘤成分,通过抑制SLC7A11和GPX4的表达诱导胃癌细胞中的ROS积累和铁死亡[15]。葫芦素B(cucurbitacin B,CuB)是一种广泛使用的三萜类化合物,其通过下调GPX4表达和增加脂质过氧化诱导鼻咽癌细胞铁死亡[16]。丹参中的二氢异丹参酮I(dihydroisotanshinone I,DT)可抑制GPX4蛋白表达,丹参酮IIA(tanshinone IIA,Tan IIA)可剂量依赖性地降低SLC7A11的表达,两者均通过引起脂质过氧化诱导铁死亡[17-18]。中草药单体二氢青蒿素(dihydroartemisinin,DHA)可显著增加细胞内Fe2+含量,进而产生ROS,ROS的产生耗尽GSH,使GPX4失活,导致脂质过氧化积累,进而诱发铁死亡[19]。DHA也可通过下调细胞中GPX4表达诱导铁死亡[20]。18-β-甘草次酸(glycyrrhetinic acid,GA)是一种从甘草中提取的活性化合物,通过抑制SLC7A11表达和GPX4活性,耗竭GSH,加剧脂质过氧化和铁死亡[21]。
1.2P53 P53基因是人类肿瘤抑制基因,包括野生型和突变型。野生型P53基因能诱导肿瘤细胞凋亡,预防肿瘤发生,而突变型P53基因则促进肿瘤细胞癌变[22]。研究表明,野生型P53通过抑制SLC7A11的表达,限制胱氨酸摄取,从而诱导细胞发生铁死亡[23]。Tan IIA可以上调野生型P53表达,抑制SLC7A11在胃癌细胞中的表达,降低细胞内半胱氨酸和GSH水平,进而诱导铁死亡[24]。野生型P53的持续激活可导致ROS水平升高并增加细胞对铁死亡的敏感性[25]。人参皂苷Rh4是人参的主要药理活性成分,可通过激活ROS/P53信号通路诱导铁死亡来抑制癌细胞增殖[26]。从中药大麻叶泽兰中提取的天然化合物泽兰内酯 (eupaformosanin,Eup)可降低突变型P53的表达,通过脂质过氧化积累、GSH耗竭和游离铁增加诱导三阴性乳腺癌细胞中的铁死亡发挥抗癌作用[27]。
1.3NRF2/HO-1 NRF2是细胞维持氧化稳态所需的关键调节因子[28]。研究表明,NRF2可以通过调节SLC7A11和HO-1来调控铁死亡[29]。HO-1上调促进血红素的降解和铁蛋白的合成,改变细胞中铁分布,通过促进铁积累和ROS产生来增加或诱导铁死亡[30]。Tagitinin C是一种从肿柄菊中分离出来的倍半萜内酯,可诱导内质网应激和氧化应激,上调NRF2在细胞中的表达,从而激活NRF2核易位,导致其下游基因HO-1的表达显著增加,游离铁增加,促进脂质过氧化[31]。胡桃酮是从山核桃绿皮中分离得到一种萘醌类化合物,可通过激活HO-1介导子宫内膜癌中血红素的降解,增加游离铁积累,从而诱导铁死亡[32]。姜黄根茎的提取物姜黄素,是一种多酚化合物,不仅直接激活HO-1,而且还通过激活NRF2上调HO-1表达,HO-1上调和GPX4下调直接触发乳腺癌细胞ROS产生,诱发铁[30]。
1.4FTH1 铁死亡是一种铁依赖性、非凋亡的细胞死亡方式,过量的铁催化芬顿反应产生高活性羟基自由基,增强脂质过氧化,引发铁死亡。铁可以储存在铁蛋白或血红素中,铁蛋白是真核细胞主要的铁储存蛋白,包括铁蛋白轻链(ferritin light chain,FTL)和FTH1两个亚基[33]。FTH1下调可使细胞内游离铁增加,诱导铁死亡。黄芩苷是从黄芩根部提取的黄酮类生物活性物质,通过下调FTH1使细胞内ROS和游离铁积累,诱导膀胱癌细胞铁死亡,体内外FTH1的过表达均阻断了黄芩苷的抗癌作用[34]。姜黄烯醇是从姜黄中分离出来的天然产物,通过 LncRNA H19/miR-19b-3p/FTH1 轴诱导肺癌细胞铁死亡[35]。穗花杉双黄酮(amentoflavone,AF)以剂量依赖性方式增加自噬相关基因LC3B、beclin1、ATG5、ATG7的表达,下调FTH1表达,增加细胞内游离铁水平,促进ROS产生,诱导铁死亡[36]。
1.5其他 齐墩果酸(oleanolic acid,OA)是一种天然存在于植物中的五环三萜类化合物,具有抗癌活性。它通过促进酰基辅酶A合成酶长链家族成员4(acyl-CoA synthetase long chain family member 4,ACSL4)介导的铁死亡,抑制宫颈癌细胞的生长和增殖[37]。油茶(camellia nitidissima chi,CNC)中主要含有黄酮类、皂苷和多酚类成分,后者通过抑制GPX4、FTH1表达和促进HO-1、P53表达,介导铁死亡途径发挥其抗结肠癌作用[38]。
姜黄素通过激活非小细胞肺癌自噬诱导铁死亡,姜黄素处理后,细胞线粒体膜破裂和线粒体嵴减少,Beclin1和LC3水平升高,SLC7A11和GPX4水平降低,铁超负荷、GSH消耗和脂质过氧化[39]。6-姜辣素(6-gingerol )是一种天然存在于生姜中的苯酚,通过抑制 USP14-beclin1促进自噬效应,增加自噬体数量、ROS和游离铁浓度来抑制肺癌细胞生长[40]。DHA通过调节AMPK/mTOR/p70S6k信号通路活性诱导自噬,加速铁蛋白降解,增加游离铁含量,促进细胞ROS积累,最终导致急性髓细胞白血病细胞铁死亡[41]。
淫羊藿素(erianin)可通过钙/钙调蛋白依赖性铁死亡抑制肺癌细胞的生长和迁移[42]。羽扇豆醇通过提高鼻咽癌细胞中AMPKα磷酸化,促进铁分泌和脂质过氧化,诱导铁死亡发挥抗癌作用[43]。丝裂原活化蛋白激酶(mitogen-activated protein kinase,MAPK)信号通路与铁死亡的靶向治疗有关,青蒿琥酯通过激活MAPK/细胞外信号调节激酶(extracellular signal-regulated kinase,ERK)和MAPK/p38通路诱导胶质母细胞瘤细胞铁死亡[44]。毛枝卷柏中的双黄酮类化合物RF-A通过上调电压依赖性阴离子通道2(voltage dependent anion channel 2,VDAC2)蛋白和下调Nedd4蛋白(VDAC2的泛素连接酶),显著诱导人乳腺癌细胞铁死亡[45]。红景天苷通过调节转铁蛋白和运铁素水平,增加细胞内Fe2+浓度和ROS产生,诱导铁死亡[46]。鸡血藤素(auriculasin )是从千斤拔中分离出的一种多酚类黄酮,通过浓度依赖方式促进ROS产生,引发结直肠癌(colorectal cancer,CRC)细胞铁死亡[47]。
2 中药与其他药物联合使用增强药物疗效
癌症治疗现在仍以药物治疗为主,获得性耐药性仍是临床治疗面临的重大挑战。联合用药可以增强药效,降低副作用,并减少或减缓耐药性发展。研究表明,一些中药及其活性成分同时具有抗癌和化学增敏作用,可以显著增强肿瘤细胞对化疗药物和靶向药物的敏感性,改善治疗效果并减少不良反应[48]。
中药及其天然产物可以通过诱导铁死亡增强化疗药物在癌症治疗中的敏感性,提高化疗疗效。例如,穿心莲内酯通过激活铁死亡途径增强结直肠癌细胞对氟尿嘧啶(5-fluorouracil,5-FU)的化学敏感性[49]。白杨素通过调节自噬和铁死亡增强胰腺癌细胞对吉西他滨的化学敏感性[50]。醉茄素A(withaferin A)通过调节Keap1/NRF2相关的EMT和铁死亡,减弱索拉非尼耐药性,增强肝细胞癌对索拉非尼的敏感性[51]。β-榄香烯与西妥昔单抗联合作用后,可显著诱导铁死亡的发生,增加KRAS突变的CRC细胞对西妥昔单抗的敏感性[52]。Ent-kaurane二萜类化合物通过抑制抗氧化系统增加细胞内ROS水平,诱导细胞铁死亡,增强肺癌细胞对顺铂的敏感性[53]。
中药及其天然产物与化疗药物联合使用,可以通过激活铁死亡发挥协同治疗效应,减少化疗药物的剂量。例如,DHA通过调节铁代谢诱导胰腺导管腺癌的铁死亡,与顺铂联合治疗可增强顺铂的细胞毒性,并显著降低其在体内外的有效浓度[54]。熊果酸和顺铂联合治疗通过协同激活自噬、铁蛋白降解、游离铁积累和脂质过氧化诱导铁死亡,增强对骨肉瘤的抑制作用[55]。银杏黄酮通过降低SLC7A11和GPX4表达诱导铁死亡,增加顺铂对非小细胞肺癌细胞的细胞毒作用[56]。熊果酸和索拉非尼联合应用可诱导SLC7A11依赖性铁死亡,对抗肿瘤有协同作用[57]。DHA和索拉非尼的联合应用显著降低了肝癌细胞HepG2中SLC7A11和HO-1蛋白的水平,对HepG2细胞具有协同抑制作用[58]。青蒿琥酯与索拉非尼联合应用,通过诱导铁死亡降低索拉非尼使用剂量[59]。
3 结论与展望
中药及其天然产物在治疗疾病方面具有独特的临床优势,包括靶点多、毒副作用少、疗效强和经济负担低,已广泛用于各种疾病的治疗,也用于癌症的辅助治疗。丹参、齐墩果酸、二氢青蒿素、姜黄素等中药及其天然产物作为铁死亡诱导剂,具有明显的抗癌活性。它们通过靶向不同通路如SLC7A11/GPX4、P53、NRF2/HO-1、FTH1等,诱导铁死亡,具有良好的治疗潜力,为临床癌症治疗提供有价值参考。穿心莲内酯、白杨素、DHA、熊果酸等具有抗癌活性的中药活性成分也可能是一种有效的化学增敏剂,可以同时靶向多个机制干扰铁死亡,增强化疗药物的药效,克服耐药性。总的来说,中药及其天然产物可能成为铁死亡治疗的潜在候选药物。许多天然产物在各种类型的癌症中显示出与传统化学疗法或靶向药物的协同反应,能更有效地降低全身毒性的风险,提高治疗效果并降低成本,为癌症治疗开辟新途径。尽管中药和天然产物在铁死亡治疗癌症方面的潜力已经被证实,但仍需要进一步深入研究来确定其效果和安全性。

