早期强化降压对高血压脑出血患者神经功能及近期预后的影响
俞凡 赵林军 吴泽生 郑娉娉
高血压脑出血(hypertensive cerebral hemorrhage,HICH)是高血压患者的严重并发症之一,起病急且进展迅速,具有较高的致残率和病死率[1]。早期血肿扩大及继发性脑水肿是导致HICH患者病情加重及预后不良的关键原因之一。越来越多学者认为在发病早期启动强化降压治疗可能有助于抑制血肿扩大,从而减轻神经功能损伤,改善临床预后[2,3]。目前关于早期强化降压与常规降压的优劣仍有争议。本次研究旨在分析早期强化降压与常规降压对HICH患者血压变化、水肿体积、血肿扩大情况、神经功能及近期预后的影响,旨在为HICH患者的血压管理提供参考依据。现报道如下。
1 资料与方法
1.1 一般资料 选取2021 年1 月至2022 年12 月期间浙江大学医学院附属杭州市第一人民医院收治的HICH 患者150 例为研究对象。纳入标准为:①符合HICH 的临床诊断标准[4],经头颅CT、核磁共振等检查结合高血压病史确诊;②发病时间<6 h;③年龄≥40 岁;④血肿体积<30 mL 并接受保守治疗;⑤入院时收缩压(systolic blood pressure,SBP)在150~220 mmHg;⑥临床资料完整。排除标准为:①严重颅内高压伴发脑疝;②格拉斯哥昏迷量表(glasgow coma scale,GCS)评分<5 分;③因颅内动脉瘤破裂、脑梗死、脑外伤、脑血管畸形、动脉瘤、恶性肿瘤、凝血功能障碍等其他疾病所致脑出血;④长期使用抗血小板药物,具有出血倾向或合并活动性上消化道出血;⑤合并严重心、肝、肾功能不全;⑥相关药物过敏或过敏体质。根据降压方案的不同将入组患者分为研究组和对照组,每组75 例。两组患者在性别构成、年龄、体重指数(body mass index,BMI)、高血压病程、发病至入院时间、合并症、吸烟史、出血部位、入院时SBP、GCS评分、血肿体积方面见表1。两组比较,差异均无统计学意义(P均>0.05)。
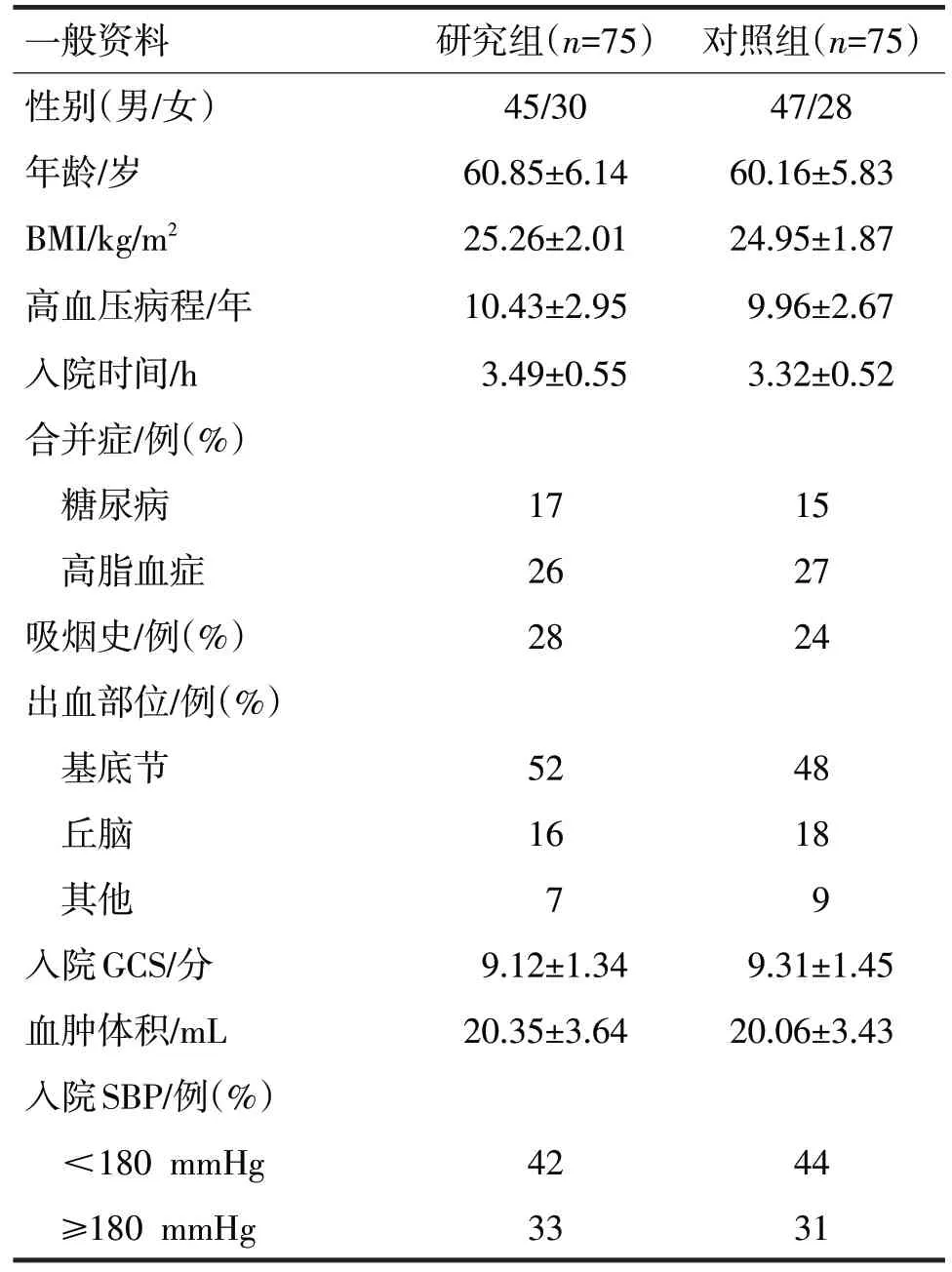
表1 两组患者一般资料比较
1.2 方法 对照组患者采用常规标准降压治疗,即SBP<180 mmHg 或平均动脉压(mean arterial pressure,MAP)<130 mmHg 者,先予严密生命体征监测、吸氧、止血等治疗,不予药物降压治疗;SBP≥180 mmHg 或MAP≥130 mmHg 时,予以降压药物控制SBP 在160~180 mmHg,MAP 在100~130 mmHg,且首次用药24 h内血压降幅≤20%。研究组采用早期强化降压治疗,即所有患者均静脉使用降压药物在入院3 h内控制SBP 至120~140 mmHg,此后改为长效口服降压药控制,或维持SBP在120~140 mmHg直至发病后1 周。静脉降压药物首选乌拉地尔100 mg稀释至50 ml 静脉泵注,口服降压药物首选依那普利片5 mg,每天1 次,视血压反应调整剂量至10~40 mg,分2~3 次服用,如血压控制不达标可加用钙离子通道阻滞剂、利尿剂。发病6 h内,如无脑疝形成及明显占位效应者,均不予以应用甘露醇。
1.3 观察指标
1.3.1 血肿变化情况 于治疗后3 d 进行头颅CT扫描,测量最大血肿面积层面血肿的最长径(a)与最长径垂直的最长径(b),按照多田公式计算血肿体积(V),V=a×b×扫描层数/2,破入脑室的血肿暂时忽略不计。统计3 d 内血肿扩大发生率,以血肿体积增大1/3或增加>12.5 mL判定为血肿扩大[5]。治疗后7 d、14 d 再次复查头颅CT,以CT 值5~23 HU 判定水肿范围,计算绝对脑水肿体积,绝对脑水肿体积(mL)=水肿与血肿复合体积-血肿体积[6]。
1.3.2 神经功能评估 分别于治疗前及治疗后7 d、14 d,采用美国国立卫生院脑卒中量表(national institutes of health stroke scale,NIHSS)评价神经功能缺损程度,总分42 分,得分越高则神经功能缺损程度越重。
1.3.3 近期预后评估 发病后90 d,采用改良Rankin 评分量表(improved Rankin rating scale,mRS)评价患者的临床预后。康复(0 分)、轻残(1~2 分)、中残(3~4 分)、重残(5 分)、死亡(6 分),计算预后良好率,预后良好率=(康复+轻残)/总例数×100%,即mRS≤2 分的人数占比。
1.4 统计学方法 采用SPSS 22.0统计学软件进行数据分析,计量资料以均数±标准差()表示,比较采用t检验;计数资料以百分率(%)表示,采用χ2检验。设P<0.05为差异有统计学意义。
2 结果
2.1 两组血肿扩大率比较见表2
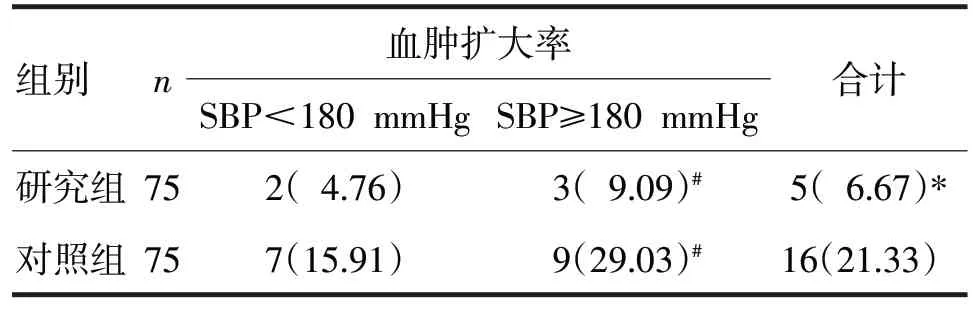
表2 两组不同SBP水平患者血肿扩大率比较/例(%)
由表2 可见,治疗3 d 内,研究组的血肿扩大率低于对照组(χ2=7.75,P<0.05),且在两组内SBP≥180 mmHg者发生血肿扩大率均较SBP<180 mmHg者更高(χ2分别=5.56、11.63,P均<0.05)。
2.2 两组不同时间点绝对脑水肿体积变化比较见表3

表3 两组不同时间点绝对脑水肿体积变化比较/mL
由表3可见,治疗3 d、7 d、14 d时,两组的绝对脑水肿体积比较,差异均无统计学意义(t分别=1.10、0.57、1.37,P均>0.05)。
2.3 两组治疗前后不同时间点NIHSS 评分比较见表4

表4 两组治疗前后不同时间点NIHSS评分比较/分
由表4可见,两组治疗前的NIHSS评分比较,差异无统计学意义(t=0.51,P>0.05),治疗7 d、14 d后,研究组NIHSS 评分均较对照组低(t分别=3.95、3.24,P均<0.05)。
2.4 两组近期预后比较见表5

表5 两组近期预后比较/例(%)
由表5 可见,研究组的总体预后良好率明显优于对照组,且研究组SBP<180 mmHg、SBP≥180 mmHg 患者的预后良好率亦明显高于对照组,SBP<180 mmHg、SBP≥180 mmHg 患者,差异均有统计学意义(χ2分别=4.08、5.05、4.19,P均<0.05)。
3 讨论
HICH 是出血性脑卒中的常见类型,约占脑卒中总数的21%~48%[7]。HICH的病情进展迅速,但其病理生理进程总体可分为三个阶段,即血肿形成、血肿扩大与血肿周围水肿带形成,而血压变化与血肿扩大、脑水肿加重密切相关,并可增加不良预后甚至死亡风险[8]。因此,血压变化尤其是发病6 h内高SBP 及大幅波动与HICH 病情及预后均息息相关,加强急性期血管管理具有重要意义[9]。
血肿扩大可导致严重占位效应,易导致血肿周围缺血半暗带以及低灌注区域的产生,是导致HICH 患者神经功能障碍恶化及预后不良的危险因素之一[10,11]。目前,临床尚缺乏促进血肿吸收的特效药物,如何合理调控血压成为HICH治疗的重点,但关于降压时机及降压范围目前仍存在较大的争议。既往观点认为,HICH 急性期血压升高属于保护性调节,一定水平的血压有助于维持脑组织血流灌注,如血压迅速降至过低水平可能引起脑组织低灌注,导致血肿周围缺血加重,可能导致颅内压升高甚至发生继发性缺血性血管事件[12]。近几年研究显示,HICH 后的血压自我调节可能存在调节失控或过度,且脑组织缺血并非单纯由组织灌注、血流量减少引起的,还与能量代谢有关,在保证脑代谢的情况下在一定范围内降压是安全的[13]。急性脑出血患者的血肿扩大多发生在发病后48 h 内,且多集中在首个24 h 内,早期合理范围内降压可能有助于降低血肿扩大趋势,且并不会加剧脑出血后周围水肿恶化程度[14]。本次研究研究组患者采取早期强化降压治疗,结果显示,研究组3 d 内血肿扩大率明显低于对照组,且无论SBP<180 mmHg还是≥180 mmHg 的患者,这种优势都存在。同时,本研究结果发现SBP≥180 mmHg 的患者血肿扩大发生率更高。提示强化降压可能有助于降低HICH患者的血肿扩大发生率,对SBP≥180 mmHg 患者的血肿扩大抑制作用较明显,SBP<180 mmHg 患者也可从早期强化降压中获益。Toyoda 等[15]研究显示,脑出血患者入院时SBP 越高,24 h 内血肿扩大发生率越高,尤其是在SBP≥150 mmHg 患者中发生率高达26.36%。相关meta 分析亦显示,对于无降压治疗禁忌证者,早期强化降压对急性自发性脑出血整体上是安全可行的,并不会导致血肿扩大、严重残疾或死亡风险增加[16]。同时,本研究还发现两组患者绝对脑水肿体积在治疗3 d 时差异并不显著,治疗7 d 时均有所增加,治疗14 d 时均基本消退,符合脑水肿的形成及消退规律,但两组间差异并不显著(P>0.05),提示早期强化降压并不会导致脑水肿体积增加。与袁方等[17]研究结果基本一致。但本次研究样本量较小,早期强化降压是否能够在降低血肿扩大风险的同时减轻脑水肿尚需进一步研究。
神经功能恶化是影响脑出血患者临床预后的主要因素之一,而入院SBP 较高被证实是早期(≤48 h)神经系统功能恶化的危险因素,这也为早期强化降压治疗提供了理论基础[18]。但也有研究表明,急性期强化降压控制SBP至140 mmHg以下尤其是120 mmHg 可能增加远端脑缺血以及早期神经功能恶化风险[19]。本次研究中,两组治疗7 d、14 d 时NIHSS 评分均逐步降低,且研究组低于对照组(P<0.05)。提示早期强化降压可能更有利于保护神经功能。同时,研究组90 d预后良好率高于对照组(P<0.05)。刘国庆等[20]研究显示,超早期强化降压(2 h内控制SBP 至120~140 mmHg)可降低HICH 患者的再出血率,改善神经功能及临床预后。有部分研究认为,急性期降压过快可能导致脑出血患者的肾脏血流灌注不足而导致肾损伤,主要是由于长期高血压本身就容易导致肾小动脉硬化,肾损伤风险较高[21]。因此,对于SBP>220 mmHg尤其是伴有肾功能不全的患者,建议持续血压监测并实施逐步降压,降压下限SBP不应低于120 mmHg。
综上所述,在完善基础治疗、保证脑代谢的基础上,对无降压治疗禁忌证的HICH 患者给予早期强化降压,控制SBP 至120~140 mmHg 并维持7 d,有助于降低早期血肿扩大率,且不增加脑水肿绝对体积,并有助于减轻神经功能缺损程度,改善近期预后。但由于血肿扩大及脑水肿形成的机制复杂,仍需进一步大样本、多中心随机对照研究分析早期强化降压的意义,并寻找最佳的血压控制范围。

