脂肪酸氧化和促分解脂质介质水平与阴茎勃起功能障碍的相关性研究
阿不来提·买买提明,许鹏,艾热提·阿皮孜,艾沙江·阿卜力,李晓东
阴茎的正常勃起是血管、神经、激素等多重因素共同介导的生理过程,其中任何一方面受损均可能引起勃起功能障碍[1]。目前导致阴茎勃起功能障碍的具体原因尚不明晰,其中阴茎血管内皮损伤被认为是诱导疾病发生、发展的重要机制之一[2]。而导致微血管损伤的原因包括病原菌侵袭、过度免疫激活、氧化应激及炎性反应增高等,其中炎性介质在勃起功能障碍中的作用也逐渐凸显[3]。多不饱和脂肪酸在炎性反应的不同阶段均具有重要作用,特别是应激条件下容易发生脂肪酸氧化,可反映患者体内炎性介质的氧化应激水平[4]。促分解脂质介质是主要由多不饱和脂肪酸酶催化氧化形成,包含多种亚族及亚型[5]。其中由二十碳五烯酸和二十二碳六烯酸衍生的消退素亚族在血管内皮相关的炎性反应中扮演重要角色,既往多项研究均表明在冠心病、动脉粥样硬化、动脉夹层等多种血管相关疾病中消退素不同亚型发挥不同调节功能[6-7],但其在勃起功能障碍中的作用尚不明晰。基于此,本研究旨在探究脂肪酸氧化和促分解脂质介质水平与阴茎勃起功能障碍的相关性,为进一步了解勃起功能障碍的发生、发展过程提供新思路,报道如下。
1 资料与方法
1.1 临床资料 选取2022年10月—2023年4月新疆医科大学第一附属医院泌尿中心诊治的勃起功能障碍患者70例作为观察组,另外选取同期健康男性70例作为健康对照组。2组年龄、BMI、病程、吸烟史、饮酒史、运动习惯、高血压患病率及糖尿病患病率等比较差异均无统计学意义(P>0.05),具有可比性,见表1。本研究已通过医院伦理委员会审批(K202209-06),参研者知情同意并签署知情同意书。
1.2 病例选择标准 (1)纳入标准:①符合我国《勃起功能障碍诊断与治疗指南》中勃起功能障碍的诊断标准[8];②患者静脉通路良好,可抽取外周静脉血进行检测;③患者既往病史、个人史等一般临床资料完整。(2)排除标准:①就诊前1周内合并泌尿系统急性感染;②合并骑跨伤、挫裂伤等阴茎外伤或白膜破裂;③合并严重的焦虑、抑郁等精神类疾病;④合并任何类型的恶性肿瘤。
1.3 观察指标与方法
1.3.1 血清脂肪酸氧化及特异性促炎性消退介质(specialized pro-resolving mediators,SPM)指标检测:2组受试者均在入组时抽取肘静脉血8 ml,室温下离心获取上层血清,通过酶联免疫吸附法(enzyme linked immunosorbent assay,ELISA)测定患者血清中过氧化脂质(lipid peroxides,LPO)、消退素D1(resolvin D1,RvD1)及消退素E1(resolvin E1,RvE1)的表达水平。LPO ELISA试剂盒由上海初态生物有限公司生产(货号为CT64099);RvD1 ELISA试剂盒由天津肽链生物科技有限公司生产(货号为TL501346);RvE1 ELISA试剂盒由上海木栾科技有限公司生产(货号为SBJ-H2195-48T)。所有ELISA检测操作步骤均按照试剂盒说明书进行,所有样本均进行复孔检测。最终各样本及试剂盒中标准品共同在LD-96A全自动酶标仪(山东莱恩德智能科技有限公司)上检测OD值,根据标准品OD值拟合浓度标准曲线并计算出各样本中LPO、RvD1及RvE1的表达水平。
1.3.2 血清睾酮检测:受试者均在入组时抽取肘静脉血5 ml,室温下离心获取上层血清,通过ELISA法测定患者血清睾酮(testosterone,T)的表达水平, ELISA试剂盒由上海初态生物有限公司生产(货号为CT60323),严格按照试剂盒说明书操作。
1.3.3 勃起功能障碍指标检测:(1)阴茎勃起硬度通过勃起硬度评分(erectile hardness score,EHS)分为1~4级,级别越高表明阴茎硬度越强;(2)通过海绵体内注射血管活性药物联合彩色双功能多普勒超声(购自武汉科尔达医疗科技有限公司,型号:BLS-X1)测定阴茎单侧动脉最大收缩期血流速度(peak systolic velocity,PSV)。
2 结 果
2.1 2组受试者血清LPO、RvD1及RvE1水平比较 观察组血清LPO水平高于健康对照组,RvD1及RvE1水平均低于健康对照组 (P<0.01),见表2。

表2 健康对照组及观察组血清LPO、RvD1及RvE1水平比较Tab.2 Comparison of serum LPO, RvD1, and RvE1 levels between healthy control group and observation group patients
2.2 2组血清睾酮和勃起功能障碍比较 2组受试者血清睾酮水平比较差异无统计学意义(P>0.01),观察组患者EHS评分及PSV均低于健康对照组 (P<0.01),见表3。

表3 健康对照组及观察组勃起功能障碍指标比较Tab.3 Comparison of erectile dysfunction indicators between healthy control group and observation group patients
2.3 血清LPO、RvD1及RvE1水平与勃起功能障碍发生的相关性分析 Pearson相关性分析表明,血清LPO水平与勃起功能障碍发生呈正相关,RvD1及RvE1水平与勃起功能障碍发生呈负相关(P<0.01);血清LPO水平与EHS、PSV呈负相关,RvD1及RvE1水平与EHS、PSV呈正相关(P<0.01),见表4。

表4 血清LPO、RvD1及RvE1水平与勃起功能障碍发生的相关性分析Tab.4 Correlation Analysis between Serum cPLA2 and F2 Isoprostaglandin Levels and Erectile Dysfunction
2.4 勃起功能障碍发生的多因素Logistic回归分析 以阴茎勃起功能障碍为因变量,以上述结果中P<0.05项目为自变量进行多因素Logistic回归分析,结果显示:血清LPO水平升高是勃起功能障碍发生的独立危险因素,RvD1及RvE1水平升高是勃起功能障碍发生的独立保护因素(P<0.01),见表5。

表5 阴茎勃起功能障碍发生的危险多因素Logistic回归分析Tab.5 Multivariate logistic regression analysis of the risk factors for penile erectile dysfunction
2.5 血清LPO、RvD1及RvE1水平对勃起功能障碍发生的预测价值分析 绘制血清LPO、RvD1及RvE1水平预测勃起功能障碍发生的ROC曲线,并计算AUC,结果显示,LPO、RvD1、 RvE1及三项联合预测勃起功能障碍发生的AUC分别为0.848、 0.858、0.911、0.969,三者联合优于各自单独预测效能(并用DeLong法对其差异进行比较)(Z/P=1.873/0.013、1.803/0.019、1.711/0.033),见表6、图1。
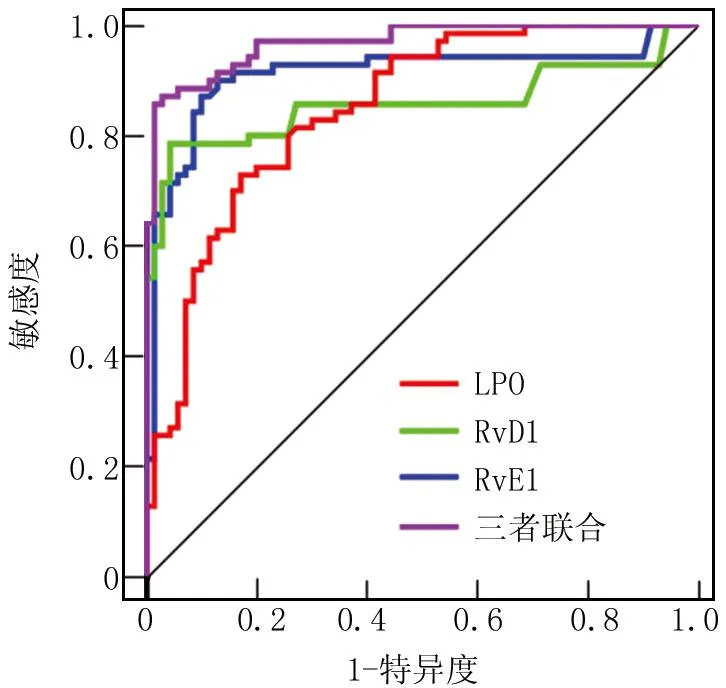
图1 各指标预测勃起功能障碍发生的ROC曲线Fig.1 ROC curves of various indicators predicting the occurrence of erectile dysfunction
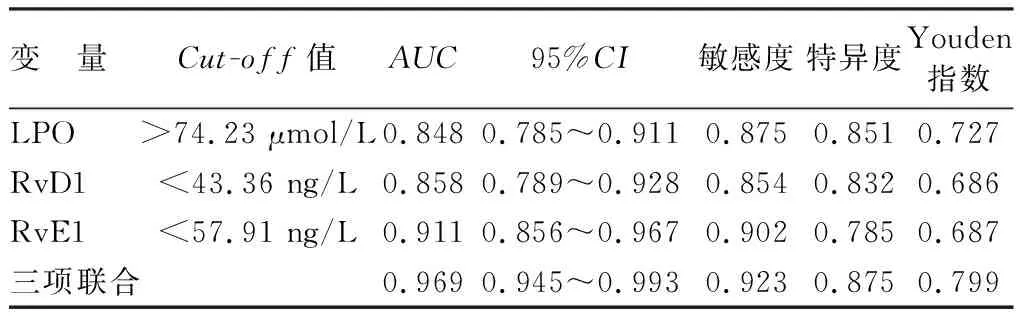
表6 血清LPO、RvD1及RvE1水平对勃起功能障碍发生的预测价值分析Tab.6 Analysis of the predictive value of serum LPO, RvD1, and RvE1 levels for the occurrence of erectile dysfunction
3 讨 论
勃起功能障碍对于男性患者不仅造成日常生活质量下降、影响生育需求,还容易导致患者出现严重负性情绪[9]。由于勃起涉及神经、血管、体液、激素等多种因素及环节,因此造成勃起功能障碍的具体机制并不明晰,可能是多因素影响的结果[10]。血管完整性、内皮功能正常及充分的动脉灌注是生理性勃起的必要因素,而血管内皮的损伤及功能破坏可能是介导勃起功能障碍的重要原因及机制[11]。血管内皮损伤可能由患者机体炎性反应升高、过度氧化应激、病原菌侵袭、物理化学损伤等导致,多种细胞因子及化学介质会参与并调节血管内皮的功能及稳定[12]。因此,聚焦可能诱导血管内皮损伤的因子对于进一步探索勃起功能障碍形成机制、早期预测疾病发生、进行相关性靶向治疗均具有重要临床意义。
有研究认为勃起功能障碍与微血管而非大血管的内皮功能障碍的相关性更强,并提出了血管扩张功能丧失的后果在阴茎微血管中比在较大的血管中更早表现出来[13]。但不论是阴茎大血管还是微血管内皮功能障碍导致勃起功能障碍,血管内皮在疾病的发生、发展中均扮演重要角色,因此介导内皮完整性破坏及功能降低的因素均可能参与勃起功能障碍的发生过程[14]。健康成年人体内,内皮细胞处于静息状态,发挥调节血管张力、维持凝血和栓溶平衡、抗炎和抗炎性细胞黏附等重要作用;然而,当内皮受到异常血流压力、病原微生物等异常刺激、免疫炎性反应升高及氧化应激水平过度激活时,内皮细胞活化并表现为促血栓形成、促炎性细胞黏附和浸润的病理表型,血管渗漏性增强,进而可能促进多种血管相关疾病发生[15]。
以往研究发现,二十碳五烯酸和二十二碳六烯酸是人体内重要的多不饱和脂肪酸,具有调控炎性反应和促进炎性反应消退的作用,而该过程中的主要有效因子是其代谢生成的促分解脂质介质[16]。促分解脂质介质是一类强效的促进急、慢性炎性反应消退的小分子物质,主要包括脂氧素、保护素、消退素和巨噬素四大类。其中,RvE1及RvD1分别是二十碳五烯酸和二十二碳六烯酸代谢产生的消退素,以往研究发现,在冠状动脉粥样硬化、血管炎、动脉夹层形成等多种血管相关性疾病中RvE1及RvD1均扮演重要角色,且主要通过调节炎性反应间接影响血管内皮功能[17-18]。LPO是脂肪酸氧化的代谢产物,也是反映机体脂肪酸氧化水平的重要指标。以往研究发现,LPO对于血管内皮具有显著的刺激作用,此外也会引起破损的血管内皮周围炎性反应微环境水平增高,进一步加重血管内皮损伤[19]。在本研究中,发现血清LPO水平升高、RvD1及RvE1水平降低均是勃起功能障碍发生的独立危险因素,与疾病具有显著相关性。分析其原因,炎性反应会介导脂肪酸异常释放并影响异前列腺素、一氧化氮等血管内皮活性物质的合成。一方面,过多的脂肪酸会氧化形成LPO等代谢产物,加重局部、全身氧化应激水平和炎性反应,进而使血管内皮损伤加重;另一方面,多种血管活性物质合成减少使血管收缩功能、血管张力均受到负面影响,上述两种机制均可能在阴茎微血管中造成更严重的影响,进而促进勃起功能障碍的发生。RvD1及RvE1作为机体内重要的促分解脂质介质,可通过与特异性受体结合调节免疫、炎性反应水平,进而减轻炎性因子对血管内皮的损伤。有研究发现,给予外源性RvD1能够增加凋亡细胞分裂周期蛋白表达,促进巨噬细胞通过受体配体相结合的方式识别并吞噬凋亡细胞,从而促进巨噬细胞的胞葬作用并减轻炎性反应水平[20]。而RvD1及RvE1的下调则会导致其与特异性受体结合发挥的抑制炎性因子分泌、促炎性反应消退作用降低,甚至可能形成炎性反应瀑布效应,加重局部的炎性反应微环境紊乱及对血管内皮的损伤。
本研究发现勃起功能障碍患者血清LPO、RvD1及RvE1水平显著变化,且与疾病发生具有显著相关性,但关于上述因子是否通过介导炎性反应影响血管内皮功能及勃起功能障碍的发生仍需进一步通过体外细胞实验探索。尽管如此,本研究发现了男性血清脂肪酸氧化水平增高、促分解脂质介质水平降低是勃起功能障碍发生的危险因素,为未来进一步探究勃起功能障碍的发生、发展机制提供新的思路。
利益冲突:所有作者声明无利益冲突
作者贡献声明
阿不来提·买买提明、李晓东:设计研究方案,实施研究过程,论文撰写;许鹏、艾热提·阿皮孜:实施研究过程,资料搜集整理,分析试验数据;艾沙江·阿卜力:进行统计学分析

