基于超高效液相色谱—串联质谱同时测定大鼠血浆中杜仲制剂的药代动力学研究
董莹莹 郭琴 高焕 张立石 柏冬
杜仲为杜仲科植物杜仲EucommiaulmoidesOliv的干燥树皮,是我国历史悠久的名贵中药材,该植物是稀有濒危植物,已被列为国家二级保护树种。它是中国最有价值的补药之一,具有养肝补肾、强身健骨、预防流产的作用[1]。现代药理学研究表明,杜仲在降低血压[2]、抑制炎症[3]、降低血糖[4]、减轻肝损伤[5]、减轻神经炎症[6]、抗骨关节炎[7]等方面具有重要作用。正是由于杜仲具有多种药理活性,在临床上应用广泛,主要用于片剂、胶囊剂、颗粒剂、配方颗粒四种剂型。
目前,虽然对杜仲的药代动力学有一些研究[8-9],但对杜仲及其制剂的药代动力学分析尚未进行研究。本研究基于超高效液相色谱—串联质谱(ultra high performance liquid chromatography tandem mass spectrometry,UPLC-MS/MS)技术建立杜仲及其制剂中原儿茶酸、京尼平苷酸、松脂醇二葡萄糖苷、无梗五加苷B、松脂醇葡萄糖苷、京尼平苷、绿原酸、咖啡酸等8个成分的同时测定方法,并应用于四种杜仲制剂的药代动力学研究。
1 材料与方法
1.1 仪器
Agilent 1260高分离度快速液相色谱仪,Agilent 6410质谱仪,美国Agilent科技公司;TGL-16MC型低温离心机;SB-5200DT超声波清洗机,宁波新芝生物科技股份有限公司;VORTEX 3型涡旋混合器,德国IKA公司
1.2 药品和试剂
杜仲饮片,江西普真药业有限公司,批号:20190322;杜仲全粒胶囊,江西普真药业有限公司,批号:Z20055116;杜仲颗粒,贵州参芪药业有限公司,批号:Z52020394;杜仲配方颗粒,广东伊芳药业有限公司,批号:20160214;京尼平苷酸、松脂醇二葡萄糖苷、无梗五加苷B、松脂醇葡萄糖苷,上海源叶生物技术有限公司,批号分别为Y02A9H57757、J06J9T65071、X26D9L78667、B21724;原儿茶酸、京尼平苷、绿原酸、咖啡酸,中国北京国家食品药品监督管理总局,批号分别为110809-200604、111828-201604、0753-200111、110885-201703;3,4-二羟基苯乙酸,美国Sigma-Aldrich 公司,批号:850217-1G;乙腈,美国Fisher Scientific公司;甲醇、甲酸,Thermo Fisher Scientific中国公司。
1.3 动物
24只清洁级雄性SD大鼠,体质量(300±20)g,购于SPF(北京)生物科技有限公司,实验动物许可证号:SCXK (京) 2016-0002,该实验经过由中国中医药科学院中医基础理论研究所医学伦理委员会批准(批准文号:2019-052)。
1.4 检测条件
安捷伦SB C18色谱柱(2.1 mm×50 mm,1.8 μm);流动相由0.1%甲酸水溶液(A)和0.1%甲酸乙腈溶液(B)组成,流速为0.3 mL/min,梯度洗脱(0~1分钟,5%B;1~3分钟,45%B;3~6.4分钟,65%B),停止时间和后处理时间分别为6.4分钟和8分钟,进样体积为2 μL,柱温为35℃。
电喷雾电离源(electrospray ionization,ESI),负离子模式扫描,多反应监测(Multiple Reaction Monitoring,MRM)模式。离子源温度为350 ℃,鞘气为氮气(99.9%),气体流速设定为12 L/min,毛细管电压为4 000 V,雾化气体压力为40 psi。待测成分定量分析离子对及质谱参数。见表1。

表1 8种化合物和内标成分(IS)的优化参数
1.5 对照品溶液的制备
分别精密称取原儿茶酸、京尼平苷酸、松脂醇二葡萄糖苷、无梗五加苷B、松脂醇葡萄糖苷、京尼平苷、绿原酸、咖啡酸对照品适量,加甲醇制成浓度分别为10.00 μg/mL、10.22 μg/mL、10.14 μg/mL、8.85 μg/mL、10.18 μg/mL、10.02 μg/mL、7.98 μg/mL、10.45 μg/mL的混合对照品溶液。用甲醇将上述混合对照品溶液稀释10个系列浓度,比例为5倍,置于在4 ℃下保存,备用。
1.6 内标溶液(IS)的制备
精密称取内标物3.4-二羟基苯乙酸适量,加甲醇制备成浓度为10.05 μg/mL的内标溶液,置于在4 ℃下保存,备用。
1.7 供试品溶液
杜仲饮片:称取杜仲饮片260 g,用8倍量去离子水煎煮40分钟,过滤后,滤渣再采用6倍量去离子水煎煮30分钟,合并滤液,减压浓缩至100 mL。全杜仲胶囊:取全杜仲胶囊过60目筛,精密称取50 g,用去离子水溶解至100 mL溶解样品。杜仲颗粒:称取杜仲颗粒135 g,用去离子水100 mL溶解样品。杜仲配方颗粒:称取杜仲配方颗粒13 g,用去离子水100 mL溶解样品。
1.8 血浆样品的制备
向100 μL血浆中加入20 μL内标物溶液(10.05 μg/mL)和310 μL酸化乙腈(300 μL乙腈+10 μL 5%甲酸)。将混合物涡旋3分钟,在冰浴中超声提取10分钟,以12 000 r/min离心10分钟。将上清液转移到干净的试管中,并通过真空冷冻干燥蒸发至干燥状态。然后加入100 μL流动相(乙腈∶水=1∶4)涡旋3分钟溶解残渣,超声提取10分钟,12 000 r/min离心10分钟后取上清液,即为血浆样品。
1.9 给药以及血浆的收集
24只雄性SD大鼠,适应性喂养一周后,随机分成4组,包括杜仲饮片组、全杜仲胶囊组、杜仲颗粒组和杜仲配方颗粒组,每组6只。实验前,大鼠禁食12小时。按照1.7项下的方法制备供试品溶液,灌胃给药,剂量分别为杜仲饮片组(104 g/kg)、全杜仲胶囊组(20 g/kg)、杜仲颗粒组(54 g/kg)、杜仲配方颗粒组(5.2 g/kg)。在给药前和给药后15分钟、30分钟、1小时、2小时、4小时、6小时、8小时、12小时、24小时摘眼球取血,置于肝素钠抗凝管中,3 000 r/min离心15分钟,取上清液即为血浆,置于-80℃下保存备用。
1.10 统计学方法
2 结果
2.1 专属性
分别对空白血浆样品,加入混合对照的空白血浆样品,以及口服给药后从大鼠收集的血浆样品,按照1.8项下方法处理后进行UPLC-MS/MS分析,所有化合物和内标物的代表性MRM色谱图如图1所示,在8种化合物和内标物的保留时间内,基质中没有出现任何干扰,说明该方法的专属性良好。

注:A为空白血浆;B为加入标准化合物和内标的空白血浆;C为口服给药从鼠中收集血浆样品,1为原儿茶酸;2为京尼平苷酸;3为松脂醇二葡萄糖苷;4为无梗五加苷B;5为松脂醇葡萄糖苷;6为京尼平苷;7为绿原酸;8为咖啡酸;9为3.4-二羟基苯乙酸(IS)。
2.2 标准曲线
将混合对照品溶液加入到空白血浆中,按照1.4项下方法操作,制成标准曲线血浆样品,测定各成分的含量,每种浓度制备三个样品。标准方程由分析物浓度与内标物浓度之比(X)和相应的峰面积比(Y)构成。采用加权最小二乘法(1/χ2)得到各化合物及其峰面积的标准回归方程。结果如表2所示,8种成分的r值均在0.9971~0.9988之间,表明所有化合物在相应范围内有良好的线性关系。
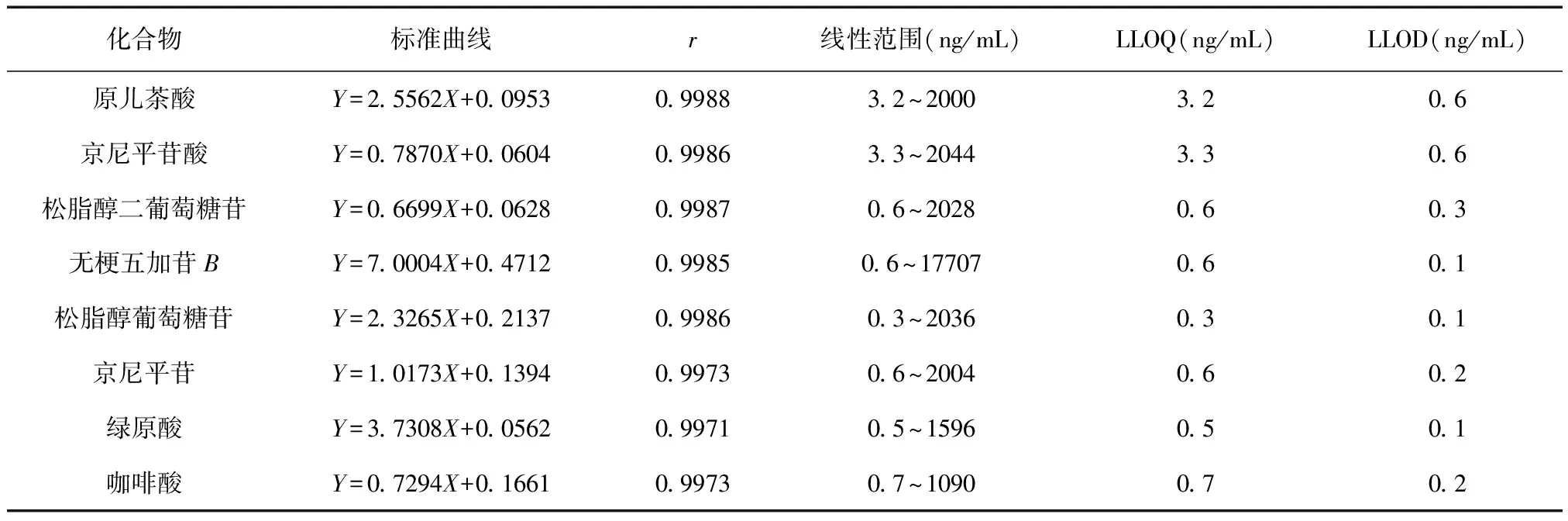
表2 8种化合物的线性回归方程r、线性范围LLOD和LLOQ(n=3)
2.3 精密度和准确度
取大鼠空白血浆100 μL,加入3种质量浓度的混合对照品溶液20 μL(高浓度为1 000 μg/mL;中浓度为200 μg/mL;低浓度为50 μg/mL)制备质控样品,每种浓度平行制备5个样品,按照1.8项下方法处理后,按照1.4项检测条件进行 UPLC-MS/MS 分析,连续测定3天,分别计算精密度和准确度。结果如表3所示,8种成分的精密度均小于15%,8种成分的准确度均在±15 %以内,这表明该方法具有良好的可靠性和重复性。
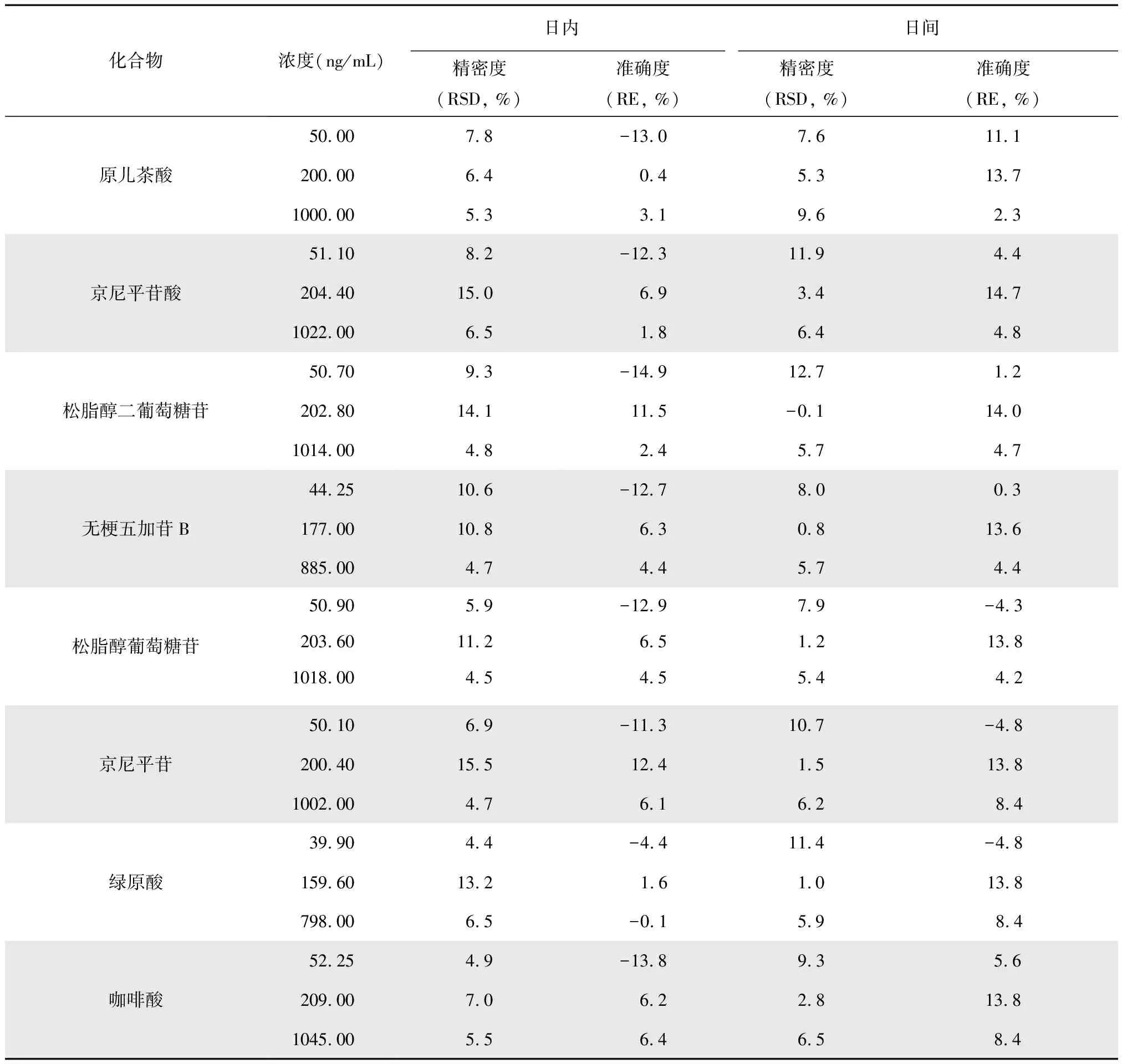
表3 8种化合物的精密度和准确度(n=5)
2.4 稳定性
取大鼠空白血浆100 μL,加入3种质量浓度的混合对照品溶液(高:1 000 μg/mL;中:200 μg/mL;低:50 μg/mL)制备质控样品,按照1.8项下方法处理后,对不同储存环境下的样品(冻融循环3次;样品在-80℃下保存15天;样品在25℃的室温下放置24小时)按照1.4项下检测条件进行 UPLC-MS/MS 分析,每种环境平行制备5个样品。结果如表4所示,8种成分的RSD均小于15%,表明血浆样品在不同环境中是稳定的。
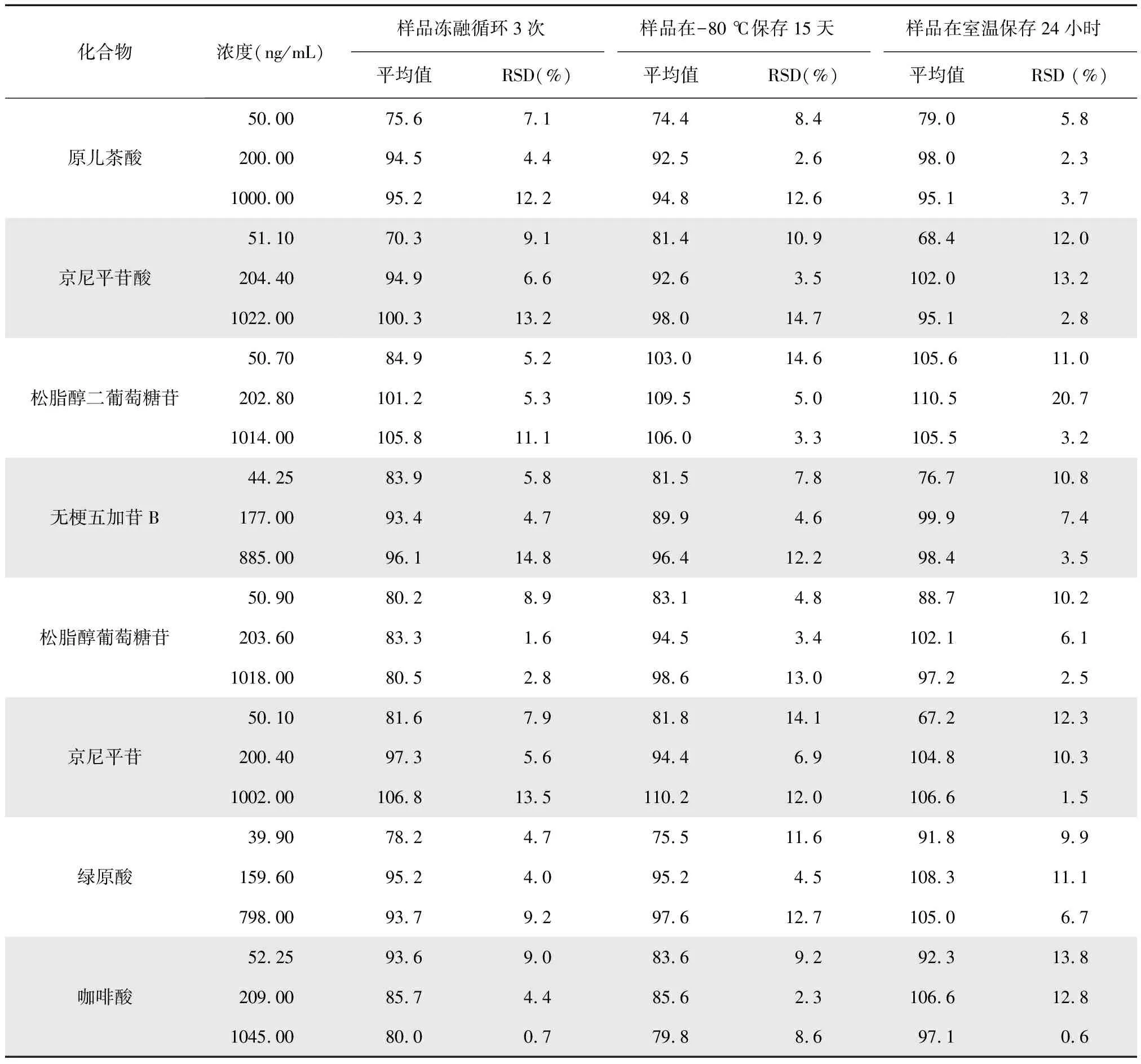
表4 8种化合物的稳定性考察(n=5)
2.5 提取回收率和基质效应
取大鼠空白血浆100 μL,加入3种质量浓度的混合对照品溶液20 μL(高:1 000 μg/mL;中:200 μg/mL;低:50 μg/mL)制备质控样品,按照1.8项下方法处理后,按照1.4项检测条件进行 UPLC-MS/MS 分析,记录各成分峰面积与内标峰面积的比值(A);取大鼠空白血浆100 μL,按照1.8项下方法处理后加入质控样品,进样分析,记录各成分峰面积与内标峰面积的比值(B);取上述高、中、低3个质量浓度的混合对照品溶液,进行分析,记录峰面积与内标峰面积的比值(C);每种质量浓度平行制备5个样品。提取回收率=A/B×100%,基质效应=B/C×100%。结果如表5所示,8种成分的提取物回收率在73.7%到95.0%之间,这表明在处理血浆样品以沉淀蛋白质的过程中,分析物没有显著损失。8种成分的基质效应范围为71.7%~130.5%,表明无明显基质干扰。
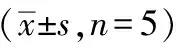
表5 8种化合物的提取回收率及基质效应
2.6 药代动力学
大鼠灌胃给药4种杜仲制剂后,采用UPLC-MS/MS分析不同采样点的血药浓度,以时间为横坐标(x),血药浓度为纵坐标(y)作图。通过Phoenix Winnonlin 8.1软件进行非房室模型分析,计算血药浓度—时间曲线下面积(AUC0-∞),半衰期(t1/2z)、达峰时(Tmax)、最大血药浓度(Cmax)、表观分布容积(Vz/F)、清除率(CLz/F)、平均驻留时间(MRT0-∞)等药代动力学参数,结果见表6、表7。

表6 口服杜仲制剂后化合物的AUC0-∞、t1/2z、Tmax和Cmax参数比较鼠只=6)

表7 口服杜仲制剂后化合物的Vz/FCl2/F和MRT0-∞参数鼠只=6)
3 讨论
杜仲包含多种活性成分,其中木脂素类成分最丰富。例如在《中华人民共和国药典》(2020年版)中,松脂醇二葡萄糖苷是杜仲质量控制的指标性成分,在调节高血压、炎症、氧化应激方面发挥着关键作用[10]。松脂醇葡萄糖苷在成骨细胞分化和基质矿化中具有生物学作用,这表明它可能在骨质疏松症和牙周炎等骨病中具有合成代谢作用[11]。据报道,京尼平苷和京尼平苷酸具有抗氧化和抗凋亡活性,是修复DEP诱导的皮肤损伤的潜在候选药物[12]。原儿茶酸可通过抗氧化和抗炎活性在脑和肝脏中发挥保护作用,其潜在机制可能是通过调节NF-κB/COX-2途径[13]。Zang H等[14]人通过顺铂诱导的AKI小鼠和人类肾脏-2细胞模型,发现无梗五加苷B是治疗AKI的潜在药物。绿原酸可剂量依赖性地抑制人肝癌细胞Hep-G2和Huh-7的活性,但不影响正常人肝细胞QSG-7701的活性和生长[15]。由于相邻羟基和分子内双键的结构,咖啡酸具有良好的抗氧化活性[16]。因此,本研究选择原儿茶酸、京尼平苷酸、松脂醇二葡萄糖苷、无梗五加苷B、松脂醇葡萄糖苷、京尼平苷、绿原酸和咖啡酸作为杜仲的指标成分进行药代动力学研究。
为了在较短时间内实现最佳的分离和获得良好的峰形,对流动相进行了考察。在本研究中,分别测试了甲醇、乙腈和水中不同比例的酸和盐。最后,选择0.1%甲酸水溶液(溶剂A)和0.1%甲酸乙腈溶液(溶剂B)作为流动相。
本研究采用液液萃取的方法处理血浆样品,采用UPLC-MS/MS进行测定,结果表明该方法具有良好的专属性、线性、精密度、准确度、提取回收率、基质效应、稳定性。杜仲补肝肾药效明确,采用该方法研究杜仲及其制剂中的8种成分在大鼠体内的药代动力学,对于进一步揭示不同杜仲制剂的药效物质基础研究具有重要意义。由于非房室模型限制条件少,适合于大部分药物,因此本研究采用非房室模型估算药代动力学参数。结果显示,不同杜仲制剂中的成分在大鼠体内药代动力学特征不同。根据血药浓度—时间曲线下面积(AUC0-∞)可得出,杜仲颗粒中的原儿茶酸、无梗五加苷B、绿原酸、咖啡酸四种成分在大鼠体内暴露高于其他剂型,全杜仲胶囊中的京尼平苷酸、松脂醇二葡萄糖苷、松脂醇葡萄糖苷、京尼平苷四种成分在大鼠体内的成分高于其他剂型。根据达峰时间(Tmax)可得出,杜仲饮片中的原儿茶酸、京尼平苷酸、咖啡酸三种成分在大鼠体内的吸收快于其他剂型,杜仲颗粒中的松脂醇二葡萄糖苷、无梗五加苷B、绿原酸三种成分在大鼠体内的吸收快于其他剂型,杜仲配方颗粒中的京尼平苷在大鼠体内的吸收快于其他剂型。通过口服给药后,8种成分在不同剂型中的表观分布容积(Vz/F)和清除率(Clz/F)差异较大,说明在体内的过程不一致。根据不同制剂的药代动力学参数来看,8种成分在AUC0-∞、t1/2z、Tmax、Cmax、Vz/F、Clz/F、MRT0-∞方面均不相同,这表明同一药物的不同剂型,它们的释药速度、起效快慢及作用强度均不相同。
综上所述,本研究基于UPLC-MS/MS法的多反应监测模式,建立同时测定原儿茶酸、京尼平苷酸、松脂醇二葡萄糖苷、无梗五加苷B、松脂醇葡萄糖苷、京尼平苷、绿原酸、咖啡酸8种成分的分析方法,并用该方法分析杜仲及其制剂在大鼠中的药代动力学,对杜仲制剂在临床应用上具有重要指导意义。

