基于超声造影特征构建列线图预测甲状腺微小乳头状癌颈淋巴结转移风险
丁姣姣, 韩 伟, 高军喜, 宋 涛
(新疆医科大学第一附属医院腹部超声诊断科, 乌鲁木齐 830054)
甲状腺乳头状癌(papillary thyroid carcinoma,PTC)是最常见的甲状腺癌类型,肿瘤直径≤1 cm的PTC又被称为甲状腺微小乳头状癌(papillary thyroid microcarcinoma,PTMC)。在所有类型的甲状腺癌中,PTMC近年来病例数逐年攀升,近3年的年均复合增长达57.4%[1]。PTMC多数预后良好,最主要的侵袭性表现是颈淋巴结转移(lymph node metastasis,LNM),易发生于颈中央区,其次是颈侧区,总的转移率可达49%[2]。修订版的美国甲状腺学会《成人甲状腺结节与分化型甲状腺癌诊治指南》[3]建议病灶直径<1 cm的低危组的患者无需行颈部淋巴结清扫。因此,颈部淋巴结状况的评估对PTMC患者进行风险分层和选择治疗方案具有重要意义。
超声检查作为首选评估方法,其诊断颈侧区LNM准确率高[4],然而早期的LNM往往表现为隐匿性淋巴结转移,加之气管、甲状腺等周围组织的遮挡,导致超声诊断中央区LNM的灵敏度只有0.33[5]。因此,探讨影响PTMC淋巴结转移的影响因素成为研究的热点。有研究指出,影响LNM的危险因素包括男性、年轻患者、多灶性、腺外侵犯[6-7]等,这些特征被广泛接受。然而,对一些重要指标仍存在争议,尤其在甲状腺结节逐步应用的超声造影(contrast-enhanced ultrasound,CEUS),其预测价值未达成共识,国内外的甲状腺结节分类指南[8]中,造影特征未被列入其中。本研究试图通过可视化的列线图构建预测模型,分析PTMC淋巴结转移的危险因素,探讨CEUS特征与LNM的相关性,从而方便临床制定适宜的诊疗方案,规范PTMC管理。
1 资料与方法
1.1 研究对象回顾性分析2020年12月1日至2021年12月31日在新疆医科大学第一附属医院行甲状腺手术治疗的PTMC患者共计404个PTMC结节病历资料。纳入标准:(1)首次外科治疗的PTMC患者,术前超声资料与临床病理资料完备;(2)均行颈中央区淋巴结清扫和/或颈侧区淋巴结清扫。排除标准:(1)有头颈部放疗史;(2)病历资料不完整。利用随机函数按7∶3的比例随机分成建模组(n=282)与验证组(n=122)。根据病理是否存在淋巴结转移,再将两组数据集分为转移组和非转移组,其中建模数据集转移组107例,非转移组175例;验证数据集转移组52例,非转移组70例。
1.2 仪器与方法
1.2.1 仪器与试剂 使用LOGIC-E9(美国)、Siemens Healthineer(西门子)彩色多普勒超声诊断仪行甲状腺常规超声及超声造影检查。LOGIC-E9超声诊断仪采用15L型(频率10.0~15.0 MHz)和9L型(频率8.4~9.0 MHz)线阵探头,Siemens Healthineer超声诊断仪采用18L6型(频率4.6~17.8 MHz)和10L4型(2.9~9.9 MHz)线阵探头。超声造影选择意大利博来科(Bracco)公司的声诺维(Sonovue)冻干粉剂(25 mg/支)造影剂。
1.2.2 研究方法 常规超声:患者仰卧位暴露颈部,采用高频探头的甲状腺模式扫查,实时调节扫查深度、聚焦位置、动态范围等,获取清晰图像后,于甲状腺结节最大横切面和纵切面留存灰阶及彩色多普勒声像图。
超声造影:清晰显示甲状腺结节及部分周围正常腺体作对比,探头轻置于患者颈部前方,保持探头不动,选择造影模式和低机械指数(MI<0.10),双幅实时动态观察。每支造影剂用5 mL 0.9%氯化钠注射液配制并经前臂肘静脉团注1.2~2.0 mL造影剂,随后注入5 mL 0.9% 氯化钠溶液冲管;同时计时并连续观察2 min,存储动态及静态图像。
甲状腺结节相关超声术语定义[8-9]:(1)纵横比>1定义为结节长轴与皮肤垂直,其前后径大于上下径或左右径。(2)边缘清晰定义为结节境界光滑完整,边缘模糊定义为结节境界与周围甲状腺实质难以区分。(3)声晕定义为甲状腺结节周围有低回声或无回声区环绕,根据声晕特征分为声晕均匀与厚薄不均。(4)钙化包括直径<1 mm的强回声定义为微钙化,直径≥1 mm的强回声定义为粗大钙化。(5)彩色多普勒超声成像分为无血流型、中央型血流、边缘型血流及混合型血流四类,即:无血流型定义为结节内未探及血流信号;边缘型血流定义为结节主要显示为血流主要集中在结节边缘,而中央血管稀少或没有;中央型血流定义为结节内部显示中央血管或放射状血流分布;混合型血流定义为结节中央和边缘的血管丰富程度相似。(6)CEUS增强速度:造影剂微泡开始进入的时间与周围实质相比快慢与否,分为快速增强、同步增强和快速增强。(7)增强强度:根据对比增强强度是否低于、等于或高于周围甲状腺实质,分为低增强、等增强与高增强。(8)增强模式通常是根据结节内造影剂微泡的进入分为向心性增强(从周围开始的增强)、放射性增强(中央向周围方向)、弥漫性增强和充盈缺损(当造影剂微泡的灌注不表现出特定的方向性时)。(9)消退模式:造影剂灌注后,根据造影剂开始廓清的时间与周围实质相比快慢与否,分为缓慢消退、同步消退和快速消退。
2 结果
2.1 基线特征随机性验证显示,建模组与验证组各自变量数据差异均无统计学意义(表1),证实了分组的随机性。人群的LNM率是39.4%(159/404),男女比例是1.00∶2.37,男性的LNM率为49.2%(59/120),高于女性35.2%(100/284),差异有统计学意义(χ2=6.883,P=0.009)。
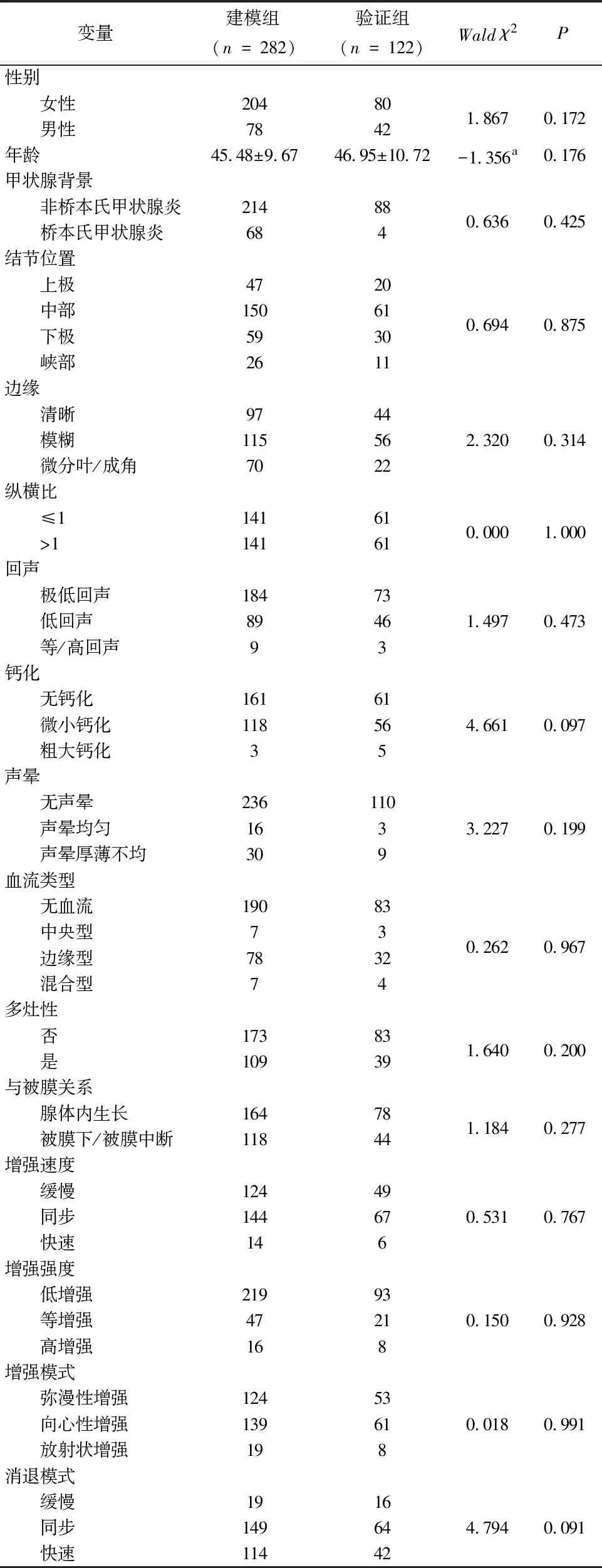
表1 建模组与验证组各变量的基线特征
2.2 建模组PTMC患者颈部淋巴结转移的单因素与多因素分析建模组PTMC患者女性204例(72.3%),男性78例(27.7%),颈淋巴结转移107例、未转移175例,单因素分析显示,颈淋巴结转移组与非转移组比较,具有统计学意义的因素分别是年龄、性别、结节边缘、声晕、多灶性、与被膜的关系、CEUS增强速度与消退模式(表2)。
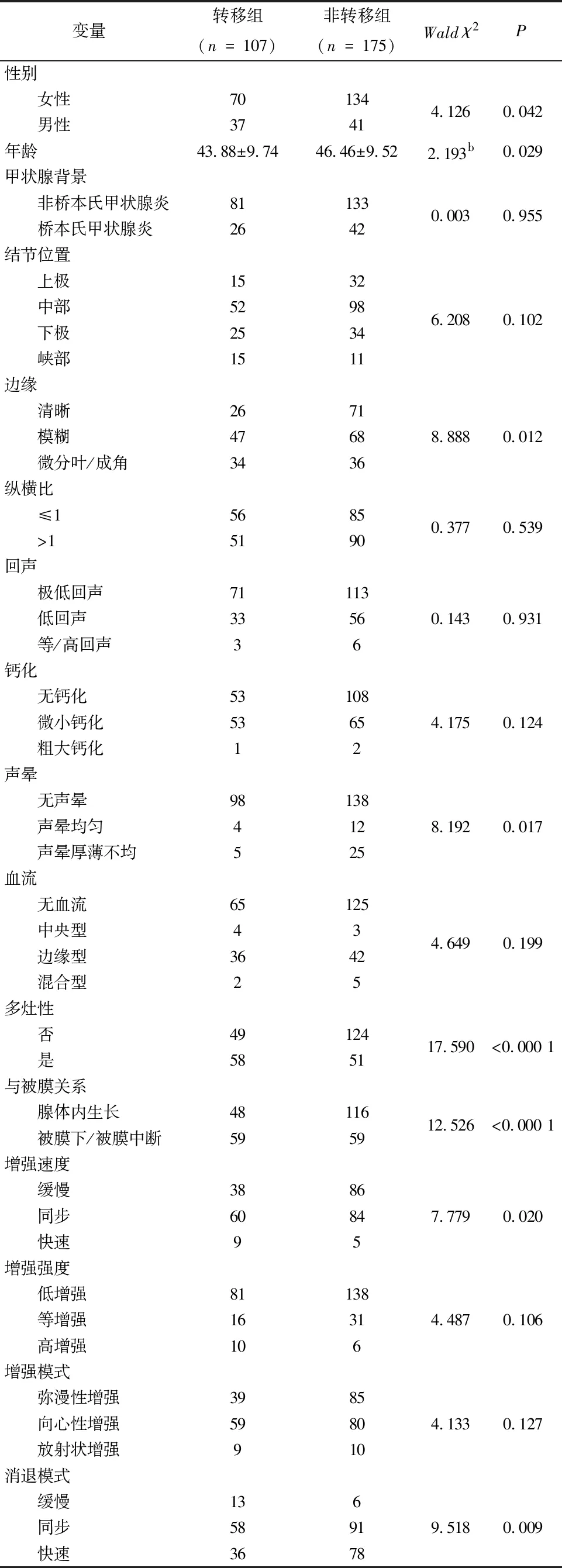
表2 建模组PTMC患者颈淋巴结转移的单因素分析
应用Logistic回归分析上述变量与颈淋巴结转移的相关性,将是否出现颈部淋巴结转移(非转移组=0、转移组=1)作为因变量Y,将上述单因素分析有差异的变量作为自变量X,变量赋值表见表3,采用向前(有条件),最终5个自变量进入预测模型(表4)。对结节超声特征而言,边缘模糊及边缘成角或微小分叶的结节更容易发生颈淋巴结转移;结节出现厚薄不均的声晕是LNM的保护因素;多灶性的PTMC出现转移风险是单发病灶的3倍;而被膜下生长或侵犯被膜的结节,出现颈淋巴结转移的风险增大1.6倍(图1)。CEUS特征方面,快速消退的结节更不易出现LNM(图2)。

表3 多因素Logistic回归分析变量赋值表
2.3 构建列线图预测模型利用R软件绘制PTMC患者颈淋巴结转移风险的列线图预测模型,根据分数尺度为各因素分配相应分数,每一因素的得分相加得到总的分数,总分对应在风险轴上的数值越大,发生颈淋巴结转移的风险也就越大(图3)。

表4 建模组PTMC患者颈淋巴结转移的多因素Logistic回归分析
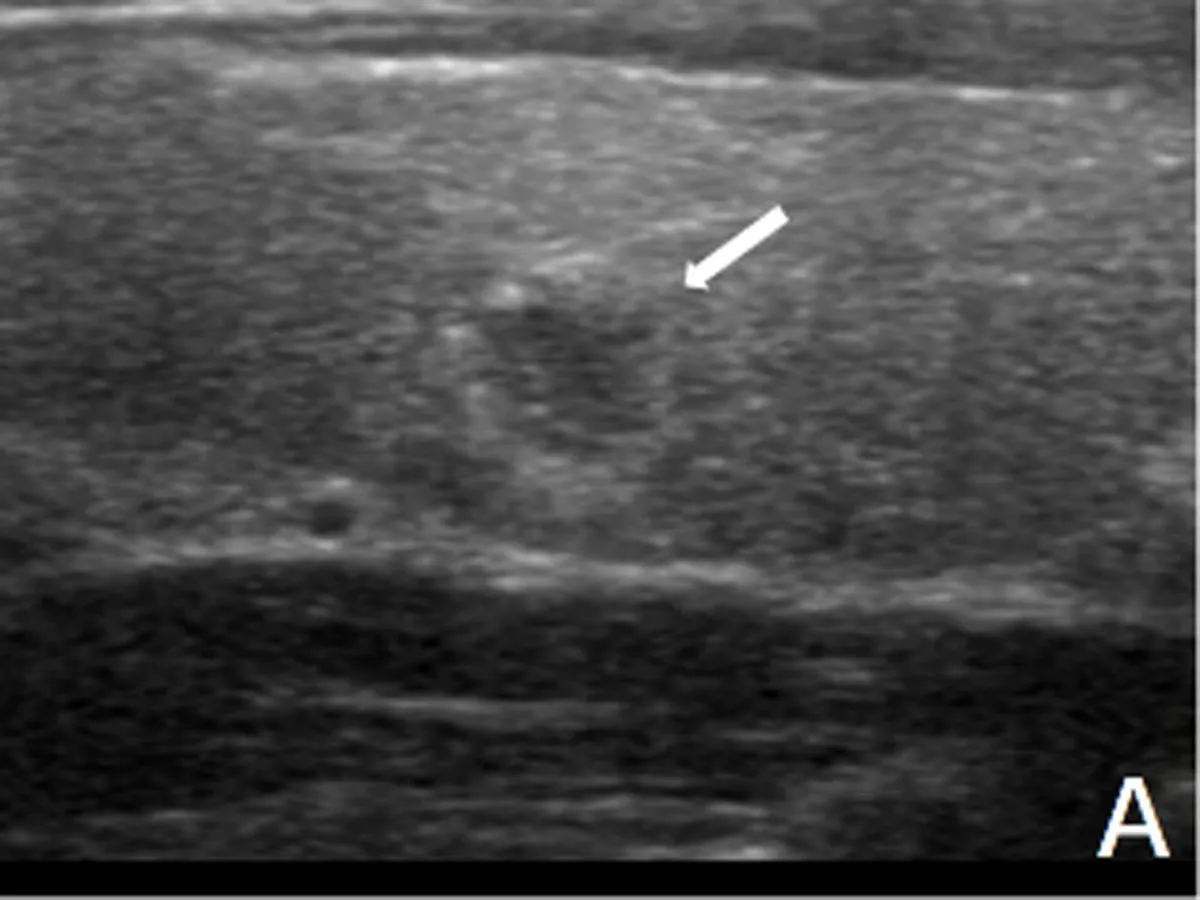
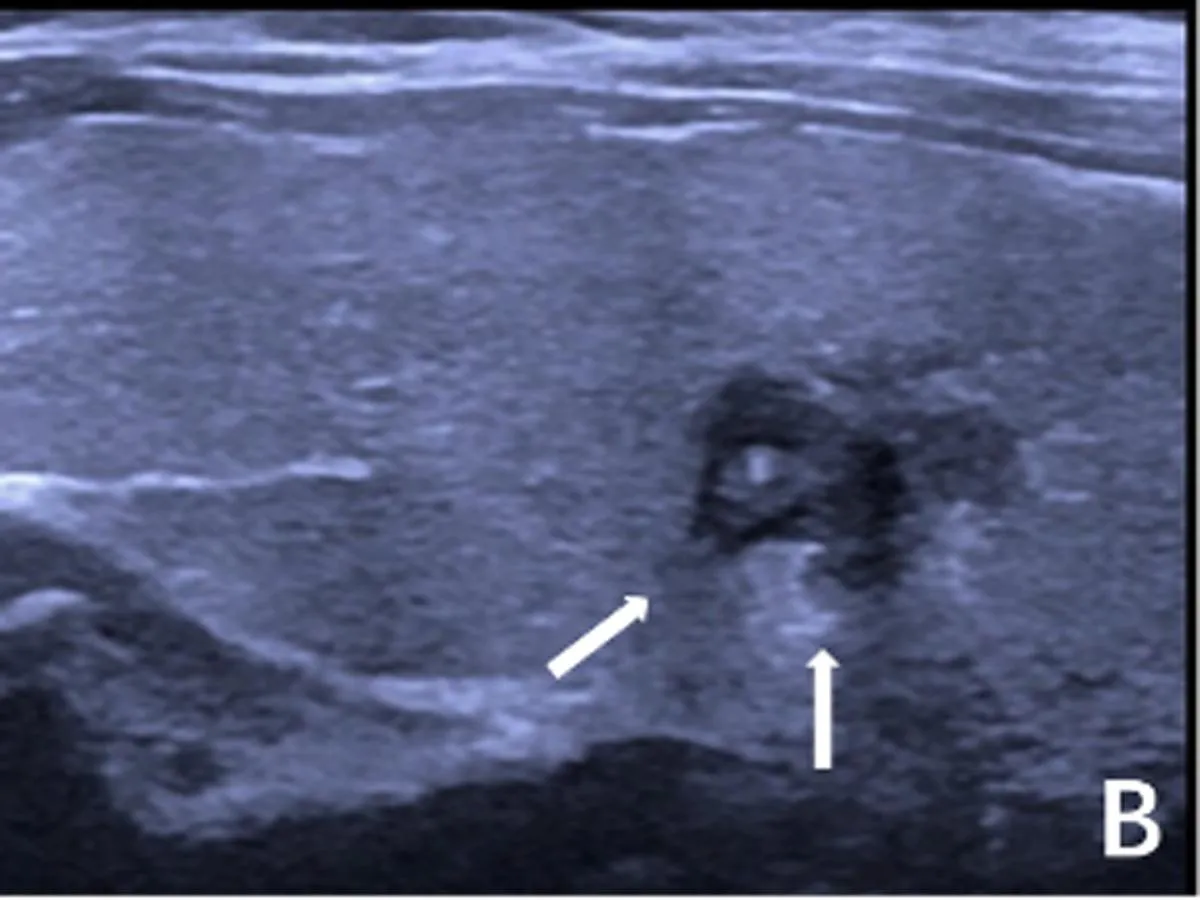
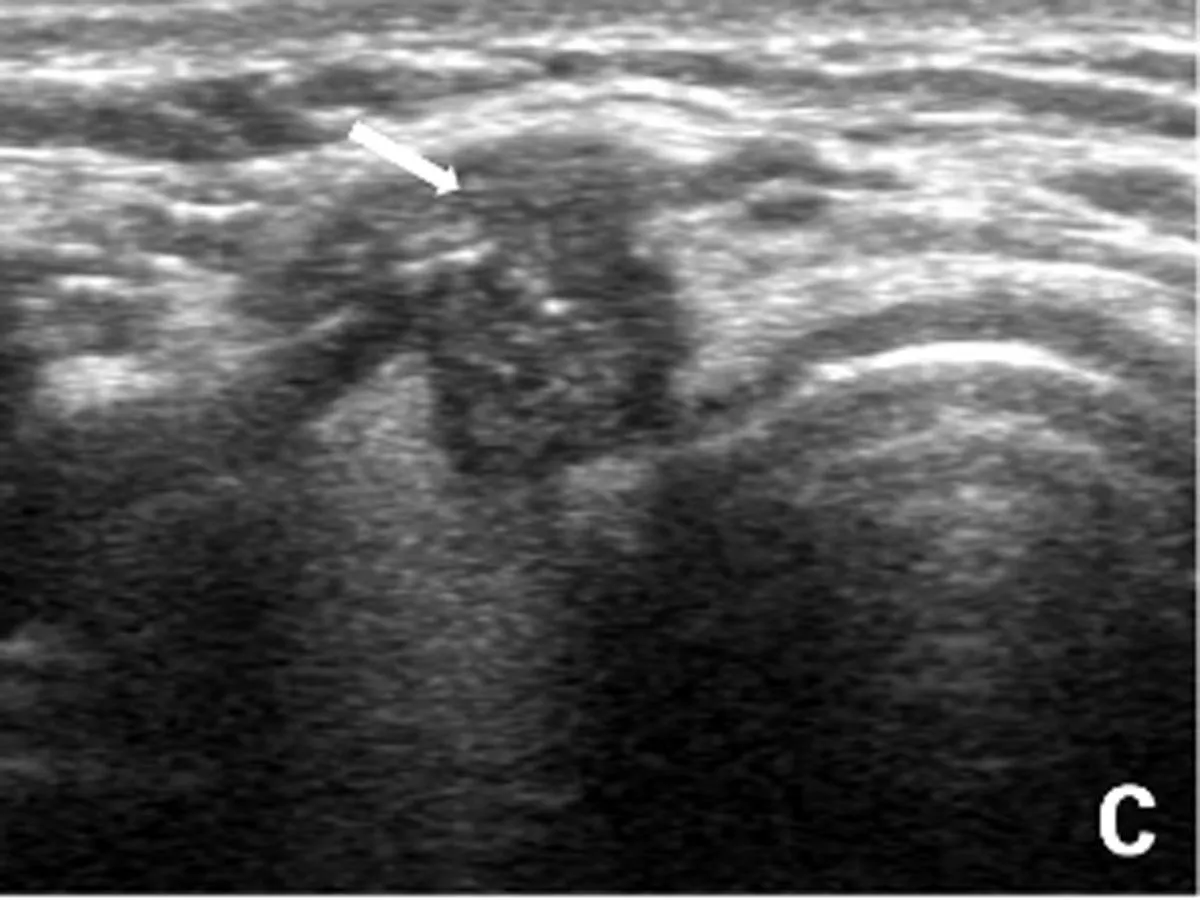
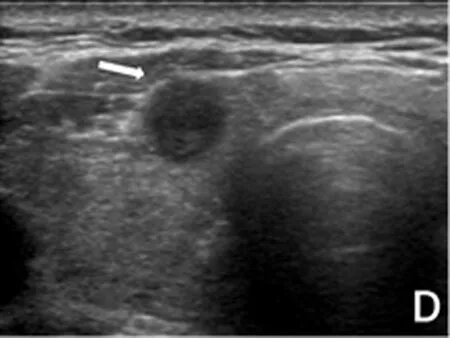
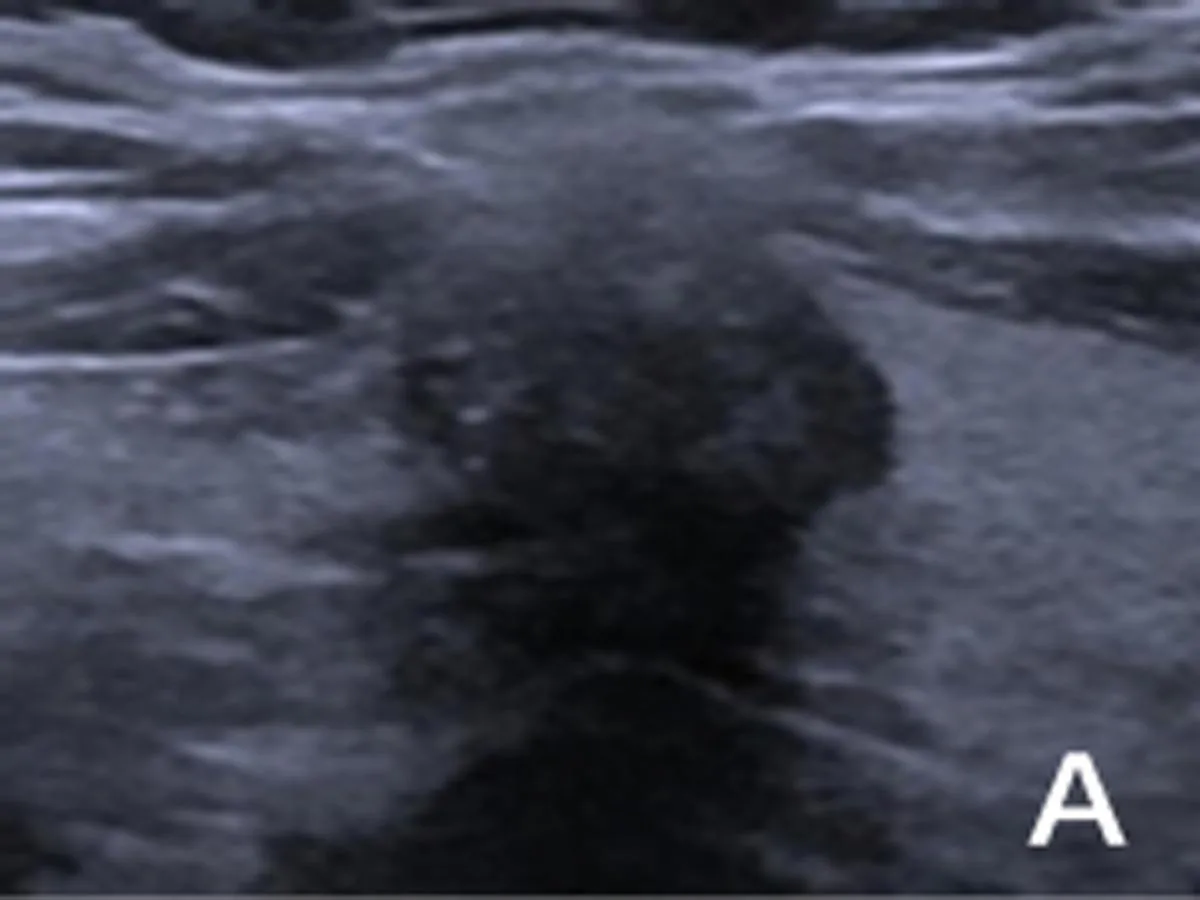
注:A.结节边缘与周围腺体境界不清;B.结节边缘呈微分叶状;C.结节突破腺体被膜,局部被膜中断(箭头所示);D.结节被膜下生长。

注: A为常规超声, B为超声造影图像, 结节呈不均匀低增强(15 s), C为快速消退(19 s)。

图3 建模组预测PTMC患者颈淋巴结转移风险的列线图
2.4 预测模型的评价以预测的概率和作为检验变量,是否出现颈淋巴结转移作为状态变量构建ROC曲线,评估模型区分力(图4)。建模组AUC为0.747(0.690~0.804),灵敏度0.65,特异度0.73。验证组AUC为0.778(0.697~0.860),灵敏度0.64,特异度0.81。
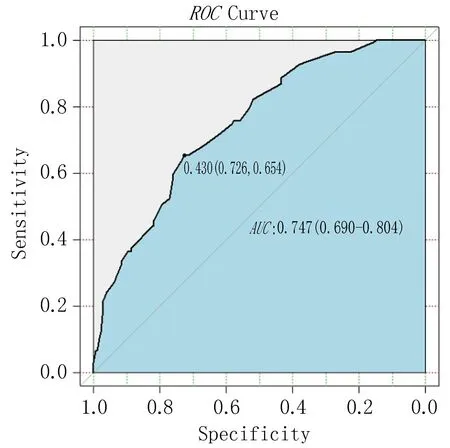
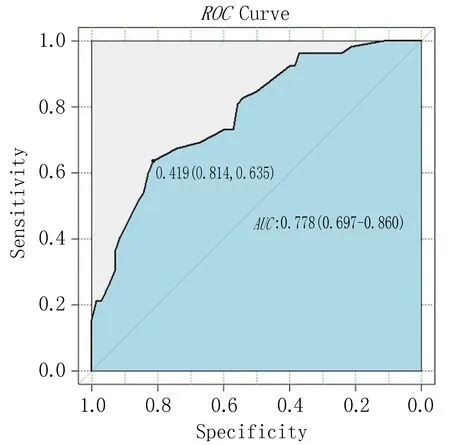
注: 左侧为建模组ROC曲线, 右侧为验证组ROC曲线。
HosmerLemeshow拟合优度检验结果显示(图5),建模组χ2=6.597(P=0.68),验证组χ2=7.466(P=0.59),绘制校准曲线,模型的实际预测结果与理想结果接近,提示术前通过危险因素预测的淋巴结转移风险与通过手术病理证实的实际发生风险之间具有良好的一致性。


注: 左侧为建模组, 右侧为验证组。
使用决策曲线分析(decision curve analysis,DCA)评价模型临床适用性(图6)。模型曲线离“ALL”线和“NONE”线较远,且建模组(红色实线)与验证组(蓝色虚线)曲线均高于其他变量(绿色虚线)。
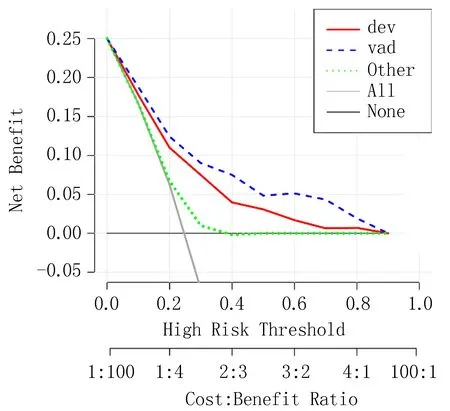
图6 列线图预测PTMC患者颈淋巴结转移风险的临床决策曲线
3 讨论
PTMC淋巴结转移最常发生于颈中央区,然而由于早期微转移和非特异性炎性增生等因素,使得基于形态学特征区分淋巴结转移与否仍然具有挑战性,LNM也常在术中病理检查才被发现。鉴于此,术前如何无创、便捷地评估LNM风险是困扰临床的实际问题。本研究选取在临床中容易获得的超声指标构建可视化预测模型,结果易于理解。
超声造影可以通过纯血池微泡造影剂实时动态评估肿瘤内血管构筑,甲状腺恶性结节由于分泌细胞因子会促进新生血管生成,使得病变组织中血管的数量、形态、结构均发生了显著变化[10],这是超声造影评估PTMC生物学特征的病理基础。本研究建模组快速消退的结节中有68.4%没有发生LNM,31.6%存在LNM,多因素分析显示,快速消退的PTMC结节更不容易发生LNM(OR=0.246,95%CI:0.078~0.773)。快速消退在一些恶性肿瘤中是特征性超声造影表现,甲状腺恶性结节更倾向于早期快速消退[11]。在本研究中,PTMC消退模式以同步(52.8%)和快速(40.4%)消退为主,在多因素分析中,通过哑变量设置得出快速消退的结节不容易发生LNM。甲状腺恶性结节快速消退的模式可能与肿瘤组织新生血管有关,其特点是肿瘤内分支增多且杂乱、管径不均匀、血流加速,加之病灶周围无包膜,与周围组织相比,造影剂廓清时间早,呈现“快出”的特点[10]。范莉芳等[12]研究认为,与之相反的缓慢的消退模式增加了LNM转移的风险,并可能与病灶内更复杂的血管结构有关。因此,PTMC的超声造影检查应全面观察整个造影剂灌注和退出的动态时期,对风险增高的患者重点关注淋巴结的超声扫查。
本研究发现边缘模糊的结节和具有微分叶、成角的结节均是PTMC发生LNM转移的危险因素。周明炀等[13]发现不规则形结节(87.2%)与边缘模糊的结节(80.3%)可能与肿瘤本身的特殊生物学行为有关,肿瘤浸润式生长方式可能导致了PTMC超声上不规则和模糊的病灶边缘。但不同的学者对结节边缘模糊的意义是有分歧的[14-15]。本组研究中404个结节,边缘模糊或微小分叶的比例占65.1%,转移组中的占比为74.2%,该特征不仅在PTMC中比例高,也是LNM的独立危险因素,这与薛坤等[16]报道的结果一致。
在甲状腺疾病中,声晕被认为可能是真纤维囊或假纤维囊,由结节的包膜或周围血管,或者是邻近受压的甲状腺实质构成。声晕在甲状腺乳头状癌不同亚型中的分布是没有差异的[17],其对淋巴结转移影响的机制尚不清楚,仍需后续进一步研究。
本研究的预测模型显示,多灶性、被膜下生长或侵犯被膜的PTMC,淋巴结转移风险分别增加了2.2倍和1.6倍,这与既往研究相符[18]。多灶性的结节可能来自不同的独立起源,这种机制可能预示着病灶具有转移能力的攻击行为,从而表现出更高的区域性LNM倾向[19-20]。虽然PTMC的病程在大多数患者中是相对缓慢的,但如果肿瘤突破腺体被膜,则会出现腺体外侵犯的风险[21]。侵犯被膜的结节在超声上可见与被膜接触、被膜轮廓向外凸出、被膜的连续性中断以及结节向外侵犯,这种行为是肿瘤更具侵袭性的标志。另外,本研究单因素分析中,更小的年龄、男性与LNM相关,但均未被纳入多因素的预测模型,分析原因可能与本研究纳入的样本量偏少有关。
本研究不足之处:(1)除超声造影外,“萤火虫”技术、剪切波弹性成像技术等也可从不同角度提示原发病灶的生物学特征,这在后续的研究中都应考虑纳入。(2)本研究主要关注了LNM风险的研究,并没有具体细分中央区和颈侧区淋巴结转移的风险,也没有细分大容量淋巴结转移[7](转移数目>5枚)的影响因素,这在后续研究中需做更细致的资料收集与分析。
本研究以5个指标建立并验证了具有较好临床获益的列线图预测模型,超声和造影特征有助于评估PTMC淋巴结转移风险,协助指导和制定个体化诊疗方案。

