利福平耐药结核病患者表型药敏试验结果分析及与Xpert MTB/RIF结果比较
万 荣,李光妹,季永静,黄 艳,刘 蕾,李明武△
1.云南省昆明市第三人民医院结核二科,云南昆明 650041;2.大理大学公共卫生学院,云南大理671000
结核病是全球面临的重大公共卫生问题,尤其是近些年耐药菌株的流行,使结核病的控制面临更加严峻的局面。耐多药(MDR)结核病是指结核病患者感染的结核分枝杆菌(MTB)经体外药物敏感性试验(以下简称药敏试验)证实至少同时对异烟肼和利福平(RIF)耐药[1]。世界卫生组织(WHO)2022年发布的《全球结核病年度报告》显示,2021年我国估算的结核病新发患者数量为78万,实验室确诊病例16 826例,仍是耐药高负担国家之一[2]。由于90%的RIF耐药株同时也对异烟肼耐药,因此,RIF耐药被认为是MDR的重要标志[3]。研究RIF耐药患者耐药情况,对后期制订合理用药方案有重要意义。笔者通过对288例RIF耐药结核病患者对一线、二线抗结核药物耐药情况进行分析,以期为临床用药提供参考。现报道如下。
1 资料与方法
1.1一般资料 回顾性收集2019年1月至2021年12月昆明市第三人民医院收治的经结核分枝杆菌及利福平耐药快速检测(Xpert MTB/RIF)鉴定为MTB感染、并对RIF耐药的288例患者的临床资料。其中经BACTEC MGIT 960 System鉴定MTB培养阴性63例,男39例、女24例,平均年龄(42.5±12.0)岁,初治肺结核30例、复治肺结核33例;MTB培养阳性225例,男148例、女77例,平均年龄(41.4±10.5)岁,初治肺结核78例、复治肺结核147例。本研究经本院医学伦理委员会审批通过(审批号:2021021806)。所有研究对象对本研究均知情同意。
1.2方法 225例MTB培养阳性患者中,除8例患者因联系不上未行药敏检测外,其余213例患者均采用微孔板比例法进行表型药敏试验,主要包括异烟肼、RIF、乙胺丁醇、链霉素、利福喷汀5种一线抗结核药及左氧氟沙星、阿米卡星、卷曲霉素、丙硫异烟胺、帕司烟肼、莫西沙星、对氨基水杨酸钠、克拉霉素、利福布汀、卡那霉素、氯法齐明11种二线抗结核药物。
1.3观察指标 比较表型药敏结果及其与Xpert MTB/RIF结果的差异。
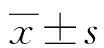
2 结 果
2.1RIF耐药结核病患者耐药情况分析 213例行微孔板药敏试验的结核病患者中,MDR患者比例最高,占53.5%(114/213),广泛耐药患者占22.5%(48/213),且男性耐药患者比例[65.7%(140/213)]高于女性[34.3%(73/213)],但差异无统计学意义(P>0.05);单耐RIF的结核病患者中,初治患者耐药发生率较高;在MDR和广泛耐药患者中,复治患者耐药发生率均高于初治患者(χ2=5.648、13.385,P<0.05)。见表1。

表1 RIF耐药结核病患者耐药情况分析[n(%)]
2.2213例行微孔板药敏试验患者中一、二线抗结核药物耐药情况 一线抗结核药物耐药率从高到低依次为RIF、利福喷汀、异烟肼、链霉素、乙胺丁醇,其耐药率分别为96.7%(206/213)、96.7%(206/213)、76.1%(162/213)、26.8%(57/213)、20.2%(43/213);二线主要抗结核药物耐药率从高到低依次为利福布汀、莫西沙星、左氧氟沙星、对氨基水杨酸钠、阿米卡星、帕司烟肼、卡那霉素、卷曲霉素、丙硫异烟胺、克拉霉素、氯法齐明,耐药率分别为93.8%(200/213)、19.2%(41/213)、18.8%(40/213)、6.1%(13/213)、4.7%(10/213)、4.7%(10/213)、4.7%(10/213)、4.2%(9/213)、1.4%(3/213)、1.4%(3/213)、0.9%(2/213)。见表2。

表2 213例行微孔板药敏试验患者中一、二线抗结核药物耐药情况[n(%)]
2.3Xpert MTB/RIF与RIF耐药表型药敏检测结果比较 本研究Xpert MTB/RIF检出RIF耐药患者288例,有75例(26.1%)显示基因耐药表型未知;进行表型药敏试验的213例患者中,有7例(3.3%)显示基因耐药表型敏感,206例(96.7%)显示基因耐药表型耐药。
3 讨 论
有学者研究发现,约80%的RIF耐药结核病患者同时并发异烟肼耐药[3],WHO推荐单耐RIF的结核病患者可按照MDR结核病患者进行治疗[4]。但由于早期耐药方案缺乏其他药物的表型药物敏感试验结果支撑,一旦这些药物已发生耐药,则会明显影响其治疗效果及预后[5]。本研究288例Xpert MTB/RIF检测RIF耐药患者中,但有26.1%耐药表型药敏试验结果为未知。因此,为进一步了解RIF耐药的结核病患者对其他结核药物的耐药情况,笔者对RIF耐药结核病患者的表型药敏试验结果进行分析,为制订有效的治疗方案提供参考。
2022全球结核病年报,再次推荐快速分子诊断检测,实现更早和更准确诊断结核病。2021年640万新发结核病病例中,仅有38%使用WHO推荐的快速分子检测[2]。GeneXpert MTB/RIF检测整合了MTB核酸及RIF耐药基因检测技术,灵敏度及特异度均较高,具有良好的可靠性[6-8]。2013年WHO将Xpert MTB/RIF作为MTB感染的首选复筛查方法,替代传统的抗酸杆菌涂片和结核菌培养[9]。有研究发现,GeneXpert MTB/RIF检测结果与RIF表型耐药检测结果具有高度一致性,可高达95%左右,已成为当前诊断MTB RIF耐药的金标准[10]。本研究以Xpert MTB/RIF检测显示的RIF耐药结核病患者288例为研究对象,其中225例RIF耐药结核病患者培养阳性;行表型药敏试验的213例患者中,表型结果显示有5例全敏,2例为单耐异烟肼,RIF耐药(包括单耐RIF、多耐、耐多、广泛耐药)206例(96.7%),与文献[13]研究结果相似。本研究中有7例(3.3%)药敏检测结果显示基因耐药表型敏感,但依据《结核病病原学分子诊断专家共识》[11],认为此种情况多为表型药敏试验耐药检测错误所致,推荐参照Xpert MTB/RIF检测结果。罗嘉韵等[12]研究Xpert MTB/RIF 检出耐药菌株92.31%,表型药敏检测为96.15%,二者灵敏度、特异度比较差异均无统计学意义(P>0.05),二者检测一致性检的Kappa 值为0.795。同时本研究发现Xpert MTB/RIF检测阳性但培养阴性63例,培养阳性有225例。方木通等[13]研究发现,在RIF耐药患者中,41.04%的患者为初治患者,说明耐药MTB的传播是RIF耐药结核病的重要来源,管理并治愈RIF耐药患者,尽早降低其传染性,是控制RIF耐药结核病的根本方法。
根据《耐药结核病化学治疗指南(2019年简版)》[1]进行耐药分类,本研究结果显示耐多药结核病例数最高达53.5%(114/213),广泛耐药的比例也高达22.5%(48/213),且2种耐药患者中以复治患者占多数。本研究发现,一线抗结核药物耐药率从高到低依次是RIF、利福喷汀、异烟肼、链霉素、乙胺丁醇,其耐药率分别为96.7%、96.7%、76.1%、26.8%、20.2%;异烟肼耐药率为76.1%,与WHO估算的全球异烟肼平均耐药水平(78%)基本一致,这也是WHO主张将RIF耐药结核病与MDR结核病同样对待的重要原因[2]。《中国结核病预防控制工作技术规范》在RIF耐药方案中,左氧氟沙星和莫西沙星位于A组内首位,可见其组成耐药方案的重要性[12]。本研究中二线抗结核药物敏感性试验发现,莫西沙星和左氧氟沙星耐药率较高(19.2%、18.8%),明显高于其他二线抗结核药物,且MDR与广泛耐药患者中,复治患者耐药发生率明显高于初治患者(P<0.05)。方木通等[13]研究结果显示,当以RIF表型耐药结果为金标准时,其耐药率达到26.30%,且复治患者耐药发生比例较多。左氧氟沙星和莫西沙星作为核心药物,若出现此类药物耐药,会明显降低治疗方案的疗效,使治疗失败率上升[14-17]。治疗强化期应选择至少4种可能有效的抗结核药物组成方案,巩固期应选择至少3种可能有效的抗结核药物组成方案[18];评估某种药品在治疗方案中能否有效,需要综合多方面因素考量,包括患者个体药物敏感性试验结果、患者感染来源者的药敏试验结果、患者是否对存在交叉耐药的药物有耐药性、患者所在地区药物耐药水平,以及在患者既往治疗失败的方案中是否包含这一药品[19-20]。因此,临床医生在制订治疗方案之前,要详细询问其用药史,同时启用分子生物学方法检查氟喹诺酮类药是否存在耐药基因突变,并对培养阳性患者进行一、二线抗菌药物药敏试验十分必要。本研究不足之处为未对分子生物学基因突变与表型药物敏感试验进行对比研究。
综上所述,RIF耐药结核病患者中,初治患者耐药发生率较高,在初治患者中开展Xpert MTB/RIF检测非常必要,MDR患者耐药多发生于复治患者,对于复治患者除常规开展Xpert MTB/RIF检测外,还必须行MTB培养及一、二线抗结核药物表型药敏试验,且氟喹诺酮类耐药率在二线药物中耐药率最高,应加强分子生物学和表型试验对氟喹诺酮类药物灵敏度检测。

