银柴胡多糖超声辅助提取工艺优化及抗氧化活性分析
王 红,彭 励,2, ,宋 乐,冯 璐,李振凯,李彦青,高 跳
(1.宁夏大学生命科学学院,宁夏银川 750021;2.宁夏天然药物工程技术研究中心,宁夏银川 750021)
银柴胡(Stellariae Radix)是我国传统中药中常用的根类药材[1],作为宁夏道地药材,其化学成分主要有甾醇类、黄酮类和生物碱等[2-4]。在传统中医临床应用中,银柴胡具有祛除小儿疳热,治疗骨蒸痨热等功效[5]。在现代医药中,银柴胡具有抗炎、抗过敏、抗癌、促进血管舒张等作用[6]。近年来,银柴胡药材主要食用方式是通过制作银柴胡粥[7]、延胡索红枣粥[8]以及与其他药材制作荷叶包饭团[9]等,综合利用率低,所以银柴胡多糖的提取及其抗氧化的研究极其重要。
目前,植物多糖的提取方法主要以水提醇沉、超声辅助法、微波辅助法为主,虽然近几年已有新兴的提取工艺并取得一定的效果,但是每种方法都有一定程度的局限性,例如:操作不易控制、设备价格昂贵等[10-11],又因植物多糖是一种极性分子,易溶于水,不溶于有机溶剂[12],因此水提醇沉是使用最广泛的方法。
植物多糖大多选择脂肪提取液为石油醚、乙醚和乙醇等有机溶剂进行除脂,此方法存在操作复杂、效率低、有机溶剂残留和污染环境等缺点[13-14]。超临界CO2萃取技术是一种新兴的、绿色的提取方法,其原理是利用超临界下的CO2低极性,高密度等特点,对物料中极性低,分子量小,亲脂性强的物质实现提取分离[15]。本课题组[16]采用超临界CO2萃取技术对实验材料进行除脂处理,相较于蔡少青等[17]以银柴胡为原料,采用乙醇、丙酮和乙醚等在索氏抽提器中回流除去非极性成分等方法,不仅减少了脱脂过程中的有机溶剂的使用,也减少多糖在脱脂过程中的损耗。同时,已有研究证明银柴胡药材具有清除自由基和活性氧的作用[18],冯娇等[19]认为此抗氧化作用与药材中含有黄酮类成分有关,也有研究报道植物甾醇也具有清除自由基作用[20],宋乐[21]证明抗氧化作用与脂质类成分有关。但银柴胡的抗氧化作用是否与多糖成分有关,需要进一步研究。
基于此,本研究以银柴胡为研究对象,采取单因素结合响应面法得到银柴胡多糖最佳提取工艺,并通过Sevag 除蛋白后得到银柴胡粗多糖,并以VC为阳性对照,DPPH·、·OH、ABTS+·清除率为指标探究其体外抗氧化活性。为银柴胡多糖在功能性药品或食品开发及传统中药药效物质基础的研究奠定了基础,也使优化后的提取工艺参数对指导银柴胡综合开发利用具有实践意义。
1 材料与方法
1.1 材料与仪器
采集3~4 年生人工栽培银柴胡 产地为宁夏同心县银柴胡规范化种植基地,经宁夏大学生科院彭励教授鉴定为石竹科繁缕属植物银柴胡的干燥根;1,1-二苯基-2-三硝基苯肼(1,1-diphenyl-2-trinitrophenylhydrazine,DPPH)上海化成工业发展有限公司;2,2-联氮-二(3-乙基-苯并噻唑-6-磺酸)(2,2'-Azin obis-(3-ethylbenzthiazoline-6-sulphonate),ABTS)上海易恩化学技术有限公司;葡萄糖对照品 HPLC≥98%,上海源叶生物科技有限公司;L-抗坏血酸 天津市凯通化学试剂有限公司;三氯甲烷、硫酸 国药集团;苯酚、正丁醇、无水乙醇、苯酚 上海广诺化学科技有限公司;硫酸亚铁 徐州天鹅化工有限公司;以上均为分析纯。
KQ-500DE 型数控超声机 昆山市超声仪器有限公司;TU-1810 型紫外可见分光光度计 北京普析通用仪器有限责任公司;HSB-Ш型循环水式多用真空泵 上海振荣科学仪器有限公司。
1.2 实验方法
1.2.1 银柴胡多糖的提取工艺流程 银柴胡药材粉碎过40 目筛,经超临界CO2萃取脱脂[16](压力35 MPa,萃取温度为47 ℃,CO2流量控制在50 L/h,萃取3 h),脱脂后粉末加水超声辅助提取(料液比1:20;超声功率100 W),将提取液过滤浓缩,分级醇沉后冻干获得银柴胡多糖粗提物,后经Sevag 法除蛋白5 次获得银柴胡粗多糖,进一步通过柱层析分离纯化获得银柴胡多糖。
1.2.2 多糖得率及含量计算
1.2.2.1 多糖粗提物得率的计算 将水提醇沉之粗提物后的多糖进行冷冻干燥,称量其重量,根据公式(1)计算多糖粗提物得率[22]。
式中,M:冷冻干燥后的银柴胡多糖粗提物质量(g),M0:银柴胡粉末质量(g)。
1.2.2.2 换算因子的测定 参照文献[22-23],采用苯酚-硫酸法进行含量测定。以葡萄糖为标准品,在482 nm 处测定吸光度,得到回归方程为Y=0.0646x-0.0803,R²=0.997。该方程在0.021~0.841 g/L 范围内呈良好线性关系。参照文献[17],精密称取经柱层析法纯化得到的银柴胡多糖,配制质量浓度为4 mg/mL的多糖溶液,再按上述回归方程求出银柴胡多糖中的葡萄糖浓度,并按照式(2)计算换算因子。
式中,W 为银柴胡多糖质量(g),C 为葡萄糖浓度(mg/mL);D 为稀释倍数。
1.2.2.3 含量的测定 准确称取多糖粉末,配制质量浓度为4 mg/mL 的多糖溶液,按1.2.2.2 中苯酚-硫酸法测得吸光度,根据公式(3)计算多糖含量:
式中,C 为样品溶液多糖浓度(mg/mL);D 为样品溶液稀释倍数;W 为样品质量(g);f 为换算因数(f=1.12)。
1.2.3 单因素实验
1.2.3.1 提取温度对银柴胡多糖粗提物的影响 固定提取时间3 h,提取次数2 次,考察提取温度(20、30、40、50、60 ℃)对银柴胡多糖粗提物得率的影响。
1.2.3.2 提取时间对银柴胡多糖粗提物的影响 固定提取温度40 ℃,提取次数2 次,考察提取时间(1、2、3、4、5 h)对银柴胡多糖粗提物得率的影响。
1.2.3.3 提取次数对银柴胡多糖粗提物的影响 固定提取温度40 ℃,提取时间3 h,考察提取次数(1、2、3、4、5 次)对银柴胡多糖粗提物得率的影响。
1.2.4 Box-Behnken 试验设计 以银柴胡多糖粗提物得率(Y)为响应值,根据单因素实验结果,设计3 因素3 水平的Box-Behnken 试验,对银柴胡多糖粗提物提取工艺进行优化,响应因素水平设计见表1。

表1 Box-Behnken 试验因素与水平设计Table 1 Box-Behnken experimental factors and horizontal design
1.2.5 银柴胡粗多糖抗氧化活性试验
1.2.5.1 清除DPPH 自由基能力的测定 将不同浓度(1.0、2.0、4.0、8.0、10.0 mg/mL)的银柴胡溶液与0.2 mmol/L DPPH-无水乙醇溶液按照体积比1:4 充分混匀,在室温下避光反应30 min,于517 nm 波长处测定吸光度。无DPPH 的反应混合物作为对照,VC作为阳性对照[24-25]。按式(4)计算DPPH 自由基清除率。
式中:A0为无样品的反应混合物溶液吸光度;A1为样品与DPPH 溶液的吸光度;A2为无DPPH的反应混合物溶液吸光度。
1.2.5.2 清除OH 自由基能力的测定 取10 mL 刻度试管,加入1 mL 的FeSO4(6 mmol/L),1 mL 的水杨酸-乙醇溶液(6 mmol/L),1 mL 样品银柴胡粗多糖溶液,加入1 mL 的H2O2启动反应,在37 ℃条件下保温30 min,以超纯水为参比,在510 nm 波长处测定吸光度[26]。清除率计算方法如下:
式中:Aa为空白对照的吸光度;Ax为加入银柴胡粗多糖或L-抗坏血酸溶液后的吸光度;Ay为不加H2O2的样品液吸光度。
1.2.5.3 清除ABTS+自由基能力的测定 0.384 g 的ABTS 以及0.066 g 过硫酸钾在100 mL 蒸馏水中,室温避光反应12 h,得到ABTS 母液。取出10 mL ABTS 母液用0.01 mol/L 磷酸缓冲液(pH7.4)调节至pH8.20,使溶液在734 nm 处的吸光度的范围为0.70±0.02。将1 mL 不同浓度(1.0、2.0、4.0、8.0、10.0 mg/mL)银柴胡粗多糖溶液与1 mL 蒸馏水和2 mL ABTS 供试液充分混匀后室温避光10 min,在734 nm 处测定吸光度。未加入ABTS 的反应混合物作为对照,VC作为阳性对照[27]。按公式(6)计算ABTS+自由基清除率。
式中:A0为无样品的反应混合物溶液吸光度;A1为样品组吸光度;A2为无ABTS 的反应混合物溶液吸光度。
1.3 数据处理
所有试验均重复3 次,数据结果用均值±标准差(SD 值)表示。使用Origin 2018 软件绘制趋势图;使用SPSS 25.0 软件进行方差分析及显著性检验;Design-Expert 10.0.7 软件对响应面试验数据进行分析。
2 结果与分析
2.1 单因素实验结果
2.1.1 提取温度对银柴胡多糖粗提物的影响 提取温度对银柴胡多糖粗提物的影响如图1 所示,提取时间和次数不变,随着提取温度增加,多糖粗提物得率呈先上升后下降趋势,在50 ℃时得率达到最大值,为27.89%,当提取温度超过50 ℃后,得率逐渐降低。这与柴美灵等[28]研究发现甘草多糖得率随提取温度的变化趋势相同。可能是因为随着温度的升高使分子运动加速了提取溶剂的渗入和植物细胞内多糖的释放,当大部分多糖释放到溶质中,由于温度升高可以使部分水溶性的多糖分解,对温度敏感的多糖结构遭到破坏[29]。所以导致60 ℃的多糖粗提物得率下降。因此超声温度以50 ℃为宜。

图1 提取温度对多糖粗提物得率的影响Fig.1 Effect of temperature on the yield of polysaccharide crude extract
2.1.2 提取时间对银柴胡多糖粗提物的影响 提取时间对银柴胡多糖粗提物的影响如图2 所示,在提取温度为40 ℃,提取次数2 次,随着提取时间延长,得率急速升高,在3 h 时,多糖粗提物得率达到最高水平为27.51%,而继续延长提取时间,得率呈下降趋势。分析其原因可能是银柴胡物料所含的多糖短时间内不能完全释放,但随着提取时间的延长,较多的多糖溶解并释放到溶质中,使得得率提高,但随时间的持续增加,会使部分多糖被分解,多糖结构破坏而降解,导致多糖得率下降[30]。因此,提取时间选择3 h为宜。

图2 提取时间对多糖粗提物得率的影响Fig.2 Effect of time on the yield of polysaccharide crude extract
2.1.3 提取次数对银柴胡多糖粗提物的影响 提取次数对银柴胡多糖粗提物的影响如图3 所示,多糖粗提物得率随提取次数的增多呈现先增加后降低的趋势,当提取次数达到2 次时,得率达到最高值,为27.91%。其原因可能是前2 次提取时,大部分多糖已经释放到溶质中,但是连续多次的提取使多糖的结构被破坏或者物料的水溶液变得黏稠,多糖溶出困难[31]。因此,选择提取次数2 次,多糖粗提物得率最高。
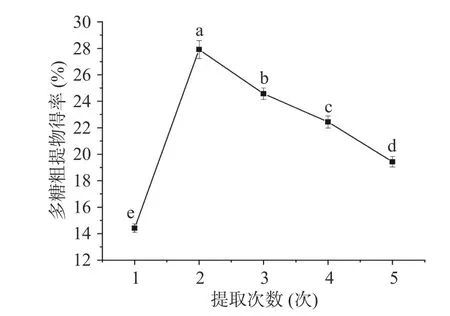
图3 提取次数对多糖粗提物得率的影响Fig.3 Effect of times on the yield of polysaccharide crude extract
通过单因素不同水平对多糖粗提物得率影响结果可见,提取温度为50 ℃、提取时间为3 h、且提取次数为2 次为银柴胡多糖提取的最佳基本条件。可以获得最高得率。并以此作为 Box-Behnken 法优化设计的依据。
2.2 Box-Behnken 法优化银柴胡多糖提取工艺
2.2.1 Box-Behnken 试验设计与结果 试验设计和结果如表2 所示。通过对数据进行线性拟合,得到银柴胡多糖粗提物的二次多元回归模型方程。

表2 Box-Behnken 优化试验设计与结果Table 2 Box-Behnken optimization experimental design and results
对银柴胡多糖粗提物回归方程进行了方差分析,结果见表3。用F值和P值评价模型的显著性。F值越大,P值越小,模型越显著。如表3 所示,该模型的F值为27.47,P=0.0001,表明该模型具有极显著意义。利用失拟项评价模型的拟合度。该模型失拟项为P=0.3108>0.05,表示拟合程度较高,表明实验值是准确可靠的,具有较高的可信度。由F值可知,三个因素对银柴胡多糖粗提物的影响程度依次为:提取时间>提取次数>提取温度,通过P值可知,B、BC、B2、C2都表现为差异极显著水平(P<0.01),A、C、AB 表现为差异显著水平(P<0.05)。

表3 回归方程的方差分析Table 3 Analysis of variance of regression equation
2.2.2 各因素之间的交互作用分析 在单因素影响多糖粗提物得率的基础上,进一步对3 个关键工艺参数超声提取温度、提取时间、提取次数的交互作用进行分析,结果见图4 所示三维响应面曲面图和等高线图,曲面图越陡峭,等高线图越接近椭圆,说明交互作用越显著[32]。如图4(a)所示,提取时间和提取次数的三维响应面图中曲面陡峭,而且二维图中等高线也呈明显的椭圆形,表明提取时间和提取次数的交互作用对多糖粗提物得率的影响极显著;由图4(b)可见,提取时间和提取温度的三维响应面图中曲面较陡峭,其中提取时间的影响比提取温度影响大,而且在二维图中等高线呈椭圆形,表明提取时间和提取温度的交互作用对多糖粗提物得率具有显著的影响;由图4(c)可以看出,三维响应面图中曲面较为平缓,而且二维等高线图趋近圆形,说明提取温度和提取次数交互作用对得率影响较小。与方差分析结果一致。通过3D 图发现曲面呈中间凸起的形状,说明曲线有最高点,也表明存在最优条件。

图4 两因素交互作用的三维响应面图和等高线图Fig.4 Three-dimensional response surface map and contour map of the interaction of two factors
2.2.3 Box-Behnken 优化工艺的验证结果 根据所得模型,通过Design-Expert10.0.7 软件对响应面进行分析,确定最佳提取条件为:提取温度49.87 ℃,提取时间3.17 h,提取次数2.33 次。在此条件下,模型预测银柴胡多糖粗提物得率为28.41%。考虑到实际应用过程中操作简便,将工艺条件修正为提取时间3.20 h、提取次数2 次、提取温度50 ℃,进一步按此工艺条件进行验证。验证结果表明,银柴胡多糖粗提物平均得率为28.24%(SD 值=0.10%,n=3),与理论值相对误差为0.17%,实际值与理论值基本相符,说明模型对银柴胡多糖粗提物提取工艺参数的优化结果可靠,具有一定的实用价值。进一步通过柱层析分离纯化后多糖含量为59.13%。
2.2.4 银柴胡粗多糖抗氧化活性测定 银柴胡粗多糖对DPPH 自由基清除率如图5(a)所示,随着银柴胡粗多糖浓度增加,对DPPH 自由基的清除能力逐渐增强。当粗多糖浓度为10 mg/mL 时,其对DPPH自由基的清除率为87.68%,此时VC的清除率为96.59%。经计算,银柴胡粗多糖清除DPPH 自由基的IC50为5.47 mg/mL。表明银柴胡粗多糖具有一定的DPPH 自由基清除能力,但其效果弱于VC。

图5 银柴胡粗多糖抗氧化活性的测定结果Fig.5 Determination of antioxidant activity of polysaccharide from Stellariae Radix
银柴胡粗多糖对OH 自由基清除率如图5(b)所示,随着银柴胡粗多糖浓度增加,对OH 自由基的清除能力逐渐增强。当粗多糖浓度为10 mg/mL 时,其对OH 自由基的清除率为97.74%,此时VC的清除率为99.75%。经计算,银柴胡粗多糖清除OH 自由基的IC50为2.40 mg/mL。表明银柴胡粗多糖对OH 自由基有较好的清除能力。
银柴胡粗多糖对ABTS+自由基清除率如图5(c)所示,银柴胡粗多糖对ABTS+自由基清除能力随着多糖浓度的升高而增加。当质量浓度达到10 mg/mL时,对ABTS+自由基清除率为99.0%,此时VC的清除率为99.85%。经计算,银柴胡粗多糖清除ABTS+自由基的IC50为1.44 mg/mL。表明银柴胡粗多糖具有较好的ABTS+自由基清除能力。
3 结论
得到最佳提取条件为提取温度50 ℃,时间3.20 h,次数2 次。在该条件下多糖的实际得率为28.24%±0.10%,多糖含量为59.13%。优化后的提取条件综合反映了各因素之间的关系,更加具有可操作性,使银柴胡多糖能够充分释放,有效避免了资源的浪费。体外抗氧化实验表明,银柴胡粗多糖对DPPH、OH、ABTS+自由基的IC50分别为5.47、2.40 和1.44 mg/mL,表明银柴胡多糖具有一定的抗氧化能力。因此,银柴胡的抗氧化不仅仅与黄酮类、甾醇类及脂质类成分密切相关,还与多糖类成分有关。
综上所述,本研究通过优化提取工艺,得到高得率的银柴胡多糖粗提物,粗提物经除蛋白之后所获得的银柴胡粗多糖具有一定的抗氧化活性。以期为银柴胡多糖在功能性药品或食品开发及传统中药药效物质基础的研究提供依据,也为银柴胡药材多元化开发利用和提高经济与社会效益提供美好前景。

