透明质酸钠的热稳定性及降解动力学模型
袁西伦,王文斌,吴剑英
透明质酸钠(sodium hyaluronate,SH)于1934 年被发现[1],是由D-葡萄糖醛酸和N-乙酰基葡糖胺之间通过糖苷键相互交联的多糖[2,3]。 其主要用在骨关节炎治疗、眼科、外科手术防粘连、医学美容、化妆品等领域[4~8]。
文献研究报道,SH 的结构中存在大量羟基,在溶液中SH 能够形成许多氢键[9~12]。 在氢键及范德华力的作用下,SH 分子形成了二级双螺旋结构,提高了稳定性[10,12,13]。 二级结构通过生物化学作用在体内形成网状三级结构[13~18]。
SH 的降解是从长链大分子裂解成小的链段反应,是聚合物的破坏反应,其降解主要表现在相对分子质量(relative molecular mass,Mr) 的变化,de Melo BAG 等[9]进行了在高温(60 ℃)及高pH(pH 12)条件下SH 的降解动力学研究。 Mondek J 等[19]研究了在37 ℃及120 ℃条件下对SH 粉末及溶液的稳定性的影响。 笔者通过分子排阻色谱法实验检测SH 的Mr,考察不同温度下的热稳定性, 并建立降解动力学模型。 另外,笔者还进行了SH 经高温作用后的稳定性研究, 结合文献分析其热稳定性变化的可能内在原因,为SH 的生产、研究提供理论指导意义。
1 材料与方法
1.1 实验材料
1.1.1 实验样品
SH(上海利康瑞生物工程有限公司,中国)。
1.1.2 主要试剂与仪器
磷酸氢二钠及磷酸二氢钠(湖南九典宏阳制药有限公司,中国);氯化钠(江苏勤奋药业有限公司,中国);聚苯乙烯磺酸钠对照品(北京润汇源公司,中国)。
Agilent 1100 型液相色谱系统、G1362A 示差折光检测器(安捷伦科技公司,美国);Shodex SB-806HQ(300 mm × 8.0 mm)凝胶柱(Agilent Technologies,美国);DHG-9245A 电热恒温干燥箱(上海一恒科学仪器有限公司,中国);Memmert hpp750 恒温恒湿箱(美墨尔特公司,德国);RFM-1.2 通风式干燥灭菌器(山东新华医疗器械股份有限公司,中国);XPR105DR 天平(梅特勒-托利多公司,瑞士);RCT 5 D S025 磁力搅拌台(艾卡公司,德国)。
1.2 方法
1.2.1 透明质酸钠在不同温度下的稳定性考察
称取适量的SH 原料(1%)、磷酸氢二钠(0.054%)、磷酸二氢钠(0.00017%)、氯化钠(0.85%)和适量注射用水,配成含1%SH 溶液,用西林瓶分装;分别在60 ℃、80 ℃、100 ℃、115 ℃和121 ℃下进行稳定性考察,不同时间点取样,检测SH 的Mr。
1.2.2 121 ℃高温灭菌后透明质酸钠稳定性考察
按照1.2.1 节配制方法配制SH 溶液, 用西林瓶分装; 在121 ℃下,F0= 8 进行高温灭菌, 然后在25 ℃、40 ℃、50 ℃和60 ℃进行稳定性考察,以及未灭菌的样品在25 ℃下进行稳定性考察, 不同时间点取样,检测SH 的Mr。
1.2.3 透明质酸钠相对分子质量检测方法
采用分子排阻色谱法 (《中国药典》2015 年版四部通则0514)检测SH 的Mr。
色谱条件:Shodex SB-806HQ(300 mm×8.0 mm)凝胶柱,0.2 mol/L 氯化钠溶液(含0.01%NaN3)溶液为流动相,柱温40 ℃,流速为0.5 mL/min,示差折光检测器。
操作步骤:取样品适量,加流动相配制成质量浓度0.5 mg/mL SH 溶液作为供试品溶液,取聚苯乙烯磺酸钠对照品适量,加流动相配制成质量浓度0.5 mg/mL聚苯乙烯磺酸钠溶液为对照品溶液; 取供试品溶液、对照品溶液各100 μL,分别注入液相色谱仪,记录色谱图,采用凝胶渗透色谱(gel permeation chromatography,GPC)专用软件处理数据,计算SH 的Mr。
1.2.4 透明质酸钠降解动力学模型构建
采用阿伦尼乌斯(Arrhenius)[20~22]动力学方程建立SH 降解动力学模型。
一级反应动力学方程式(1),转换成对数形式方程式(2),对SH 的Mr 与时间(t)的关系按照一级反应方程式(2)进行拟合。
式中:Mr 为任意时间SH 的相对分子质量;Mr0为Mr的起始值;k 为相应条件下反应降解速率常数;t 为稳定性考察时间。
阿伦尼乌斯(Arrhenius) 动力学方程式(3),其对数形式为方程式(4),利用不同温度下SH 的降解常数与相应的绝对温度按方程式(4)进行拟合,计算得活化能Ea(kJ/mol),建立SH 的降解动力学方程。
式中:k 为反应降解速率常数;A 为前因子;Ea 为活化能(kJ/mol);R 为气体常数,8.314 J/(mol·K);T 为绝对温度(K)。
1.2.5 数据处理
所有实验数据采用Origin2021 软件进行绘图、相关动力学分析与回归分析。
2 结果
2.1 透明质酸钠在不同温度下相对分子质量变化
2.1.1 透明质酸钠的相对分子质量与温度和时间的关系
SH 在100 ℃、115 ℃、121 ℃条件下, 其Mr 随时间的变化趋势逐渐下降 (图1); 在60 ℃、80 ℃条件下,其Mr 随时间的变化趋势逐渐下降(图2)。
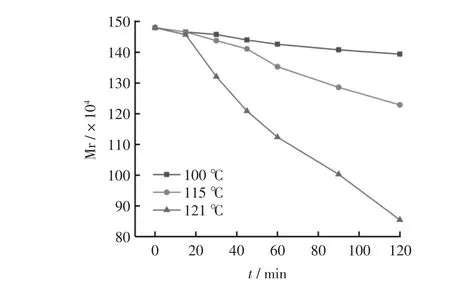
图1 SH 在100 ℃、115 ℃、121 ℃下Mr 随时间变化趋势图Fig.1 Trend graph of Mr of SH changed with time at 100 ℃,115 ℃and 121 ℃
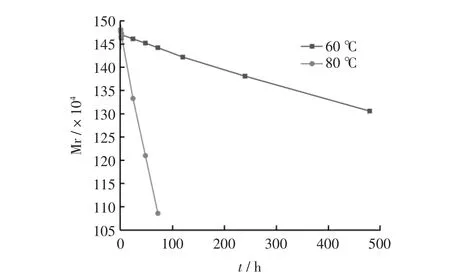
图2 SH 在60 ℃、80 ℃下Mr 随时间变化趋势图Fig. 2 Trend graph of Mr of SH changed with time at 60 ℃and 80 ℃
2.1.2 透明质酸钠的对数相对分子质量与时间和温度关系
将SH 的lnMr 与时间(t)做线性拟合,其具有较高的相关性,说明SH 的热降解属于一级动力学;图3是SH 在60 ℃、80 ℃下lnMr-t 的线性拟合图, 图4是SH 在100 ℃、115 ℃、121 ℃下lnMr-t 的线性拟合图。

图3 SH 在60 ℃、80 ℃下lnMr-t 的线性拟合图Fig.3 Linear fitting plot of lnMr-t of SH at 60 ℃and 80 ℃
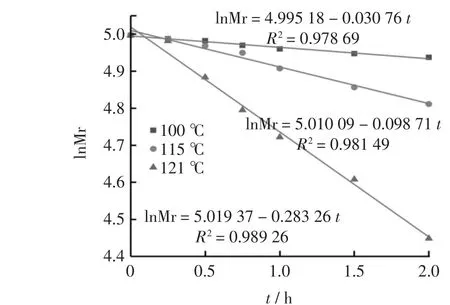
图4 SH 在100 ℃、115 ℃、121 ℃下lnMr-t 的线性拟合图Fig.4 Linear fitting plot of lnMr-t at 100 ℃,115 ℃and 121 ℃
2.1.3 透明质酸钠在不同温度的降解常数与温度关系
SH 在60 ℃、80 ℃、100 ℃、115 ℃和121 ℃的降解常数与温度关系见表1, 根据阿伦尼乌斯(Arrhenius)动力学方程式(4)做lnk-1/T×1000 的线性拟合(图5)。根据线性拟合得到的斜率计算,得到SH 的热降解活化能Ea=120.012 kJ/mol,SH 热降解动力学方程式为lnk=lnA-120.012/RT。 笔者实验的SH 热降解活化能与文献报道基本一致,董科云等[23]研究的SH 热稳定性降解活化能为116 ~118 kJ/mol,Tømmeraas K 等[22]研究的在浓度0.1 mol/L HCl 中SH 降解活化能为137 kJ/mol,Caspersen MB 等[24]在pH值中性条件下SH 降解活化能为127 kJ/mol。
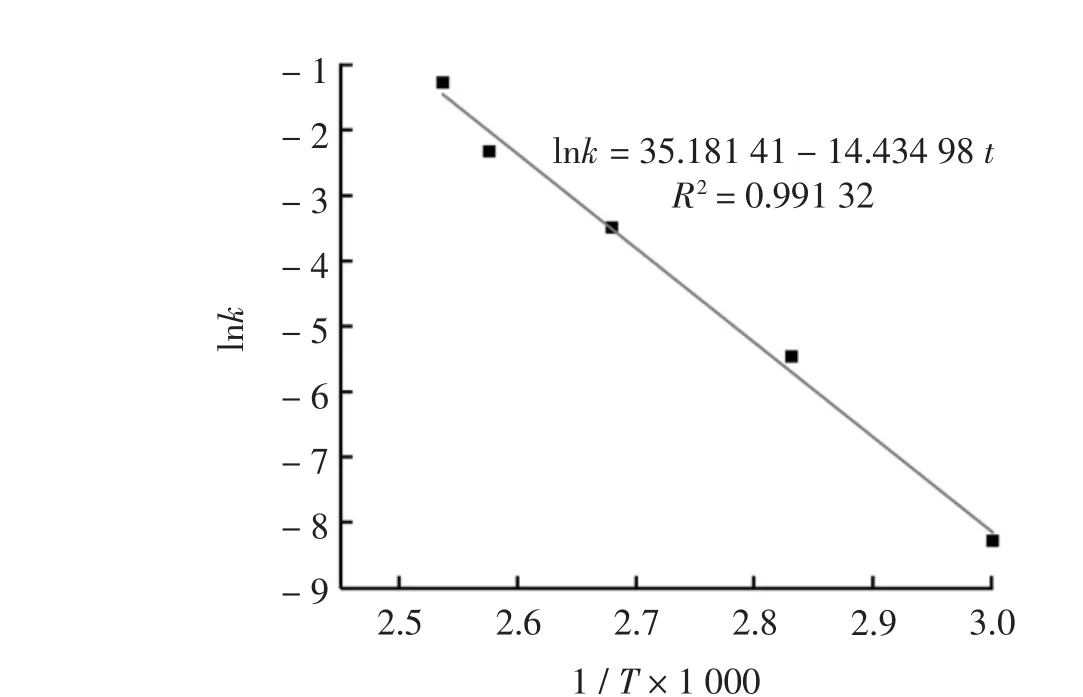
图5 SH 的lnk-1/T×1000 线性拟合图Fig.5 Linear fitting plot of lnk-1/T×1000 of SH
2.2 121 ℃灭菌后透明质酸钠的稳定性
根据阿伦尼乌斯(Arrhenius)理论计算得到了SH热降解动力学方程式,这样就可以推算出SH 在不同温度下的稳定性,但根据中国药品监督管理局法规要求,用于注射用的药品、医疗器械尽可能地进行终端灭菌。 经过121 ℃高温灭菌后SH 稳定性如何,是否与该热降解动力学模型一致。 为此,进行了121 ℃高温作用后SH 的稳定性研究。
SH 注射液经121 ℃、F0=8 min 灭菌后,在25 ℃、40 ℃、50 ℃和60 ℃进行稳定性考察, 考察SH Mr 的变化。 50 ℃和60 ℃,进行lnMr-t 的线性拟合(图6),其相关系数(R2)分别是0.80870、0.99016,60 ℃具有较好的相关性,属于一级反应动力学,而50 ℃条件下其线性相关性较差。 表明高温作用后的SH 在50 ℃条件下的稳定性,其热降解不属于一级动力学。 40 ℃稳定性考察的lnMr-t 的线性拟合(图7),其R2是0.84761,相关性较差;将Mr 与t 关系按照ExpDec1模型进行非线性拟合(图8),R2=0.98016,具有较好的相关性, 说明高温作用后SH 在40 ℃条件下降解也不属于一级动力学。 经高温灭菌和未灭菌的SH 在25 ℃稳定性考察,进行lnMr-t 线性拟合(图9),其R2分别是0.32102 和0.98985。 结果表明,未经高温作用的SH 在25 ℃条件下的lnMr-t 线性良好(R2=0.98985),其热降解属于一级动力学。 而高温作用后SH 在25 ℃条件下的lnMr-t 相关性较差(R2=0.32102), 将其Mr 与t 按照ExpDec2 模型进行非线性拟合(图10), 拟合结果为R2=0.99331,具有很好的相关性, 说明经高温作用后SH 在25 ℃条件下的降解也不属于一级动力学。
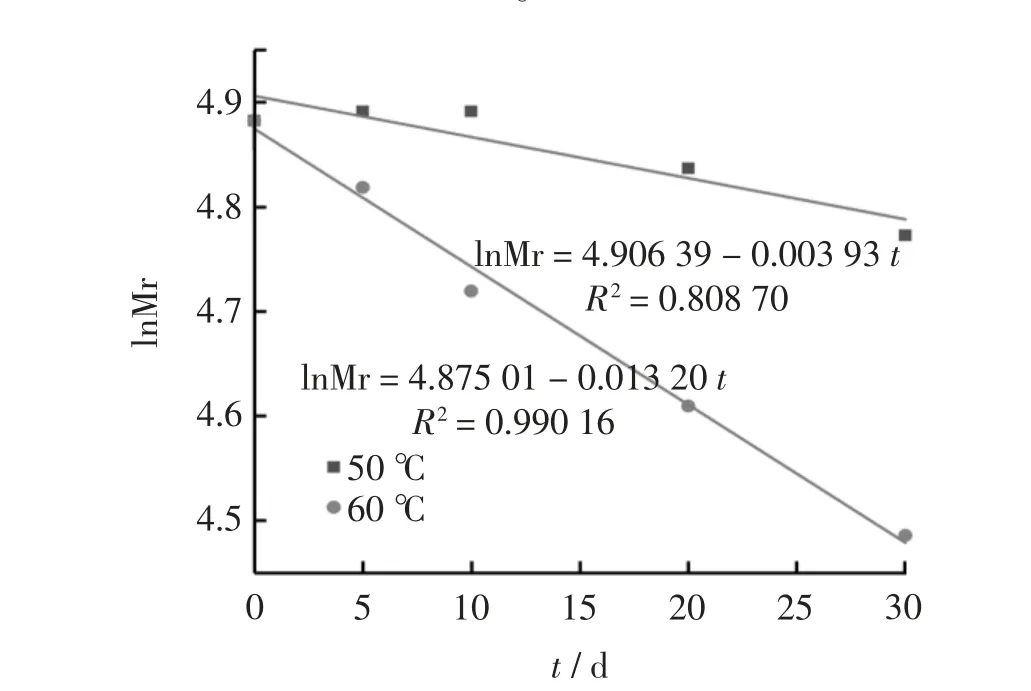
图6 灭菌后SH 在50 ℃、60 ℃条件下lnMr-t 的线性拟合图Fig.6 Linear fitting plot of lnMr-t of SH at 50 ℃and 60 ℃after sterilization
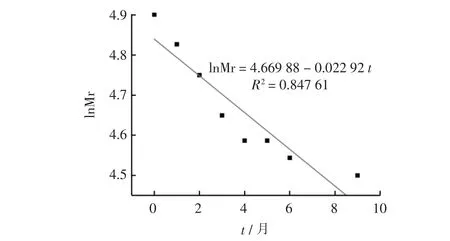
图7 灭菌后SH 在40 ℃条件下lnMr-t 的线性拟合图Fig. 7 Linear fitting plot of lnMr-t of SH at 40 ℃after sterilization
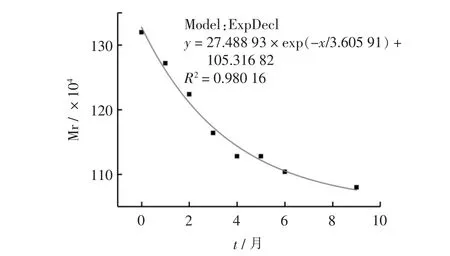
图8 高温灭菌后SH 在40 ℃条件下Mr-t 的曲线拟合图Fig. 8 Curve fitting plot of Mr-t of SH at 40 ℃after high-temperature sterilization
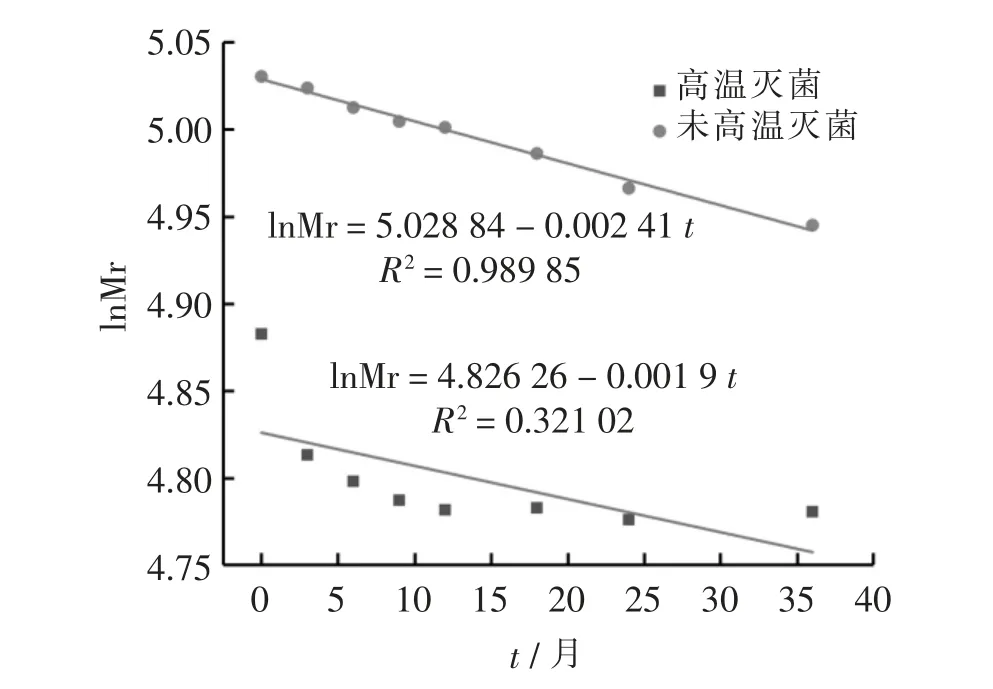
图9 高温灭菌后和未灭菌的SH 在25 ℃条件下lnMr-t 的线性拟合图Fig. 9 Linear fitting plot of lnMr-t at 25 ℃for SH after hightemperature sterilization and non-sterilization
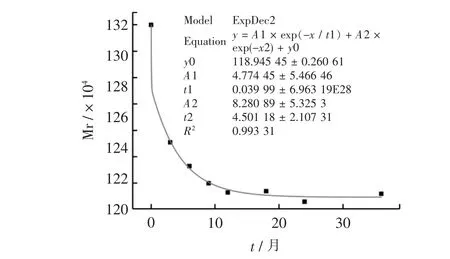
图10 高温灭菌后SH 在25 ℃条件下Mr-t 的曲线拟合图Fig.10 Curve fitting plot of Mr-t of SH at 25 ℃after high-temperature sterilization
3 讨论
已有多篇文献报道了SH 的热稳定性研究,但至今未检索到SH 经过高温灭菌(121 ℃)后其稳定性变化的研究。 笔者通过SH 高温灭菌后不同温度条件下稳定性的研究,结合文献分析其热稳定性变化的可能内在原因,为SH 的生产、研究提供理论指导。
在60 ℃、80 ℃、100 ℃、115 ℃和121 ℃下SH Mr的lnMr 与t 的线性拟合R2分别是0.98877、0.99976、0.97869、0.98149 和0.98926,均具有较好的相关性,属于一级降解动力学,其热降解活化能Ea =120.012 kJ/mol,与文献报道基本一致。
经高温灭菌后(121 ℃),SH 在25 ℃、40 ℃、50 ℃和60 ℃下Mr 的lnMr 与t 的线性拟合相关系数(R2)分别是0.32102、0.84761、0.8087 和0.99016,除60 ℃具有较好的线性相关性,属于一级降解动力学,其他25 ℃、40 ℃、50 ℃下其线性相关性都较差,不符合一级动力学, 而未经过高温作用的SH 在25 ℃稳定性的线性R2是0.98985,具有较好的相关性,其降解属于一级动力学。 从上可以看出, 经高温作用后,SH 的热稳定性动力学发生了变化。
已有大量文献报道,SH 结构中存在大量羟基,SH 中可以形成许多氢键, 氢键对SH 的稳定性起到关键作用。Scott JE、Tigwell MJ[10]研究表明,在室温下,SH 很稳定,即使使用高碘酸氧化,其降解也很慢;在37 ℃时,SH 的构象发生改变, 其氢键处于可能过渡态状态,可能空间位阻效应和过渡态能量都对抗性糖胺聚糖的氧化起作用,SH 中的氢键活化能大约为8.4 ~12.6 kJ/mol,SH 的氧化之前需要先破坏聚合物乙二醇基中羟基的氢键, 多篇文献表明[12,25,26],SH 在溶液中发生可逆构象转变。笔者实验及多篇文献[22,23,27]都表明,50 ℃时Mr 下降不明显;>60 ℃时,SH 的分解速率随温度呈指数增长。 这可能是SH 的氢键作用,在>60 ℃时,其氢键被打开,SH 的稳定性很差;在<60 ℃、>37 ℃时,SH 的构象发生改变,其氢键处于可能过渡态状态;<37 ℃时, 由于氢键作用,SH 很稳定;SH 在溶液中,随着温度的变化,其氢键(断开-耦合)、构象,会发生可逆转变。
经过高温灭菌后的SH 在60 ℃以上的条件下,其打开的氢键可能很难再恢复,其稳定性主要受到了60 ℃的环境因素影响,降解很快,其稳定性的lnMr-t线性拟合的R2达到0.99016,具有很好的相关性,降解仍然属于一级动力学。 而当低于60 ℃后,SH 的氢键、构象具有可逆转变的特点,其氢键可能会逐步恢复,氢键处于过渡状态,加上稳定性的环境温度等多重因素影响, 在早期其降解速度也较快,4 ~6 个月后,被打开的氢键逐步恢复,其相对分子质量下降也逐步变慢;因为这些多重因素的影响,其降解不符合一级动力学。 另外,未经过高温作用的SH 在25 ℃稳定性考察中,由于其氢键未经高温断开,其稳定性的lnMr-t 线性拟合的R2是0.98985, 具有较好的相关性,其降解很慢,也属于一级动力学;从另外一个维度可能也说明,由于高温对其氢键的作用,经高温作用后的SH 稳定性与未经过高温作用的SH 不一样。 因此,高温作用后的SH 稳定性,在>60 ℃仍符合一级降解动力学机制;<60 ℃的稳定性, 可能由于氢键处于过渡态, 其早期降解速度也较快,4 ~6 个月后,被打开的氢键可能逐步恢复, 其Mr 下降也逐步变慢,因为多重因素的影响,其降解不属于一级动力学。 至于经高温作用后SH 热稳定性动力学变化的真正内在原因还需要进一步研究证实。
经高温作用后SH 热稳定性动力学发生变化的发现,这对SH 制备、研究有一定的指导意义。 在进行SH 的生产时,为了减少SH 的降解,尽量在<60 ℃的条件下进行,最好在<37 ℃下制备;进行SH 注射液仿制药研究时(法规要求高温湿热灭菌),由于从市场上购买的参比制剂(高温湿热灭菌)一般都是在生产日期后6 个月以上的,其Mr 已经快速下降,因此购买的参比制剂不能从0 d 开始进行稳定性考察,也无法做到从生产日期开始就进行对比研究,因此只能从参比制剂生产日期开始后相对应的月份进行稳定性对比研究。
4 结论
SH 的热降解属于一级动力学机制, 不同温度的降解常数也符合阿伦尼乌斯(Arrhenius)反应动力学定律,SH 的热降解活化能Ea=120.012 kJ/mol, 与文献报道基本一致。
高温作用后的SH 稳定性,在>60 ℃属于一级降解动力学;但<60 ℃时,SH 的初始降解速度也较快,4 ~6 个月后,其Mr 下降逐步变慢,其降解不属于一级动力学。
高温作用后的SH 热稳定性动力学变化, 对其SH 制备、研究具有一定指导意义。 在进行SH 的生产时,尽量在<60 ℃条件下进行,最好在<37 ℃下制备。进行SH 注射液等仿制药研究时,只能从参比制剂生产日期开始后相对应的月份进行稳定性对比研究。

