年轻老年帕金森病病人认知障碍的影响因素及其预测模型构建
崔晓芳,路 筱,余红梅*,韩红娟
1.山西医科大学公共卫生学院,重大疾病风险评估山西省重点实验室,煤炭环境致病与防治教育部重点实验室,山西 030001;2.山西医学期刊社有限责任公司
帕金森病(Parkinson's disease,PD)是一种进行性神经退行性疾病,是第二常见的神经退行性疾病,影响2%~3%的65 岁以上人口[1-2]。随着对疾病认识的不断加深,PD 的临床诊断标准不断更新[3-4]。在更新的诊断指南中引入了非运动症状(NMS)和前驱症状的概念[5],认知障碍(cognitive impairment,CI)即属于非运动症状中的一种,表现为认知速度迟缓、抽象思维受损和推理困难。认知障碍可能在PD 不同阶段发生[6],严重影响病人的生活质量和功能,增加照顾者负担和健康相关费用[2]。认知障碍根据程度可分为轻度认知障 碍(mild cognitive impairment,MCI)和帕金森病痴呆(Parkinson's disease dementia,PDD)。MCI 的概念来自阿尔茨海默病的研究,被认为是正常衰老和痴呆之间的过渡阶段[7-8]。Yarnall 等[9]应用不同的认知测试截断标准,发现PD 病人的MCI 患病率不同,在低于1.0、1.5、2.0 个标准差下,PD 病人MCI 患病率分别为65.8%、42.5%和22.4%。此外,有研究显示,与年龄匹配的对照组相比,PD 病人发生MCI 和PDD 的风险几乎增加了6 倍[2]。因此,早期识别PD 病人认知障碍并及早给予针对性的干预至关重要。在临床实践中发现,部分PD 病人在疾病诊断时已经发生MCI,提示PD 病人的认知障碍等非运动症状可能先于运动症状出现[10],故挖掘早期可识别病人认知障碍的指标对减缓甚至逆转PD 病人认知障碍具有重要的临床意义。国外有学者提出,应考虑PD 病人MCI 前期阶段(pre-PD-MCI)的概念[11]。一项荟萃分析显示,PD 病人的年龄、运动症状总体严重程度、言语障碍、发病年龄、教育水平、抑郁症和性别等因素与MCI 或PDD 的发展独立相关[12]。但该研究未对PD 病人的年龄进行细分,而年龄是影响老年人各项生理功能和心理功能变化的重要变量之一。将老年人视为一个同质群体,忽略了老年人群体中存在的差异[13],通过细分与老年人年龄相关的各种特征,有利于为老年人制定更具针对性的干预策略和相关政策。一般来说,老年人分为年轻老年人(60~<75 岁)和年长老年人(≥75 岁)。且已有研究表明,年轻老年人和年长老年人的生活和经历不同[14-15],故推测不同年龄PD 病人的病程进展及各种运动症状和非运动症状表现和影响存在差异。本研究以年轻老年PD 病人为研究对象,探讨年轻老年PD病人认知功能的相关影响因素,并尝试利用这些相关因素构建预测模型,旨在为早期识别年轻老年PD 病人认知障碍并进行针对性的干预提供参考。
1 对象与方法
1.1 研究对象
所有受试者均来自帕金森病进展标志物倡议(The Parkinson Progression Marker Initiative,PPMI)数据库(http://www.ppmi-info.org),该数据库自2010年开始持续收集数据。根据PPMI 协议,所有研究程序都得到了参与者所属当地机构审查委员会批准,所有参与者在加入研究前都签署了书面知情同意书[16]。本研究共纳入164例PD 病人。纳入标准:1)完成第5年蒙特利尔认知评估量表(Montreal Cognitive Assessment,MoCA)随访,随访数据完整;2)首次疾病诊断即为特发性PD;3)年龄60~<75 岁。
1.2 资料收集
1.2.1 一般资料
包括性别、家族史、年龄、受教育年限、首发症状年龄、病程。
1.2.2 认知功能
采用MoCA进行评估。MoCA由Nasreddine根据临床经验并参考简易精神状态评价量表(MMSE)中的认知项目编制而成,是一个用于对认知功能异常进行快速筛查的评定工具,包括注意与集中、执行功能、记忆、语言、视结构技能、抽象思维、计算和定向力8 个认知领域,测试时间较短,总分为0~30 分。以26 分为截断值,即≥26 分为认知功能正常,<26 分为有认知障碍。量表灵敏度为90%,特异度为75%[17-19]。
1.2.3 日常生活活动能力
采用国际帕金森和运动障碍协会统一帕金森病评定量表第2部分(MDS-UPDRSⅡ)进行评定。MDS-UPDRSⅡ共13 个项目,总分为0~52 分,得分越高提示病人日常生活活动能力越差[20]。MDS-UPDRSⅡ在PD 病人中具有良好的可靠性和有效性,是监测疾病进展的良好工具。国际帕金森和运动障碍协会统一帕金森病评定量表第1部分(MDS-UPDRSⅠ)侧重非运动方面,MDS-UPDRSⅡ侧重运动方面,本研究考虑到MDS-UPDRSⅠ存在与认知功能相关的测评,为避免干扰,故将MDS-UPDRSⅠ也纳入分析。
1.2.4 运动功能
采用国际帕金森和运动障碍协会统一帕金森病评定量表第3 部分(MDS-UPDRS Ⅲ)评估PD 病人的运动功能。MDS-UPDRS Ⅲ包括18 个大项和33 个小项,用于评估PD 病人的运动迟缓、震颤和强直、冻结步态等。采用5 级评分,其中0 分表示正常,1 分表示轻微,2 分表示轻度,3 分表示中度,4 分表示重度,满分132 分,得分越高提示病人运动功能障碍越严重[21]。
1.2.5 焦虑
采用状态特质焦虑量表(STAI)评定。STAI 于1970 年出版,1983 年修订,由状态焦虑量表(S-AI)和特质焦虑量表(T-AI)2 个分量表组成,S-AI 表用于评估焦虑,T-AI 表用于评估焦虑倾向,T-AI 和S-AI 各有20 个项目,总分均为20~80 分,得分越高提示焦虑程度越严重[22-23]。
1.2.6 抑郁
采用老年抑郁症量表-15(GDS-15)评定。GDS-15排除了与抑郁症躯体症状相关的项目,且是一维量表[24],在临床评估中具有较好的可靠性和有效性[25]。总分0~15 分,得分5~<10 分为轻度抑郁症,得分≥10 分为中度至重度抑郁症[26]。
1.3 统计学方法
采用SPSS 25.0 和R 4.2.1 处理数据。除MoCA评分外,其他指标均有缺失数据,缺失数据采用多重插补法进行数据填充。数据中符合正态分布的定量资料采用均数±标准差(±s)表示,两组比较采用独立样本t检验,多组比较采用方差分析;不符合正态分布的定量资料采用中位数(四分位数间距)[M(IQR)]表示,两组比较采用秩和检验;定性资料采用例数、百分比(%)表示,两组或多组比较采用χ2检验;将单因素分析中有统计学意义的变量纳入Liogistic 回归分析,以受试者工作特征(ROC)曲线下面积、Hosmer-Lemeshow检验评价模型的预测能力,并基于多变量模型构建预测列线图,使用校准图进行模型内部验证。本研究采用双侧检验,以P<0.05 为差异有统计学意义。
2 结果
2.1 PD 病人认知障碍影响因素的单因素分析
根据MoCA 评分将164 例病人分为认知正常(PD-NC,≥26 分)组和认知下降(PD-CI,<26 分)组,其中PD-NC组101例,PD-CI组63例,认知障碍发生率为38.4%。单因素分析结果显示,两组病人年龄、受教育年限、首发症状年龄以及MDS-UPDRSⅡ、MDS-UPDRSⅢ、GDS-15、S-AI、T-AI、STAI、MoCA 评分等比较,差异均有统计学意义(P<0.05)。见表1。
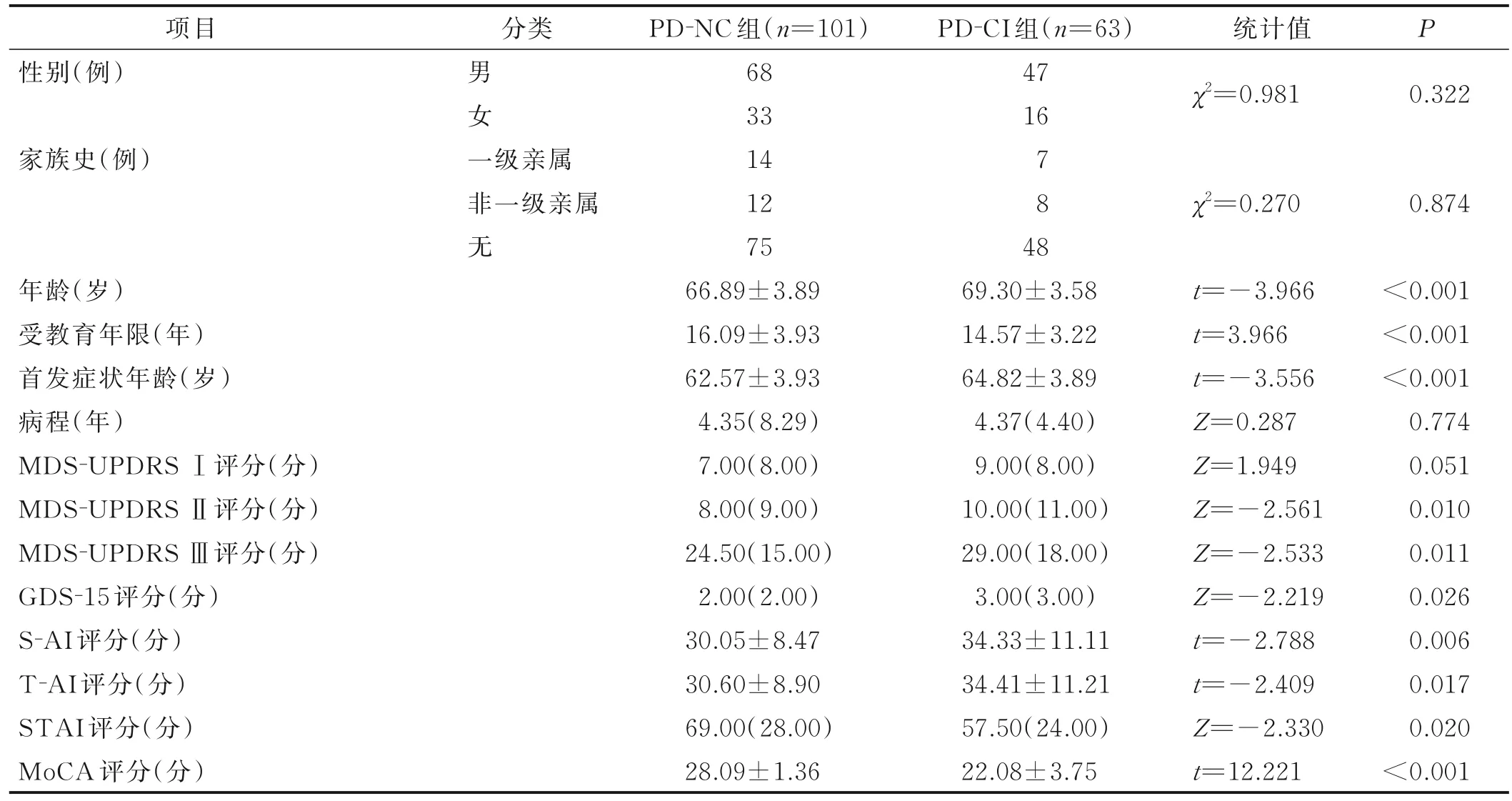
表1 PD 病人认知障碍影响因素的单因素分析
2.2 PD 病人认知障碍影响因素的多因素分析
将单因素分析中有统计学意义的因素(年龄、受教育年限、首发症状年龄以及MDS-UPDRSⅡ、MDS-UPDRSⅢ、GDS-15、S-AI、T-AI、STAI 评分)作为自变量,将病人认知功能分组作为因变量(PD-NC=0,PD-CI=1)进行Logistic回归分析。自变量均以原值代入。结果显示,年龄、受教育年限和MDS-UPDRSⅡ评分、MDS-UPDRSⅢ评分进入回归方程。回归分析结果见表2。
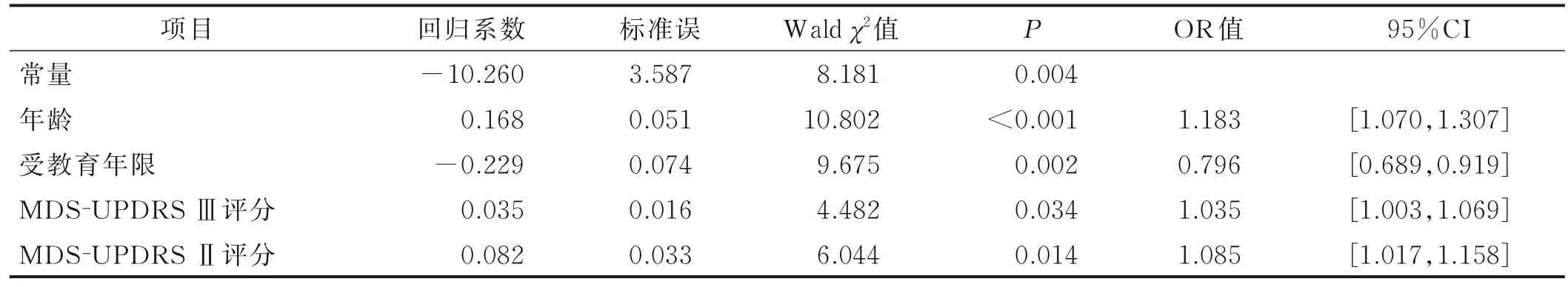
表2 影响PD 病人认知功能的Logistic 回归分析
2.3 PD 病人认知障碍预测模型及列线图
采用影响PD 病人认知障碍的因素构建风险预测模型,Logit(P)=-10.260+0.168×年龄-0.229×受教 育 年 限+0.035×MDS-UPDRS Ⅲ评 分+0.082×MDS-UPDRSⅡ评分。
构建的预测模型ROC 曲线下面积为0.815,表明模型预测能力尚可,见图1。此外,绘制校准曲线进行列线图模型的内部验证,校正曲线接近理想曲线,见图2。Hosmer-Lemeshow拟合优度检验显示,χ2=8.550(P=0.355),表明列线图模型与实际风险具有较好的一致性。

图1 PD 病人认知功能预测模型的ROC 曲线

图2 PD 病人认知功能预测模型的校准曲线
3 讨论
3.1 一般资料
本研究结果显示,年龄是PD 病人认知功能的影响因素[OR=1.183,95%CI(1.070,1.307)],即年龄的增加会导致老年人认知能力下降,与以往对老年人认知功能影响因素的研究结果[12,27]一致。此外,受教育年限较长是PD 病人认知功能的保护因素[OR=0.796,95%CI(0.689,0.919)],此研究结果与目前研究结果[12,28]一致。但已有证据表明,教育水平对认知的影响并不是唯一的[29]。一项研究显示,较低和较高的教育水平均会导致老年人认知功能受损,即较高的教育水平并不能防止老年人认知能力下降,教育水平与认知变化的风险密切相关[30],但该研究针对的是中国老年人,非PD 病人,关于PD 病人受教育年限与认知功能之间是否也存在相似的关系还有待进一步研究。
3.2 日常生活活动能力
多因素分析结果显示,MDS-UPDRSⅡ评分进入回归模型,是PD 病人认知功能的影响因素。MDS-UPDRSⅡ主要用于测量PD 病人运动方面的日常生活活动能力,已有研究表明,MDS-UPDRSⅡ可有效评价PD 病人的日常生活活动能力[31]。本研究结果显示,MDS-UPDRSⅡ评分越高,认知功能受损风险越大[OR=1.085,95%CI(1.107,1.158)]。日常生活能力又分为基本日常生活能力(BADL)和工具性日常生活能力(IADL)。基本日常生活能力包括进食、洗澡、梳洗、排便、如厕、移动、爬楼梯等。工具性日常生活能力涉及对认知功能要求更高的任务[32-34],包括使用电话购物、做饭、做家务、乘坐公共交通工具外出、服药、理财、梳洗、使用家用电器、锁门、约会、谈论最近发生的事、爱好和休闲活动等。在临床中,部分PD 病人在PD 诊断时已经经历认知功能受损,即病人可能具备基本的生活自理能力,但工具性日常生活能力已经受损。一项以意大利老年人为研究对象的大型人群研究描述了痴呆症的8 年发病率,单因素分析结果显示,日常生活活动、工具性日常生活能力在总样本、认知正常的受试者和MCI 受试者中均显示出对痴呆的预测作用。此外,在多变量分析中,IADL 是总样本和MCI受试者向痴呆转变的最有力预测因子[35]。还有研究显示,PD 病人认知功能与日常生活能力受损有关,认知和日常生活能力之间的联系在很大程度上取决于IADL,但与BADL 受损相关性不显著。认知正常的病人整体日常生活能力与认知之间的相关性无统计学意义,但认知与IADL 之间的相关性显著,提示可能需要敏感的认知评估措施识别相关的认知障碍[36]。PPMI 数据库中采用国际帕金森和运动障碍协会统一帕金森病评定量表(MDS-UPDRS)对PD 病人日常生活活动能力进行测评,MDS-UPDRSⅠ侧重非运动方面,MDS-UPDRSⅡ侧重运动方面,为避免干扰,本研究将MDS-UPDRSⅠ也纳入分析。但MDS-UPDRS未对BADL 和IADL 进行区分,这可能对早期识别PD病人认知障碍造成影响。此外,现有研究多为PD 病人认知障碍对日常生活能力的影响研究,关于日常生活能力对认知功能的影响研究较少。当病人认知障碍出现时会削弱其日常生活能力,两者可能相互影响。考虑到大多数PD 病人可能存在难以识别的认知障碍,而目前医护人员对PD 病人轻度认知障碍对日常生活能力的影响重视不足,可能是由于人们认为除了痴呆之外的认知障碍不会对日常生活产生实质性影响。但随着PD 进展,发生PDD 的风险增加,高达80%的病人在最初诊断的15~20 年发生PDD,提示对认知障碍的早期干预很有必要。因此,未来研究可深入探讨日常生活能力对PD 病人认知功能的影响及其机制,并可在现有日常生活能力评估工具基础上区分BADL 和IADL,甚至可进一步明确认知相关的IADL,为早期识别PD 病人认知障碍提供方法,为早期干预奠定基础。
3.3 运动功能
Logistic回归分析显示,MDS-UPDRSⅢ评分进入回归模型,是PD病人认知功能的影响因素,即MDS-UPDRSⅢ评分越高,认知功能受损的风险越大[OR=1.035,95%CI(1.003,1.069)]。MDS-UPDRS Ⅲ主 要 用 于 对PD 病人的运动检查,包括姿势稳定性、震颤、手部和腿部动作的灵活性、冻结步态等条目。多项研究表明,痴呆症和PD 与体力活动减少有关,这甚至在诊断前几年就有所显示[37-38]。有研究使用活动记录器对586 例PD 病人进行研究,探讨MMSE 评分与能量消耗之间的关系,结果显示两者存在相关性[39]。还有研究显示,与认知功能正常的PD 病人相比,发生MCI 的PD 病人冻结步态发生率更高[40],PDD 病人具有更长时间的久坐行为,较不活跃的身体行为与评估视觉结构、注意力和执行功能的测试得分较低有关,但与语言流利性、记忆力和语言表现无关,这表明身体行为特征可以部分反映认知恶化[41],提示运动评估在进一步理解、筛查、诊断、预测和监测PD 病人认知障碍方面具有潜力。已有研究显示,总体认知功能及执行力、注意力和定向功能减退可能增加中老年人PD 前驱期检出概率[42],提示应早期关注PD 认知功能和运动症状及其关系,将对PD 病人认知障碍的干预关口前移。
4 不足之处
1)认知评估不准确。2012 年,国际帕金森病和运动障碍学会在推荐的对PD 病人认知功能的诊断标准中提到,PD 病人认知功能的诊断除需进行有限的神经心理测试外,还应至少有两项测验评分低于正常对照组平均值1.5 个标准差[43]。本研究根据对认知功能进行综合评估的MoCA 评分结果对PD 病人认知功能进行判定,存在一定局限性,今后研究可联合区域认知状态评估量表,如霍普金斯词语学习测验修订版 (HVLT-R)、语义流畅性测试(SF)、数字字母排序测试 (LNS)对PD病人认知功能进行更准确评估。2)样本量有限,可能影响结果的准确性。本研究仅以年轻老年PD 病人为研究对象,纳入的样本量较少,可能遗漏影响认知功能的因素。如本研究也将抑郁对PD 病人认知功能的影响纳入分析,虽然在单因素分析时,PD-NC 组和PC-CI组抑郁得分差异有统计学意义,但抑郁并未进入回归模型,这与以往研究结果[36]不一致。已有研究表明,抑郁症状对PD 病人认知功能有影响,抑郁症状预示着PD 病人未来的认知能力下降[36]。但也有对中年老年人认知功能发展特点及影响因素的大样本、纵向数据分析结果显示,老年人患有抑郁症时不太可能出现认知功能下降[44]。因此,抑郁对老年人认知功能的影响、在不同疾病老年人中抑郁对认知功能的影响是否存在差异需进一步研究。3)模型未验证。考虑到本研究纳入的样本量偏小,本研究未对病例进行建模组和验证组的拆分,虽然建立了比较简易的预测模型且结果显示模型尚可,但并未验证该模型在不同特征PD 病人中的有效性和可行性,下一步研究可尝试将构建的预测模型应用于临床,以验证模型的准确性。

