格隆溴铵立体异构体杂质的毛细管电泳测定
——推荐一个药物分析实验
李凤,孟然然,张含智,屈颖娟,康经武,*
1 西安文理学院化学工程学院,西安市食品安全检测与风险评估重点实验室,西安 710065
2 中国科学院上海有机化学研究所,生命过程小分子调控重点实验室,上海 200032
3 弈柯莱生物科技(上海)股份有限公司,上海 200241
手性是自然界的基本属性之一。目前上市的药物中,56%的药物含有手性中心,其中88%的手性药物是以外消旋物(racemate)的形式存在的。尽管手性药物对映体具有相同的物理化学性质,但它们在药理、毒理学、药效学、药代动力学方面却有着明显的差异。因此与外消旋体的药物相比,单一构型的手性药物在疗效和安全性方面更有优势[1]。如20世纪50年代著名的反应停事件,(R)-构型沙利度胺具有镇静及止吐作用能够有效减缓妊娠反应;而(S)-构型对映体却有较强的致畸作用。21世纪初的“手性转换”政策极大地鼓励了制药公司发展单一手性药物。这一政策规定,原来按消旋体形式销售的手性药物如果发展成单一手性化合物,就可以按新药申报而重新获得专利保护期限[2]。随着单一构型的手性药物数量的不断攀升,为了提高手性药物的质量控制水平,发展用于手性药物的分析方法和技术具有十分重要的意义。
色谱技术是最主要的也是最重要的一类手性化合物的分析技术。在色谱技术中,高效液相色谱(HPLC)、气相色谱(GC)、超临界流体色谱(SFC)以及毛细管电泳(CE)是应用最多的几种技术[3–5]。HPLC技术应用比较普遍,方法通用性强、精确、灵敏、快速并且可重复性好,其主要缺点是色谱柱昂贵并且需要消耗大量的有机溶剂。毛细管电泳是一种与HPLC互补的手性分离技术,特别适合可电离的高极性手性化合物的分离分析。CE具有多种分离模式,包括毛细管区带电泳(CZE)、胶束电动色谱(MEKC)、非水相毛细管电泳(NACE)、毛细管等速电泳(ITP)、毛细管等点聚焦(IEF)等,大大扩大了毛细管电泳手性分离方法的适用范围[6–8]。相对于其他色谱技术,毛细管电泳突出的优点是样品需要量少(可以分析单细胞)、分离时间短及分离效率高。毛细管电泳在生物大分子、药物及其代谢物、阴/阳离子及手性化合物的分离等方面表现出独特的分离性能。20世纪备受关注的人类基因组计划能够提前完成,毛细管电泳技术做出了巨大的贡献。近年来,芯片毛细管电泳、毛细管电泳-质谱联用(CE-MS)等新技术的不断发展,使CE在生命科学、医药研究、天然产物及食品分析等领域仍有广泛的应用前景[9,10]。
本论文从药物分析实验的角度,介绍了毛细管电泳方法测定抗胆碱类药物格隆溴铵对映体的含量分析方法,侧重点在于介绍毛细管电泳分析方法及手性分离机理,以及将毛细管电泳技术应用于手性药物对映体分离分析的特点。
1 实验目的
熟悉毛细管电泳仪的工作原理及基本操作;了解不同类型环糊精的理化性质,及其作为手性选择剂实现手性分离的机理;掌握毛细管电泳用于药物格隆溴铵对映体分离的方法。
2 实验原理
手性化合物立体异构体的色谱分离需要采用手性选择剂作为手性固定相。与HPLC的手性固定相不同,毛细管电泳的手性分离是将手性选择剂加入到缓冲溶液中,使对映体与手性选择剂之间形成可逆的非对映的复合物,具有不同的电泳淌度从而实现分离。Stephen等曾提出一个理论模型来解释毛细管电泳中实现手性分离的原理[11]。一对对映异构体A、B与手性选择剂C之间可以存在以下两个动态的平衡:
其中,μ1、μ2、μA、μB分别为游离的异构体A、B以及异构体与手性选择剂C形成的复合物的电泳淌度。K1、K2分别为对映异构体A、B与手性选择剂C之间的结合常数。如果A、B与手性选择剂C形成的瞬时非对映异构体复合物稳定常数K1、K2不同,对映体自身的电泳淌度与形成复合物的淌度也不同,将会导致两个异构体的表观电泳淌度不同(如公式1、2)。其中非对映异构体之间的电泳淌度差越大,越易实现手性分离。
环糊精(cyclodextrin,CD)是一类超分子主客体化合物,也是毛细管电泳中常用的手性选择剂。它是由直链淀粉在芽孢杆菌产生的环糊精葡萄糖基转移酶作用下生成的一系列寡糖大环化合物[12,13]。通常CD含有6–12个D-吡喃葡萄糖单元,其中研究的较多的是含有6、7、8个葡萄糖单元的分子,分别称为α、β、γ-环糊精(图1)。环糊精的立体结构近似于去顶圆锥,具有疏水的空腔及亲水的外表面。其疏水的空腔可以与手性小分子或基团发生包结作用,从而实现手性分离。环糊精表面存在大量羟基,通过对这些羟基进行修饰可以得到不同类型的中性环糊精、负电环糊精以及正电环糊精。目前在手性分离中应用较多的环糊精衍生物,包括羟丙基修饰的β-CD(HP-β-CD)、硫酸化的环糊精、磺丁基修饰的环糊精等。
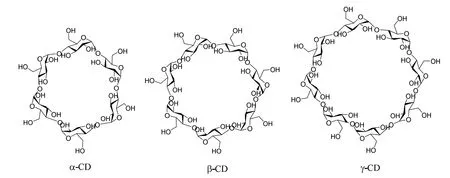
图1 α、β、γ-三种环糊精的结构图
格隆溴铵是一种季铵类抗胆碱药物,作为蕈毒碱受体M3拮抗剂,可以抑制乙酰胆碱与受体的相互作用[14,15]。它具有抑制胃液分泌及调节胃肠蠕动的作用,适用于胃及十二指肠溃疡、慢性胃炎、胃酸分泌过多等[16]。格隆溴铵的四级季铵盐结构可以限制其穿过血脑屏障,因此引起的副作用比非极性抗胆碱药如山莨菪碱、硫酸阿托品要小的多。格隆溴铵结构中具有两个手性中心,因此共存在4个立体异构体(图2)。目前在售的格隆溴铵药物为R,S-构型以及S,R-构型的混合物(优映体,有活性的异构体),因此其异构体杂质主要包括S,S-构型以及R,R-构型的异构体。
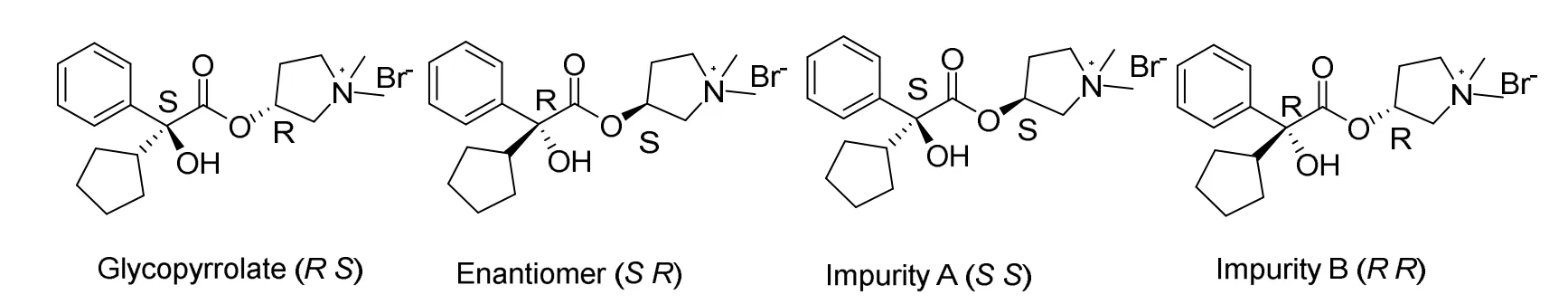
图2 格隆溴铵及其立体异构体的绝对构型
本实验中采用以硫酸化-β-环糊精(HS-β-CD)作为手性选择剂的毛细管电泳手性分析方法,实现了格隆溴铵四种立体异构体的高效分离。研究表明,手性毛细管电泳法是测定药物手性异构体杂质的有效方法。
3 实验部分
3.1 实验试剂
羟丙基-β-环糊精(HP-β-CD)、羟丙基-γ-环糊精(HP-γ-CD)、硫酸化-β-环糊精(HS-β-CD)以及硫酸化-γ-环糊精(HS-γ-CD)购于Fluka公司;γ-环糊精(γ-CD)、β-环糊精(β-CD)以及α-环糊精(α-CD)购于美国Sigma-Aldrich公司。格隆溴铵光学异构体由中国药品检验所提供,磷酸购于上海凌风化学试剂有限公司;氢氧化钠购于上海大合化学品试剂有限公司;磷酸氢二钠购于上海阿拉丁试剂有限公司。所用试剂除注明外均为分析纯。实验用水为超纯水。
3.2 实验仪器
P/ACE MDQ毛细管电泳仪(Beckman Coulter,CA,USA)配有PDA检测器,数据通过装有32 Karat Software的惠普计算机采集;熔融石英毛细管柱(50 μm×60 cm,有效长度49.5 cm,河北鑫诺科技有限公司)。
3.3 实验步骤
3.3.1 溶液的配制
电泳运行背景电解质溶液用时现配。背景电解质溶液为50 mmol∙L-1的磷酸氢二钠含40 mg∙mL-1的HS-β-CD,最终的pH由稀释的磷酸调至2.5。格隆溴铵用超纯水配制成1 mg∙mL-1的样品溶液。
3.3.2 毛细管电泳仪的操作
优化后的毛细管电泳仪的参数如下:进样方式采用压力进样,进样压力1.4 kPa×5 s;分离电压-12 kV(其中C、D、E以及F分离电压为12 kV);检测波长210 nm。新毛细管柱在30 psi压力条件下用0.1 mol∙L-1NaOH溶液处理30 min,再分别用超纯水、背景电解质冲洗5 min。每次运行间隔用0.1 mol∙L-1NaOH、超纯水、背景电解质各冲洗5 min。
4 结果与讨论
4.1 手性选择剂的比较
实验尝试了多种环糊精及其衍生物,包括5种中性的环糊精、2种带负电的环糊精HS-β-CD和HSγ-CD作为手性选择剂用于分离4个格隆溴铵立体异构体。发现只有HS-β-CD和HS-γ-CD可以使4个立体异构体实现完全的基线分离(图3)。虽然这两种环糊精具有相近的分离选择性,但是各异构体的出峰顺序不同。考虑到HS-γ-CD的价格远远高于HS-β-CD,在接下来的实验中我们选择了HS-β-CD作为手性选择剂,对毛细管电泳的分离条件进行了优化。
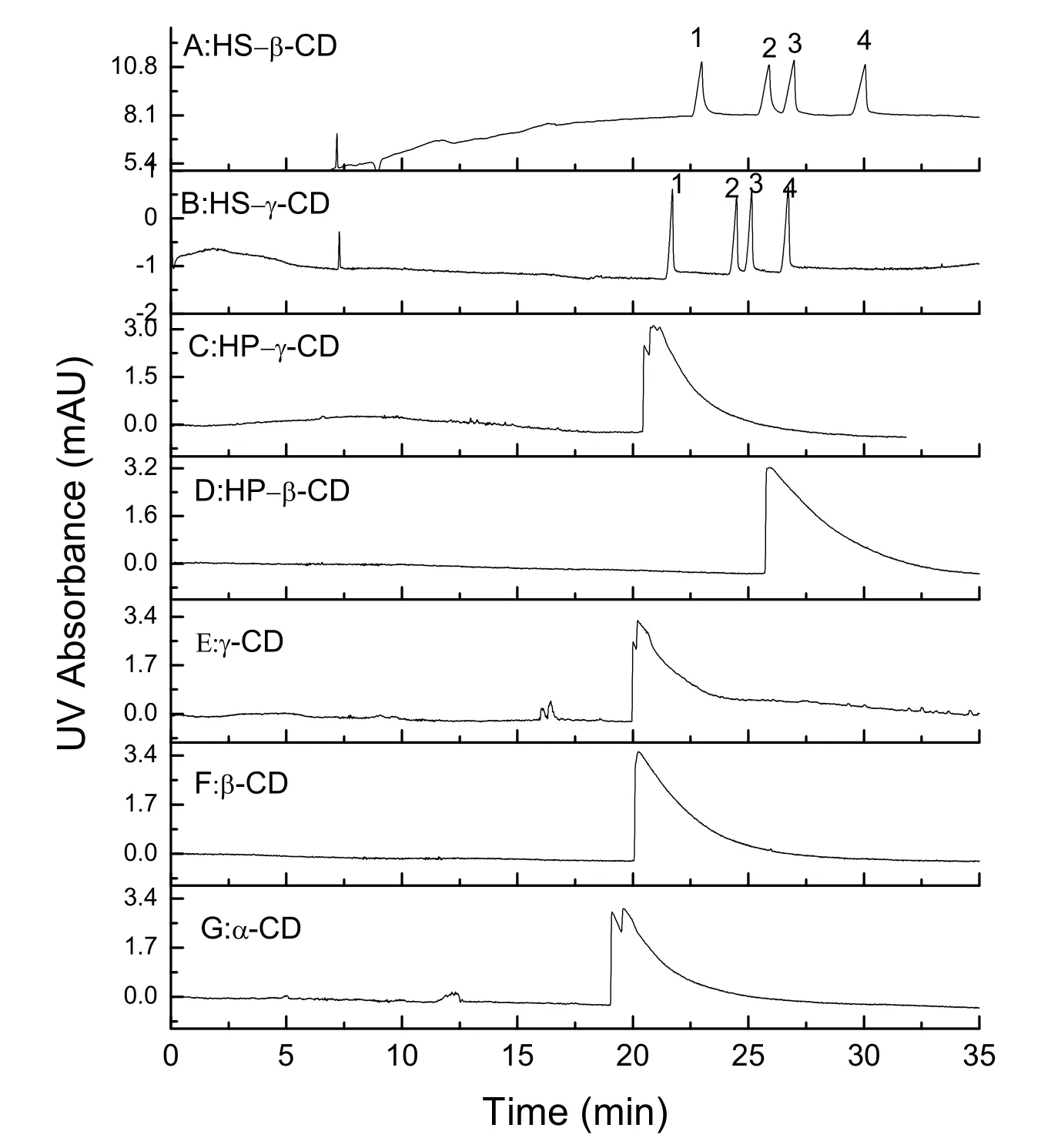
图3 不同类型环糊精作为手性选择剂时的分离选择性比较
4.2 毛细管电泳分离条件的优化
我们首先考察了手性选择剂HS-β-CD浓度对格隆溴铵异构体分离的影响。从图4中可以看出随着HS-β-CD浓度的增加,分离度逐渐提高,同时各异构体的迁移时间也相应缩短。由于HS-β-CD带有较多的负电荷,当它的浓度过大时会导致电流大大增加,使基线波动较大。因此,综合考虑分离度和分析时间的影响,我们选择最终环糊精的浓度为40 mg∙mL-1。接下来,我们对背景电解质缓冲盐磷酸氢二钠的浓度进行了优化。我们发现随磷酸氢二钠浓度的增加,分离度略有提高(图5)。但是当浓度增加时溶液的粘度也会增加,导致化合物的电泳淌度减小,迁移时间延长。因此,磷酸氢二钠的浓度也不宜过高。综合分析,选择最终磷酸氢二钠的浓度为50 mmol∙L-1。
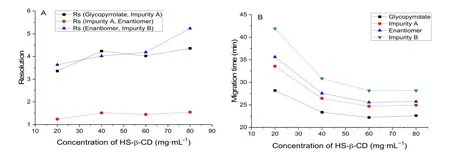
图4 环糊精浓度对分离度(A)和迁移时间(B)的影响
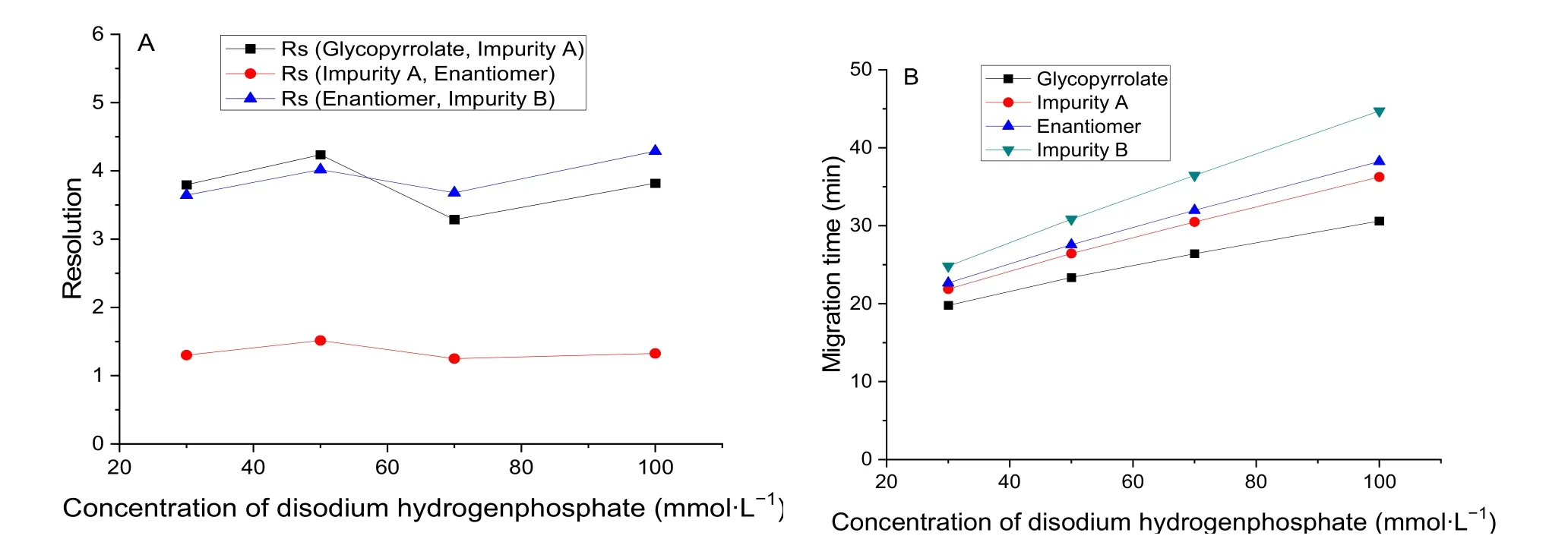
图5 磷酸氢二钠浓度对分离度(A)和迁移时间(B)的影响
背景电解质溶液的pH也是毛细管电泳分离中一个非常重要的参数,它不仅会影响溶液的电渗流,同时也会影响带电化合物的解离状态。如图6所示,当pH小于3.0时,无论各异构体的分离度还是迁移时间变化均不大;当pH超过3.0时,分离度就会显著降低同时迁移时间开始延长,因此最终我们选择pH为2.5。分离电压和柱温对分离的影响我们同样进行了考察。分离电压的增大会缩短迁移时间,然而电压增大而产生的焦耳热又会导致分离度的降低。同样,柱温的升高也会导致迁移时间的缩短以及焦耳热的产生进而影响基线噪声。并且当柱温过高时,手性化合物与环糊精的手性识别可能会受到影响,因而我们并不建议在过高的柱温下进行分离。

图6 缓冲溶液pH对分离度(A)和迁移时间(B)的影响
综合考虑分离度和迁移时间,我们选择-12 kV的分离电压和20 °C的柱温。经过优化后的毛细管电泳分离图如图7所示,可以看出各异构体完全实现了基线分离。实验条件:背景电解质为50 mmol∙L-1的磷酸氢二钠(调至pH 2.5)含40 mg∙mL-1的HS-β-CD;柱温20 °C,-12 kV的分离电压;检测波长210 nm;峰1:Glycopyrrolate(R,S),峰2:杂质A(S,S),峰3:Enantiomer(S,R),峰4:杂质B(R,R)
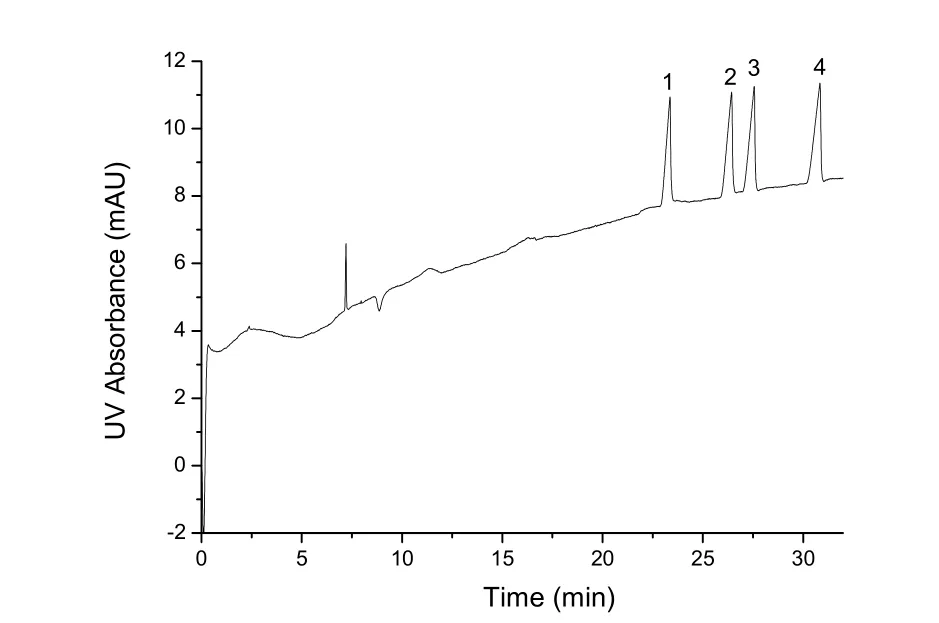
图7 格隆溴铵及其立体异构体的电泳分离图
4.3 毛细管电泳分离条件的验证
在优化的条件下,考察了该方法的线性范围、精密度、定量限以及检测限,实验结果见表1。方法的检测限为0.005 mg∙mL-1,定量限为0.015 mg∙mL-1,线性范围为0.015–2.0 mg∙mL-1。方法的精密度主要从峰面积以及迁移时间的重复性来考察。峰面积日内重复性6.92%–10.77%,日间重复性0.63%–11.69%。迁移时间日内重复性0.03%–0.16%,日间重复性1.60%–1.84%。该方法具有较好的重复性,能够满足日常药物分析的需要。

表1 方法确证数据
5 数据处理
5.1 记录毛细管电泳分离条件
包括:仪器型号、柱长、柱内径、进样方式、进样量、温度、分离电压、检测波长等。
5.2 定性分析
分别进样,记录色谱图,读取保留时间。
5.3 定量分析
采用归一化或标准曲线的方法。
6 注意事项
电极和毛细管柱不能接触,样品溶液的样品瓶与缓冲溶液的液面要保持平衡。每次分析前毛细管柱需要进行冲洗和平衡,温度的变化也会影响分离结果,这对于实验的可靠性和重现性特别重要。
7 实验组织
本实验共用时4–6 h,在平衡毛细管柱期间,可以穿插讲授和讨论药典四部通则中0542毛细管电泳法、学习毛细管电泳仪的使用方法以及配制标准溶液等。同时进行系统性试验的考察,学生分组计算和讨论重复性(相对标准偏差,RSD)、毛细管理论板数(n)、分离度(R)、拖尾因子(T)、线性范围、检测限(LOD)和定量限(LOQ)等。
实验开展过程中涉及到毛细管电泳仪的使用及手性分离技术,建议本实验向大学二年级下学期或三年级上学期的学生开设。该实验的考核内容由预习报告、课堂表现、实验操作和实验报告组成,各部分占比分别为20%、20%、30%和30%。
8 结语
药物分析是一门发展药物分析方法、研究药物质量规律的科学。而药品质量直接影响药品的安全性和有效性,与人类健康与生命安全密切相关。而以“反应停”事件为代表的手性药物安全越来受到重视,将本实验引入教学中,激发了学生的学习热情,启发学生思考,增强学生的专业责任感和认同感。同时,也提升了教学的学术深度,有助于培养学生的创新意识和综合实践能力。

