天然气藏中酸气H2S与CO2协同转化研究进展
于姗,张洪华,付梦瑶,段元刚,段超,黄靖元,唐春,黄泽皑,周莹
(1 油气藏地质及开发工程国家重点实验室,四川 成都 610500;2 西南石油大学新能源与材料学院,四川 成都 610500)
2021 年,中国原油对外依存度高达72%,天然气对外依存度达到46%。为保障国家能源安全,减少对国外油气资源的依赖度,迫切需要加大国内煤和油气等资源的开发力度。随着前期常规优质油气资源的枯竭,攻克非常规油气田开采中的关键技术以实现非常规油气田的绿色清洁开采和利用,是科学家们迫在眉睫的任务。酸性气藏是一种典型的非常规气藏,我国累计探明酸性气藏储量逾万亿立方米,开发潜力巨大。酸性气藏中除含有甲烷外,还有大量的酸性气体(主要为H2S 与CO2),由于H2S 与CO2的生成原因不同,其在不同环境的气藏中分布规律也有一定差异。以亚洲最大的整装海相气田普光气田为例,其H2S 与CO2气体的体积分数分别为15.2%和8.6%;而在四川元坝气田中,其H2S与CO2气体的体积分数则分别为5.2%和6.4%[1]。H2S 是剧毒气体,CO2是影响碳中和进程的关键温室气体,两者均会对社会和环境产生负面影响。因此,实现H2S 与CO2的有效转化处理对气田的低碳绿色开发至关重要。
现有气田开采过程中先通过脱硫脱碳工艺将气藏中的H2S与CO2与CH4等分离,然后将H2S与CO2通过克劳斯工艺送入高温燃烧炉(>1173K)和催化床,将H2S中的S资源转化为硫黄进行回收利用,反应过程能耗高,同时产生SOx毒副尾气[2]。此外,整个处理过程中CO2基本不参与反应,最后直接作为尾气排空处理。受限于高反应能耗以及大量的CO2排放,现有气田的H2S 与CO2处理工艺已经难以满足绿色低碳发展的需求。在双碳背景下,发展新型的H2S与CO2转化处理工艺已势在必行。
H2S是重要的氢源和硫源,CO2是重要的碳源,如果两者之间能协同转化,则可能得到一系列高值化学品,如氢气、合成气(H2和CO 的混合气)、硫黄和二硫化碳等,实现变废为宝、变害为利。从20 世纪80 年代,国内外的学者就开始致力于H2S与CO2协同转化的研究。早期的研究主要聚焦于热反应,随着其他技术的发展,21 世纪以来国内外的学者也开始将一些新型的催化技术应用于H2S与CO2协同转化的研究,包括光催化、电催化和等离子体催化等。本文将不同的催化技术进行分类,主要综述H2S 与CO2协同转化的相关研究进展,以期为H2S与CO2协同高值转化回收利用提供一些思路。
1 H2S与CO2协同转化热反应
1.1 发展历史
H2S 与CO2协同转化在热化学反应中的研究最为广泛,本文首先对热化学反应的发展历程进行总结并分析。1987 年,德国的Bülow 等[3]研究了在不同分子筛上H2S 与CO2生成COS 和H2O 的反应。该作者指出在300K时H2S与CO2的反应平衡常数非常低,仅为6.7×10-6,当H2S 与CO2的摩尔比为1∶4时,对应的H2S转化率仅为0.5%。但使用A型和X型分子筛时,H2S的转化率可以达到70%。该作者认为这是由分子筛对水的强吸附能力使得反应平衡移动所引起的。分子筛上的弱配位阳离子和碱性氧原子是反应的催化活性位点,可有效促进H2S的解离吸附,进而促进反应发生。此外,该作者认为在NaX 分子筛体系中,CO2的化学吸附能力要明显弱于H2S,分子筛中每个超笼(分子筛吸附的基本结构单元)可吸附0.4个CO2或1.13个H2S分子,因此H2S 的解离吸附比CO2的化学吸附对促进反应过程的发生更加重要。随后,Boddenberg 等[4]也在Y 型和X型分子筛上进行了该反应研究,并得到了类似的结论。但是在此类文献中,本文作者认为H2S与CO2生成COS 是一种毒副反应,并未深入探究H2S与CO2资源的协同转化利用。
1991 年,美国的Bowman[5]在专利中首次提出了利用H2S 与CO2协同转化实现H2S 中氢资源和硫资源的回收利用。Bowman 具体给出了两种可能的反应途径:一种是在高温下(>1173K)H2S 与CO2直接反应生成CO、S2和H2O,CO 再进一步发生水煤气反应生成H2和CO2;另一种是在相对温度较低和使用脱水剂的情况下(873~1173K),H2S 与CO2反应生成COS和CS2,COS和CS2在高温下进一步分解生成S2和CO,CO再发生水煤气反应生成H2。两种反应途径相比而言,前者工艺相对更为简单,后者则由于在第一步反应中使用了脱水剂使得反应平衡不断右移,进而有利于提升总体的反应效率。
与此同时,美国加州大学伯克利分校的Lynn和Towler[6]系统评估了H2S与CO2两者协同转化的可能性,通过热力学分析研究指出在1173~1673K 反应区间,相较于单独的H2S反应体系,引入等比例的CO2后,体系中S2的生成量提升了1 倍,证明了H2S 对CO2分解反应的促进作用。该作者指出这是由于H2S 分解反应生成的H2可与CO2发生逆水气反应,通过H2的消耗促进了反应平衡向右移动。此时随着反应温度的进一步升高,受热力学平衡的影响,S2的生成量显著增加,COS的生成量则会下降。但此时克劳斯逆反应过程(S2和H2O反应生成SO2和H2S)也会加剧,使得体系中SO2的生成量逐渐增加。该作者强调为了保证高温下S2的收率,反应结束后需要快速低温淬火,以免在缓慢降温过程中S2再转化为H2S 和COS。如果在1173K下增加体系的反应压力,体系中S2的生成量会减少,但是COS 的含量会增加。Towler 也研究了不同H2S 与CO2比例对产物分布的影响,发现在1173K和1atm(1atm=101325Pa)下,当H2S 的体积分数为CO2的6%时,S2在含硫物种(H2S、S2、SO2)中的平衡分布达到最大值。此外,在温度为1173K、H2S 与CO2的摩尔比为1∶1 时,体积分数10%以内的水蒸气对反应体系中各个产物的影响均不大。在1173K 和0.98atm 下,当H2S的体积分数为CO2的67%时,S2的收率达到最高值0.167,相比于没有CO2存在下提升了36%。结合实验,该作者进一步证实了反应体系中有H2、CO、和S2的生成,COS则是主要的副产物。S2可以通过冷却回收,COS 可以水解重新生成H2S 与CO2,剩下的H2和CO 则可用作合成气生成燃料或烃类化合物。
1.2 工艺流程设计和经济性评估
在前述研究基础上,Lynn 和Towler[7-8]设计了H2S 与CO2协同转化的完整工艺流程(图1),并对其进行了详细的经济性评估。在相同的日产硫黄能力前提下,该工艺的直接固定成本是配备有SCOT尾气处理单元的克劳斯工厂的60%,SCOT 尾气处理单元的主要作用是将硫黄回收装置中存在的各种形态的硫(如COS、CS2、SO2等)还原和水解为H2S,从而提升硫回收率。其中,反应炉的成本占了固定成本的45%左右;运行成本则很大程度上取决于低压蒸汽的成本。在一些大型的配套工艺和设施完整的炼油厂,此类低压蒸汽的成本低廉,使得该工艺的运行成本会略低于克劳斯及其配套尾气处理工艺。如果进一步考虑将CO 和H2O 用作原料气生成H2等,则该工艺还可产生额外的效益。然而,如果将该工艺用于天然气井口等,则可能需要额外通过燃料给反应供热,此时该工艺的运行成本比克劳斯及其配套工艺高50%。
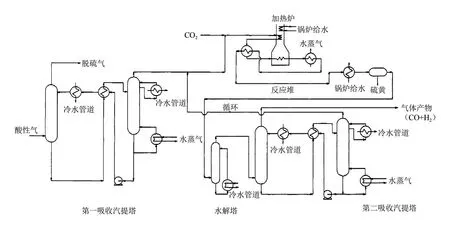
图1 用于替代克劳斯工艺的H2S与CO2协同转化的整体工艺流程
类似地,2015年,意大利的Manenti团队[9-11]在此基础上进一步通过化工软件模拟,给出了H2S与CO2协同转化制取合成气的工艺流程。Manenti等指出可将H2S 与CO2协同转化看成是将传统克劳斯工艺中的空气氧化过程转化为CO2氧化,因此其相比于克劳斯工艺相关设备改造成本不大。以煤炭气化过程为例,考虑到CO2减排产生的附加收益、生成的合成气和硫黄经济价值和较低的工艺改造成本,Manenti 等预估对于中型的煤炭气化厂,其能在2个月左右开始得到投资回报,并产生1800万欧元(2015年)的年收入。
1.3 高温下H2S与CO2直接转化
基于前述研究基础,美国马里兰大学的Gupta等[12-13]研究了在高温(1323~1473K)下H2S 与CO2协同转化制备合成气的产率与温度及H2S 与CO2投料比的关系,发现在1345K 以下时,CO2的引入会一定程度抑制H2S 的转化,但在1345K 以上时,CO2会促进H2S的转化过程。当H2S与CO2投料比为3∶2 时,在1323~1473K 这一温度反应区间,随着温度的增加,体系中H2生成量逐渐减少,CO生成量则出现了增加,使得生成的合成气的H2/CO比例从7∶1 降到1∶1 左右,但合成气生成总量维持在1.5%~2%区间。1473K 时,当反应体系中H2S 与CO2的投料比从4∶1 下降到1∶4 之后,生成的合成气总量下降了约一半,H2/CO 的比例则从4.5 左右下降到0.5 以下。一般而言,用作燃气发动机燃料或是合成氨的合成气的H2/CO 比例在0.3~1.2 区间。该作者由此指出如果制备得到的合成气要用于上述用途,酸气中CO2的比例应尽量高于40%。
2016 年,阿联酋的Raj 等[14]通过动力学模拟研究了1300~1800K 下H2S 与CO2协同转化过程中H2S与CO2投料比、反应温度、反应停留时间对反应产物H2/CO和S2分布的影响,并研究了体系中可能存在的含硫副产物(COS、SO2和S2O 等)的分布情况。和前述研究类似,动力学模拟结果表明H2S与CO2的转化具有协同促进作用,高温(>1473K)有利于合成气的生成,但也会增加含硫副产物的生成量。同时该作者还发现CO2的投料比对S2的收率有明显影响:低CO2浓度时,CO2促进H2S 分解占主导作用,S2的生成量相应增加;高CO2浓度时,S2则会与CO2中的氧生成含硫副产物;要想减少COS的生成,反应温度应尽量高一些,反应停留时间也应长一些。
1.4 中低温下H2S与CO2催化转化
相比于高温下H2S 与CO2的直接转化反应,部分研究学者认为中低温下H2S 与CO2催化转化容易发生催化剂的中毒和硫黄堵塞等问题,因此不具有显著优势[10]。然而,目前已有不少研究表明在中低温的反应条件下催化剂的引入能显著提升H2S 与CO2协同转化的反应活性,且催化剂在长时间下可维持较好的稳定性。Towler早期通过动力学分析发现反应体系中H2S的解离是反应的决速步,因此引入了促进H2S 分解的催化剂二硫化钼(MoS2)。MoS2具有独特的层状结构,由于其活性高、稳定性好和成本低等优点,在加氢脱硫领域已经有很长的发展历史,被广泛应用于原油加氢脱硫及超低硫清洁油品的生产[15]。他们发现在1173K下MoS2可有效催化该反应过程的发生,但并未对此进行深入研究[6]。随后,Keener等[16]研究了CoMo硫化物在738~973K 和1atm 条件下催化H2S 与CO2协同转化的过程,并估算得到在CoMo 硫化物催化剂存在的条件下时反应的活化能为114.4kJ/mol。在H2S 与CO2投料比为1时,738K下H2S的转化率仅为理论转化率的12%;随着温度升高,反应的催化活性也得到了提升,848K 下H2S 的转化率达到了理论转化率的40%(即1.7%)。
2006 年,伊拉克的Naman 等[17]进行了3 种Cd系催化剂(CdS、CdSe 和CdTe)在598~798K 下催化H2S 与CO2协同转化的研究。在该反应体系中,该作者主要聚焦于碳氢产物的检测,并检测到了CH4、H2和痕量C2H6的生成。作者指出无论是使用哪种Cd 系催化剂,在CO2存在下体系的H2生成量都得到了明显提升。在3种催化剂中,CdSe的催化活性最高,体系生成的甲烷最多,其次是CdTe,活性最低的是CdS,但上述3 种催化剂均还处于实验室研究阶段,且由于其含有剧毒的Cd 元素,其商业化前景还有待进一步研究。另外,在此研究中作者对反应体系中H2S 与CO2的投料比并未进行过多涉及。
华东理工大学的李平团队[18]研究发现,在673~1073K下,使用价格低廉、常用作促进剂和催化材料的MgO 能显著提升H2S与CO2的转化率。尤其是MgO 碱性适中,有利于CO2的吸附活化[19-21],且在高硫化物电位的还原条件下具有强稳定性[22]。长时间测试表明,在78h内体系始终保持着稳定的催化活性和产物选择性。除了MgO 以外,该作者还研究了CaO、γ-Al2O3、NiO/MgO 及NiO/γ-Al2O3等催化剂的催化活性,其中γ-Al2O3因具有比表面积大、吸附性能好、热稳定性优良等优点,在医药、化工、冶金和废气治理等领域有广泛应用[23]。研究发现不同催化剂的催化活性较空白实验虽然有显著提升,但是彼此之间的活性差异并不大(表1)。结合反应体系催化活性对空速变化不敏感、不同催化剂的比表面积大小对比、反应前后催化剂晶体结构的变化和对H2S 与CO2吸脱附能力差异,该作者推测该体系的反应机理主要为自由基反应,而非催化反应中常见的吸附-反应机理。加拿大Behie等[24]也得到了类似的研究结果,还认为虽然COS 经常被认为是该反应的主要副产物,但模拟分析结果表明COS在1073K以后的生成量并不多。
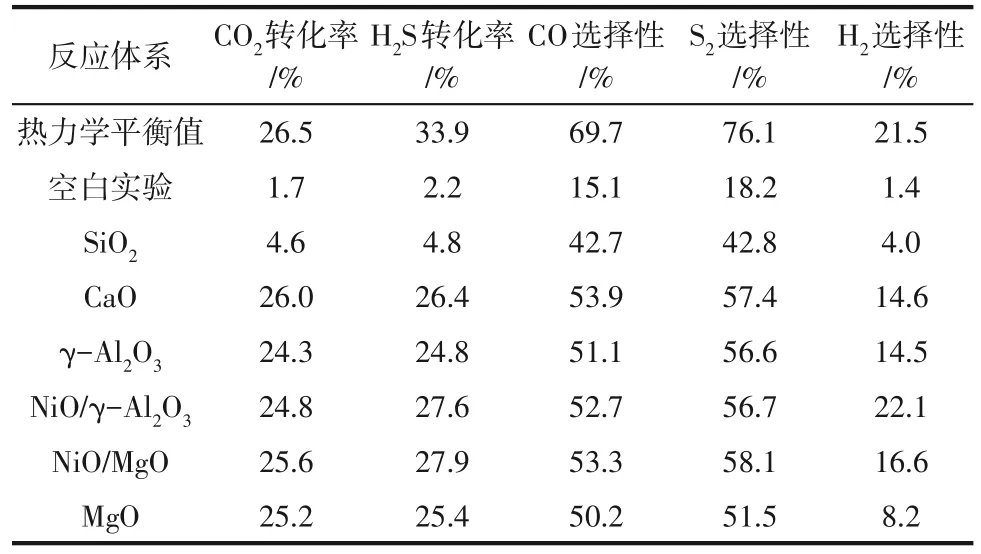
表1 1073K、100000h-1空速条件下,V(H2S)∶V(CO2)∶V(N2)=3∶3∶14时,使用不同催化剂时H2S与CO2的转换率以及各种产物的选择性(均为摩尔分数)[18]
在天然气处理得到的酸气中,除了H2S 与CO2外,往往还含有少量水蒸气,加拿大的Gambarotta等[25]研究了在一系列金属硫化物和氧化物存在下H2S/CO2/H2O(体积比为60/60/1)的反应,发现NiS的催化活性最高(表2)。在873K 的条件下,体系中主要的反应产物有H2、CO、SO2和S2。此外,作者也研究了在不同催化剂体系中H2O 对H2S 与CO2协同转化的影响,发现在FeS 催化剂中H2O 对CO产率影响较小,但对其他协同反应的产物影响较大。而在NiS 催化剂中H2O 对协同反应中CO 和H2的生成有明显的抑制作用,但该作者并未给出明确的原因。在没有H2O的情况下,NiS体系中的H2生成速率和CO生成速率可分别达到0.11mol/(h·molcat)和0.04mol/(h·molcat)。在反应120h 后,该体系仍保持着良好的催化活性。值得一提的是,在该反应体系中并未检测到COS或CS2等产物。
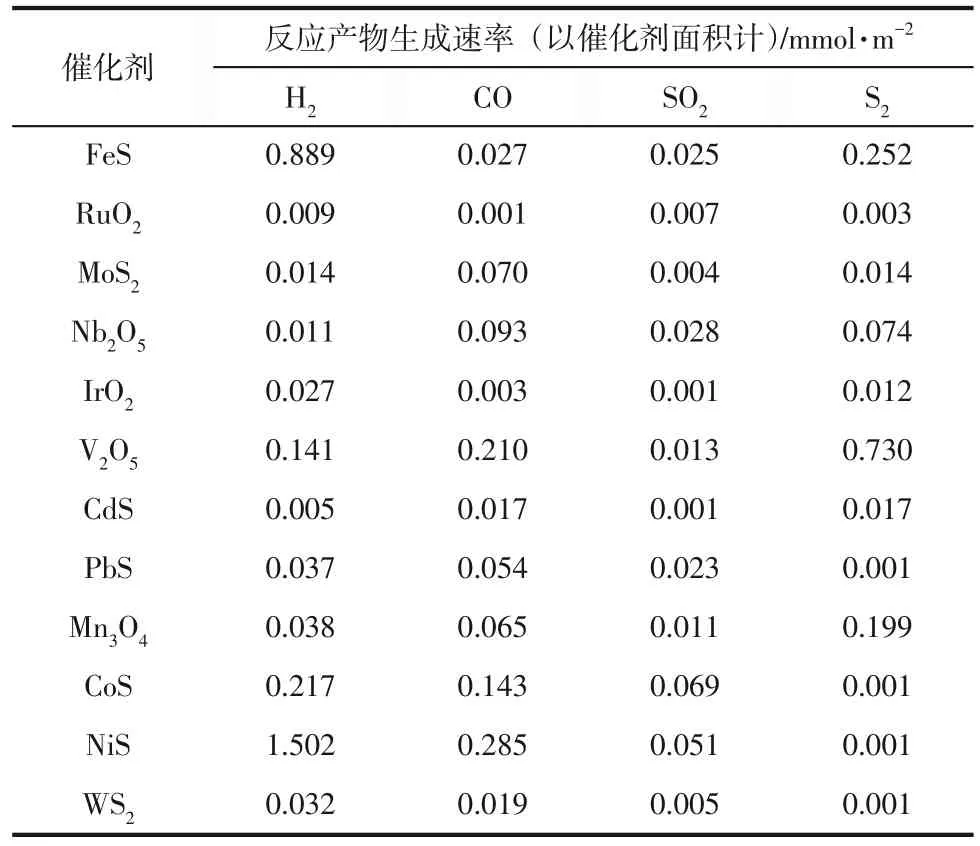
表2 873K下V(H2S)∶V(CO2)∶V(H2O)=60∶60∶1时不同催化剂5h内催化H2S与CO2协同转化的效率[25]
COS 通常被认为是H2S 与CO2协同转化的副产物,但它同时也是用于合成杀虫剂等化学制剂的重要原料。近来,中国科学院大学环境材料与污染控制技术研究中心的郝郑平研究团队[26]开展了CoMo硫化物在低温下(573K,10atm)用于催化H2S 与CO2协同转化制备COS 的研究。通过热力学分析,该作者认为在573K下CS2的生成和COS的分解都受到了抑制,因此COS 是H2S 与CO2协同转化的主要产物。在实验过程中,该作者也的确没有观察到其他产物如CS2和S2的生成。实验结果表明升温和提高H2S 与CO2的投料比有利于COS 的生成,但增加压力对COS 产率影响不大。当反应经过诱导期达到稳定后,CoMo 硫化物的活性明显高于单独的Co硫化物或是MgMo硫化物催化剂,其COS的生成量可达到热力学上的理论转化率(6%,CO2/H2S/He为1.33/0.67/98)。通过对反应前后的催化剂进行自由基信号分析等方式,该作者指出CoMo 硫化物催化剂中的S空位是实现高催化活性的关键。结合理论计算,作者发现相比于CO2,H2S 更容易通过硫空位在MoS2表面形成化学解离吸附生成S 原子,S 原子通过与CO2中的C 原子的范德华作用力活化诱导CO2,进而促进了C—S 的形成。与此同时,Co原子的引入可以促进H2S与CO2在MoS2表面的共同吸附,从而使得催化活性进一步提升。
2 光催化H2S与CO2协同转化反应
2.1 发展历史
光催化反应可直接使用太阳能作为供能单元驱动化学反应发生,是一种较为绿色的催化方法。1972 年,日本科学家Fujishima 等[27]证明了在紫外光驱动下,TiO2可分解H2O 制氢。从热力学上讲,H2S 的分解能(33.3kJ/mol,298K)明显低于H2O的分解能(237.2kJ/mol,298K),可更容易实现H2S 的制氢反应。1982 年,Grätzel 等[28]从实验上证明了可将H2S 光催化分解制氢,为实现H2S 的高值转化利用提供了新的策略。本文作者团队[29-35]也在光催化分解H2S领域展开了一系列研究,包括首次开发了MnS/In2S3等一系列光催化剂用于H2S分解制氢,并将H2S 中的硫资源定向转化为硫代硫酸钠(大苏打)等硫化学品。相比而言,光催化CO2转化反应则是一个较为复杂的反应,涉及多个电子和质子的参与,可能产生CO、HCOOH、HCHO、CH3OH、CH4和C2化合物等多种反应产物[36-42]。虽然目前光催化单组分H2S 或CO2转化的研究报道较多,但是光催化H2S 与CO2同时转化的研究还相对有限。
2.2 研究进展
González-Núñez 等[43]报道了在紫外光作用下,在乙腈和水的混合溶液中,H2S 可促进CO2还原为甲酸。该工作为光催化H2S 与CO2的协同反应提供了有效参考,但缺乏了对硫产物的深入研究。Guzman 等[44]以ZnS 为光催化剂进行了CO2还原反应,发现在Na2S 水溶液中CO2的还原得到了促进(图2)。Na2S 在溶液中主要是以HS-的形式存在,而H2S 在碱性溶液中也是以HS-的形式存在,因此该作者认为如果在体系中引入H2S,也能有效起到捕获空穴的作用,从而促进CO2的还原。该研究为光催化H2S与CO2协同转化提供了有效的理论基础。类似地,西班牙的Corma 团队[45]使用锐钛矿型掺铜二氧化钛(Cu-TiO2)进行了光催化CO2还原研究。在紫外光照射下,以Na2S 作为电子给体的催化活性要明显优于卤素盐,反应体系生成HCOOH、CO和H2的能力均显著高于其他卤素盐体系(表3),进一步证明了光催化H2S与CO2协同转化的可行性。
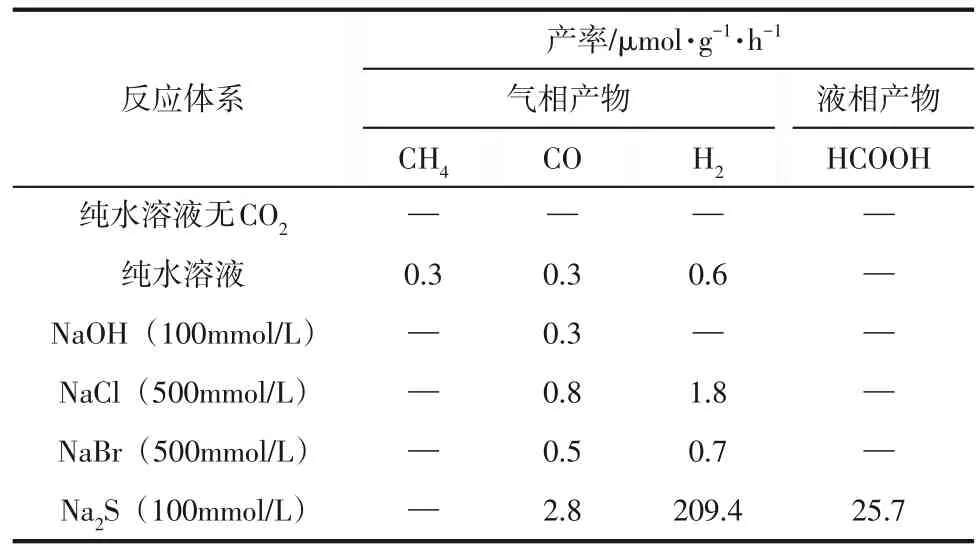
表3 Cu-TiO2在不同反应溶质中的光催化CO2还原产率[39]
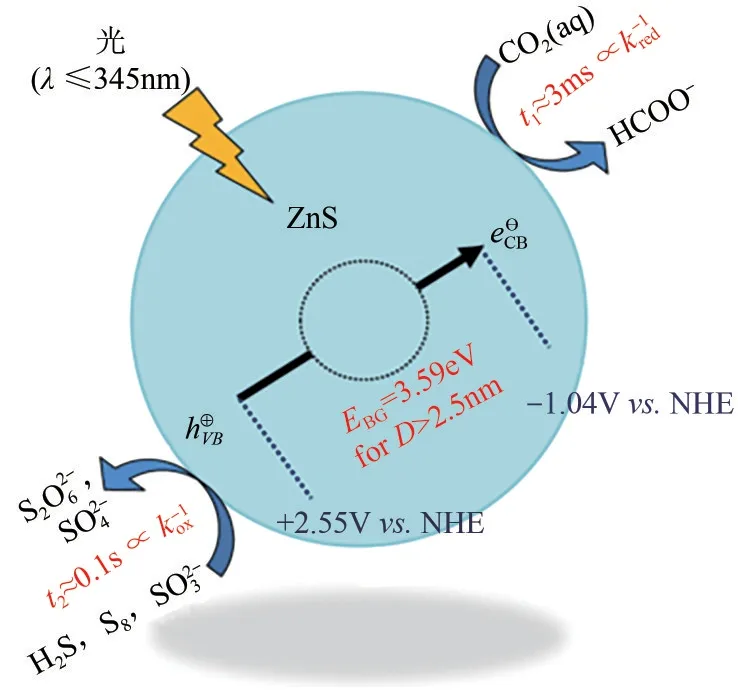
图2 含硫体系中光催化CO2为甲酸盐的反应机理
近来,南京大学朱文磊等[46]以高度分散的异质结材料CdS/TiO2∶Cu为催化剂进行光催化CO2还原时,发现引入H2S 可显著促进CO2的光还原过程。H2S 的存在消耗了光生空穴,促进光生电子-空穴的分离,且H2S 分解产生大量质子,使得CO 和H2的生成速率显著增加,达到未加H2S 时的1.4 倍和68.9倍。此外,在光催化反应中CdS催化剂经常会发生硫的自氧化造成光腐蚀现象,H2S中的硫优先氧化可有效避免CdS的光腐蚀现象,从而延长催化剂的寿命。通过调整H2S 的初始浓度,体系的CO/H2的比例可控制在1.07~7.21 之间,以满足不同化学合成的要求。因此,此类光催化H2S 与CO2协同转化反应也是一种具有潜力的合成气生产方法。
3 电催化H2S与CO2协同转化反应
近年来,应用于单组分H2S 或CO2转化的电催化技术发展迅速,逐渐有团队开始关注使用电催化技术开展H2S 与CO2协同转化研究,以获得高附加值产物[47-52]。2018 年,李灿院士研究团队[53]首次提出了光伏-电催化实现H2S与CO2协同转化为高附加值产品的方法。如图3所示,他们使用石墨烯层包裹的氧化锌纳米颗粒(rZnO@G)作为阴极,改性工业石墨碳(G/GCS)作为阳极,乙二胺四乙酸螯合铁(EDTA-Fe3+/EDTA-Fe2+)作为氧化还原对。在反应过程中,CO2被溶解在1-乙基-3-甲基咪唑四氟硼酸盐离子液体和少量水中,随后在阴极室中电催化还原为CO,此时阴极室也可检测到少量H2。同时,H2S 鼓泡进入阳极室后,生成了黄色沉淀,XRD 测试结果表明该黄色沉淀为单质硫。该作者采用开路电压为1.72V的商用平面硅太阳能电池直接驱动正极和负极反应,并将模拟天然气(Ar/CH4/CO2/H2S 为60/20/19/1,体积比)直接通入该体系,在体系中成功得到了CO 和S。该工作展示了一种光伏-电催化酸性气CO2与H2S综合利用方法,在中性条件下将H2S 与CO2转化为高附加值产品,为酸性气藏中天然气的净化提供了新的思路。
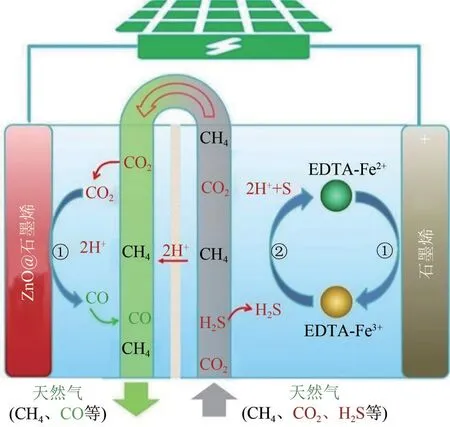
图3 光驱动的电化学协同转化H2S与CO2
2021年,上海交通大学的周保学团队[54]构建了新型的电化学反应体系,将H2S 与CO2协同转化为CO和元素S。在阳极室中,该作者使用基于I-/I3-循环的氧化还原体系,将H2S 快速氧化为S。在阴极室中,该作者则用基于聚四氟乙烯和钴酞菁(CoPC)修饰的多孔炭气体扩散电极(GDE),将CO2快速高选择性地还原为CO。由于CO2在GDE上的强化传质和催化剂CoPC 的存在,体系具有较高的法拉第效率(95%)。在电流密度大于50mA/cm2的情况下,该系统的最大能量效率超过72.41%,是以前报道的H2S 处理系统的12.5 倍。体系中S 和CO 的产率分别为24.94mg/(cm2·h)和19.93mL/(cm2·h)。通过模型分析,他们认为在现有天然气净化技术中H2S 与CO2同步利用的运行成本略低于单一利用H2S的运行成本(表4)。
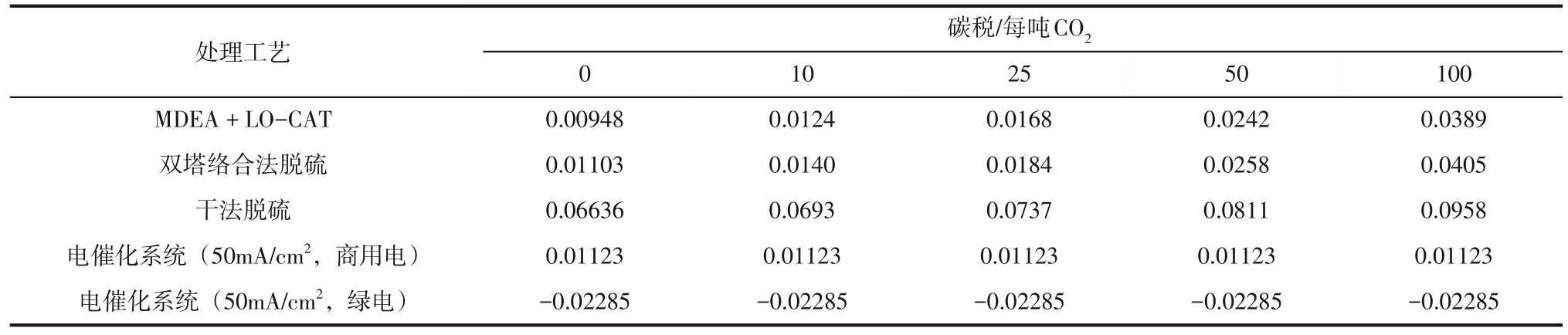
表4 常用处理工艺和H2S与CO2电催化系统估算的每立方米气体运行成本[54]
除酸性天然气藏同时含有H2S 与CO2外,沼气中也通常同时含有H2S 与CO2。电催化技术也可应用于具有相似气体组成的沼气系统。中国科技大学的李文卫团队[55]开发了一种微生物催化的电化学系统,通过H2S 与CO2协同转化,同时实现了CO2减排、沼气净化和硫回收等多个目标。在阳极室中,H2S 在Fe2+/Fe3+离子对作用下被完全脱除,并选择性地转化为元素硫颗粒。在阴极室中,微生物催化菌落将CO2选择性催化转化为甲烷,且体系具有较高的甲烷生成率(甲烷体积分数可达98.3%)。该系统在连续运行过程中表现出稳定的性能,在沼气提质和回收硫黄方面具有很大的实际应用潜力。
4 等离子体催化H2S 与CO2协同转化反应
与热催化法相比,等离子体具有非平衡性质,因此可在较低温度下诱导气体发生物理和化学反应的能力。目前已有研究表明可将等离子体技术应用于H2S 与CO2协同转化制合成气,并实现长期连续稳定运行[56]。中国科学院山西煤炭化学研究所的房克功等[23,57]以工业上常见的Al2O3为催化剂,通过在其表面负载MoS2,使得H2S 与CO2可协同转化生成H2和CO,且H2S 与CO2的转化率较单独的Al2O3得到了显著提升,且催化体系在50h 内没有明显失活。与此同时,他们还发现可利用不同的H2S 与CO2进料比实现产物H2和CO 的比例调控。在此基础上,他们进一步开发了Ni-Mo 硫化物/Al2O3催化剂,并研究了不同的Ni/Mo 比例对H2S 与CO2协同转化反应体系转化率的影响,认为调整Ni和Mo的摩尔比可调控粒子的尺寸和能带结构,进而提升Al2O3的氧化还原能力。当催化剂中Ni/Mo投料比在5/3 时,H2S 与CO2的转化率可分别达到98.9%和49.0%。由此可见,等离子体技术可以在一定条件下完成对H2S 与CO2的资源化转化。但是这一过程的实现需要较高的电压输入,使得体系耗能较大[58-59]。另一方面,极高的电压也可能引起反应室温度升高,对设备的安全性造成影响。
5 H2S与CO2协同转化方法的优劣势
结合对上述各种H2S 与CO2协同转化处理方法的介绍,表5对各种催化技术的具体优劣势进行了总结。

表5 H2S与CO2协同转化技术对比
相比于各种催化技术,高温下H2S 与CO2直接热反应可在传统的克劳斯工艺基础上进行工艺改造升级,且现有的经济性评估分析表明其相比于克劳斯工艺具有一定的经济优势,但是高能耗仍是该反应面临的一大挑战。
热催化技术具有处理量大、工艺改造成本低等优点,且有良好的研究基础,目前已经可以在中低温下进行H2S 与CO2协同定向转化。但是由于热催化法的反应温度要明显高于光催化和电催化等,能耗也相对较高,且反应过程中产生的水蒸气的重整反应对H2S 与CO2协同转化的影响还不明确,限制了热催化的实际应用。
光催化技术具有能量来源广、绿色无污染的优点。但受限于太阳光的能量密度,转化效率较低,且硫产物的转化过程目前还缺乏认识,CO2转化产物也相对热催化更加复杂。目前,尚无光催化技术应用于H2S与CO2协同转化的经济性评估研究。
电催化技术反应条件温和、催化活性较高,而且在反应过程中不产生COS 和SO2等副产物,在H2S与CO2协同转化的研究中具有较好的应用前景。但是目前对H2S 与CO2反应机制探讨还不够充分(如硫产物复杂、多质子参与CO2转化产物复杂),电极材料设计及处理工艺开发还不够完善,电极成本较高,反应的耐用性和稳定性研究还需加强,且经济性评估有待加强。
等离子体催化技术相对于热催化技术具有能量效率高等优势,但其对于工况条件的环境要求较高,环境的湿度和杂质气体对其活性影响较大。目前尚未见湿度和杂质气体等对等离子体催化反应体系的影响研究。
6 结语与展望
随着碳中和进程的推进,现有克劳斯工艺已难以满足酸气H2S 与CO2的低碳高值处理要求,H2S与CO2的协同转化研究在未来势必受到科学工作者的更多关注。早期的H2S 与CO2的协同转化研究主要集中在高温下H2S 与CO2直接发生热反应,近来的研究则主要集中在低温下的热催化反应和等离子体催化、常温下的光催化、电催化反应。本文分别从热反应、光催化、电催化和等离子体催化角度详细阐述了H2S 与CO2协同转化的研究进展,并对比了各种技术应用于H2S 与CO2协同转化的优劣势,以期促进H2S与CO2协同转化技术的发展。
从工业应用的角度来看,目前高温热转化/热催化技术H2S 与CO2协同转化处理研究相对较多,且其在原有克劳斯工艺上的改造成本也相对较小,处理能力强,可应用于大型天然气净化厂。但在当前碳中和背景下,通过化石能源燃烧的供热方式不够理想。未来可以考虑通过太阳光聚光产生的热量驱动热催化反应进行,以减少化石能源的使用,实现碳减排。
光催化技术具有能量来源广、绿色无污染的优点,在碳中和背景下有良好的应用潜力。但是太阳光日照能量密度低导致光催化效率较低,现阶段还难以应用于实际。未来可以考虑通过太阳能聚光的方式提升太阳光的单位辐照能量密度,结合太阳光聚光产生的热效应提升催化效率。此外,也可以通过将电催化与光催化相结合,通过额外的电场输入提升体系的能量密度,进而提升反应的转化效率。
电催化技术在近年来发展迅速,若能将电催化技术与绿电结合,则可较好地满足双碳发展需求,优势明显。近期可考虑将电催化技术应用于野外小型天然气井的H2S与CO2处理,开展应用示范研究。此外,开发高催化活性、耐腐蚀、低成本的电极材料和膜材料、提升催化体系的稳定性,都是未来电催化H2S 与CO2协同转化的重要发展方向。在绿电成本大幅下降的将来,电催化技术有望成为工业上重要的H2S与CO2协同转化处理技术。
等离子体催化技术应用于H2S 与CO2协同转化具有较好的催化活性,但体系的高能量输入和装置安全性需要引起研究者重视。设计高效的反应器,使气体与电子流能够更好地接触,同时开发高效的催化剂,在提升转化率的同时降低能量输入,以降低反应室温度,增强安全性,都是未来该催化技术需要重点研究的内容。
需要说明的是,虽然本文中的大部分文献研究均以酸性天然气中的H2S 与CO2协同转化为前提,但在此类文献的实际研究过程中,并未充分考虑天然气藏的特点和工况条件。如前言所述,不同天然气藏中酸性气H2S 与CO2的比例会有明显差异。因此,不同H2S 与CO2比例下催化剂的筛选和反应条件的调控等都应是研究中的重要内容,但现有文献中对H2S 与CO2不同比例下的协同转化研究非常有限。另外,通过脱硫脱碳后得到的H2S 与CO2混合气体中还往往含有少量CH4和水汽等,而此类气体对H2S 与CO2协同转化反应的影响研究仍较少,其对反应路径的影响还不明确。因此,在后续的研究过程中,必须结合天然气藏的特点和工况条件开展H2S 与CO2协同转化相关研究。此外,虽然上述各种技术均已被应用于H2S 与CO2协同转化研究,但其对应的经济性评估分析整体还较为缺乏,完善各种技术的经济性评估,是未来应用上述技术开展H2S与CO2协同转化的必然发展趋势。

