卒中模拟病的研究现状及新进展:热点问题及预测方案
陈晓曼,张硕
0 前言
对于急性缺血性卒中患者,越早进行血管内治疗和应用药物静脉溶栓越有利于挽救缺血半暗带、降低死亡率和致残率[1]。这要求专科医生在短时间内对急性缺血性卒中患者进行诊断、鉴别、评估并决定治疗方法。由于急诊医生接诊时间和辅助检查手段有限,导致一部分临床症状为卒中样表现的患者被诊断为急性缺血性卒中,而经过最终临床确诊排除。这类临床表现类似于急性卒中发作的神经功能缺损表现,如突发语言、肢体活动障碍、意识改变等,但最终证实为非卒中疾病的临床综合征,称为卒中模拟病(stroke mimics,SM)。SM 目前没有确切的定义,一般认为具有突发语言或肢体活动障碍、意识改变等类似卒中样发作症状的一系列疾病,患者最终确诊为急性缺血性卒中以外的其他疾病的一组临床综合征。在治疗急性缺血性卒中时,尽早识别SM有助于避免延误原发疾病的诊治及不必要的针对于缺血性脑血管病再通治疗[2,3]。
1 卒中模拟病(SM)
1.1 卒中模拟病(SM)的发生率
因为设置的研究背景、医疗条件及入选标准不同,关于SM 的发生率没有统一结论,大致占所有拟诊急性卒中患者的5%~30%。据一项系统综述评估,SM 约占因疑似卒中发作入院人数的25%[4]。Garg等[5]在2019年发表的一项研究中,回顾性分析了2013年8月至2017年12月在急诊科接受阿替普酶治疗的所有疑似急性缺血性卒中患者,其中报告了27.3%的SM。而在另一项前瞻性研究中,Matuja等[6]招募了1403例来自坦桑尼亚全国各地公立和私立医院的转诊患者,其中30.6%被认为患有卒中,其中6.6%被诊断为SM。
1.2 卒中模拟病(SM)的疾病谱和临床特点
SM的疾病谱病因较多,常见病因有:癫痫、复杂型偏头痛、周围性眩晕、颈髓疾病、高血压脑病、感染、中毒、代谢性疾病等,其他病因包括颅内占位性病变、脱髓鞘疾病、脑卒中后症状复现、转换障碍、主动脉夹层等[7-12],见表1。在Lee 等[13]研究中,回顾性统计了270 例于2016年7月1日至2017年9月30日在该学术综合卒中中心经远程卒中评估且接受溶栓的患者,其中64 例(23.7%)被诊断为SM,包括偏头痛26 例(40.6%)、转换障碍12 例(18.8%)、脑病7例(10.9%)和其他19例(28.4%)。

表1 常见卒中模拟病及鉴别要点
癫痫发作可能表现为发作后神经功能缺损,比如Todd 麻痹,是一种以暂时性肢体无力或偏瘫为特征的神经系统异常,通常发生在癫痫发作后,没有持久的后果,与卒中引起的癫痫发作难以鉴别[14]。
长期以来,突发性头晕和眩晕一直被认为是一种重要的SM相关症状,而多项研究表明,孤立性头晕、眩晕、平衡障碍和卒中之间的关联非常低。其中,只有平衡障碍是已知的预测脑血管病的症状。眩晕和头晕本身是周围前庭疾病的征兆,而平衡障碍通常是小脑卒中的表现[15-17],听力损失和症状持续时间可能有助于眩晕的鉴别诊断,存在听力损失通常由梅尼埃病或迷路炎引起[9]。
复杂型偏头痛同样可以表现为局灶性神经功能缺损,比如偏瘫性偏头痛,除偏头痛症状外还可表现为肢体无力、感觉异常、言语障碍等,临床少见,但也可能被误诊为卒中[18]。偏头痛性眩晕的诊断是在有发作性眩晕史的患者中确定的,这些患者有当前的偏头痛或偏头痛病史,并且在至少2 次眩晕发作期间有以下症状之一:偏头痛、畏光、恐音或先兆[9]。
代谢类疾病也可引起急性局灶性神经功能损坏,常见原因如低血糖,低血糖导致脑细胞能量储备不足,导致活性膜离子泵失效,从而导致细胞毒性水肿,严重的低血糖可能表现为与脑血管病相似的弥散受限[19,20]。严重低钠血症症状包括轻度低钠血症时的嗜睡和意识模糊,以及明显较低水平的癫痫发作、昏迷和呼吸停止,但也可能出现局灶性神经系统症状[21]。低钾血症或酒精或药物中毒也会导致短暂的局灶性神经症状。
颅内占位病变如肿瘤可能对周围血管产生外源性压迫导致血管分布区域的神经功能缺损,表现出类似卒中的症状[22]。此外,精神心理疾病、心脏疾病及其他系统疾病表现为类似卒中发作的症状也有相关报道[15,23-27]。
当患者怀疑为急性缺血性卒中,且既往有脑卒中病史,症状表现为卒中后残余局灶性神经功能缺损的短暂恶化,或先前卒中相关局灶性神经元功能缺损的暂时复发,但影像学表现不支持有新发脑缺血病灶时,需要考虑卒中后症状再现(poststroke recrudescence,PSR)的情况[28],在临床实践并不少见,见图1。PSR通常存在诱因,比如全身感染、精神心理因素(如卒中后抑郁伴有躯体化障碍)、使用镇静药物和麻醉剂等,症状归因于既往脑卒中,在对诱发条件进行治疗后,症状得到缓解。
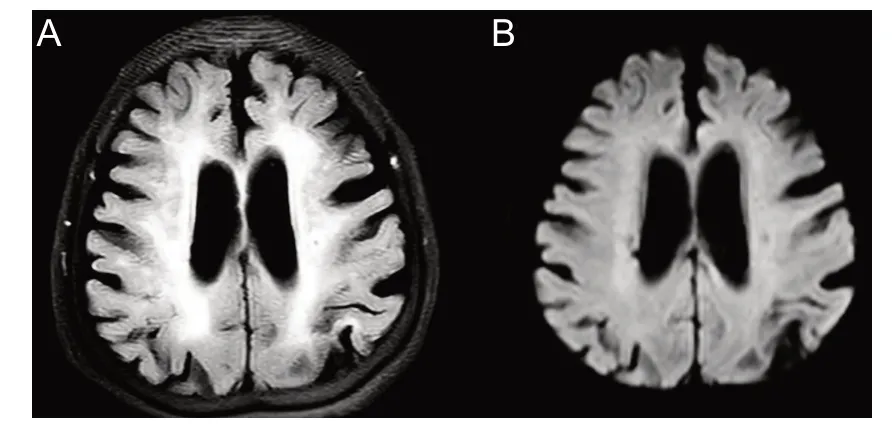
图1 卒中模拟病1例--新冠感染和感染后脑卒中后症状再现
1.3 卒中模拟病(SM)的静脉溶栓安全性
2019年美国心脏协会/美国卒中协会急性缺血性卒中早期处理指南认为静脉注射重组组织型纤溶酶原激活物(recombinant tissue-type plasminogen activator,rt-PA)的益处是时间依赖性的,在治疗窗口内的早期治疗会带来更大的益处[29]。为了确保在窗口期内(发病6 h内)符合条件的患者最大可能接受静脉溶栓,应尽可能迅速地进行评估和治疗。但溶栓使用率的增加和从急诊室至溶栓时间的减少可能导致急诊和神经科医师对SM的误判。关于SM患者静脉溶栓后风险的讨论,Esmaeili等[30]对165例静脉溶栓的患者(其中10例SM)进行评估,所有患者在接受静脉溶栓前和接受静脉溶栓后24 h 均接受了脑部CT 检查,这些病例均未出现脑出血或其他rt-PA并发症,所有患者功能结果良好,改良Rankin 量表评分≤1 分。这些结果证实了静脉注射rt-PA的总体安全性,以及在急诊科对没有已知禁忌症的患者迅速决定静脉溶栓的必要性。另一项研究统计了516例接受静脉溶栓的患者(其中75例SM),SM患者中有1例患者出现了脑出血,而无口舌水肿或严重颅外出血并发症的病例,结果强调了在SM中静脉溶栓的安全性。因为与静脉溶栓治疗的随后确诊的急性缺血性卒中患者相比,症状性颅内出血并发症的风险较低[31]。以上研究表明,尽管静脉溶栓可能会产生不良影响,但对于有急性缺血性卒中症状的急诊室患者,即使患者最终诊断为SM,在最有效的时间内给予静脉溶栓的益处也可能超过并发症风险。但是临床上,应该关注静脉溶栓可能会对自发性脊髓硬膜外血肿及主动脉夹层造成极大不利影响,恶化病情[32-34]。
2 卒中模拟病(SM)与急性缺血性卒中的鉴别诊断
2.1 影像学检查鉴别卒中模拟病(SM)与缺血性卒中
在大多数急诊科,CT是疑似颅内病变的患者主要的影像学检查方式[35],头部非增强CT检查是疑似急性缺血性卒中病例的初始影像学检查,但非增强CT 在急诊卒中中心的主要作用是排除颅内出血。
急性卒中溶栓与时间有关,一旦CT检查完成,必须迅速开始治疗。因此,SM被无意中溶栓的风险增加。早期识别SM对于避免颅内出血的风险、rt-PA治疗的相关成本及重症监护室或卒中病房的额外护理成本非常重要。在这种情况下,使用包括增强CT动脉血管成像(CTA)和CT灌注成像(CTP)在内的多模式大脑成像可以提高对SM 的检测[36-38]。CTA 用于检查脑部血管主要是动脉血管,通过注射造影剂,对于观察颅内动脉有无发生狭窄等情况有较高的临床意义;CTP可以提供有关脑实质毛细血管水平血流动力学的重要信息,反映脑组织灌注量的变化。与CT 相比,磁共振成像对于识别急性脑梗死更敏感[39],并有助于区分SM和急性缺血性卒中患者。弥散加权MRI是最敏感的诊断工具,可以很早显示缺血性病灶,尤其是症状在短时间得以缓解的患者,并且在确定病因是否为急性缺血性卒中时非常有用。MRI 的优势是能对较小的腔隙或栓塞病变和后颅窝缺血具有更高的敏感性,更容易评估梗死时间,不仅提高了使用静脉溶栓和血管内治疗的急性再灌注治疗的比率,而且改善了患者的预后[4,40]。但对于急诊卒中患者,美国卒中协会发布的急性缺血性卒中早期处理指南不推荐在符合条件的患者静脉溶栓前进行磁共振检查,对于符合溶栓条件的患者,非增强CT可有效排除脑出血,不应进行过多的影像学检查而延误溶栓治疗[29]。时间和医疗资源[41]限制了MRI在急诊环境中的可用性及便捷性,神经科医生通常选择将MRI作为将患者进入病房诊治后的进一步主要检查之一。磁共振弥散加权成像(diffusion weighted imaging,DWI)在卒中后不到1 h,甚至10 min 即可检测到病灶高信号,是一个非常敏感的序列,但在有些少见情况下,急性脑梗死在DWI上没有高信号,即弥散阴性脑梗死,可能是因为梗死灶不大或其他原因所致(见图2)。因此,对于症状不清、影像学未见责任病灶的患者,神经系统及其他专科系统评估可能更为安全。
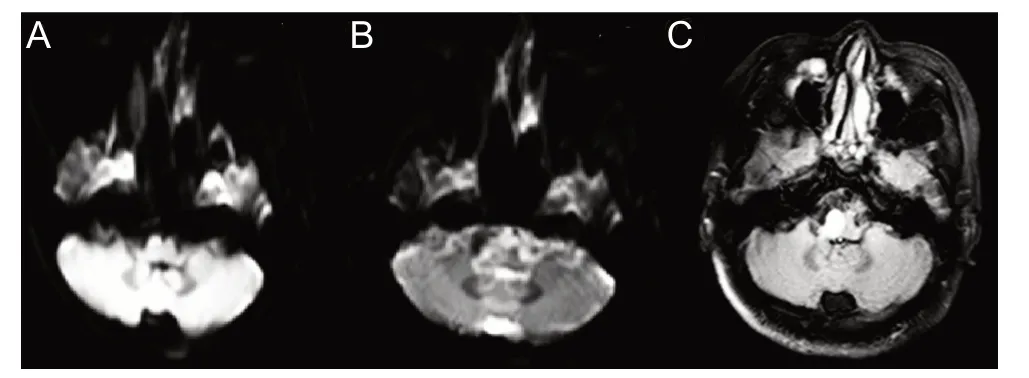
图2 急性延髓梗死1例
2.2 卒中模拟病(SM)与急性缺血性卒中的临床预测
在卒中急诊,短时间内可以根据病史和临床体征帮助快速识别SM。Kvistad 等[42]发现除了轻微的卒中症状外,较低的年龄、女性、无心肌梗死史、入院时收缩压低、感觉丧失和无面部轻瘫与SM有关。此外,仅基于病史和临床特征的SM预测量表有助于在急诊科识别SM。2014年Syed等[43]分析设计了一种远程卒中模拟评分--TM 评分。TM 评分基于与SM 独立相关的因素,包括年龄,病史(心房颤动、高血压、癫痫发作),面瘫及美国国立卫生研究院卒中量表(National Institutes of Health Stroke Scale,NIHSS)评分>14分,通过逻辑回归分析得到获得变量的对应整数评分,得到TM评分量表,随着TM评分的增加,患SM障碍的可能性逐渐降低。FABS 量表是由Goyal 等[44]研究设计的一种评分系统,通过分析SM 队列与急性卒中患者的人口统计学和临床特征,发现SM患者更年轻,有房颤病史的可能性更小,有癫痫病史的可能性更大,收缩压<150 mm Hg;此外,SM不太可能出现面瘫,更有可能出现孤立的感觉症状,获得对应变量并分配二进制值,构建了一个直观的评分系统FABS,随后进一步分析表明,评分为0~2 分的患者极有可能为急性脑血管病,评分为5~6 分的患者更倾向于患有SM。在FABS 的基础上,Qin等[45]提出了一种简化的FABS量表,即sFABS,该研究认为,根据溶栓治疗指南,一些类似卒中的症状,如孤立的感觉障碍和癫痫发作症状,已被列为排除标准和相对排除标准。因此在决定溶栓的患者中,孤立感觉障碍和癫痫病史对预测SM 的能力比较低,将这2项去除,得到更为简单的但也有良好预测效果的SFABS量表。Khan等[46]提出了一种在紧急情况下预测SM的算法,该研究分析来源于以往研究确定的风险因素,包括年龄、高血压、高血脂、糖尿病、房颤史、偏头痛史、癫痫史及精神病史,构建了一个新的SM预测量表,称为Khan评分,它有助于识别具有高度特异性的SM,得分越高,SM的可能性越大。
一项研究[47]回顾性分析了257例(17例为SM)患者,通过单因素逻辑回归分析构建了一种新的决策树,仅根据年龄、偏头痛和精神病史预测SM的风险。同时,该研究以外部验证的方式,以4种SM预测量表为标注,对所有患者进行评分,进一步进行诊断试验,对上述4种量表的总体诊断效能进行了比较,结果发现TMS识别SM的ROC曲线下面积最高,但是4种量表总体诊断效能差异未见明显统计学意义。在近年1 项研究[48]中,也比较了FABS和TMS量表,并基于神经网络模型可得到多层感知器(multi-layer perceptron,MLP)构建预测模型。通过验证,该模型的总体诊断效能优于FABS和TM评分,但模型中的隐藏层是无法通过临床特征解释和表达的。虽然其预测效能较好,目前该研究还无法开发出基于MLP模型的具体评分系统,临床实用性较差。
急诊医生在接诊卒中样患者,尤其是溶栓时间窗内的患者时,须警惕SM的可能。尽管静脉溶栓在SM患者的出血性并发症发生风险很低,但这些并发症一旦发生,可能会危及生命,甚至需要紧急手术干预。因此,在众多的SM患者中,预防不必要的静脉溶栓及血管内治疗至关重要,同时对于原发性疾病的及时治疗对于患者的预后有积极的意义。但权衡早期溶栓的获益与SM患者溶栓的风险,不建议为了鉴别出所有的SM而对溶栓时间窗内的患者进行过多检查,以免延误大部分真性卒中患者最佳治疗时机。识别区分SM 和卒中的临床特征是一项挑战,在需要对卒中患者紧急诊治的情况下,耗时较短的非增强CT检查和仅依据病史及临床体征的SM评估量表及预测模型的结合可能会更好地识别“真性”卒中和“假性”卒中,是目前卒中早期诊疗过程中,亟待解决的临床热点问题之一。

