慢性肾脏病患者骨质疏松和心血管钙化情况与骨代谢标志物的相关性
夏凤芝 张凯
山东省单县东大医院肾内科,菏泽市 274300
慢性肾脏病(chronic kidney disease,CKD)是由多种原因引起的慢性肾脏结构和/或功能异常,并发症多、危害性大,是全球性的公共卫生问题[1]。相关研究报告指出,矿物质和骨代谢紊乱是CKD常见并发症,可引起免疫功能下降,诱发心血管钙化和骨质疏松等,严重影响患者预后[2-3]。因此,准确地评估CKD患者矿物质和骨代谢紊乱具有实际意义,可能对纠正矿物质和骨代谢紊乱、降低骨骼病变与心脑血管系统损伤发生风险具有一定的指导作用[4]。目前,临床上关于CKD患者心血管钙化、骨质疏松、骨代谢标志物水平的研究较多[5]。然而,关于CKD患者的骨代谢指标与生化指标和骨质疏松、心血管钙化发生情况之间的相关性研究较为少见。本研究探讨不同CKD分期患者骨质疏松和心血管钙化情况与骨代谢标志物的相关性,现报告如下。
1 资料与方法
1.1 一般资料 选取2020年1月12日至2022年2月1日我院收治的412例CKD患者作为研究对象。纳入标准:(1)符合美国K/DOQI指南[6]中CKD相关诊断标准;(2)年龄≥18岁;(3)临床病历资料完整。排除标准:(1)肾病综合征或肾小管酸中毒者;(2)合并结核性疾病或(和)恶性肿瘤者;(3)甲状腺功能异常或长期接受糖皮质激素、雌激素受体调节剂治疗者;(4)神志异常或合并神经系统疾病者;(5)正参与其他研究者。根据CKD分期标准[7],将研究对象分为CKD 3期组[估算肾小球滤过率(estimated glomerular filtration rate,eGFR)30 mL/(min·1.73 m2)~59 mL/(min·1.73 m2)]46例、CKD 4期组[eGFR 15 mL/(min·1.73 m2)~29 mL/(min·1.73 m2)]54例、CKD 5期组[eGFR<15 mL/(min·1.73 m2)]312例,另取60例同期健康体检者作为对照组。CKD匀3期组中,男性25例、女性21例;年龄35~77(54.22±10.33)岁;体质量指数(body mass index,BMI)18~28(22.52±2.61) kg/m2;原发病:糖尿病肾病14例、高血压肾病12例、慢性肾小球肾炎16例、其它4例。CKD 4期组中,男性29例、女性25例;年龄34~78(54.31±10.35)岁;BMI 18~28(22.58±2.63) kg/m2;原发病:糖尿病肾病16例、高血压肾病13例、慢性肾小球肾炎19例,其它6例。CKD 5期组中,男性182例、女性130例;年龄32~79(54.36±10.32)岁;BMI 18~29(22.61±2.60)kg/m2;原发病:糖尿病肾病94例、高血压肾病72例、慢性肾小球肾炎122例、其它24例。对照组中,男性32例、女性28例;年龄35~75(54.19±10.40)岁;BMI 19~27(22.57±2.52)kg/m2。CKD 3期组、CKD 4期组、CKD 5期组和对照组性别、年龄、BMI差异均无统计学意义,CKD 3期组、CKD 4期组和CKD 5期组原发病差异无统计学意义(均P>0.05),具有可比性。入组人员均签署研究知情同意书,本研究经医院伦理委员会审核并批准。
1.2 观察指标 采集疾病组入院后翌日、对照组体检当天清晨空腹静脉血5 mL,以8 cm为离心半径,3 000 r/min离心10 min,取上层血清,保存在-80℃冰箱中备用待检。
1.2.1 生化指标和骨代谢指标水平 采用美国雅培公司c16000全自动生化分析系统检测所有研究对象血清钙、磷、血肌酐水平。通过计算公式,(140-年龄)×体重(kg)÷血肌酐(μmol/L),男性再乘以系数1.23,女性再乘以系数1.04,计算出eGFR,一应操作遵循仪器说明书完成。应用酶联免疫吸附法检测血清全段甲状旁腺激素(intact parathyroid hormone,iPTH)水平,一应操作遵循试剂盒说明书完成,试剂盒购自美国DLS公司。应用罗氏化学发光法检测血清骨碱性磷酸酶(bone alkaline phosphatase,BALP)、1型前胶原氨基端肽(type 1 procollagen N-terminal peptide,P1NP)、β-1型胶原C-末端交联肽(β-crosslinked C-terminal telopeptide of type 1 collagen, β-CTX)水平,相关仪器和配套试剂均购自Roche公司。
1.2.2 骨质疏松情况 采用ASY-00409双能X线骨密度检测仪(购自美国Hologic公司)检测所有研究对象的骨密度,并参照中国老年学学会骨质疏松委员会制定的骨质疏松标准[8],评估所有研究对象骨质疏松情况。
1.2.3 心血管钙化情况 应用胸腹部CT评估所有研究对象主动脉和冠状动脉的钙化情况,以血管CT值≥130 HU作为心血管钙化的诊断标准。应用彩色多普勒超声检测评估所有研究对象心脏瓣膜钙化情况。心脏瓣膜钙化判定标准:主动脉瓣、二尖瓣、三尖瓣瓣叶或瓣环存在1个及以上>1 mm的强回声。
1.2.4 血清炎症因子水平 采用酶联免疫吸附法检测疾病组患者血清白细胞介素(interleukin,IL)-6、肿瘤坏死因子(tumor necrosis factor,TNF)-α、C反应蛋白(C-reactive protein,CRP)水平,应操作遵循试剂盒说明书完成,所有试剂盒均购自深圳晶美生物工程有限公司。
1.3 统计学处理 应用SPSS 22.0软件对数据进行统计分析。计数资料以例数和百分数表示,比较采用χ2检验。正态分布的计量资料以(x±s)表示,多组间均数的比较采用单因素方差分析,两两比较采用SNK-q检验;非正态分布的计量资料以M(P25,P75)表示,比较采用H检验。采用Spearman秩相关分析不同分期CKD患者骨质疏松和心血管钙化情况与骨代谢标志物的相关性。P<0.05为差异具有统计学意义。
2 结 果
2.1 各组生化指标的比较 CKD 3、4、5期组eGFR水平均低于对照组;随着CKD分期增加,CKD患者eGFR水平降低(均P<0.05)。CKD 3、4、5期组血清磷、iPTH水平均高于对照组;随着CKD分期增加,CKD患者血清磷、iPTH水平均升高(均P<0.05)。以上内容见表1。

表1 各组生化指标的比较 (x±s)
2.2 各组骨代谢指标的比较 CKD 3、4、5期组血清BALP、P1NP、β-CTX水平均高于对照组;随着CKD分期增加,CKD患者血清BALP、P1NP、β-CTX水平均升高(均P<0.05),见表2。
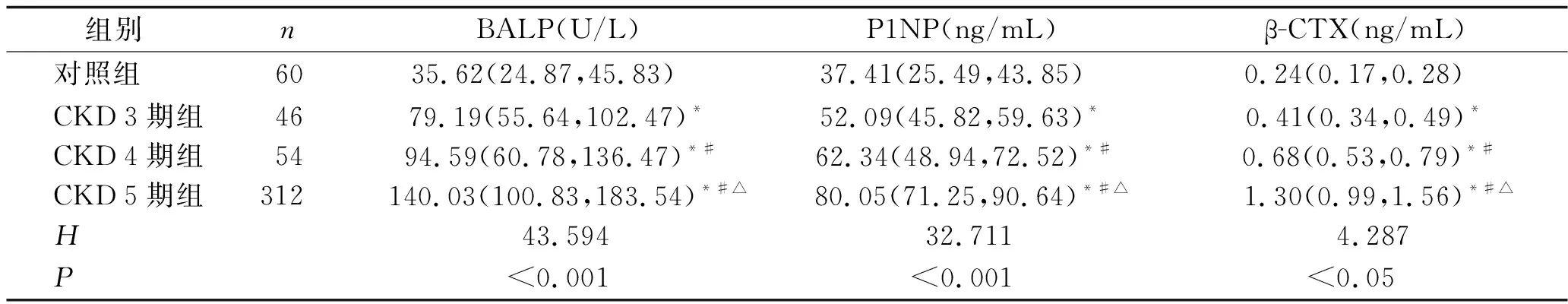
表2 各组骨代谢指标的比较 (x±s)
2.3 各组骨质疏松与心血管钙化情况的比较 CKD 5期组骨质疏松发生率高于对照组、CKD 3期组和CKD 4期组;CKD 3、4、5期组心血管钙化发生率均高于对照组;CKD 5期组心脏瓣膜钙化发生率高于对照组、CKD 3期组和CKD 4期组(均P<0.05),见表3。

表3 各组骨质疏松与心血管钙化情况的比较 [n(%)]
2.4 CKD患者骨质疏松、血管钙化、心脏瓣膜钙化与骨代谢标志物水平的相关性 Spearman秩相关分析结果显示,CKD患者骨质疏松、心血管钙化、心脏瓣膜钙化的发生与eGFR、血清钙水平均呈负相关,与血清磷、iPTH、BALP、P1NP、β-CTX水平均呈正相关(均P<0.05),见表4。
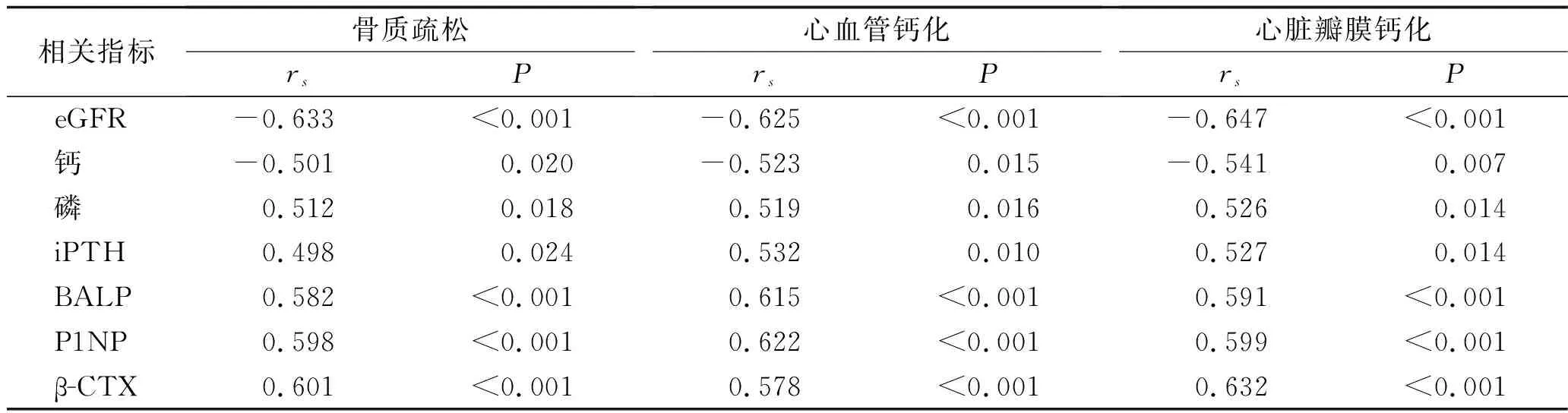
表4 CKD患者骨质疏松、心血管钙化、心脏瓣膜钙化情况与骨代谢标志物水平的相关性分析
2.5 不同分期CKD患者血清炎症指标水平的比较 随着CKD临床分期增加,CKD患者血清IL-6、TNF-α、CRP水平均升高(均P<0.05),见表5。

表5 不同分期CKD患者血清炎症指标水平的比较 (x±s)
3 讨 论
相关研究报告,CKD会引发多种临床表现,且不同分期CKD患者的临床表现存在一定的差异[9]。其中CKD 1~2期患者往往表现为腰膝酸软、夜尿增多等,极少患者出现轻度贫血。随着病情的不断进展,CKD 3期患者会出现胃肠道反应、内分泌紊乱、神经肌肉病变等明显症状,病情严重的患者甚至会有生命危险[10-11]。矿物质和骨代谢紊乱是CKD常见并发症,若未及时治疗,可能引起机体骨骼成分、结构发生明显改变,继而增加心血管事件和骨质疏松的发生风险,严重威胁患者的生存质量[12]。骨活检是目前诊断CKD患者矿物质和骨代谢紊乱的金标准,但其为有创检查,不利于临床推广普及[13]。因此,寻求有效的诊断、评估CKD病情的方法尤其重要,骨代谢指标是近年来关注的热点。
本研究结果发现,CKD 3、4、5期组血清磷、iPTH水平均异常,且患者血清磷、iPTH水平的异常程度随着CKD分期的增加越发明显;同时,CKD 5期组血清钙水平低于CKD 3、4期组和对照组。其原因可能为:肾脏主要滤过、重吸收和排出机体内的磷。CKD患者的肾小球滤过功能下降,影响尿磷排泄,致使血清磷水平升高;磷是钙敏感受体活性的调节因子,钙敏感受体可负性调节甲状旁腺激素分泌以控制钙离子平衡,高水平的磷可抑制钙敏感受体活性,促使甲状旁腺激素分泌增加,导致钙浓度降低[14]。这在Gao等[15]的研究报告中得以佐证:正常生理状态下,血清钙、磷、iPTH水平存在动态平衡,而CKD患者的上述平衡被打破,从而会表现出钙磷代谢异常和甲状旁腺功能亢进。本研究中,CKD 3、4、5期组血清BALP、P1NP、β-CTX水平均高于对照组,且随着CKD临床分期的增加,上述各项指标水平升高,这和蔡志岳等[5]的研究结果一致。BALP是一种由成骨细胞分泌的糖蛋白,其在机体内的含量不受eGFR的影响,可刺激机体内钙化,在反映骨转换状态方面具有较高的特异性。P1NP作为骨形成标志物之一,可有效地反映1型胶原合成与转换状态[16]。β-CTX是破骨细胞骨吸收过程中降解的特异性产物,是目前临床公认的骨吸收标志物之一。上述血清骨代谢指标水平的异常升高可能和肾小球滤过功能降低密切相关,肾小球滤过功能越差,机体内矿物质和骨代谢紊乱状态越显著。
Spearman秩相关分析结果显示,CKD患者骨质疏松、心血管钙化、心脏瓣膜钙化的发生与eGFR、血清钙水平均呈负相关,而与血清磷、iPTH、BALP、P1NP、β-CTX水平均呈正相关。这提示了eGFR和血清骨代谢指标水平均与CKD患者骨质疏松、心血管钙化密切相关。其原因可能为:血清钙、磷和iPTH表达异常可能影响骨钙的重吸收,继而影响细胞内钙超载和间质纤维化,引起骨痛、骨折和转移性钙化等过程,间接影响了血管钙化,最终增加心血管钙化和骨质疏松的风险。而BALP、P1NP和β-CTX水平的升高往往反映了CKD患者矿物质和骨代谢紊乱程度的加剧,继而增加骨质疏松和心血管钙化的风险[17-19]。本研究中,CKD 3、4、5期组血清IL-6、TNF-α、CRP等炎症细胞因子水平均依次升高。其原因可能是:肾脏在调节血清尿酸水平中起着重要作用,CKD患者分期越高,肾脏功能越差,导致尿酸水平升高,进而促进NLRP3炎症小体的异常激活,致使炎症细胞因子大量分泌[20]。
综上所述,随着CKD患者分期增加,矿物质和骨代谢紊乱越来越明显,且eGFR和血清骨代谢指标水平的异常程度增大,心血管钙化和骨质疏松风险增加。

