加味柴胡疏肝散基准样品HPLC 指纹图谱及关键质量属性量值传递规律研究
姜艳雯 ,邹恺平,陈梦娇 ,刘 顺,江志伟,曹 园*,龚冠闻*
1.南京中医药大学附属医院,江苏省中医院,江苏 南京 210000
2.南京中医药大学第一临床医学院,江苏 南京 210000
柴胡疏肝散(Chaihu Shugan Powder,CSP)是理气剂的代表方,载于明末医家张介宾所著《景岳全书》,主治胁肋疼痛、肝失疏泄等疾病[1]。加味柴胡疏肝散(Modified Chaihu Shugan Powder,MCSP)是在CSP 的基础上将芍药定为赤芍,加砂仁、法半夏、麸炒白术、木香以及厚朴花而成。本方以柴胡疏肝解郁、调畅肝气为君药,醋香附行气解郁,川芎活血止痛,二药相合共为臣药,助君药解肝胆气滞,促进气血津液的运行[2]。以陈皮、麸炒枳壳理气健脾[3],法半夏、麸炒白术降逆和胃,砂仁、木香、厚朴花消食行滞,赤芍养血柔肝、缓急止痛为佐药,甘草补益脾气,兼调诸药,亦为使药之用。虽由CSP加味,却可使其疏肝解郁、行气止痛之力大增,同时增加脾胃调理之用,脾胃健运,脏腑才能和顺协调,肝气调达,元气才能充沛,因此本方更适用于胆源性胰腺炎的治疗。
该方能有效减轻患者临床症状、改善黄疸指标、促进胰腺周围渗出的吸收,而且能促进早期肠内营养的应用,帮助患者减少脓毒症和器官功能不全的发生率,对于控制慢性胆囊炎、胆囊术后综合征也有非常好的疗效[4-6]。关于MCSP 的量值传递以及饮片的质量评价研究尚未见有文献报道。对MCSP 进行质量评价是保证临床用药安全有效的基础,亦是中药生产现代化和质量标准科学化的关键[7-9]。当前制剂的研究应以中药中特定核心质量物质的溯源和传递进行分析,对整体质量的动态变化进行控制,为MCSP 的可行性及质量提供保障[10-11],因此有必要开展MCSP 的量值传递规律研究以及饮片的质量评价。
本研究制备了40 批MCSP 基准样品,建立其指纹图谱,利用主成分分析(principal component analysis,PCA)和因子分析等化学计量学分析,结合指标性成分含量以及转移率,进行量值传递分析及整体质量研究,为中药复方制剂后续开发提供科学理论依据,也为经典名方CSP 的进一步研究打下基础。
1 仪器与材料
1.1 仪器
Waters Acquity Arc 型高效液相色谱仪,沃特世科技中国有限公司;Kudos SK6200H 型超声波清洗器,上海科导超声仪器有限公司;Cmdieip 型黑晶电陶炉3500 W,德国凯盟迪艾普公司;BP-211D 型电子分析天平,十万分之一,德国赛多利斯公司;AX224 型电子分析天平,万分之一,美国欧豪斯公司;HH-S6型数显恒温水浴锅,济南欧莱博科学仪器有限公司;RT-02A 型高速粉碎机,泓荃制药机械公司;HGZF-9203 型电热恒温鼓风干燥箱,上海精宏实验设备有限公司;煎药壶3.6 L,康舒旗舰店。
1.2 试剂
对照品去氢木香内酯(批号B21026)、芸香柚皮苷(批号220106)、新橙皮苷(批号B21390)、阿魏酸(批号131110A)、橙皮素(批号B20184)、橙皮苷(批号B20182)、咖啡酸(批号B20660)、柚皮苷(批号B21594)、芍药苷(批号B21148)、芍药内酯苷(批号B21149)、柴胡皂苷A(批号B20146)、柴胡皂苷D(批号B20150)、甘草苷(批号Z10J8X39611),质量分数均≥98%,均购自上海源叶生物科技有限公司;对照品甘草酸(批号160902,质量分数≥98%)、川陈皮素(批号210710,质量分数≥93%)均购自南京聚康医药化工有限公司。乙腈,色谱纯,美国Tedia 公司;磷酸,分析纯,成都市科隆化学品有限公司;屈臣氏纯净水,长江和记有限公司;其他试剂为分析纯。
1.3 饮片
不同产地及批次饮片经南京中医药大学附属医院江苏省中医院制剂部周琴妹主任中药师鉴定,柴胡为伞形科柴胡属植物柴胡BupleurumchinenseDC.的干燥根、陈皮为芸香科柑橘属植物橘Citrus reticulataBlanco 的干燥成熟果皮、香附为莎草科莎草属植物莎草CyperusrotundusL.的干燥根茎、川芎为伞形科藁本属植物川芎LigusticumchuanxiongHort.的干燥根茎、枳壳为芸香科柑橘属植物酸橙CitrusaurantiumL.的干燥未成熟果实、甘草为豆科甘草属植物甘草GlycyrrhizauralensisFisch.的干燥根和根茎、赤芍为毛茛科芍药属植物芍药Paeonia lactifloraPall.的干燥根、木香为菊科风毛菊属植物木香AucklandialappaDecne.的干燥根、砂仁为姜科豆蔻属植物阳春砂AmomumvillosumLour.的干燥成熟果实、半夏为天南星科半夏属植物半夏Pinellia ternate(Thunb.) Breit.的干燥块茎、厚朴花为木兰科厚朴属植物厚朴MagnoliaofficinalisRehd.et Wils.的干燥花蕾、白术为菊科苍术属植物白术AtractylodesmacrocephalaKoidz.的干燥根茎,以上饮片符合《中国药典》2020 年版项下相关规定。
通过随机数表法对表1 中MCSP 的饮片进行随机组合,其中对柴胡、川芎、陈皮、麸炒枳壳、木香及赤芍的指标性成分需进行产地分析,因此收集了不同产地多批次的饮片,其余6 味作为共有药味,重复使用,分别为厚朴花(批号220701,产地四川)、麸炒白术(批号220703,产地安徽)、法半夏(批号2207016,产地甘肃)、砂仁(批号20220901-01,产地云南)、醋香附(批号220702,产地河南)、甘草(批号220601,产地甘肃),随机组合结果见表2。

表1 MCSP 饮片来源信息Table 1 Source information of MCSP herbal pieces

表2 MCSP 随机组合Table 2 Random combination of MCSP
2 方法与结果
2.1 MCSP 基准样品的制备
MCSP 的样品煎煮方式参照《医疗机构中药煎药室管理规范》2009 年版的相关规定进行,以临床常用处方:柴胡、醋香附、赤芍、麸炒枳壳、川芎、陈皮、木香、砂仁、麸炒白术、法半夏、厚朴花以及甘草,加水至药面上方2~5 cm,浸泡30 min,武火(电陶炉2 200 W)煮沸后再煎煮30 min,200目滤网滤过,滤液放凉,二煎文火(电陶炉600 W)煎煮20 min,200 目滤网滤过,合并2 次滤液,加水调整体积为200 mL,即得MCSP 基准样品。
2.2 MCSP 基准样品指纹图谱研究
2.2.1 色谱条件 色谱柱为Waters X Select HSS T3柱(150 mm×4.6 mm,3.5 µm);流动相为乙腈-0.2%磷酸水溶液,梯度洗脱:0~5 min,0~5%乙腈;5~8 min,5%~8%乙腈;8~55 min,8%~20%乙腈;55~75 min,20%~30%乙腈;75~90 min,30%~35%乙腈;90~110 min,35%~65%乙腈;110~120 min,65%~5%乙腈;检测波长254 nm;体积流量1 mL/min;进样体积10 μL;柱温30 ℃。
2.2.2 供试品溶液的制备 精密吸取“2.1”项下制备的样品1 mL,70%甲醇超声15 min,定容至5 mL量瓶中,摇匀,静置,取上清液过0.22 μm 滤膜,即得。
2.2.3 对照品溶液的制备 分别取芍药苷、芍药内酯苷、橙皮苷、柚皮苷、橙皮素、新橙皮苷、阿魏酸、去氢木香内酯、甘草苷、甘草酸、咖啡酸、川陈皮素、芸香柚皮苷适量,精密称定,加甲醇配制成质量浓度为60.9、59.5、61.4、64.7、60.8、59.0、61.0、59.4、92.3、51.8、60.4、59.5、58.8 μg/mL 的混合对照品溶液。
2.2.4 指纹图谱方法学考察
(1)参照峰的选择:指纹图谱中,柚皮苷的含量较高,且色谱峰稳定,故选择柚皮苷(峰18)作为指纹图谱的参照峰,计算指纹图谱中各共有峰的相对保留时间和相对峰面积。
(2)精密度考察:取同一批MCSP 基准样品(S1),参照“2.2.2”项下方法制备供试品溶液1 份,按“2.2.1”项下色谱条件连续进样6 次,计算各共有峰相对保留时间和相对峰面积,结果显示,各共有峰相对保留时间的RSD 均<0.70%,相对峰面积的RSD 均<2.44%,表明仪器精密度良好。
(3)重复性考察:取同一批MCSP 基准样品(S1),参照“2.2.2”项下方法平行制备供试品溶液6 份,按“2.2.1”项下色谱条件进样,计算各共有峰相对保留时间和相对峰面积,结果显示各共有峰相对保留时间的RSD 均<0.07%,相对峰面积的RSD均<2.57%,表明该方法重复性好。
(4)稳定性考察:取同一批MCSP 基准样品(S1),参照“2.2.2”项下方法制备供试品溶液1 份,按“2.2.1”项下色谱条件,分别于制样后0、2、4、8、12、24 h 进样,计算各共有峰相对保留时间和相对峰面积,结果显示,各共有峰相对保留时间的RSD 均<0.13%,相对峰面积的RSD 均<2.13%,表明供试品溶液在24 h 内稳定性良好。
2.2.5 指纹图谱的建立及相似度的分析 取40 批MCSP 基准样品,按“2.2.2”项下方法制备,按“2.2.1”项下色谱条件进行测定。采用国家药典委员会“中药色谱指纹图谱相似度评价系统”(2012 版)软件对样品指纹图谱进行分析。以样品S1 的指纹图谱作为参照谱进行指纹匹配(平均数法,时间窗0.1 min),确定了29 个共有峰,并生成对照指纹图谱(R),40 批MCSP 基准样品的HPLC 指纹图谱叠加图见图1。40 批MCSP 基准样品(S1~S40)相似度结果分别为0.981 0、0.979 0、0.967 0、0.985 0、0.982 0、0.980 0、0.923 0、0.977 0、0.960 0、0.949 0、0.961 0、0.983 0、0.961 0、0.977 0、0.990 0、0.966 0、0.989 0、0.988 0、0.979 0、0.993 0、0.982 0、0.995 0、0.991 0、0.977 0、0.988 0、0.946 0、0.989 0、0.945 0、0.984 0、0.985 0、0.996 0、0.974 0、0.992 0、0.980 0、0.959 0、0.990 0、0.994 0、0.973 0、0.988 0、0.992 0。相似度均大于0.90,结果表明40 批MCSP 基准样品整体相似性较好。

图1 40 批MCSP 基准样品HPLC 的叠加指纹图谱和对照指纹图谱 (R)Fig.1 HPLC superimposed fingerprints of 40 batches of MCSP material benchmarks and its control fingerprint (R)
2.2.6 色谱峰指认及归属 将40 批MCSP 基准样品的对照图谱和各单味药的供试品溶液以及混合对照品溶液进行比较,结果见图2。指认出其中13 个共有峰,分别为咖啡酸(7 号峰)、芍药内酯苷(9号峰)、芍药苷(11 号峰)、阿魏酸(13 号峰)、甘草苷(15 号峰)、芸香柚皮苷(17 号峰)、柚皮苷(18号峰)、橙皮苷(19 号峰)、新橙皮苷(20 号峰)、橙皮素(22 号峰)、甘草酸(25 号峰)、川陈皮素(26号峰)、去氢木香内酯(29 号峰)。

图2 混合对照品和MCSP 样品的HPLC 图Fig.2 HPLC of mixed reference substances and MCSP sample
通过比对,发现大部分单味药的特征峰可传递到全方基准样品的对照谱图中,见图3。其中,峰21 归属于柴胡;峰7、29 归属于木香;峰9、11、14、16 归属于赤芍;峰13 归属于川芎;峰25、27归属于法半夏;峰15、23~25、27、28 归属于甘草;峰1、3~5 归属于醋香附;峰1~3、5、6、10、16、17、26 为麸炒枳壳与陈皮的共有峰;峰8、12、19、22 归属于陈皮;峰18、20 归属于麸炒枳壳。砂仁、厚朴花、麸炒白术在此条件下没有色谱信息。可见采用“2.2.2”项下工艺制备MCSP 样品时其主要成分从饮片-标准煎液形成较为完整的传递,且归属关系较为清晰。

图3 MCSP 基准样品与各单味药归属峰传递Fig.3 MCSP material benchmarks and attribution peak transmission of each single herb
2.3 指标性成分含量测定方法的建立
2.3.1 色谱条件
(1)柴胡皂苷A:色谱柱为Waters X Select HSS T3 柱(150 mm×4.6 mm,3.5 µm);流动相为乙腈-0.2%磷酸水溶液,洗脱梯度:0~3 min,0~5%乙腈;3~5 min,5%~22%乙腈;5~25 min,22%~36%乙腈;25~60 min,36%~50%乙腈;60~75 min,50%~25%乙腈;75~90 min,25%~5%乙腈;检测波长210 nm;体积流量1 mL/min;进样体积10 μL;柱温30 ℃。
(2)芍药内酯苷、芍药苷、阿魏酸、芸香柚皮苷、柚皮苷、橙皮苷、橙皮素、新橙皮苷、去氢木香内酯方法:同“2.2.1”项。
2.3.2 供试品溶液的制备
(1)柴胡皂苷A:精密量取MCSP 基准样品10 mL,置分液漏斗中,用水饱和正丁醇提取4 次,每次20 mL,合并滤液,用氨试剂洗至澄清,弃去洗液,蒸干,残渣加适量甲醇溶解,转移至5 mL 量瓶中,加甲醇至刻度,摇匀,静置,过0.22 μm 滤膜,检测柴胡皂苷A 的含量。
(2)芍药内酯苷、芍药苷、阿魏酸、芸香柚皮苷、柚皮苷、橙皮苷、橙皮素、新橙皮苷、去氢木香内酯:同“2.2.2”项下制法制备供试品溶液,检测芍药内酯苷、芍药苷、阿魏酸、芸香柚皮苷、柚皮苷、橙皮苷、橙皮素、新橙皮苷、去氢木香内酯的含量。
2.3.3 阴性样品溶液的制备 按处方量分别称取缺川芎、缺麸炒枳壳陈皮、缺木香、缺赤芍以及缺柴胡阴性处方,按“2.1”项下MCSP 基准样品制法制得相应的阴性样品,再按“2.2.2”项下制法制备阴性样品溶液。
2.3.4 对照品溶液的制备 分别取芍药内酯苷、芍药苷、阿魏酸、芸香柚皮苷、柚皮苷、橙皮苷、橙皮素、新橙皮苷、去氢木香内酯适量,精密称定,加甲醇配制成质量浓度分别为386.2、399.6、77.2、72.1、213.0、396.8、154.8、157.2、80.8 µg/mL 的混合对照品溶液;再称取柴胡皂苷A 适量,精密称定,加甲醇配制成质量浓度为613.7 µg/mL 的柴胡皂苷A 对照品溶液。
2.3.5 单味饮片含量测定溶液的制备 麸炒枳壳、陈皮、川芎、柴胡、木香以及赤芍含量测定供试品溶液的制备参照《中国药典》2020 年版各项下。
2.3.6 专属性考察 取“2.3.2”~“2.3.4”项下的供试品溶液、混合对照品溶液和阴性样品溶液,按“2.3.1”项下液相色谱条件进样测定,结果如图4 所示,10 种指标成分色谱峰于其相邻色谱峰之间的分离度良好,各阴性样品溶液色谱图在待测成分出峰位置无干扰,表明该方法下10 种成分专属性良好。

图4 MCSP 基准样品、阴性样品及对照品的HPLC 图Fig.4 HPLC of MCSP material benchmark, negative sample, and reference substance
2.3.7 线性关系考察 取不同质量浓度的指标性成分对照品溶液,采用“2.3.1”项下色谱条件进样测定,以质量浓度为横坐标(X),峰面积为纵坐标(Y),绘制标准曲线并计算线性回归方程,结果分别为柴胡皂苷AY=1.0×106X-12 375,R2=0.999 7,线性范围29.90~477.80 μg/mL;芍药苷Y=792 786X-17 584,R2=0.999 6,线性范围31.20~499.50 μg/mL;芍药内酯苷Y=326 798X-7 448.4,R2=0.999 3,线性范围30.20~482.80 μg/mL;橙皮苷Y=906 338X+604.76,R2=0.999 5,线性范围31.00~496.00 μg/mL;柚皮苷Y=674 948X-5 622.8,R2=0.999 9,线性范围41.60~665.50 μg/mL;新橙皮苷Y=622 048X-1 982.4,R2=0.999 6,线性范围30.70~491.30 μg/mL;橙皮素Y=154 174X+99.582,R2=0.999 6,线性范围30.20~483.80 μg/mL;阿魏酸Y=2.0×106X-1 148.7,R2=0.999 6,线性范围30.10~482.30 μg/mL;芸香柚皮苷Y=337 993X-1793,R2=0.999 5,线性范围28.20~450.50 μg/mL;去氢木香内酯Y=865 769X-615.74,R2=0.999 2,线性范围15.80~252.50 μg/mL;结果表明指标成分在各自的线性范围内线性关系良好。
2.3.8 精密度考察 取MCSP 基准样品(S1),按“2.3.2”项下(1)制备供试品溶液1 份,按“2.3.1”项下方法1 色谱条件,连续进样6 次;按“2.3.2”项下(2)制备供试品溶液1 份,按“2.3.1”项下方法2 色谱条件,连续进样6 次,各指标成分柴胡皂苷A、芍药苷、芍药内酯苷、橙皮苷、柚皮苷、新橙皮苷、橙皮素、阿魏酸、芸香柚皮苷、去氢木香内酯峰面积的RSD 值分别为2.06%、0.57%、0.70%、1.22%、0.12%、2.12%、0.78%、1.50%、2.44%、1.56%,均小于3%,表明仪器精密度良好。
2.3.9 稳定性考察 取MCSP 基准样品(S1),参照“2.3.2”项下(1)方法制备供试品溶液1 份,按“2.3.1”项下方法1 色谱条件,分别在制样后0、2、4、8、12、18、24 h 进行测定;参照“2.3.2”项下(2)方法制备供试品溶液1 份,按“2.3.1”项下方法2 色谱条件,分别在制样后0、2、4、8、12、18、24 h 进行测定,各指标成分柴胡皂苷A、芍药苷、芍药内酯苷、橙皮苷、柚皮苷、新橙皮苷、橙皮素、阿魏酸、芸香柚皮苷、去氢木香内酯峰面积的RSD值分别为1.73%、0.59%、0.65%、0.78%、0.68%、1.44%、0.26%、0.92%、2.13%、1.89%,均小于3%,结果表明供试品溶液在24 h 内稳定。
2.3.10 重复性考察 取MCSP 基准样品(S1),按“2.3.2”项下(1)方法平行制备6 份供试品溶液,按“2.3.1”项下方法1 色谱条件进样检测;按“2.3.2”项下(2)方法平行制备供试品溶液6 份,按“2.3.1”项下方法2 色谱条件进样检测,各指标成分柴胡皂苷A、芍药苷、芍药内酯苷、橙皮苷、柚皮苷、新橙皮苷、橙皮素、阿魏酸、芸香柚皮苷、去氢木香内酯峰面积的RSD 值分别为1.86%、1.52%、1.25%、1.38%、1.75%、2.47%、1.73%、1.69%、2.57%、1.76%,均小于3%,表明该方法的重复性良好。
2.3.11 加样回收率考察 精密称定已测知指标性成分含量的MCSP 基准样品(S1)6 份,分别按已知质量浓度的100%加入柴胡皂苷A 对照品溶液,按“2.3.2”项下(1)制备供试品溶液,并按“2.3.1”项下方法1 进样,检测得到柴胡皂苷A 的峰面积,计算其平均加样回收率为98.77%,RSD 为1.66%。
精密称定已测知指标性成分含量的MCSP 基准样品(S1)6 份,分别按已知质量浓度的100%加入对照品溶液,按“2.3.2”项下(2)制备为供试品溶液,并按“2.3.1”项下方法2 的条件进样检测,得到各成分的峰面积,计算得到芍药内酯苷、芍药苷、阿魏酸、芸香柚皮苷、柚皮苷、橙皮苷、新橙皮苷、橙皮素、去氢木香内酯的平均加样回收率分别为101.46%、102.07%、101.22%、102.57%、101.22%、102.75%、102.33%、102.05%、100.93%,其对应的RSD 值分别为1.40%、0.36%、0.61%、1.43%、1.74%、0.30%、0.98%、1.12%、1.02%。
2.4 MCSP 基准样品指标成分在饮片-水煎液间的量值传递分析
按“2.3.2”项下方法制备供试品溶液,按“2.3.1”项下色谱条件进行40 批MCSP 基准样品中10 个指标性成分的含量测定,各饮片按照《中国药典》2020年版进行含量测定,结果见表3。按公式计算饮片-样品中各指标成分含量的转移率[12],考察各指标性成分传递规律,分析异常值,结果见表4,不同产地的饮片指标性成分含量存在的差异,结果见表5。
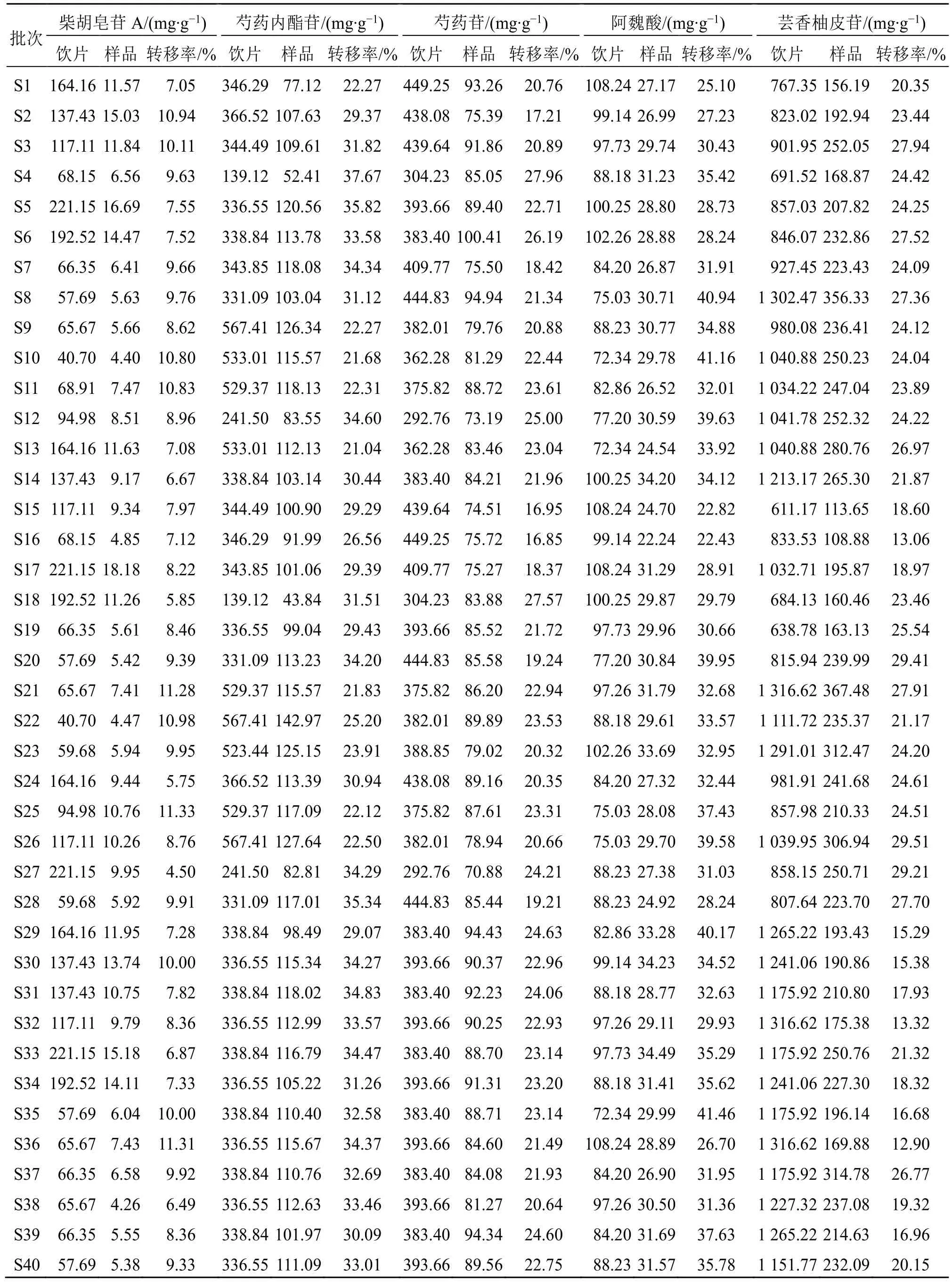
表3 饮片-基准样品中的含量及转移率Table 3 Content and transfer rate in herbal piece-benchmark sample
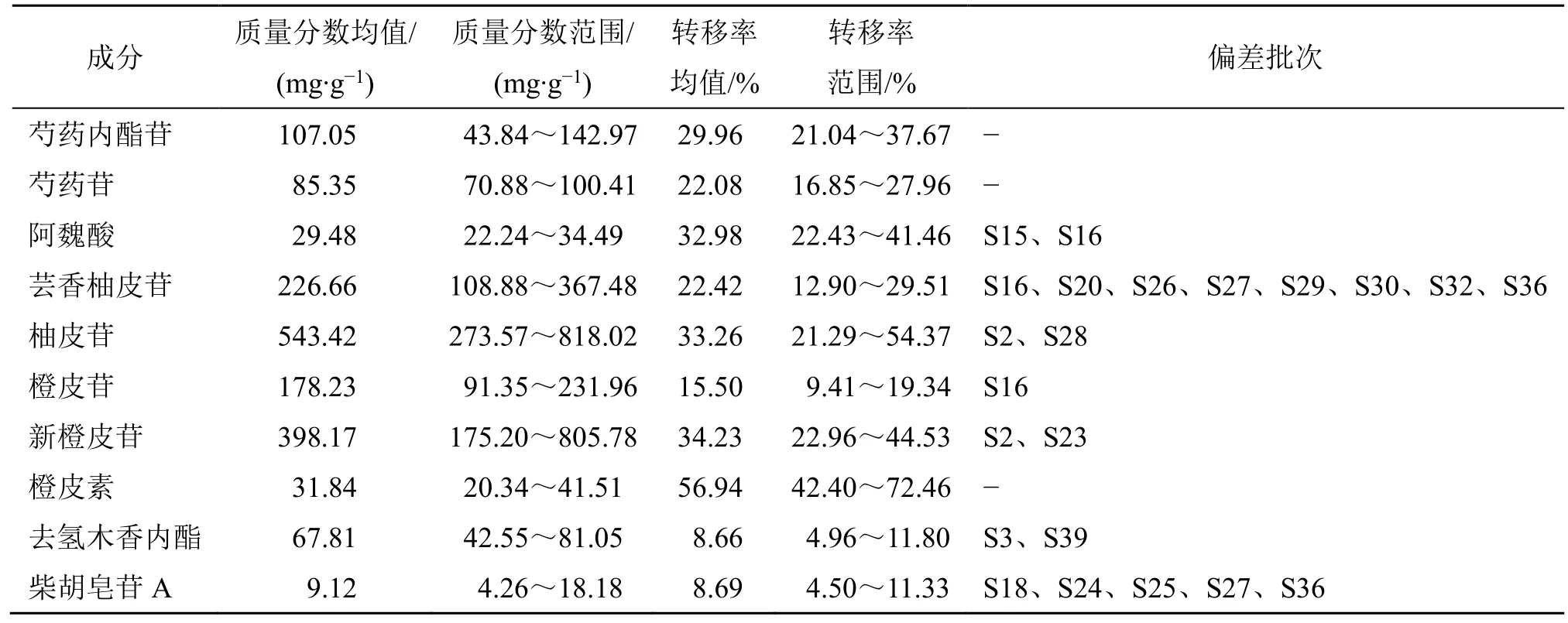
表4 样品含量及转移率分析Table 4 Sample content and transfer rate analysis
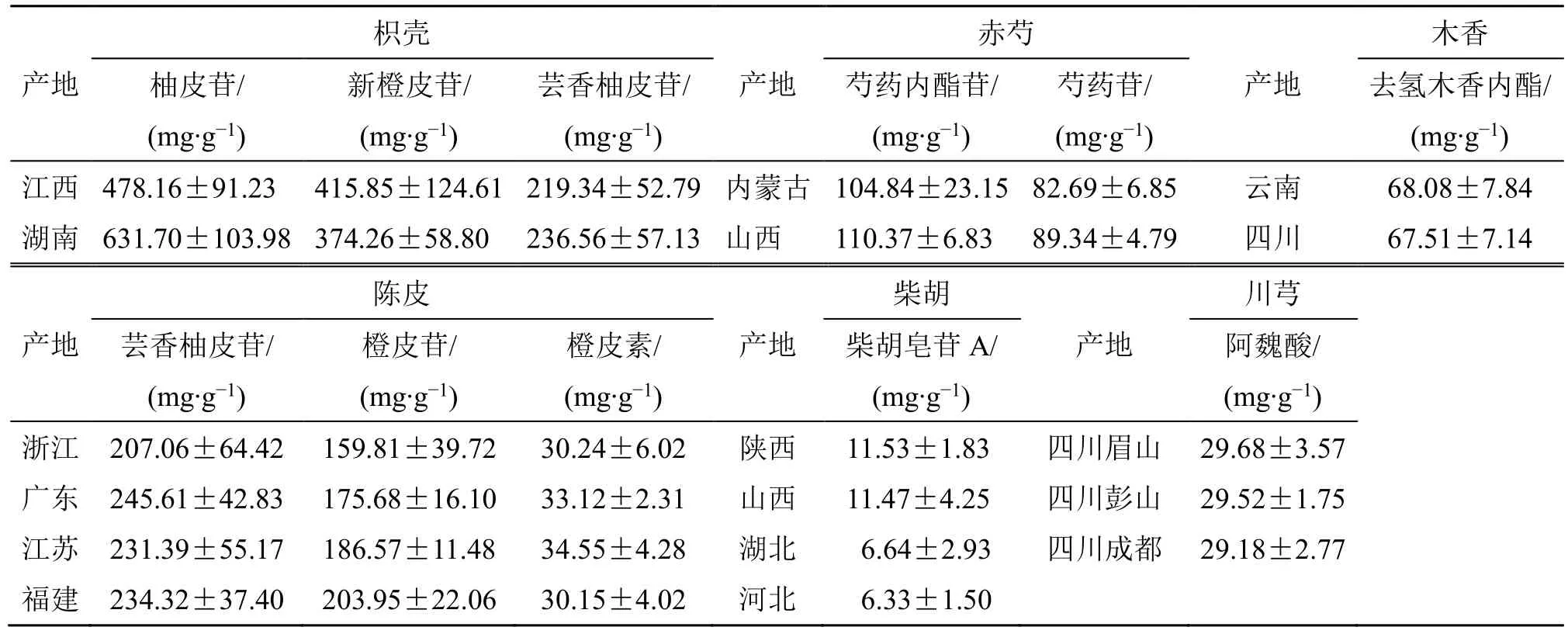
表5 HPLC 测定MCSP 中6 味饮片在不同产地下的指标性成分含量差异Table 5 Differences in content of indicator components of six herbs in MCSP under different origins determined by HPLC
转移率=wm/WM
w表示基准样品中有效成分的质量分数,m表示基准样品质量,W表示饮片中有效成分的质量分数,M表示饮片量
2.5 基于PCA 及因子分析对多批次饮片含量比较
PCA 是一种非监督的多元统计分析方法,可将多个指标转换为少数几个主成分,在不丢失太多信息的基础上,通过线性变换,将原始众多相关性的指标重新组合成新的相互独立的综合指标(主成分)来代替原始指标充分反映原始数据的信息[13-14],进一步构建因子模型,通过降维将少数具有代表性的综合因子诠释全部变量,将关系变量进行整理、归纳,从而揭示影响指标的最大因素。
为了进一步阐明MCSP 样品中各化学成分的差异,在多成分定量分析的基础上,采用PCA 及因子分析进一步深化研究,以所测定的10 个指标性成分的含量作为变量,导入至SIMCA 软件进行分析与比较,结果见图5。继而将含量进行标准化处理,导入SPSS 26.0 软件进行因子分析,其中KMO 与Bartlett 球形检验是检验因子分析适用性的相关测试,一般情况下,KMO>0.6 即可接受因子分析,本研究中,KMO 值为0.632 0,Bartlett 球形检验是用来判断相关矩阵是否为单位矩阵,如果为单位矩阵,表示各变量互相独立,不适合做因子分析,其显著水平值需要在0.05 以下,值越小表明原始变量之间的相关矩阵越不可能是单位矩阵,越适合做因子分析,本研究中Bartlett 球形检验的显著水平值为0.001(远小于0.05),表明数据可以进行因子分析,具体见表6。以累积贡献率>80%作为判定依据,提取到6 个成分,其累积方差贡献率为83.444%,表明这6个主成分可以代表83.444%的共有峰信息,因此可作为基准样品质量的评价指标。初始特征值和方差贡献率见表7。
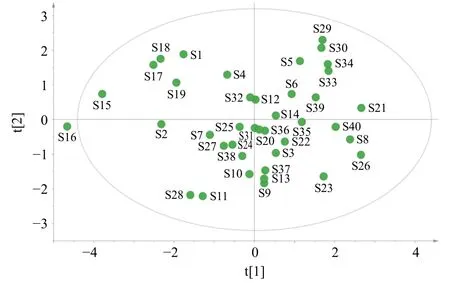
图5 MCSP 样品PCA 得分图Fig.5 PCA scores plot of MCSP samples

表6 KMO 和Bartlett 球形度检验结果Table 6 KMO and Bartlett sphericity test results

表7 特征值和方差贡献率Table 7 Characteristic value and variance contribution rate

表8 主成分因子载荷矩阵Table 8 Principal component factor loading matrix
用Kaiser 标准化最大方差法处理得到旋转成分矩阵,结果见表8。根据各色谱峰在6 个主成分上的载荷值,可提取出每个主成分所反映的信息。在主成分1 中芸香柚皮苷、橙皮苷、橙皮素是对第1主成分影响较大的特征向量,主要与陈皮有关;阿魏酸和柚皮苷是对第2 主成分影响较大的特征向量,主要与川芎、麸炒枳壳有关;芍药内酯苷是对第3 主成分影响较大的特征向量,主要与赤芍有关;而第4 主成分与柴胡皂苷A 呈高度正相关,是对其影响较大的特征向量,主要与柴胡有关;对第5 主成分影响较大的特征向量是去氢木香内酯;对第6主成分影响较大的特征向量是芍药苷,主要与赤芍有关。
选用6 个主成分因子对40 批MCSP 基准样品进行综合评价,以累积方差贡献率为分配系数,计算各批次样品主成分因子得分及综合得分,并对综合得分进行排序,建立一种客观的中药质量评价手段,结果见表9。综合得分(F)公式[15]:F=方差贡献率×相应的因子得分=0.291 4F1+0.153 6F2+0.121 3F3+0.099 9F4+0.085 6F5+0.082 4F6(F1~F6分别为主成分1~6 得分)。对综合得分排名前10的批次进行分析发现,麸炒枳壳以产地江西的批次占地居多,赤芍以内蒙古产地的居多,木香以云南产地的居多,川芎以四川彭山的居多,而陈皮与柴胡4 个产地平均分布,考虑这2 味饮片在市面上产地复杂,后期会增加批次,进一步细化分析,这也为选拔优质药材提供理论依据,为制剂开发提供更全面的质量评价。

表9 40 批MCSP 的主成分因子得分及综合排序Table 9 Principal component factor scores and comprehensive ranking of 40 batches of MCSP
3 讨论
3.1 色谱条件分析
本研究前期考察了不同提取溶剂的色谱信息,当70%甲醇作为溶剂时,图谱中色谱峰信息最丰富;各溶剂谱图的色谱信息丰富度依次为70%甲醇>50%甲醇>90%甲醇>纯甲醇>50%乙醇>70%乙醇>95%乙醇>无水乙醇。考察不同超声时长:5、10、15、20、30 min,发现15 min 以后指标性成分峰面积趋于稳定。依据现有文献[16],考虑到全方中极性较大的皂苷类、黄酮类成分较多,先后考察了甲醇、乙腈、不同比例的磷酸水相等因素,最后选用乙腈-0.2%磷酸水溶液为洗脱剂,以保证峰形的对称和平滑。综合考察结果确定前处理方法为取MCSP 样品1 mL,加入70%甲醇,超声15 min 后定容至5 mL,滤过。该方法保证了本研究过程的科学性与可靠性,也为类似方剂的研究提供了参考。
3.2 指标成分的选择
本研究前期对MCSP 基准样品进行200~400 nm 全波长扫描,比较分析不同波长条件下的峰数目、峰形、分离度等参数。发现在254 nm 处饮片中指标性成分的特征峰信息丰富且分离度较好,为了更好的体现饮片中指标性成分的特征峰信息,选取254 nm 对MCSP 样品指纹图谱进行考察,但柴胡皂苷类成分经过富集后在210 nm 处才有较大吸收,考虑其在本方中处于君药的地位,且柴胡皂苷类成分也具有明确的药理作用[17-18],故参考相关文献增加其含量测定方法[19-20],考察其传递规律,依据不同萃取次数后柴胡皂苷含量的变化,最后确定以水饱合正丁醇萃取4 次的方法进行研究,因此本实验选择210、254 nm 作为研究全方中多成分含量的检测波长。
通过对各单味药饮片的单煎液与全方的对比,发现大部分单味药的特征峰可传递到全方中,其中以麸炒枳壳与陈皮居多,其次是甘草、赤芍、醋香附、法半夏,木香、川芎、柴胡。因本研究采用了水煎煮的制备方法,臣药之一香附因其挥发性成分较多,而本方并未进行挥发油或蒸馏液的收集,故在基准样品中未检测到α-香附酮,这也说明从水煎液-基准样品的制备过程中,挥发油类成分有损失,且高效液相色谱仪有一定的检测限,故未能检测出相应成分[21],后续研究中将引入气相技术,构建更加完整的指纹图谱,揭示以臣药醋香附为代表的多个含有挥发性成分饮片的量值传递特征[22]。其次由于法半夏的炮制工艺需要用到甘草,液相中峰形较好且可指认的峰与甘草重复,半夏本身的成分在此方法下并未发现故未对法半夏深入研究,而甘草的临床使用目的是用于调和诸药,故在后续实验中也未将其纳入计划。
综合全方HPLC 指纹图谱以及药典相关规定,选择柴胡、赤芍、川芎、麸炒枳壳、陈皮、木香6 味以其所含芍药内酯苷、芍药苷、阿魏酸、芸香柚皮苷、柚皮苷、橙皮苷、橙皮素、新橙皮苷、去氢木香内酯、柴胡皂苷A 等具有明确药理活性的成分作为指标性成分进行定量考察[23-27]。
3.3 量值传递研究
通过指纹图谱量值传递研究发现,除主要药效成分为挥发油的厚朴花、麸炒白术、砂仁、醋香附这几味药外[28-30],大部分饮片的特征峰在饮片与基准样品间可以较为完整地传递。其中赤芍中指标性成分为芍药内酯苷以及芍药苷,其样品含量以及转移率均在平均值的70%~130%,未出现离散数据,说明该药物在全方中量值传递稳定,且2 个产地成分含量相似;川芎中指标性成分为阿魏酸,其质量分数为22.24~34.49 mg/g,木香中的指标性成分为去氢木香内酯,其质量分数为42.55~81.05 mg/g,大部分批次符合±30%的波动幅度,结合图5 可知这2 味饮片在不同产地不同批次的情况下含量也很稳定,分析其偏差数据出现的原因可能是因为煎剂易在过滤时少许沉淀附着在筛网上产生些许损耗,导致一些成分含量降低,后续会进一步增加批次,细化研究,减少误差与偶然性[31];麸炒枳壳、陈皮作为同科饮片[32-33],其成分相似,麸炒枳壳中特征性成分主要是芸香柚皮苷、柚皮苷以及新橙皮苷,陈皮中主要为芸香柚皮苷、橙皮苷与橙皮素,因芸香柚皮苷是共有成分,故其偏差较大,成分含量离散值较多,其余4 个成分含量大多符合±30%范围,分析原因可能是从药材到饮片的炮制、储藏过程中存在杂质,水分过多或过少导致,继而导致部分转移率的偏差,考虑是否根据实际情况将不同产地不同批次的饮片勾兑后投料,确保后续饮片和制剂质量的均一和稳定;柴胡作为君药[34-35],其主要化学成分为皂苷、黄酮、挥发油等,不同产地的柴胡中柴胡皂苷A 含量差距较大,陕西>山西>河北>湖北,因此建议对不同产地成分进行具体分析,以减少误差。
针对制剂的开发研究,决定其性能稳定疗效突出的关键在于突破基准样品的质量控制技术以及通过研究饮片-基准样品的关键质量属性在不同环节间的量值传递规律,才能不断提高中药的质量控制水平[36],本实验所测得的转移率大部分都在其均值的±30%范围内,总结原因可能是不同产地不同批次的药材在制备过程中受煎煮环境、储藏环境等因素影响导致指标成分转移率相差较大,后期制剂生产可考虑适当剔除部分批次转移率过低的饮片或采用混批投料方式来保证量值传递的均一性。后续研究将进一步增加基准样品研究产地与批次,以期建立更加具有代表性的基准样品相关质量标准[37]。
4 结论
经典名方是中医药传承与发展的基础和关键,研发改进经典名方不仅满足现代的用药需求,还能推动中医药事业的发展。但是经典名方的研究面临诸多问题,如药材溯源、剂量折算、临床效果等[38]。因而建立中药全产业链的品质传递过程关键评价技术体系是目前保障中药质量和疗效的关键[39]。MCSP 是在经典名方柴胡疏肝散的基础上进行的改进,本研究建立了MCSP 基准样品的指纹图谱,首先对其进行相似度分析,再根据色谱峰归属,将29个共有峰归属于9 味饮片,并指认出13 个化学成分。利用指纹图谱,建立多指标含量测定方法,结合转移率、化学计量学对MCSP 的量值传递过程进行研究分析,初步建立了科学稳定的基准样品质量评价方法,以期为MCSP 的后续开发及相关制剂的质量控制提供依据。同时,本研究所测定的10 个指标成分,来源于6 味饮片,其中9 个指标成分所归属的5 味饮片属于经典名方柴胡疏肝散,因此本研究也在一定程度上揭示了柴胡疏肝散中部分成分的量值传递关系,也为柴胡疏肝散的进一步研究打下了基础。
利益冲突所有作者均声明不存在利益冲突

