红簕钩中1 个新的齐墩果烷型降三萜
陈文娇,宁小燕#,黄美芳,卢澄生, ,梁臣艳, ,冯 旭, ,韦建华, *,王柳萍,
1.广西中医药大学药学院,广西 南宁 530200
2.广西优势中成药与民族药开发工程技术研究中心,广西 南宁 530200
3.广西中医药大学 中药学国家级实验教学示范中心,广西 南宁 530200
红簕钩为蔷薇科(Rosaceae)悬钩子属RubusL.植物梨叶悬钩子RubuspirifolicusSmith 的根和茎,别名铜罗紧、过山标、黄钻、红簕菜,广泛分布于广西来宾、金秀、蒙山、藤县、苍梧、岑溪等地[1-2]。作为广西民族特色药材,资源优势,疗效确切,具有活血止血、祛风散湿、消肿止痛的功效,常用于风湿性关节痛、肝脾肿大、慢性腹泻、月经不调、外伤等症,有“祛湿王”之称[3-4]。目前国内外对红簕钩的化学成分和药理作用研究较少。本课题组前期发现红簕钩中含三萜、鞣质、甾醇、黄酮等成分,并从红簕钩醋酸乙酯部位中分离鉴定29 个化合物[5-7],包括26 个三萜、2 个甾醇和1 个多酚类化合物。从中分离得到的三萜类成分均为五环三萜,推测此类化合物可能为红簕钩的主要特征性成分。现代研究发现,五环三萜类化合物具有抗肿瘤、肝保护、抗炎、神经系统保护等药理活性[8-9]。为进一步探究红簕钩的三萜类化学成分,丰富该植物的化学成分结构类型,阐明该药物的药效物质基础,本实验继续对红簕钩醋酸乙酯部位化学成分进行研究,并从中分离得到16 个化合物,分别鉴定为3,4-裂环-3-去甲基-齐墩果烷-4(23),13(18)-二烯-2,28-二羧酸[2,3-seco-3-nor-olean-4(23)-en-2,28-dioic acid,1]、acanthochlamic acid(2)、2α,3β-dihydroxyolean-13(18)-en-28-oic acid(3)、3-表-2-氧代-坡模醇酸(3-epi-2-oxopomolic acid,4)、2α,3α,19α,22α-tetrahydroxyurs-12-en-28-oic acid(5)、23-O-galloylarjungenin(6)、2α,3α,19α,24-四羟基齐墩果-12-烯-28-羧酸(2α,3α,19α,24-tetrahydroxyolean-12-en-28-oic acid,7)、bellericagenin B(8)、roburgenic acid(9)、2β,3β,19α-三羟基齐墩果-12-烯-23,28-二羧酸(2β,3β,19α-trihydroxyolean-12-ene-23,28-dioic acid,10)、2α,3β,23-trihydroxylup-20(29)-en-28-oic acid 28-O-β-D-glucopyranoside(11)、熊果酸(ursolic acid,12)、山楂酸(maslinic acid,13)、科罗索酸(corosolic acid,14)、坡模酸(pomolic acid,15)、齐墩果酸(oleanolic acid,16)。其中化合物1 为新化合物,命名为梨叶悬钩子酸A;化合物2~3、5~6、8~10 为首次从悬钩子属中分离得到,所有化合物均为首次从该植物中分离得到。
1 仪器与材料
Agilent G6230 型飞行时间质谱仪(美国Agilent公司);Bruker AVANCE II 500 型核磁共振波谱仪(德国Bruker 公司);赛默飞世尔NICOLET iS10 型中红外光谱仪(美国赛默飞世尔公司);岛津LC-20AR 型半制备液相色谱仪、岛津 LC-2030 PLUS 型高效液相色谱仪、岛津UV2401PC 型紫外可见分光光度仪(日本岛津公司);中低压半制备-REVELERIS X2 型液相色谱仪(美国格雷斯戴维森公司);Hypersil GOLDTM C18柱(250 mm×10 mm,5 μm,美国赛默飞世尔公司);BP211D 型电子分析天平(德国赛多利斯公司);EYELA OSB-2100 旋转蒸发仪(上海爱朗仪器有限公司);ZF-6 型三用紫外分析仪(上海嘉鹏科技有限公司);Sephadex LH-20(美国Pharmacia 公司);ODS 反相硅胶(40~60 μm,天津博纳艾杰尔科技有限公司);AB-8 大孔吸附树脂(天津市光复精细化工研究所);柱色谱硅胶(100~200、200~300 目,国药集团化学试剂有限公司);硅胶薄层板(青岛海洋化工有限公司);甲醇、乙腈(色谱纯,Fisher);所用常规试剂均为分析纯(四川西陇科学有限公司)。
红簕钩于2021 年1 月采于广西都安,经广西中医药大学廖月葵高级实验师鉴定为蔷薇科悬钩子属植物梨叶悬钩子R.pirifoliusSmith 的根和茎。标本(RPS-202101)存于广西中医药大学中药化学实验室。
2 提取与分离
干燥红簕钩粗粉50.0 kg,采用10 倍量80%乙醇回流提取3 次(2、2、1 h),减压浓缩得到总浸膏(8.2 kg)。总浸膏加适量水悬浮,依次用石油醚(60~90 ℃)、醋酸乙酯、正丁醇萃取,回收溶剂后得到石油醚部位浸膏(44.4 g),醋酸乙酯部位浸膏(823.5 g),正丁醇部位浸膏(3 691.2 g)和水部位浸膏(3 487.8 g)。醋酸乙酯部位浸膏700.0 g,经大孔吸附树脂(AB-8)柱色谱分离,乙醇-水系统(H2O→20%→30%→40%→60%→80%→95%)梯度洗脱,得到10 个组分(Fr.A~J)。Fr.F(53.0 g)经硅胶柱色谱分离,经氯仿-甲醇(30∶1→1∶1)梯度洗脱,得到7 个组分(Fr.F-1~F-7)。Fr.F-1(3.35 g)依次经ODS 中低压柱色谱(甲醇-水40∶60→70∶30,8.0 mL/min)、硅胶柱色谱(氯仿-甲醇1∶0→1∶1)和半制备HPLC(甲醇-水51∶49,3.0 mL/min)分离纯化,得到化合物5(16.1 mg,tR=33.4 min)。Fr.F-5(12.6 g)经ODS 中低压柱色谱(甲醇-水30∶70→85∶15,8.0 mL/min)分离,得到8 个组分(Fr.F-5-1~F-5-8)。Fr.F-5-4(1.4 g)依次经硅胶柱色谱(氯仿-甲醇20∶1→3∶1)和半制备HPLC(甲醇-水51∶49,一次制备;乙腈-水30∶70,二次制备,3.0 mL/min)分离纯化,得到化合物11(2.0 mg,tR=18.8 min)。Fr.F-5-5(3.5 g)经硅胶柱色谱(氯仿-甲醇30∶1→3∶1)分离,得到9 个组分(Fr.F-5-5-1~F-5-5-9)。Fr.F-5-5-3 经半制备HPLC(甲醇-水57∶43,3.0 mL/min)分离纯化,得到化合物7(4.4 mg,tR=28.8 min)。Fr.F-5-5-4(0.7 g)依次经Sephadex LH 20(氯仿-甲醇1∶1)和半制备HPLC(甲醇-水53∶47,3.0 mL/min)一次制备分离,得到化合物9(3.4 mg,tR=23.8 min)和组分Fr.F-5-5-4-(2)。Fr.F-5-5-4-(2) 经半制备HPLC(乙腈-水35∶65,2.0 mL/min)二次制备纯化,得到化合物8(5.9 mg,tR=31.0 min)、10(4.9 mg,tR=32.0 min)和6(1.9 mg,tR=33.6 min)。Fr.I(27.0g)经硅胶柱色谱(氯仿-甲醇49∶1→0∶1)分离,得到7 个组分(Fr.I-1~I-7)。Fr.I-1 和Fr.I-2(13.0 g)合并后经硅胶柱色谱(石油醚-醋酸乙酯,20∶1→0∶1)分离,得到8 个组分(Fr.I-1-1~I-1-8)。Fr.I-1-3(0.3 g)依次经Sephadex LH-20(氯仿-甲醇1∶1)和半制备HPLC(甲醇-水76∶24,3.0 mL/min)分离纯化,得到化合物2(3.4 mg,tR=27.8 min)和1(1.9 mg,tR=32.4 min)。Fr.I-1-6(1.4 g)经ODS 中低压柱色谱(甲醇-水,70∶30→95∶5),得到8 个组分在(Fr.I-1-6-1~I-1-6-8),其中Fr.I-1-6-7 中析出的白色粉末为化合物16(36.5 mg)。Fr.I-1-8(4.9 g)经ODS 中低压柱色谱(甲醇-水30∶70→90∶10)分离,得到8 个组分(Fr.I-1-8-1~I-1-8-8)。Fr.I-1-8-4(1.21 g)经硅胶柱色谱(石油醚-醋酸乙酯7∶1→1∶1),半制备HPLC甲醇-水(67∶37,3.0 mL/min)一次制备分离、乙腈-水(44∶56,3.0 mL/min)二次纯化,得到化合物4(1.7 mg,tR=41.1 min)。Fr.I-1-8-6(0.4 g)经硅胶柱色谱(石油醚-醋酸乙酯6∶1→1∶1)和半制备HPLC(甲醇-水70∶30,3.0 mL/min)分离纯化,得到化合物15(9.3 mg,tR=33.0 min)。Fr.I-1-8-7(0.3 g)经硅胶柱色谱(石油醚-醋酸乙酯5∶1→2∶1)和半制备HPLC(甲醇-水90∶10,3.0 mL/min)分离纯化,得到化合物12(24.5 mg,tR=19.4 min)。Fr.I-3(3.6 g)经ODS 中低压柱色谱分离,甲醇-水系统(60∶40→100∶0,8.0 mL/min)梯度洗脱,得到7 个组分(Fr.I-3-1~I-3-7)。Fr.I-3-4(0.60 g)经硅胶柱色谱(石油醚-醋酸乙酯4∶1→1∶1)和半制备HPLC(乙腈-水65∶35,3.0 mL/min)分离纯化,得到化合物3(7.5 mg,tR=15.1 min)。Fr.I-3-6(0.72 g)经硅胶柱色谱(石油醚-醋酸乙酯3∶1→1∶1)和半制备HPLC(甲醇-水82∶18,3.0 mL/min)分离纯化,得到化合物13(1.3 mg,tR=15.9 min)和14(4.4 mg,tR=17.2 min)。
3 结构鉴定

图1 化合物1 的结构及主要的HMBC、1H-1H COSY 和ROESY 相关信号Fig.1 Structure and key HMBC, 1H-1H COSY and ROESY correlations of compound 1
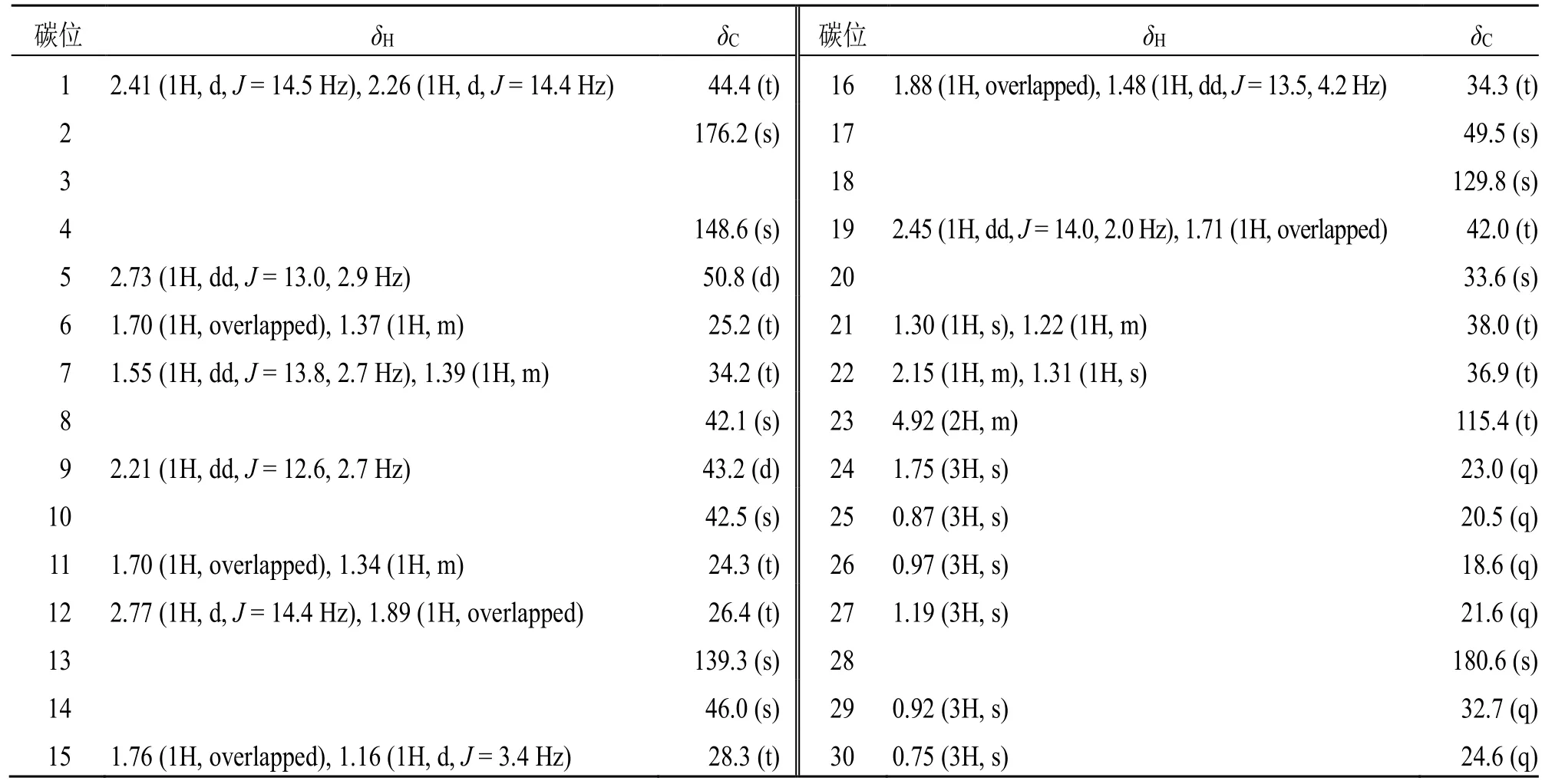
表1 化合物1 的1H-NMR (500 MHz) 和13C-NMR (125 MHz) 数据 (CD3OD)Table 1 1H-NMR (500 MHz) and 13C-NMR (125 MHz) data of compound 1 (CD3OD)
化合物2:白色针状结晶(甲醇)。ESI-MSm/z:455 [M-H]−。1H-NMR (500 MHz, CD3OD)δ: 4.91(2H, s, H-23), 4.72 (1H, s, H-29), 4.60 (1H, s, H-29),2.71 (1H, dd,J= 13.0, 3.0 Hz, H-5), 1.75 (3H, s,H-24), 1.70 (3H, s, H-30), 1.03 (6H, s, H-26, 27), 0.84(3H, s, H-25);13C-NMR (125 MHz, CD3OD)δ: 180.1(C-28), 176.1 (C-2), 151.9 (C-20), 148.8 (C-4), 115.2(C-23), 110.2 (C-29), 57.5 (C-17), 50.9 (C-5), 50.4(C-19), 48.5 (C-18), 44.1 (C-1), 44.0 (C-14), 43.0(C-9), 42.0 (C-10), 41.9 (C-8), 39.8 (C-13), 38.1(C-22), 33.8 (C-7), 33.3 (C-16), 31.7 (C-15), 30.9(C-21), 26.8 (C-12), 25.3 (C-6), 23.8 (C-11), 23.1(C-24), 20.2 (C-25), 19.5 (C-30), 16.4 (C-27), 15.1(C-26)。以上数据与文献报道基本一致[11],故鉴定化合物2 为acanthochlamic acid。
化合物3:白色无定型粉末。ESI-MSm/z: 495[M+Na]+。1H-NMR (500 MHz, CD3OD)δ: 3.65 (1H,t,J= 10.1 Hz, H-2), 2.96 (1H, d,J= 9.0 Hz, H-3),1.22 (3H, s, H-23), 1.03 (3H, s, H-27), 0.99 (3H, s,H-24, 26), 0.95 (3H, s, H-25), 0.81 (3H, s, H-29), 0.79(3H, s, H-30);13C-NMR (125 MHz, CD3OD)δ: 180.6(C-28), 139.1 (C-13), 129.8 (C-18), 84.5 (C-3), 69.7(C-2), 56.8 (C-5), 52.1 (C-9), 49.5 (C-17), 48.6 (C-1),45.6 (C-14), 42.7 (C-8), 42.0 (C-19), 40.5 (C-4), 39.6(C-10), 38.0 (C-21), 36.9 (C-22), 36.1 (C-7), 34.3(C-16), 33.6 (C-20), 32.7 (C-29), 29.3 (C-23), 28.3(C-15), 26.3 (C-12), 24.7 (C-30), 22.9 (C-11), 21.5(C-27), 19.5 (C-6), 18.4 (C-26), 18.2 (C-25), 17.4(C-24)。以上数据与文献报道基本一致[10],故鉴定化合物3 为2α,3β-dihydroxyolean-13(18)-en-28-oic acid。
化合物4:白色无定型粉末。ESI-MSm/z: 485[M-H]−。1H-NMR (500 MHz, CD3OD)δ: 5.29 (1H,t,J= 3.2 Hz, H-12), 3.50 (1H, s, H-3), 2.51 (1H, s,H-18), 1.38 (3H, s, H-27), 1.19 (3H, s, H-29), 1.00(3H, s, H-24), 0.96 (3H, s, H-25), 0.92 (3H, d,J= 6.7 Hz, H-30), 0.84 (3H, s, H-23), 0.79 (3H, s, H-26);13C-NMR (125 MHz, CD3OD)δ: 215.5 (C-2), 182.4(C-28), 140.2 (C-13), 128.8 (C-12), 83.7 (C-3), 73.6(C-19), 55.1 (C-18), 52.2 (C-1), 51.1 (C-5), 49.1(C-17), 48.6 (C-9), 43.6 (C-10), 43.1 (C-20), 42.9(C-14), 42.8 (C-4), 41.5 (C-8), 39.0 (C-22), 33.7(C-7), 29.6 (C-15), 27.3 (C-21), 27.2 (C-23), 27.0(C-29), 26.6 (C-16), 24.7 (C-27), 24.5 (C-11), 21.9(C-24), 20.1 (C-6), 17.1 (C-26), 17.0 (C-30), 16.6(C-25)。以上数据与文献报道基本一致[12],故鉴定化合物4 为3-表-2-氧代-坡模醇酸。
化合物5:白色无定型粉末。ESI-MSm/z: 503[M-H]−。1H-NMR (500 MHz, CD3OD)δ: 5.27 (1H,t,J= 3.4 Hz, H-12), 3.92 (1H, ddd,J= 11.9, 4.2, 3.1 Hz, H-2), 3.67 (1H, dd,J= 11.9, 4.3 Hz, H-23), 3.32(1H, d,J= 2.5 Hz, H-3), 2.45 (1H, s, H-18), 1.36 (3H,s, H-27), 1.15 (3H, s, H-29), 0.98 (3H, s, H-25), 0.98(3H, s, H-23), 0.95 (3H, d,J= 6.7 Hz, H-30), 0.86(3H, s, H-24), 0.80 (3H, s, H-26);13C-NMR (125 MHz, CD3OD)δ: 180.6 (C-28), 139.8 (C-13), 129.5(C-12), 80.1 (C-3), 75.7 (C-22), 73.2 (C-19), 67.2(C-2), 55.8 (C-18), 54.8 (C-17), 49.3 (C-5), 48.2(C-9), 43.2 (C-14), 42.5 (C-1), 41.4 (C-8), 41.3(C-20), 39.5 (C-4), 39.3 (C-10), 35.6 (C-21), 34.0(C-7), 29.2 (C-23), 29.0 (C-15), 26.7 (C-29), 25.2(C-27), 24.7 (C-11), 22.4 (C-24), 19.3 (C-6, 16), 17.5(C-26), 16.9 (C-25), 16.4 (C-30)。以上数据与文献报道基本一致[13],故鉴定化合物5 为2α,3α,19α,22αtetrahydroxyurs-12-en-28-oic acid。
化合物6:白色无定型粉末。ESI-MSm/z: 679[M+Na]+。1H-NMR (500 MHz, CD3OD)δ: 7.08 (1H,s, H-2'), 5.30 (1H, t,J= 3.5 Hz, H-12), 4.20 (1H, d,J= 11.3 Hz, H-23a), 4.05 (1H, d,J= 11.2 Hz, H-23b),3.74 (1H, td,J= 11.5, 4.5 Hz, H-2), 3.43 (1H, d,J=9.6 Hz, H-3), 3.22 (1H, d,J= 6.4 Hz, H-19), 3.04 (1H,brs, H-18), 1.28 (3H, s, H-27), 1.17 (3H, s, H-25),1.04 (3H, s, H-30), 0.92 (3H, s, H-29), 0.83 (3H, s,H-26), 0.75 (3H, s, H-24);13C-NMR (125 MHz,CD3OD)δ: 182.5 (C-28), 168.3 (C-7'), 146.6 (C-3',5'), 144.9 (C-13), 139.9 (C-4'), 124.6 (C-12), 121.6(C-1'), 110.0 (C-2', 6'), 82.5 (C-19), 78.1 (C-3), 69.3(C-2), 66.8 (C-23), 49.6 (C-5), 49.4 (C-9), 47.8 (C-1),46.7 (C-17), 45.2 (C-18), 44.1 (C-4), 42.6 (C-14), 40.8(C-8), 39.1 (C-10), 36.0 (C-20), 34.0 (C-22), 33.5(C-7), 29.5 (C-21), 29.3 (C-16), 28.7 (C-29), 28.6(C-15), 25.1 (C-27), 25.0 (C-30), 24.9 (C-11), 19.5(C-6), 17.8 (C-26), 17.3 (C-25), 13.7 (C-24)。以上数据与文献报道基本一致[14],故鉴定化合物 6 为23-O-galloylarjungenin。
化合物7:白色无定型粉末。ESI-MSm/z: 503[M-H]−。1H-NMR (500 MHz, CD3OD)δ: 5.31 (1H,d,J= 3.7 Hz, H-12), 3.89 (1H, m, H-2), 3.74 (1H, d,J= 2.5 Hz, H-3), 3.64 (1H, d,J= 11.4 Hz, H-24b),3.39 (1H, d,J=11.4 Hz, H-24a), 3.24 (1H, d,J=3.7 Hz, H-19), 3.04 (1H, brs, H-18), 1.30 (3H, s, H-27),1.08 (3H, s, H-29), 0.95 (3H, s, H-30), 0.94 (3H, s,H-26), 0.93 (3H, s, H-25), 0.73 (3H, s, H-23);13C-NMR (125 MHz, CD3OD)δ: 182.3 (C-28), 144.7(C-13), 124.7 (C-12), 82.4 (C-19), 74.6 (C-3), 67.0(C-2), 65.8 (C-24), 50.0 (C-5), 48.9 (C-9), 46.7(C-17), 45.4 (C-4), 45.2 (C-18), 42.7 (C-14), 42.4(C-1), 40.9 (C-8), 39.3 (C-10), 36.0 (C-20), 34.2(C-7), 34.0 (C-22), 29.5 (C-15), 29.4 (C-21), 28.7(C-29), 28.6 (C-16), 25.1 (C-30), 25.1 (C-27), 25.0(C-11), 23.1 (C-23), 19.5 (C-6), 17.7 (C-25), 17.2(C-26)。以上数据与文献报道基本一致[15],故鉴定化合物7 为2α,3α,19α,24-四羟基齐墩果-12-烯-28-羧酸。
化合物8:白色无定型粉末。ESI-MSm/z: 519[M-H]−。1H-NMR (500 MHz, CD3OD)δ: 5.31 (1H,t,J= 3.3 Hz, H-12), 4.04 (1H, d,J= 11.6 Hz, H-23a),4.03 (1H, d,J= 11.4 Hz, H-24b), 3.83 (1H, td,J=11.4, 4.5 Hz, H-2), 3.62 (1H, d,J= 11.4 Hz, H-24a),3.51 (1H, d,J= 11.6 Hz, H-23b), 3.45 (1H, d,J= 9.7 Hz, H-3), 3.24 (1H, d,J= 3.7 Hz, H-19), 3.05 (1H,brs, H-18), 1.30 (3H, s, H-27), 1.01 (3H, s, H-25),0.95 (3H, s, H-30), 0.93 (3H, s, H-29), 0.74 (3H, s,H-26);13C-NMR (125 MHz, CD3OD)δ: 182.3 (C-28),144.7 (C-13), 124.6 (C-12), 82.4 (C-19), 79.5 (C-3),69.8 (C-2), 64.5 (C-23), 62.6 (C-24), 49.3 (C-9), 48.4(C-5), 48.2 (C-4), 47.5 (C-1), 46.7 (C-17), 45.2(C-18), 42.6 (C-14), 40.7(C-8), 39.0 (C-10), 36.0(C-20), 34.0 (C-22), 33.7 (C-7), 29.5 (C-21), 29.4(C-15), 28.7 (C-29), 28.6 (C-16), 25.1 (C-11), 25.1(C-30), 25.0 (C-27), 19.8 (C-6), 17.6 (C-26), 17.3(C-25)。以上数据与文献报道基本一致[16],故鉴定化合物8 为bellericagenin B。
化合物9:白色无定型粉末。ESI-MSm/z: 533[M-H]−。1H-NMR (500 MHz, CD3OD)δ: 5.31 (1H,t,J= 3.2 Hz, H-12), 4.26 (1H, d,J= 2.1 Hz, H-3),4.22 (1H, dd,J= 11.4, 3.7 Hz, H-2), 4.00 (1H, d,J=10.2 Hz, H-23a), 3.80 (1H, d,J= 10.2 Hz, H-23b),3.24 (1H, d,J= 3.7 Hz, H-19), 3.05 (1H, brs, H-18),1.30 (3H, s, H-27), 0.95 (3H, s, H-30), 0.93 (3H, s,H-29), 0.91 (3H, s, H-25), 0.77 (3H, s, H-26);13C-NMR (125 MHz, CD3OD)δ: 182.4 (C-28), 178.8(C-24), 144.6 (C-13), 124.8 (C-12), 82.4 (C-19), 70.7(C-3), 67.5 (C-23), 67.1 (C-2), 55.0 (C-4), 48.3 (C-9),46.7 (C-17), 45.8 (C-5), 45.2 (C-18), 42.8 (C-14), 42.7(C-1), 40.6 (C-8), 39.9 (C-10), 36.0 (C-20), 34.0(C-22), 33.8 (C-7), 29.5 (C-21), 29.4 (C-15), 28.7(C-29), 28.6 (C-16), 25.2 (C-30), 25.0 (C-27), 24.9(C-11), 21.0 (C-6), 17.7 (C-26), 14.8 (C-25)。以上数据与文献报道基本一致[17],故鉴定化合物9 为roburgenic acid。
化合物10:白色无定型粉末。ESI-MSm/z: 517[M-H]−。1H-NMR (500 MHz, CD3OD)δ: 5.32 (1H,t,J= 3.2 Hz, H-12), 3.73 (1H, d,J= 9.7 Hz, H-2),3.63 (1H, td,J= 10.7, 4.1 Hz, H-3), 3.25 (1H, d,J=3.7 Hz, H-19), 3.05 (1H, brs, H-18), 1.30 (3H, s,H-27), 1.11 (3H, s, H-29), 1.02 (3H, s, H-30), 0.95(3H, s, H-26), 0.93 (3H, s, H-25), 0.75 (3H, s, H-24);13C-NMR (125 MHz, CD3OD)δ: 182.3 (C-28), 181.5(C-23), 144.7 (C-13), 124.5 (C-12), 82.4 (C-19), 81.0(C-3), 69.3 (C-2), 55.2 (C-4), 52.9 (C-5), 49.4 (C-9),48.1 (C-1), 46.7 (C-17), 45.2 (C-18), 42.6 (C-14), 40.8(C-8), 39.3 (C-10), 36.0 (C-20), 34.0 (C-22), 33.5(C-7), 29.5 (C-21), 29.4 (C-15), 28.7 (C-29), 28.5(C-16), 25.1 (C-27), 25.0 (C-30), 24.8 (C-11), 21.8(C-6), 17.6 (C-25), 17.3 (C-26), 12.8 (C-24)。以上数据与文献报道基本一致[18],故鉴定化合物10 为2β,3β,19α-三羟基齐墩果-12-烯-23,28-二羧酸。
化合物11:白色无定型粉末。ESI-MSm/z: 673[M+Na]+。1H-NMR (500 MHz, CD3OD)δ: 5.49 (1H,d,J= 8.2 Hz, H-1'), 4.71 (1H, d,J= 1.8 Hz, H-29a),4.60 (1H, s, H-29b), 3.83 (1H, dd,J= 11.7, 0.9 Hz,H-6'a), 3.69 (1H, overlapped, H-6'b), 3.65 (1H, m,overlapped, H-2), 3.48 (1H, d,J= 11.1 Hz, H-23a),3.41 (1H, m, H-3), 3.24 (1H, d,J= 11.0 Hz, H-23b),3.00 (1H, td,J= 10.9, 4.7 Hz, H-19), 1.69 (3H, s,H-30), 1.00 (3H, s, H-25), 0.95 (3H, s, H-26), 0.93(3H, s, H-24), 0.66 (3H, s, H-27);13C-NMR (125 MHz, CD3OD)δ: 176.1 (C-28), 151.8 (C-20), 110.3(C-29), 95.2 (C-1'), 78.8 (C-5'), 78.4 (C-3'), 78.1(C-3), 74.1 (C-2'), 71.1 (C-4'), 69.9 (C-2), 66.2(C-23), 62.4 (C-6'), 57.9 (C-17), 51.9 (C-9), 50.6(C-18), 48.4 (C-5, 19), 48.2 (C-1), 44.1 (C-4), 43.7(C-8), 42.0 (C-14), 39.3 (C-10), 39.2 (C-13), 37.5(C-22), 34.8 (C-7), 32.8 (C-16), 31.4 (C-21), 30.7(C-15), 26.8 (C-12), 22.2 (C-11), 19.5 (C-30), 19.0(C-6), 18.3 (C-25), 16.6 (C-26), 15.1 (C-27), 13.6(C-24)。以上数据与文献报道基本一致[19],故鉴定化合物11为2α,3β,23-trihydroxylup-20(29)-en-28-oic acid 28-O-β-D-glucopyranoside。
化合物12:白色无定型粉末。ESI-MSm/z: 479[M+Na]+。1H-NMR (500 MHz, CD3OD)δ: 5.24 (1H,s, H-12), 3.17 (1H, d,J= 9.7 Hz, H-3), 1.13 (3H, s,H-27), 0.98 (9H, d,J= 6.9 Hz, H-23, 24, 29), 0.89(3H, d,J= 6.2 Hz, H-30), 0.86 (3H, s, H-25), 0.78(3H, s, H-26);13C-NMR (125 MHz, CD3OD)δ: 181.7(C-28), 139.7 (C-13), 126.9 (C-12), 79.7 (C-3), 56.8(C-5), 54.4 (C-18), 43.3 (C-9, 17), 40.8 (C-14), 40.4(C-8), 40.0 (C-4), 39.8 (C-19), 38.1 (C-1, 20), 34.3(C-22), 31.8 (C-7), 29.2 (C-21), 28.8 (C-10), 27.9 (C-15,23), 25.3 (C-2), 24.4 (C-16), 24.1 (C-11), 21.6 (C-30),19.5 (C-6), 17.8 (C-26), 17.6 (C-29), 16.4 (C-24), 16.0(C-25)。以上数据与文献报道基本一致[20-21],故鉴定化合物12 为熊果酸。
化合物13:白色无定型粉末。ESI-MSm/z: 471[M-H]−。1H-NMR (500 MHz, CD3OD)δ: 5.28 (1H,t,J= 3.6 Hz, H-12), 3.65 (1H, ddd,J= 11.4, 9.9, 4.5 Hz, H-2), 2.94 (1H, d,J= 9.6 Hz, H-3), 2.90 (1H, dd,J= 13.8, 3.9 Hz, H-18), 1.19 (3H, s, H-27), 1.05 (3H,s, H-25), 1.04 (3H, s, H-23), 0.98 (3H, s, H-30), 0.94(3H, s, H-29), 0.86 (3H, s, H-26), 0.84 (3H, s, H-24);13C-NMR (125 MHz, CD3OD)δ: 145.5 (C-13), 123.3(C-12), 84.5 (C-3), 69.5 (C-2), 56.7 (C-5), 49.1 (C-9),48.2 (C-1), 47.8 (C-17), 47.4 (C-19), 43.0 (C-14), 42.8(C-18), 40.6 (C-4), 40.5 (C-8), 39.3 (C-10), 35.0(C-21), 33.9 (C-7, 22), 33.6 (C-29), 31.6 (C-20), 29.3(C-23), 28.9 (C-15), 26.4 (C-27), 24.6 (C-16), 24.1(C-11), 24.0 (C-30), 19.6 (C-6), 17.8 (C-24), 17.4(C-26), 17.1 (C-25)。以上数据与文献报道基本一致[22],故鉴定化合物13 为山楂酸。
化合物14:白色无定型粉末。ESI-MSm/z: 495[M+Na]+。1H-NMR (500 MHz, CD3OD)δ: 5.27 (1H,s, H-12), 1.15 (3H, s, H-23), 1.05 (6H, s, H-25, 27),1.00 (3H, s, H-24), 0.92 (3H, d,J= 6.0 Hz, H-30),0.88 (3H, s, H-29), 0.84 (3H, s, H-26);13C-NMR (125 MHz, CD3OD)δ: 181.8 (C-28), 139.8 (C-13), 126.7(C-12), 84.5 (C-3), 69.5 (C-2), 56.7 (C-5), 54.4(C-18), 49.1 (C-17), 48.3 (C-1, 9), 43.3 (C-14), 40.8(C-4), 40.5 (C-8), 40.4 (C-19, 20), 39.2 (C-10), 38.1(C-22), 34.2 (C-7), 31.8 (C-21), 29.5 (C-23), 29.2(C-15), 25.3 (C-16), 24.5 (C-11), 24.1 (C-27), 21.6(C-30), 19.5 (C-6), 17.8 (C-25), 17.6 (C-24), 17.5(C-29), 17.2 (C-26)。以上数据与文献报道基本一致[23],故鉴定化合物14 为科罗索酸。
化合物15:白色无定型粉末。ESI-MSm/z: 471[M-H]−。1H-NMR (500 MHz, CD3OD)δ: 5.27 (1H,t,J= 3.3 Hz, H-12), 3.14 (1H, dd,J= 11.4 , 4.7 Hz,H-3), 2.49 (1H, s, H-18), 1.32 (3H, s, H-27), 1.18 (3H,s, H-29), 0.97 (3H, s, H-23), 0.94 (3H, s, H-25), 0.92(3H, d,J= 6.7 Hz, H-30), 0.79 (3H, s, H-26), 0.77(3H, s, H-24);13C-NMR (125 MHz, CD3OD)δ: 182.3(C-28), 140.0 (C-13), 129.4 (C-12), 79.8 (C-3), 73.6(C-19), 56.7 (C-5), 55.1 (C-18), 48.3 (C-9), 48.6(C-17), 43.1 (C-20), 42.6 (C-14), 41.1 (C-8), 39.9(C-1), 39.8 (C-4), 39.0 (C-22), 38.1 (C-10), 34.2(C-7), 29.6 (C-15), 28.7 (C-23), 27.9 (C-2), 27.3(C-21), 27.1 (C-30), 26.6 (C-16), 24.8 (C-27), 24.7(C-11), 19.6 (C-6), 17.5 (C-26), 16.6 (C-29), 16.3(C-25), 15.9 (C-24)。以上数据与文献报道基本一致[24-25],故鉴定为化合物15 为坡模酸。
化合物16:白色无定型粉末。ESI-MSm/z: 455[M-H]−。1H-NMR (500 MHz, CD3OD)δ: 5.23 (1H,d,J= 3.6 Hz, H-12), 3.14 (1H, dd,J= 11.4, 4.8 Hz,H-3), 2.84 (1H, dd,J=13.9 , 4.1 Hz, H-18), 1.15 (3H,s, H-27), 0.96 (3H, s, H-30), 0.94 (3H, s, H-26), 0.93(3H, s, H-29), 0.90 (3H, s, H-25), 0.82 (3H, s, H-24),0.77 (3H, s, H-23);13C-NMR (125 MHz, CD3OD)δ:181.9 (C-28), 145.2 (C-13), 123.6 (C-12), 79.7 (C-3),56.8 (C-5), 49.1 (C-9), 47.6 (C-17), 47.2 (C-19), 42.9(C-14), 42.7 (C-18), 40.5 (C-8), 39.8 (C-1, 4), 38.2(C-10), 34.9 (C-21), 34.0 (C-22), 33.8 (C-7), 33.6(C-29), 31.6 (C-20), 28.8 (C-15), 28.7 (C-23), 27.9(C-2), 26.4 (C-27), 24.5 (C-11), 24.1 (C-16), 24.0(C-30), 19.5 (C-6), 17.7 (C-26), 16.30 (C-24), 15.9(C-25)。以上数据与文献报道基本一致[26],故鉴定化合物16 为齐墩果酸。
4 讨论
本实验从红簕钩醋酸乙酯部位中分离得到16个三萜类化合物,其中化合物1 为新化合物,所有化合物均为首次从该植物中分离得到。据文献报道,这些化合物有较好的药理活性,acanthochlamic acid(2)具有抗H1N1 流感作用[27],2α,3β-dihydroxyolean-13(18)-en-28-oic acid(3)、roburgenic acid(9)、熊果酸(12)、山楂酸(13)、科罗索酸(14)、坡模酸(15)、齐墩果酸(16)具有抗癌活性[17,28-33],3-表-2-氧代-坡模醇酸(4)具有抗氧化作用[34],bellericagenin B(8)具有抗菌活性[35],2α,3β,23-trihydroxylup-20(29)-en-28-oic acid 28-O-β-D-glucopyranoside(11)有较强的抗神经炎作用[19]。本研究丰富了红簕钩的化学成分,以期为该植物的药效物质基础提供科学依据,为其进一步开发利用提供参考,促进民族药资源的开发利用。
利益冲突所有作者均声明不存在利益冲突

