胱抑素C对慢性心力衰竭急性失代偿期老年患者的预后价值
张忠武 林璋 王世红
心力衰竭(heart failure ,HF)是各种心血管疾病的最终阶段,在我国35 岁以上的人群中,心力衰竭的标化患病率达到1.3%,预计患者人数达到890 万[1]。随着年龄增加,心衰的发病率和患病率也呈上升趋势,60 ~79 岁的人群发病率为3.09%,而80 岁及以上的人群高达7.55%[2]。慢性心力衰竭急性加重是心衰病程中的一个特殊阶段,也是老年患者住院的主要原因[3]。心衰从“稳定”到“失代偿”的过渡通常是逐渐发生的,客观的心衰加重指标有助于慢性心衰急性失代偿患者的诊断、评估和预防心衰加重。胱抑素C(cystatin C,CysC)是一种敏感反映肾功能变化的内源性生物标志物,同时也参与了多种心血管系统疾病的病理生理过程。目前的研究发现,HF 患者的CysC 水平明显升高,并且与心力衰竭患者的心脏功能和N 末端脑钠肽前体(N-terminal pro-brain natriuretic peptide,NT-ProBNP)水平呈正相关[4-5]。同时,CysC 水平的升高可能与HF 患者全因死亡和再住院风险的增加有关[6]。在急性心力衰竭患者中,CysC 也被认为是指导危险分层、预测新发心力衰竭和12 个月内死亡率的理想生物指标。然而,在慢性心力衰竭急性失代偿这种最常见的急性心力衰竭类型中,尤其是在老年患者中,对于CysC 的研究较为有限,缺乏关于其水平与疾病评估、疗效评价和预后的关系的数据。因此,本研究旨在探究慢性心力衰竭急性失代偿的老年患者在住院期间血清CysC 浓度的变化与病情严重程度之间的关系,并研究其在疾病治疗效果评估和预后评价中的价值。
1 资料与方法
1.1 一般资料
本研究纳入了2019 年1 月—2021 年12 月在福建省老年医院就诊的324 例老年患者(年龄≥65 岁)。其中男性193 例,女性131 例,年龄62 ~93 岁,平均(78.4±7.2)岁。其中,109 例慢性心力衰竭急性失代偿期患者为失代偿组,101 例慢性心力衰竭代偿期患者为代偿组,114 例心功能正常的患者为对照组。慢性心力衰竭纳入标准:存在心衰的症状和(或)体征;左室射血分数(left ventricular ejection fraction,LVEF)<40%或利钠肽升高,并符合至少以下一条:(1)左心室肥厚和(或)左心房扩大。(2)心脏舒张功能异常[7]。失代偿组纳入标准:在慢性心力衰竭诊断基础上,出现心衰症状和(或)体征的加重,需要调整药物治疗[7]。排除标准:终末期恶性肿瘤、围手术期急性心力衰竭、急性肺栓塞、正在接受血液透析、终末期肾功能不全、严重肝脏疾病、自身免疫性疾病。本研究经过医院医院伦理委员会批准[伦审科研第(20231103)号]。
1.2 方法
收集患者的人口学数据、病史、症状和体征,根据纽约心功能(New York Heart Function,NYHA)分级对心衰患者进行心功能分级。所有患者均接受经胸心脏彩色多普勒超声检查(transthoracic color doppler ultrasound of the heart,TTE),测量左室内径(left ventricular inner diamete,LVED) 和LVEF。24 h 内抽取静脉血样,检测血常规、肝功能、肾功能、CysC 和NT-proBNP 等指标。
1.3 观察指标
根据中国改良的简化肾脏病饮食改良研究公式(the modification of diet in renal disease equation,MDRD 公式)估算肾小球滤过率(glomerular filtration rate,GFR):GFR[mL/(min·1.73 m2)]=175×血肌酐-1.234×年龄-0.179×[0.79(女性)]估算肾小球滤过率。失代偿组治疗后复查CysC、NTproBNP,重新进行NYHA 心功能评价:Ⅰ级:日常活动量不受限制,一般体力活动不引起过度疲劳、心悸、气喘或心绞痛;Ⅱ级:一般体力活动引起过度疲劳、心悸、气喘或心绞痛;Ⅲ级:休息时无症状,但小于一般体力活动即可引起过度疲劳、心悸、气喘或心绞痛;Ⅳ级:休息状态下也出现心衰症状,体力活动后加重[7]。并同时进行临床疗效判定(显效:心功能改善2 级,症状、体征消失;有效:心功能改善1 级,症状体征有所改善;无效:心功能无明显变化或加重)[7]。
1.4 随访
对所有入选患者第3、6、9、12 个月进行电话随访,终点事件为心衰再入院及心源性死亡。以1 年内出现心血管事件患者为事件组,未发生心血管事件患者为非事件组。
1.5 统计学方法
采用SPSS 19.0 统计学软件进行分析。计量资料以(±s)表示,进行t检验;计数资料用n(%)表示,行χ2检验。两因素之间相关性采用Pearson 相关分析,多因素分析用Logistic 多元逐步回归分析。通过ROC 曲线,计算预测心血管事件(心衰失代偿再入院和心源性死亡)的敏感度和特异度。P< 0.05 为差异有统计学意义。
2 结果
2.1 各组临床特征、实验室指标及超声心动图指标对比
失代偿组与代偿组、心衰组(失代偿组+代偿组)与对照组在高血压、房颤、心率、CysC、GFR、肌酐、NTproBNP、LVEF 方面对比,差异均有统计学意义(P< 0.05),且随着心功能恶化,上述指标呈现出逐步升高或降低趋势,见表1、表2。
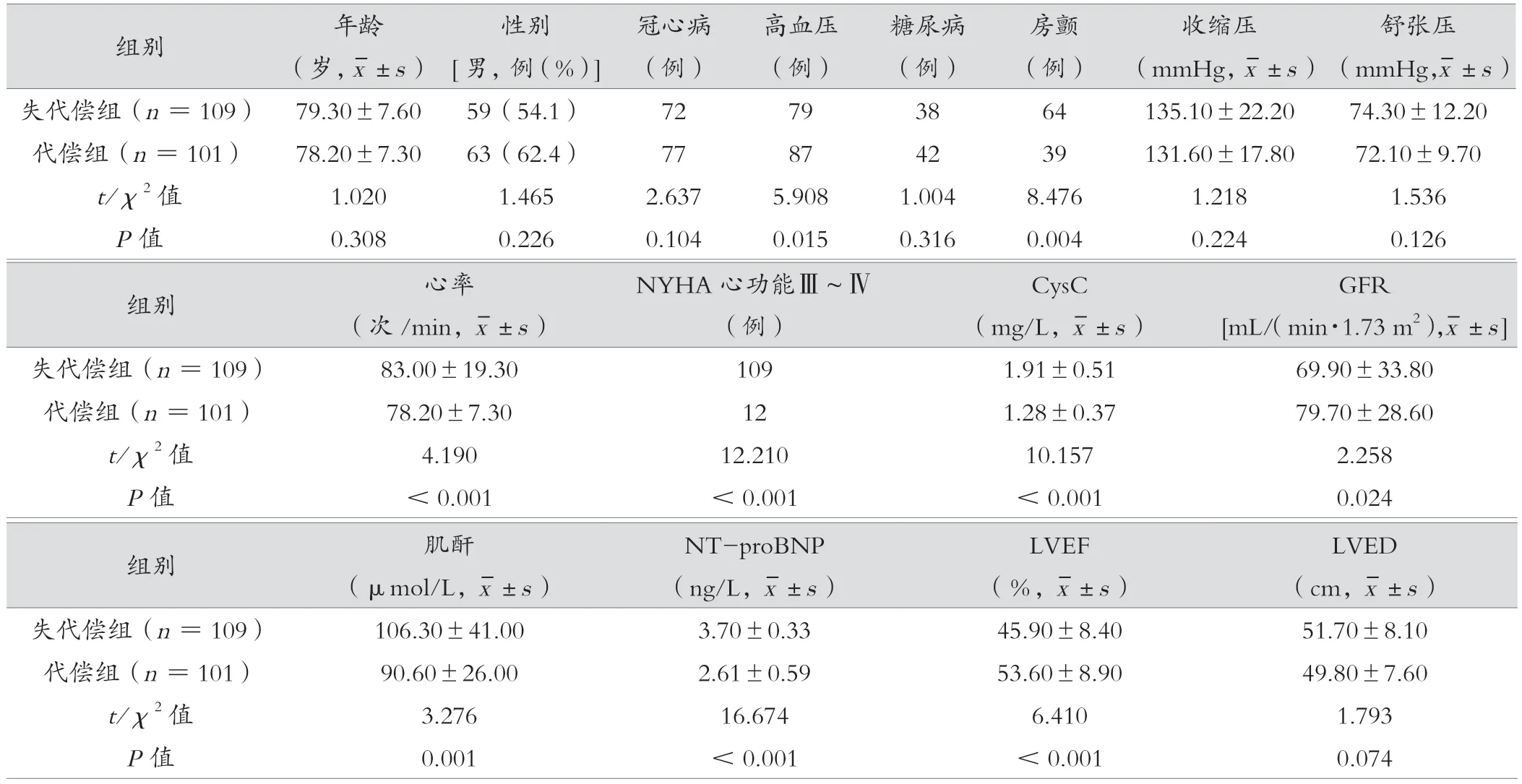
表1 失代偿组与代偿组一般资料及实验室、超声数据比较
2.2 CysC 与各指标相关性分析
CysC 与年龄、NYHA 心功能分级、肌酐、NT-proBNP、LVED 呈正相关(r=0.209、0.578、0.575、0.718、0.311,P< 0.05);与GFR、LVEF 呈负相关(r=-0.495、-0.527,P< 0.05)。采用偏相关分析校正年龄、GFR、肌酐的影响后,CysC 与NYHA 心功能分级、NT-proBNP、LVEF 相关(r=0.519、0.660、-0.459,P< 0.05)。
2.3 失代偿组治疗前后对比
失代偿组治疗后CysC、NT-proBNP 及心功能分级均有明显下降,差异有统计学意义(P< 0.05),而在GFR及肌酐方面治疗前后相比,差异无统计学意义(P> 0.05),见表3。根据NYHA 分级变化判断临床疗效,治疗达到有效及显效组治疗后CysC 水平(1.41±0.43)mg/L,无效组(2.75±0.49)mg/L,两组较治疗前分别下降(0.49±0.32)mg/L和(-0.68±0.41)mg/L,两组下降差值差异有统计学意义(t=9.83,P< 0.05)。以治疗后NT-proBNP 下降≥30%为治疗有效组,下降小于30%为无效组,有效组治疗后CysC 水平(1.38±0.41)mg/L,无效组(2.13±0.74)mg/L,较治疗前分别下降(0.51±0.32)mg/L 和(-0.12±0.59)mg/L,两组下降差值差异有统计学意义(t=6.69,P< 0.05)。

表3 心衰失代偿组治疗前后指标对比
2.4 事件组与非事件组对比
在109 例心衰失代偿患者中,出现了8 例住院死亡,住院病死率为7.3%。在1 年的随访中,28 例(25.7%)患者出现心功能恶化再次入院治疗,10 例(9.2%)出现心脏性死亡,总心血管事件发生率(心功能恶化再入院或心脏性死亡)为42.2%。两组在年龄、性别、既往病史方面差异无统计学意义(P> 0.05)。以1 年内出现心血管事件患者为事件组,未发生心血管事件患者为非事件组,事件组的CysC、NT-proBNP、LVED 水平明显高于非事件组;而入院收缩压水平、GFR、LVEF 低于非事件组,差异均有统计学意义(P< 0.05),见表4。经过Logistic 回归分析发现,CysC 水平和NT-proBNP 值是失代偿心衰患者1 年内发生心血管事件的独立预测因素,见表5。

表4 事件组与非事件组指标对比
2.5 胱抑素C 对心衰失代偿患者心血管事件预测
应用ROC 曲线得出CysC 曲线下面积0.805,预测心血管事件最佳截点为1.77 mg/L,其敏感度89.1%,特异性66.7% ;NT-proBNP 曲线下面积0.791,最佳预测截点为7 597.2 ng/L,敏感度56.5%,特异性92.1%,见图1。
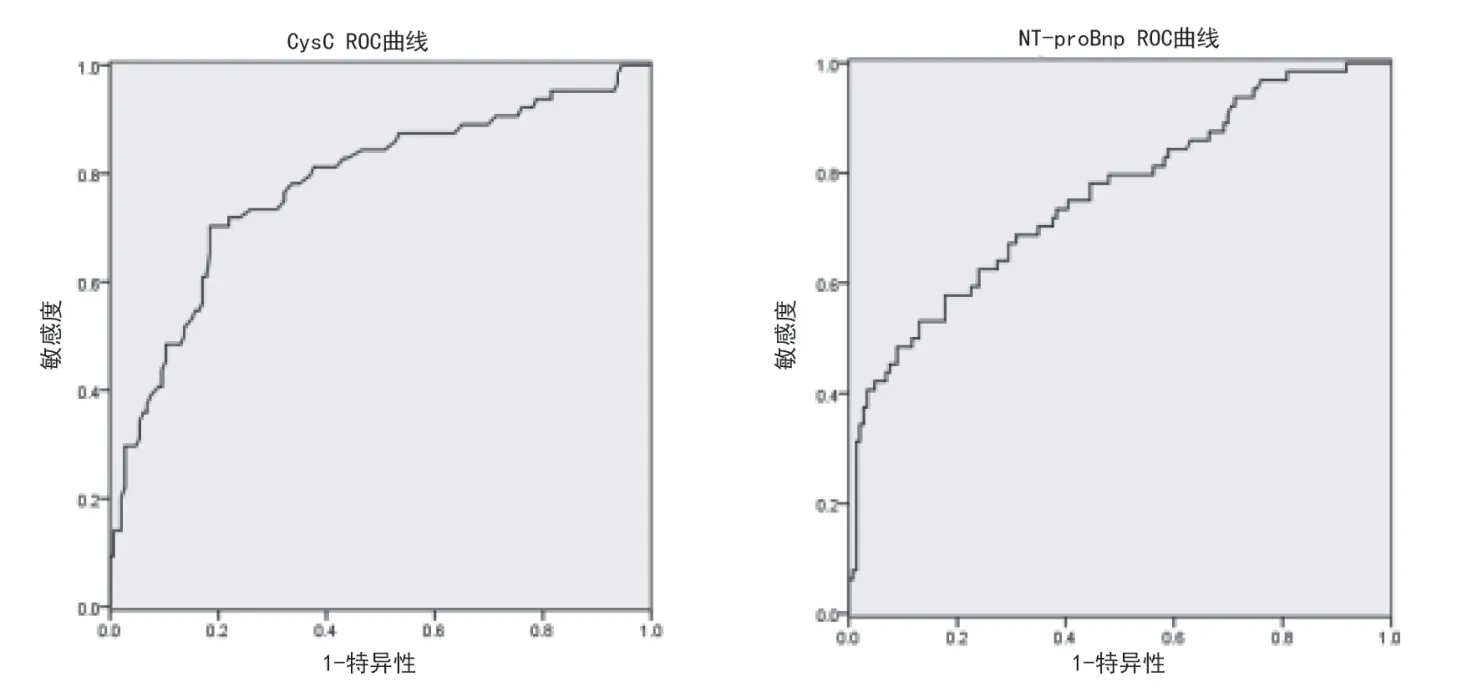
图1 老年心衰患者心血管事件预测ROC 曲线
3 讨论
CysC 是半胱氨酸蛋白酶抑制剂家族的一个成员。它受饮食和骨骼肌降解的影响较小,年龄、性别和其他因素也影响有限。最初,国内外学者普遍认为CysC 是一种敏感的肾功能生物标志物。然而,随着认识的深入,本研究发现CysC 也参与慢性心力衰竭(HF)的病理过程。CysC 水平升高与HF患者全因死亡和再住院风险的增加有关,而这种风险的增加可能与肌酐或尿素氮无关,进一步加强了CysC 在HF 患者中的应用价值[8]。
本研究发现,高水平的CysC与较差的NYHA心功能分级、升高的NT-proBNP 水平和降低的LVEF 有显著相关性。这揭示了在慢性心力衰竭急性失代偿的老年患者中,可以通过CysC 水平来评估患者的心功能和疾病严重程度。同时,在失代偿组治疗后,症状缓解和心功能改善的同时,CysC 和NTproBNP 的水平也明显降低。不论是以NYHA 分级还是NTproBNP 水平来评估临床治疗的效果,治疗有效组的CysC 水平都显著低于治疗无效组。因此,在慢性心力衰竭急性失代偿这种特殊且常见的病症中,即使是老年人群,CysC 仍然是一个理想的指标,可以用来指导病情观察和评估治疗效果。这与国外学者将CysC 作为心力衰竭的早期筛查和治疗目标一致[9-10]。
本研究中,发现事件组(心功能恶化再入院或心脏性死亡)的CysC 水平显著高于非事件组。Logistic 回归分析显示,CysC 水平及NT-proBNP 是失代偿心衰患者1 年内发生心血管事件的独立预测因素。这些结果表明,高CysC 与老年慢性心衰急性失代偿患者短中期心脏不良预后密切相关。肾脏的GFR 是心力衰竭患者全因死亡的可靠预测指标,其敏感度优于纽约心功能分级和左室射血分数。在心衰急性失代偿患者中,急性肾损伤(AKI)的发病率高达25%[11],准确评估GFR 对于疾病判断和早期基于指南的药物干预至关重要。在临床实践中,通常使用基于血清肌酐的公式来计算肾功能,然而血清肌酐(sCr)在肌肉减少症高发(如老年HF 患者)的疾病中准确性较低,进而影响了心衰治疗策略的制定。胱抑素C 可以更早、更准确地反应肾功能的变化,并可反映肾脏疾病的临床前状态[12-13],中国专家共识也推荐CysC 作为优于肌酐的心衰生物指标物[14]。另一方面,国外的研究也发现CysC 及基于CysC 公式计算的肾小球滤过率不能准确反映急性心力衰竭患者的GFR 变化[15]。因此,在老年慢性心力衰竭急性失代偿患者中,CysC 有助于指导临床决策和判断预后,但笔者也推荐联合使用多种生物标志物而非单一生物标志物。
CysC 与HF 患者的全因死亡风险存在阈值依赖的效益关系,每升高1 mg/L 的CysC 水平,全因死亡风险增加1 倍。RAFOULI等[16]研究发现,在急性心衰患者中,CysC 水平升高≥0.4 mg/L 时,60 d 终点事件的风险增加约45%。本研究通过ROC 曲线分析得出,CysC 在预测心血管事件方面的最佳截点为1.77 mg/L,其敏感度为89.1%,特异性为66.7%,其预测价值优于NTpro-BNP。CysC 与心血管疾病不良结局的风险相关,并且这种关系与肾功能无明显相关[17-18]。Cys-C 可能通过影响心室重构、凝血功能、脂质过氧化、动脉粥样硬化、平滑肌细胞功能和内皮细胞功能、炎症反应等来对心血管系统造成损害。在慢性心力衰竭急性失代偿的老年患者中高水平的CysC 对短中期不良预后具有良好的预测价值;对于高CysC 患者,通过早期预防、积极干预能有效降低其心血管事件风险,研究结果为后续中国心力衰竭诊断和治疗指南标准制定提供了一定借鉴。
本研究存在着一些局限性。首先,该研究为单中心研究,样本量相对较小。其次,未能排除肥胖、炎症、容量负荷以及利尿剂使用等多种可能影响CysC 水平的因素,这可能对试验结论产生影响。
综上所述,CysC 与慢性心衰急性失代偿患者的NYHA心功能分级、NT-proBNP 水平呈正相关,与LVEF 值呈负相关,可作为指导临床疗效的理想指标。同时,CysC 在预测慢性心衰急性失代偿患者短中期再入院及心源性死亡方面具有预测价值,其最佳截点值为1.77 mg/L。

