基于电位滴定法测定氧化铁粉中氯离子
史伟萍,陈志桐,董娜娜,郭彦英
(河钢集团邯钢公司,河北 邯郸 056003)
0 引言
由于热轧钢板表面黏附着大量氧化铁皮,在进入冷轧工序前,需经过酸洗工艺去除表面的氧化铁皮,否则,带钢会在冷轧过程中产生质量缺陷[1-5]。为了节约资源,同时减少环境污染,酸洗工序产生的废液由酸再生系统进行回收再利用,在此过程中,将废液中的铁离子转化成氧化铁粉[6]。氧化铁粉是无机颜料和磁性材料的重要原料,具有很高的附加价值[7-8]。不同的应用领域对氧化铁粉的品质提出了不同的要求。影响氧化铁粉品质的因素主要有杂质元素(如硅、钙、锰、硫、铝和氯等)和其物理性能(如比表面积、松装密度和颗粒度等)。氯离子作为杂质元素之一,需要重点监控检测,主要是由于氧化铁粉中氯离子含量过高,在后续磁性材料生产过程中会腐蚀设备、污染环境、制约磁性铁氧体的生产工艺,对成品性能产生不利影响[9-11]。GB/T 24244—2009《铁氧体用氧化铁》标准[12]对不同品级氧化铁粉中氯离子含量做了严格的规定,最高不超过0.25%。因此,准确检测氧化铁粉中氯离子含量十分重要。标准要求采用自动电位滴定法分析氧化铁粉中的氯离子含量,但未明确该方法的测试条件,对于使用磷酸的原因也并未进行说明。针对上述问题,本文通过优化自动电位定法测定氧化铁粉中的氯离子含量的分析条件,使分析结果更加准确、可靠。
1 实验准备
1.1 仪器
T50 型自动电位滴定仪(瑞士梅特勒—托利多分析仪器公司)、复合银环智能电极DMi141-SC(瑞士梅特勒—托利多分析仪器公司)和电子天平(Sartorius科学仪器公司)。
1.2 试剂
1)硝酸银(AgNO3)标准溶液(0.01 mol/L):称取1.76 g AgNO3(分析纯),加水溶解并定容至1 000 mL棕色容量瓶中。使用前,利用自动电位滴定仪进行标定。
2)氯离子(Cl-)标准溶液(0.1 mg/mL):称取0.164 9 g 氯化钠工作基准试剂(500~600 ℃灼烧至恒重),加水溶解并定容至1 000 mL 容量瓶中。
3)10%硝酸(体积分数)、10%磷酸(体积分数)和10%醋酸(体积分数)。
4)氧化铁粉标准样品:GSB 03—1552—2003(上海材料研究所)。
2 实验方法
2.1 仪器状态检验
首先,对仪器的状态进行确认,具体操作如下:取10 mL Cl-标准溶液(0.1 mg/mL),加50 mL 去离子水,采用0.01 mol/L AgNO3标准溶液进行滴定,滴定结果为(100±1)×10-6,说明仪器状态良好。
2.2 实验操作
称取一定量的氧化铁粉试样,加50 mL 去离子水、10 mL 10%磷酸,以0.01 mol/L 的AgNO3标准溶液作为滴定试剂,利用自动电位滴定仪进行滴定。自动电位滴定仪通过电位值变化自动识别终点,并根据计算公式进行计算,结果以百分含量(质量比)表示。每次完成分析检测,要对电极、加液管及搅拌桨进行清洁,防止残留在电极、加液管及搅拌浆上的氧化铁粉及氯化银沉淀对下一次测试造成影响,同时,也能防止电极表面氧化,导致信号传输延迟,影响分析结果。
2.3 分析结果计算
氯离子在试样中质量分数为:
式中:V 为消耗AgNO3标准溶液的体积,mL;V0为空白消耗AgNO3标准溶液的体积,mL;c 为AgNO3标准溶液的浓度,mol/L;m 为试样量,g;35.45 为氯的相对原子质量,g/mol。
3 实验内容
3.1 称样量
称样量对检测结果和检测成本有着很大影响。称样量过少,缺少取样代表性,分析结果误差大,对生产不能起到较好的指导作用。称样量过大,滴定试剂消耗量大,增加检测成本,而且过多的试样会延长滴定时间,影响报出结果的时效性。氧化铁粉生产试样,w(Cl-)大多在0.1%~0.3%之间,使用0.01 mol/L AgNO3标准溶液测定,当AgNO3标准溶液消耗达2 mL左右时,既能满足仪器精度要求,又能兼顾检测成本。通过理论计算,得出氧化铁粉试样称样量在0.24~0.71 g 之间。因此,将称样量定为0.5 g,并选取不同氯离子含量的氧化铁粉试样和标准样品进行试验,确定称样量的合理性。具体试验操作如下:分别称取w(Cl-)为0.1%、0.2%和0.3%左右的氧化铁粉试样以及w(Cl-)为0.1%的氧化铁粉标准样品各4 个,加入10 mL 10%磷酸、50 mL 去离子水,对氧化铁粉试样及标准样品中的氯离子含量进行测定,结果如表1 所示。
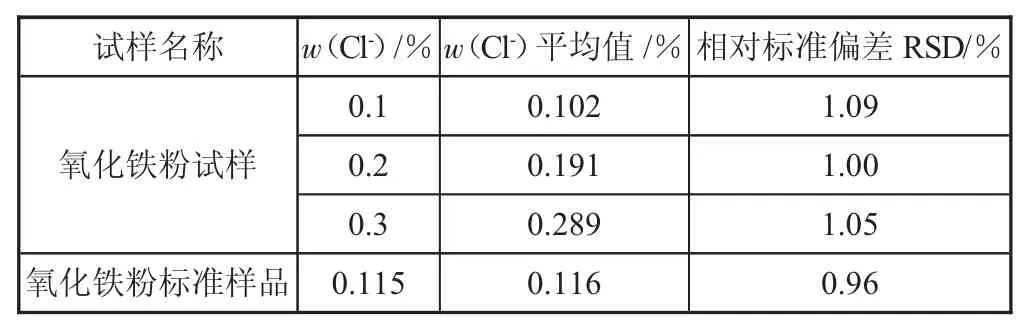
表1 不同氯离子含量的氧化铁粉和标准样品分析结果(n=4)
从表1 的分析结果可以看出,称样量为0.5 g 时,w(Cl-)为0.1%、0.2%和0.3%的氧化铁粉试样分析结果的相对标准偏差(RSD)分别为1.09%、1.00%和1.05%。分析结果的重复性能够满足生产要求。同时,对w(Cl-)为0.1%的氧化铁粉标准样品进行了四平行测试,其相对标准偏差为0.96%,稍优于氧化铁粉试样,可能是由于氧化铁粉标准样品的均匀性更好一些。因此,称样量取0.5 g 能够满足分析要求。
3.2 酸的种类
选取磷酸、硝酸和醋酸进行对比实验,讨论测定氧化铁粉中氯离子时,加酸与否及加入酸的种类对分析结果的影响。每组试验平行分析4 次,实验结果如表2 所示。
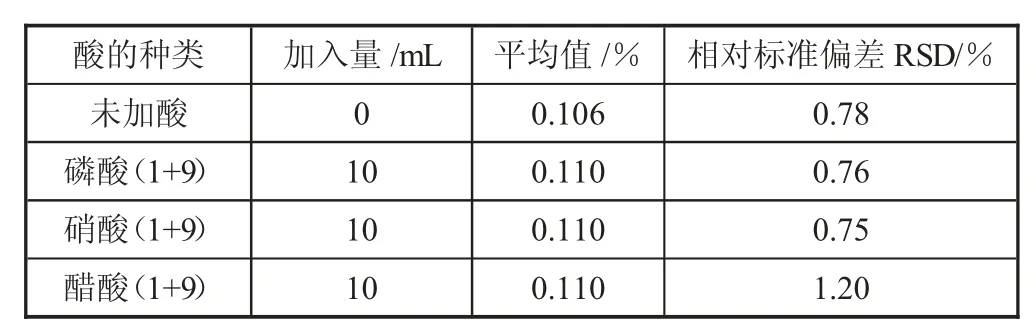
表2 酸的种类对分析结果的影响
从表2 中数据可以看出,相对于加入酸的试样,未加酸的试样分析结果偏低,说明在分析时为试样提供酸性环境更有利于氯离子溶出。但无论是加入磷酸、硝酸还是醋酸,对分析结果均无显著影响。硝酸和醋酸均具有较强的挥发性和腐蚀性,在稀释配制及使用过程中易对人身、设备及环境造成危害。磷酸因黏性大,不易挥发,在配制及使用过程中对人身和环境更为友好。因此,选择磷酸更为合适。对于未加酸试样,氧化铁粉在滴定杯壁上有明显黏附现象,这可能也是导致其结果偏低的原因之一。加酸后的试样,氧化铁粉在滴定杯上的黏附现象得到明显改善,使用后的滴定杯也更容易清洗。
3.3 搅拌时间
氧化铁粉表面具有丰富的孔结构,氯离子物理吸附于氧化铁粉表面。由于氯离子易溶于水的特性,加水后,氧化铁粉分散于水溶液中,大部分吸附于氧化铁粉表面的氯离子能够很快溶出,并分散于水溶液中。但是,难免有小部分氯离子吸附较为牢固,不易脱附。充分搅拌能够使氯离子更充分地溶出,分析结果更为准确可靠。因此,利用w(Cl-)为0.1%左右的氧化铁粉标准样品考察滴定前搅拌时间对分析结果的影响,实验结果如图1 所示。
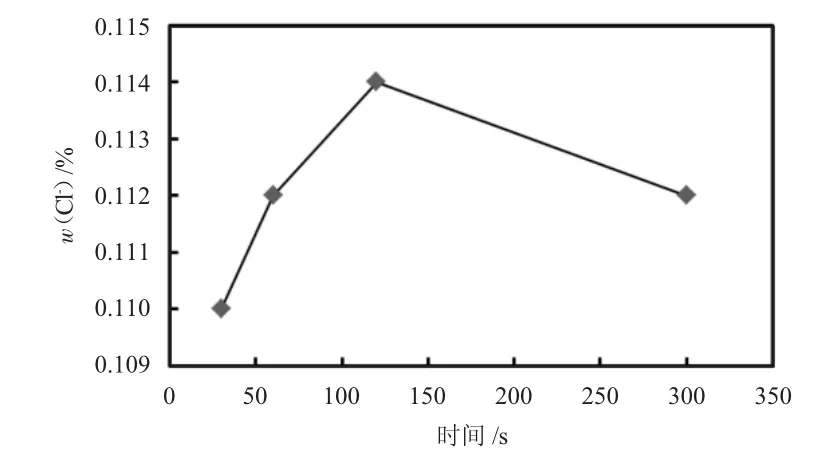
图1 搅拌时间对分析结果的影响
从图1 分析结果可以看出,随着搅拌时间的延长,氯离子分析结果有所增加。当搅拌时间为60 s时,w(Cl-)为0.112%。搅拌时间延长至120 s,w(Cl-)为0.114%,相较于搅拌时间为60 s 时,氯离子分析结果有所增加。继续增加搅拌时间至300 s,w(Cl-)为0.112%,相对于120 s 结果有所下降,结果重复性及相对标准偏差变差。这可能是在酸性条件下,氯离子与氢离子结合生成易挥发的氯化氢,过长的搅拌时间使得氯化氢挥发所致。当搅拌时间为120 s 时,已能够使吸附于氧化铁粉表面的氯离子完全溶出。因此搅拌时间为120 s 较为合适。
3.4 回收率测定
本文实验的准确度由加标回收实验来验证,采用经多次分析结果稳定可靠的生产试样进行加标回收。称取0.5 g 试样4 份,分别加入10 mL 和20 mL 质量浓度为0.1 mg/mL 的氯离子标准溶液(相当于加入1.0 mg 和2.0 mg 的氯离子)分析氯离子含量,计算氯离子的回收率,结果如表3 所示。
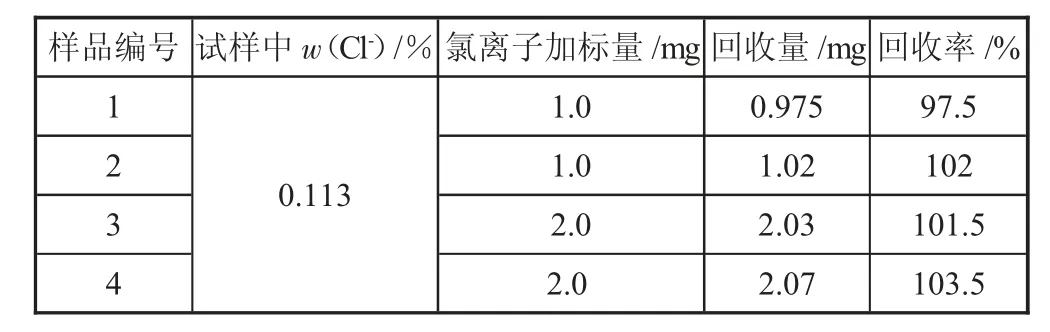
表3 加标回收试验
从表3 中数据可以看出,加标回收率在97.5%~103.5%之间,准确度符合试验要求,能够满足日常生产检验的要求。
4 结语
本文通过对称样量、是否加入酸、酸的种类以及搅拌时间等条件进行优化,进一步提高了自动电位滴定法测定氧化铁粉中氯离子含量分析结果的准确性。实验结果表明:经优化后的方法所得分析结果的准确度及精密度均较好,现已应用于生产检验。影响分析结果的条件因素有很多,在开发及建立分析方法时,我们要尽可能全面考虑,并对影响因素进行考察,优化分析条件,尽量减小或消除影响。同时,兼顾环保要求及分析成本,这样才能更好地服务于生产。

