脑电生物反馈联合酒石酸唑吡坦片治疗急性缺血性卒中后睡眠障碍临床观察

摘要 目的:观察脑电生物反馈联合酒石酸唑吡坦片治疗急性缺血性卒中后睡眠障碍的临床疗效。方法:选取2022年2月1日至2023年8月31日福建省老年医院神经内科收治的急性缺血性卒中后睡眠障碍患者77例作为研究对象进行回顾性调查。根据治疗方案分为对照组(n=42)和观察组(n=35),对照组采用酒石酸唑吡坦片口服治疗,观察组采用脑电生物反馈联合酒石酸唑吡坦片治疗。2组均治疗2周,比较2组干预前后匹兹堡睡眠质量指数(PSQI)评分及睡眠时间、觉醒次数及觉醒时间,并评定临床疗效。结果:治疗后2组PSQI评分、睡眠时间、觉醒次数及觉醒时间均较本组治疗前改善(Plt;0.05),且观察组治疗后改善优于对照组(Plt;0.05);观察组总有效率高于对照组(Plt;0.05)。结论:脑电生物反馈联合酒石酸唑吡坦片显著改善急性缺血性卒中后睡眠质量,疗效肯定。
关键词 脑电生物反馈;酒石酸唑吡坦片;急性缺血性卒中;睡眠障碍;卒中后睡眠障碍
Clinical Observation of Electroencephalographic Biofeedback Combined with Zolpidem Tartrate in the Treatment of Sleep Disorders after Acute Ischemic StrokeGUO Xiumei,WU Jing
(Fujian Provincial Geriatric Hospital,Department of Neurology,Fuzhou 350003,China)
Abstract Objective:To observe the clinical efficacy of EEG biofeedback combined with Zolpidem tartrate tablets in the treatment of sleep disorders after acute ischemic stroke.Methods:A retrospective study was conducted on 77 patients with sleep disorders after acute ischemic stroke in the Department of Neurology of Fujian Geriatric Hospital from February 1,2022 to August 31,2023.According to the treatment plan,they were divided into control group(n=42) and observation group(n=35).The control group received oral treatment with Zolpidem tartrate tablets.The observation group was treated with EEG biofeedback combined with Zolpidem tartrate tablets.The two groups were treated for 2 weeks.The Pittsburgh Sleep Quality Index(PSQI) score,sleep time,wake times and wake time of the two groups were compared before and after the intervention,and the clinical efficacy was evaluated.Results:After treatment,PSQI score,sleep time and sleep time,wake frequency and wake time in 2 groups were improved compared with that before treatment(Plt;0.05),and the improvement in observation group was better than that in control group(Plt;0.05).The total effective rate of observation group was higher than that of control group(Plt;0.05).Conclusion:EEG biofeedback combined with Zolpidem tartrate tablets can significantly improve sleep quality after acute ischemic stroke.
Keywords Electroencephalographic biofeedback; Zolpidem tartrate tablets;Acute ischemic stroke; Sleep disorders; Sleep disturbance after stroke
中图分类号:R743.3文献标识码:Adoi:10.3969/j.issn.2095-7130.2024.05.002
卒中是指各种原因引起急性脑部血液循环障碍引起局部或全面性脑功能缺损综合征,具有高发病率、高复发率等特点,分为急性缺血性卒中和急性出血性卒中2种类型,其中急性缺血性卒中患病率明显高于急性出血性卒中[1]。睡眠障碍是指各种原因引起睡眠—觉醒调节系统紊乱造成睡眠功能障碍,导致异常睡眠质量或睡眠行为的一组临床综合征,严重影响患者生命质量、生理心理功能以及社会功能。卒中相关睡眠障碍(Stroke-related Sleep Disorders,SSD)是指卒中前已有睡眠障碍在卒中后持续存在或加重,或卒中后首次出现。研究表明卒中患者发病前患有睡眠障碍高达50%,睡眠障碍可加重卒中或导致卒中复发率增高;同时,卒中后亦常继发睡眠障碍,即卒中后睡眠障碍(Post-stroke Sleep Disorders,PSSD),持续时间长,最早可于卒中发病后3 d内出现[2]。本研究回顾性研究脑电生物反馈联合酒石酸唑吡坦片改善急性缺血性卒中睡眠障碍的临床疗效。现报道如下。
1 资料与方法
1.1 一般资料 选取2022年2月1日至2023年8月31日福建省老年医院神经内科急性缺血性卒中患者77例作为研究对象,根据治疗方案分为对照组(n=42)和观察组(n=35),对照组中男23例,女19例,年龄62~80岁,平均年龄(78.40±10.29)岁,原发性高血压26例,糖尿病20例,吸烟12例,饮酒15例。观察组中男17例,女18例,年龄61~83岁,平均年龄(76.57±8.79)岁,原发性高血压22例,糖尿病19例,吸烟13例,饮酒12例。2组一般资料经统计学分析,差异均无统计学意义(均Pgt;0.05),具有可比性。本研究经福建省老年医院伦理委员会审批通过(伦理审批号:20240313)
1.2 诊断标准 1)符合《中国急性缺血性脑卒中诊治指南2018》诊断标准,即急性起病的局灶神经功能缺损,影像学MRI-DWI阳性或者症状持续时间>24 h;2)符合《中国精神障碍分类与诊断标准第三版》(Chinese Classification of Mental Disorders-3rd Edition,CCMD-3)中睡眠障碍的标准,即入睡困难、睡眠时间短、易醒等。
1.3 纳入标准 1)符合《中国急性缺血性脑卒中诊治指南2018》急性缺血性卒中诊断标准;2)符合《中国精神障碍分类与诊断标准第三版(CCMD-3)睡眠障碍诊断标准;3)发病前无睡眠障碍病史,发病后可独立完成量表的评估与填写;4)受试者知情同意。
1.4 排除标准 1)其他类型脑血管疾病如脑出血、短暂性脑缺血发作、肿瘤相关机械压迫等;2)精神疾病或心理疾病正在服用药物者;3)交流或意识障碍,无法配合完成静脉溶栓治疗;4)对酒石酸唑吡坦片药物过敏;5)严重心肝肾功能不全、血液系统或多器官功能衰竭。
1.5 治疗方法 2组患者均予急性缺血性卒中常规治疗控制病情,包括抗血小板聚集、调脂、降压、降糖、抗凝、营养支持等,可能影响睡眠的因素如尿频、咳嗽等对症治疗,构建良好睡眠环境。对照组采用酒石酸唑吡坦片(Stilnox)[赛诺菲(杭州)制药有限公司,国药准字J20140021]10 mg/晚,睡前30 min口服。观察组在对照组治疗的基础上加用脑电生物反馈治疗,即脑电α波或θ波训练,应用脑功能(障碍)治疗仪(常州雅思医疗器械有限公司,型号:YS7002型)治疗,6次/周,1次/d,约30 min/次,疗程均为2周。
1.6 观察指标 1)2组基线资料,包括姓名、性别、年龄、合并疾病、吸烟、饮酒;2)磁共振影像资料,由福建省老年医院影像科提供,磁共振仪器(上海联影公司,型号:uMR560,1.5 T);3)睡眠血氧器(上海贝瑞电子科技有限公司,型号:BM2000A),监测内容包括睡眠时间、觉醒时间、觉醒次数;4)采用匹兹堡睡眠质量指数(Pittsburgh Sleep Quality Index,PSQI)评估睡眠质量。
1.7 疗效判定标准 根据干预2周后的PSQI评分和(或)睡眠改善情况将睡眠疗效分为4级,分别为临床治愈、显效、有效、无效。临床治愈:PSQI评分≤5分,睡眠时间恢复正常水平即夜间睡眠时间>6 h,睡眠深沉,清晨醒后精神饱满,无疲乏、困倦感。显效:6分≤PSQI评分≤10分,睡眠时间较治疗前增加>3 h,睡眠质量明显改善,醒后无疲乏、困倦感。有效:11分≤PSQI评分≤15分,睡眠时间较治疗前有增加,但增加<3 h,睡眠质量有一定程度改善,但醒后有疲乏、困倦感。无效:PSQI评分≥16分,睡眠障碍症状未改善,甚至加重[3]。总有效率=(临床治愈+显效+有效)例数/总例数×100%。
1.8 统计学方法 采用SPSS 26.0统计软件进行数据分析,计量资料以均数±标准差(±s)描述,2组间比较采用t检验。计数资料以[例(%)]描述,采用χ2检验,以Plt;0.05为差异有统计学意义。
2 结果
2.1 2组患者干预前后PSQI评分及睡眠监测指标比较 干预后2组患者PSQI评分及睡眠监测指标睡眠时间、觉醒次数及觉醒时间与本组干预前比较差异均有统计意义(Plt;0.05),且观察组干预后与对照组比较,PSQI评分更低,睡眠时间更长,而觉醒次数更少,觉醒时间更短,差异均有统计学意义(Plt;0.05)。见表1。
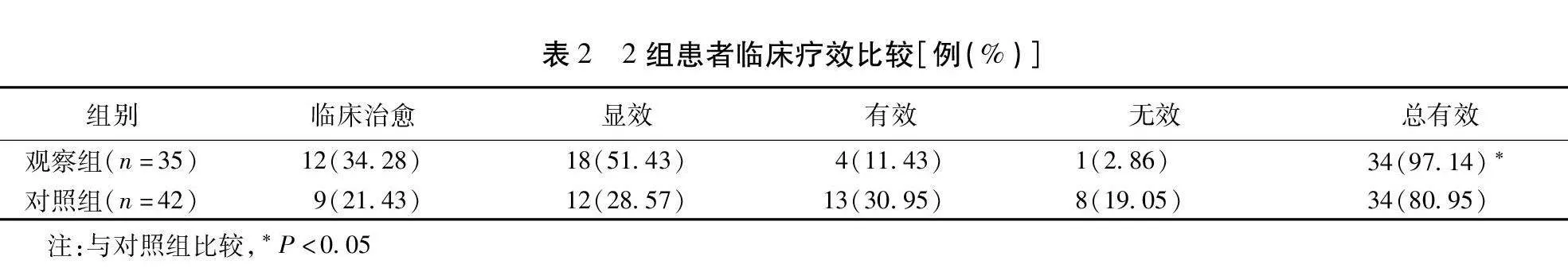
2.2 2组患者临床疗效比较 观察组总有效率为97.14%(34/35),对照组总有效率为80.95%(34/42),观察组总有效率高于对照组(χ2=11.30,P=0.01)。见表2。
3 讨论
急性缺血性卒中亦称急性脑梗死,是脑血管病最常见类型,由多种发病机制及多种病因导致的脑缺血综合征,有“黄金”治疗时间。在最佳时间窗内,使用动脉取栓、静脉溶栓可大大挽救脑组织,改善预后,但仍有部分预后不良,可能并发卒中后睡眠障碍[4],影响神经功能恢复,加剧病情或诱发新的脑血管病[5]。急性缺血性卒中后睡眠障碍机制尚不明确,可能与急性缺血性卒中引起觉醒或睡眠调节系统等中枢神经系统损伤或神经递质失衡相关[6-7]。卒中后睡眠障碍是卒中后常见并发症,发病率高达78%[8]。本研究中急性缺血性卒中后睡眠障碍的发病率为47.53%,与文献相符[9]。若出现急性缺血性卒中后睡眠障碍,需及早进行治疗,促进神经功能修复,避免由急性睡眠障碍转为慢性睡眠障碍,影响急性缺血性卒中的预后。《卒中相关睡眠障碍评估与管理中国专家共识2023》明确指出药物治疗首选非苯二氮艹卓类如唑吡坦、右佐匹克隆等以及光照、针灸、经颅微电流、音乐等物理治疗改善患者卒中后睡眠障碍。
酒石酸唑吡坦片属于非苯二氮艹卓类镇静催眠药物,选择性作用于γ-氨基丁酸受体而发挥镇静催眠作用,具有半衰期短、后遗效应、不良反应小及药物依赖性风险低等优点,在临床应用广泛[10-11]。脑电生物反馈治疗是一种非侵入式物理疗法,亦是有效新型睡眠障碍治疗方案,通过训练增加患者脑电波中α波或θ波,减轻精神及肌肉紧张,最终让患者自主控制脑电波,减少睡眠觉醒次数,缩短睡眠潜伏期及觉醒时间,提高睡眠效率,进而改善睡眠质量,具有无不良反应、无创及疗效稳定等优势[12]。本研究中对照组采用酒石酸唑吡坦片辅助睡眠,观察组为酒石酸唑吡坦片联合脑电生物反馈治疗,2组干预后较干预前PSQI评分均降低,觉醒时间、觉醒次数减少,睡眠时间延长,且干预后PSQI评分及觉醒时间、觉醒次数、睡眠时间改善均优于对照组(Plt;0.05)。观察组临床疗效明显优于对照组(Plt;0.05),说明药物联合物理治疗是更有效治疗睡眠障碍的方案,符合相关文献报道[13-14]。
综上所述,卒中易并发睡眠障碍,睡眠障碍可加重或诱发卒中。临床工作中需要在卒中常规治疗基础上,加强卒中后睡眠障碍的管理。脑电生物反馈联合酒石酸唑吡坦片较单一的药物治疗可更进一步提高睡眠质量,疗效确切,临床应用价值更高,值得推广。
利益冲突声明:无。
参考文献
[1]CAMPBELL B C V,KHATRI P.Stroke[J].The Lancet,2020,396(10244):129-142.
[2]张亚男,王赞.卒中相关睡眠障碍[J].中国卒中杂志,2023,18(5):497-501.
[3]任晓兰,朱亚芹,孙艳军,等.脑电生物反馈联合重复经颅磁刺激治疗对老年睡眠障碍患者的影响[J].中国老年学杂志,2022,42(13):3231-3234.
[4]CAI H,WANG X P,YANG G Y.Sleep disorders in stroke:an update on management[J].Aging and disease,2021,12(2):570-585.
[5]ZHANG Y,XIA X,ZHANG T,et al.Relationship between sleep disorders and the prognosis of neurological function after stroke[J].Frontiers in Neurology,2022,13:1036980.
[6]KATZAN I L,THOMPSON N R,WALIA H K,et al.Sleep-related symptoms in patients with mild stroke[J].Journal of Clinical Sleep Medicine,2020,16(1):55-64.
[7]MAESTRI M,ROMIGI A,SCHIRRU A,et al.Excessive daytime sleepiness and fatigue in neurological disorders[J].Sleep and Breathing,2020,24(2):413-424.
[8]KIM J,KIM Y,YANG K I,et al.The relationship between sleep disturbance and functional status in mild stroke patients[J].Annals of rehabilitation medicine,2015,39(4):545-552.
[9]YOON C W,PARK H K,BAE E,et al.Sleep apnea and early neurological deterioration in acute ischemic stroke[J].Journal of Stroke and Cerebrovascular Diseases,2020,29(2):104510.
[10]PARAISO R L M,ROSE R H,FOTAKI N,et al.The use of PBPK/PD to establish clinically relevant dissolution specifications for zolpidem immediate release tablets[J].European Journal of Pharmaceutical Sciences,2020,155:105534.
[11]XIANG T,CAI Y,HONG Z,et al.Efficacy and safety of Zolpidem in the treatment of insomnia disorder for one month:a meta-analysis of a randomized controlled trial[J].Sleep Medicine,2021,87:250-256.
[12]LOU S,XUE X.Application of electroencephalographic(EEG) biofeedback therapy in the rehabilitation of patients with chronic diseases[J].Psychiatry Research,2020,293:113371.
[13]EDINOFF A N,WU N,GHAFFAR Y T,et al.Zolpidem:efficacy and side effects for insomnia[J].Health psychology research,2021,9(1):24927.
[14]WANG Y,SALAS R M E.Semin Neurol[J].Approach to Common Sleep Disorders,2021,41(6):781-794.

