研究西妥昔单抗联合FOLFOX6方案治疗转移性大肠癌的临床效果
杜心仪,钱垠


【摘要】目的 研究转移性大肠癌患者联合使用西妥昔单抗和常规化疗(FOLFOX6方案)治疗的效果及不良反应情况。方法 选取2020年1月至2022年12月南京市中医院收治的转移性大肠癌患者86例,根据随机数字表法分为对照组(FOLFOX6方案,43例)和观察组(西妥昔单抗联合FOLFOX6方案,43例)。两组患者治疗周期均为12周。比较两组患者临床疗效,治疗前后肿瘤标志物指标、外周血T细胞亚群水平、临床症状积分,以及治疗期间不良反应发生情况。结果 观察组患者临床总有效率高于对照组;与治疗前比,治疗后两组患者血清癌胚抗原、糖类抗原199、糖类抗原242,外周血CD8+百分比,临床症状积分指标均降低,且观察组低于对照组;与治疗前比,治疗后观察组外周血CD4+、CD3+百分比及CD4+/CD8+比值均升高,且观察组更高(均P<0.05);两组不良反应总发生率比较,差异无统计学意义(P>0.05)。结论 在常规化疗治疗的基础上,联合运用西妥昔单治疗转移性大肠癌的临床疗效突出,可降低患者肿瘤标志物水平,提高免疫功能,改善患者症状,且安全性良好。
【关键词】西妥昔单抗 ; FOLFOX6方案 ; 转移性大肠癌 ; 肿瘤标志物 ; 疗效
【中图分类号】R574.61【文献标识码】A【文章编号】2096-3718.2023.20.0069.03
DOI:10.3969/j.issn.2096-3718.2023.20.023
大腸癌为一种消化道恶性肿瘤疾病,更是一种高致死率的癌症类型。因其早期检出率比较低,大多数大肠癌患者在首次接受诊断时,疾病已经进入到了晚期或是出现癌细胞转移,其中转移性大肠癌患病概率较高,常见转移部位是肝脏与肺部,患者接受常规化疗,可在一定程度上抑制病情进展,但整体上患者五年生存率较低,因此其治疗已经成为大肠癌疾病治疗的难点和重点。西妥昔单抗药物是单克隆抗体靶向药物,以表皮生长因子受体(EGFR)为特异性靶点,通过和肿瘤细胞上的EGFR特异性结合,阻断细胞内信号转导途径,加速肿瘤细胞凋亡,进而使肿瘤病灶缩小,同时其还能提升肿瘤对于放化疗治疗的敏感性[2]。本研究旨在分析FOLFOX6方案联合西妥昔单抗药物治疗转移性大肠癌的疗效,现报道如下。
1 资料与方法
1.1 一般资料 选取南京市中医院2020年1月至2022年12月收治的86例转移性大肠癌患者,根据随机数字表法分为两组,每组43例。对照组患者男性22例,女性21例;年龄47~81岁,平均(63.14±2.24)岁;类型:结肠癌13例,直肠癌30例;远端转移:肺转移12例,肝转移13例,淋巴结转移10例,腹腔转移8例。观察组患者男性23例,女性20例;年龄46~82岁,平均(63.16±2.28)岁;类型:结肠癌12例,直肠癌31例;远端转移:肺转移13例,肝转移14例,淋巴结转移9例,腹腔转移7例。两组患者一般资料对比,差异无统计学意义(P>0.05),组间具有可比性。纳入标准:①符合《结肠癌规范化诊疗指南(试行)》 [3]中的相关诊断标准;②经影像学检查确诊;③肝、肾功能正常。排除标准:①对本研究中药物过敏;②伴有其他系统恶性肿瘤。本研究经南京市中医院医学伦理委员会批准,且患者均已签署知情同意书。
1.2 治疗方法 给予对照组患者FOLFOX6方案,第
1天静脉滴注注射用奥沙利铂(先声药业有限公司,国药准字H20093899,规格:50 mg),用药剂量为100 mg/m2;第1天静脉滴注亚叶酸钙注射液(江苏恒瑞医药股份有限公司,国药准字H20000584,规格:0.1 g∶10 mL),用药剂量为400 mg/m2,2 h内完成滴注;氟尿嘧啶注射液(天津金耀药业有限公司,国药准字H12020959,规格:0.25 g∶10 mL),用药剂量为400 mg/m2,先静脉推注,然后以2 400 mg/m2,持续静脉滴注46 h,第1、2天;3周重复1次,4个疗程后对治疗效果进行评定。
在对照组的基础上给予观察组西妥昔单抗注射液(Merck Healthcare KGaA,注册证号SJ20171039,规格:100 mg),首次运用剂量控制为400 mg/m2,后每周以250 mg/m2维持量治疗,1次/周。在用药之前,需给予盐酸帕诺洛司琼注射液(湖南科伦制药有限公司,国药准字H20223448,规格:1.5 mL∶0.075 mg),静脉滴注0.225 g,地塞米松磷酸钠注射液[上海现代哈森(商丘)药业有限公司,国药准字H41021924,规格:1 mL∶5 mg]静脉推注5 mg。3周为1疗程,两组患者均治疗4个疗程。
1.3 观察指标 ①临床疗效。治疗后患者病灶全部消失,无新病灶为完全缓解(CR);病灶缩小幅度≥ 30%,无新病灶为部分缓解(PR);病灶缩减,但没有到达PR诊断标准,增加没有到达PD为疾病稳定(SD);全部病灶增加≥ 20%,出现新病灶,为疾病进展(PD) [3]。治疗总控制率=CR率+PR率+SD率。②肿瘤标志物。采集患者治疗前后的外周静脉血5 mL,以3 000 r/min,离心10 min取血清,运用电化学发光法检测癌胚抗原、糖类抗原199、糖类抗原242。③外周血T淋巴细胞亚群水平测定。采集患者治疗前后的外周静脉血5 mL,抗凝处理,溶血素去红细胞后,以流式细胞仪[安捷伦生物(杭州)有限公司,型号:NovoCyte D1040]检测CD3+、CD4+、CD8+百分比,并计算CD4+/CD8+比值。④临床症状积分。以疾病症状神疲乏力、腹胀、腹痛、便中带血、舌质症状评估,各项满分4分,分数高代表症状明显[4]。⑤不良反应情况。治疗期间,记录患者消化道反应、皮疹、神经毒性、变态反应发生情况。
1.4 统计学方法 用SPSS 23.0统计学软件分析数据,计数资料以[例(%)]表示,采用χ2检验;计量资料经S-W法检验证实符合正态分布,以( x ±s)表示,组间比较采用独立t检验,治疗前后比较采用配对t检验。以P<0.05为差异有统计学意义。
2 结果
2.1 两组患者临床疗效比较 与对照组比,观察组患者总控制率更高,差异有统计学意义(P<0.05),见表1。
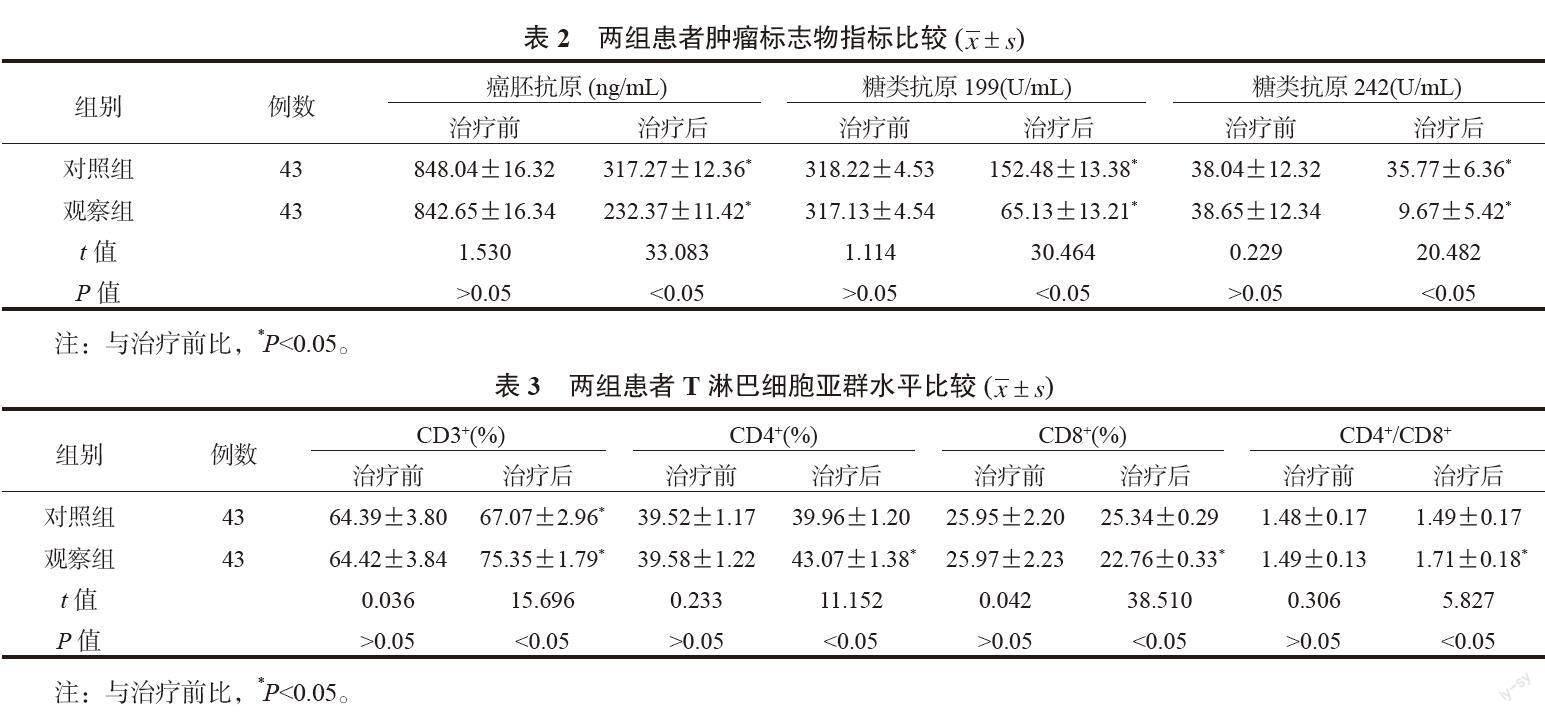
2.2 两组患者肿瘤标志物指标比较 与治疗前比,治疗后两组患者血清肿瘤标志物指标均降低,且观察组更低,差异均有统计学意义(均P<0.05),见表2。
2.3 两组患者外周血T淋巴细胞亚群水平比较 与治疗前比,治疗后两组患者CD3+百分比和观察组患者CD4+百分比、CD4+/CD8+比值均升高,观察组CD8+百分比降低,且与对照组比,观察组CD3+、CD4+百分比及CD4+/CD8+比值更高,CD8+百分比更低,差异均有统计学意义(均P<0.05),见表3。
2.4 两组患者临床症状积分比较 与治疗前比,治疗后两组患者各项临床症状积分均降低,且观察组更低,差异均有统计学意义(均P<0.05),见表4。
2.5 两组患者不良反应情况比较 两组患者不良反应总发生率比较,差异无统计学意义(P>0.05),见表5。
3 讨论
对于转移性大肠癌患者,临床常采用FOLFOX6化疗方案,其中奥沙利铂药物作为一种铂类衍生物,为具有细胞毒作用的抗癌药物,可在机体内转化为烷化结合物,后作用在肿瘤细胞的DNA上,产生链内与链间的交联作用,抑制DNA合成,抑制肿瘤细胞增殖;5-氟尿嘧啶是尿嘧啶的同类物,可作用在处于S期的肿瘤细胞,被活跃分裂的肿瘤所优先摄取,进入细胞中转变成5-氟尿嘧啶脱氧核苷酸,对DNA合成产生影响[5]。
近年来,靶向药物治疗成为抗肿瘤治疗的新方向,具有不良反应小、特异性高等优势,运用在转移性大肠癌治疗中也发挥了较好的治疗作用。西妥昔单抗药物目前被广泛应用在转移性大肠癌治疗中,患者普遍存在表皮生长因子过度表达,和预后不良存在密切的联系,而西妥昔单抗可特异性结合肿瘤细胞上的EGFR,会将肿瘤细胞的增殖传导阻断,阻滞肿瘤细胞生长,诱导肿瘤细胞凋亡,进而发挥抑制肿瘤进展的目的[6-7]。
癌胚抗原为多糖蛋白复合物癌胚抗原之一,糖类抗原199为肿瘤标志物之一,其水平在大多数肿瘤组织中呈现为不同程度上的升高。糖类抗原242是一种唾液酸化的糖类抗原,是近年来应用于临床的一种较新的肿瘤标志物,其水平与病情严重程度呈正相关[8-9]。本研究中,治疗后观察组患者肿瘤标志物指标低于对照组,疾病总控制率高于对照组;且两组患者不良反应总发生率比較,差异无统计学意义,这一结果表明,转移性大肠癌患者在经FOLFOX6方案联合西妥昔单抗药物治疗之后,肿瘤病灶得到了有效的控制。
转移性大肠癌患者随着病情进展会有免疫力降低的现象,而测定CD4+、CD3+、CD8+,可明确患者免疫情况,CD4+ T淋巴细胞可诱导和辅助细胞及体液免疫,CD8+ T淋巴细胞通过抑制细胞产生抗体及毒素进而对细胞及体液免疫产生抑制作用,CD4+/CD8+可衡量机体免疫功能,其比值降低则表明机体免疫功能受损。本研究中,治疗后观察组患者CD3+、CD4+百分比及CD4+/CD8+比值更高,CD8+百分比及临床症状各项积分均更低,提示在常规化疗治疗的基础上,联合运用西妥昔单治疗转移性大肠癌,可使患者症状和免疫功能改善,患者预后良好。西妥昔单抗药物治疗具备逆转肿瘤细胞耐受性的作用,可将DNA修复阻断,能够和奥沙利铂药物和5-氟尿嘧啶药物协同作用,发挥出较强的抗肿瘤治疗效果[10]。
综上,在常规化疗治疗的基础上,联合运用西妥昔单治疗转移性大肠癌的临床疗效突出,可降低患者肿瘤标志物指标,提高免疫功能,改善患者临床症状,且安全性良好。但本研究考察时间有限,关于患者的远期预后情况还需要进一观察研究。
参考文献
[1]周晶, 卫真真, 浦匀舟, 等. 左金丸逆转KRAS突变型大肠癌西妥昔单抗耐药的作用机制研究[J]. 上海中医药杂志, 2023, 57(5): 37-45.
[2]江璧锋, 林华明. 西妥昔单抗对转移性大肠癌患者血清CEA、CA199水平的影响[J]. 吉林医学, 2018, 39(1): 124-126.
[3]中华人民共和国国家卫生和计划生育委员会. 结肠癌规范化诊疗指南(试行)[J/CD]. 中国医学前沿杂志(电子版), 2013, 5(8): 50-55.
[4]李婧. 附子理中汤联合化疗方案对脾肾阳虚型晚期转移性大肠癌患者的临床疗效观察[D]. 南宁: 广西中医药大学, 2021.
[5]KOSUGI C, KODA K, ISHIBASHI K et al. Safety of mFOLFOX6/XELOX as adjuvant chemotherapy after curative resection of stage III colon cancer: phase II clinical study (The FACOS study)[J]. Int J Colorectal Dis, 2018, 33(6): 809-817.
[6]张壮苗, 邓黎黎, 张岩, 等. 下调整合素β1对大肠癌细胞的西妥昔单抗化疗敏感性的影响及机制研究[J]. 广西医科大学学报, 2021, 38(12): 2272-2278.
[7]于登峰, 张文俊, 张福杰, 等. 西妥昔单抗联合SOX方案治疗大肠癌患者的效果及对血清miR-29b和miR-92a-1水平的影响[J]. 胃肠病学和肝病学杂志, 2020, 29(1): 53-57.
[8]王国杰, 翟得欣, 任洋洋, 等. 结肠镜联合CEA、CA242在诊断结肠息肉癌变中的作用及结肠息肉癌变相关因素分析[J]. 罕少疾病杂志, 2022, 29(6): 89-91, 101.
[9]陶晓军, 陈桂明, 陈林琴, 等. 肿瘤标志物CEA、CA199和AFP在直结肠恶性肿瘤诊断中的应用及对近期有效率的影响[J]. 河北医药, 2018, 40(24): 3753-3755, 3759.
[10]薛鹏龙, 李梦丽, 霍礼超, 等.西妥昔单抗联合FOLFOX4/FOLFIRI治疗晚期结肠癌的Meta分析[J]. 现代肿瘤医学, 2019, 27(5): 817-823.

