八珍汤联合体外高频治疗对恶性肿瘤增效减毒作用分析
段胜红,龙再慧*,向秋月,李 铭,陈 照,唐伟慧,胡 为,黄杰夫,潘 银,牟艳林,崔红梅
(1.湖北恩施利川市中医院肿瘤科,湖北 利川 445400;2.湖北省红十字医院,武汉 430000)
恶性肿瘤是危害人类生命和健康安全的重要病因,其以侵袭转移性强和无限增殖为主要特征,发病部位可涉及机体所有器官[1]。据2018 年全球癌症统计数据显示,2018 年全世界约有1 810 万恶性肿瘤新发病例,死亡病例约有960 万例,而在全球范围内,中国恶性肿瘤发病率及病死率均位居中等甚至偏上位置,甚至部分恶性肿瘤疾病如肝癌、胃癌及食管癌发病率和病死率位居全球50%以上,故恶性肿瘤在我国的防控形势非常严峻[2-3]。目前恶性肿瘤的治疗仍以西医化疗方法为主,但化疗药物在清除癌细胞的同时,对机体内正常的细胞亦会产生较大的伤害性,具体表现为胃肠道反应、皮疹、脱发、骨髓抑制等,不仅严重影响患者生活质量,同时易造成化疗中断,降低治疗效果[4]。目前,对化疗产生的不良反应临床西医干预手段虽不缺乏,但治疗效果并不理想。中医治疗恶性肿瘤疾病注重辨证施治,重视将个性化治疗和整体观相结合,治疗目标以平衡阴阳、调和脏腑功能为主,联合化疗、放疗、手术等西医治疗方法可起到增效减毒的作用[5]。八珍汤来源于《瑞竹堂经验方》,有健脾益胃、气血双补功效,被广泛用于多种恶性肿瘤疾病化疗、放疗以及手术治疗后的辅助治疗中,疗效突出[6-7]。基于此,本研究在化疗基础上联合应用八珍汤和体外高频治疗,旨在克服化疗治疗、单纯中医治疗及高频治疗之间的缺陷,发挥优势互补、协同增敏作用,减轻化疗给患者带来的痛苦,改善肿瘤患者生存质量,现报道如下。
1 资料与方法
1.1 一般资料 选择我院肿瘤科2021 年1 月-2022 年1 月期间住院行化疗治疗的恶性肿瘤患者100例进行研究,采用随机数字表法分成2 组,各50 例。观察组男29 例,女21 例,年龄30 ~70 岁,平均(52.40±5.11)岁;病程6 个月~3 年,平均(1.50±0.35)年;恶性肿瘤类型:呼吸道肿瘤23 例,消化道肿瘤15 例,泌尿生殖系统肿瘤12 例。对照组男31 例,女19 例,年龄28 ~70 岁,平均(52.35±5.07)岁;病程6 个月~4 年,平均(1.52±0.33)年;恶性肿瘤类型:呼吸道肿瘤24 例,消化道肿瘤16 例,泌尿生殖系统肿瘤10 例。2 组一般资料相比,差异无统计学意义(P>0.05)。
1.2 诊断标准 西医参照《中国常见恶性肿瘤诊治规范》[8]中关于恶性肿瘤的诊断标准及分期规定。中医证型参照《中药新药临床研究指导原则》[9],属于气血两虚型:主症包括神疲乏力,自汗,气短,面色萎黄或苍白;次症包括头晕目眩,口唇、爪甲及眼睑颜色淡白,失眠,心悸,肢体麻木,偏瘦,女性月经量少甚至闭经;舌淡白,脉弱。
1.3 纳入标准 1)所有入组患者均经超声、CT 及病理组织切片等检查明确诊断为恶性肿瘤;2)年龄20 ~75 岁;3)Karnofsky(KS)评分>60 分,预计生存期超过3 个月;4)近1 个月未曾接受过其他抗肿瘤治疗;5)所有患者均自愿参加研究且签署书面知情同意书。
1.4 排除标准 1)临床资料不完整者;2)精神病患者;3)合并严重肝肾功能障、心脑血管疾病、血液系统疾病及自身免疫系统重大疾病者;4)有化疗药物禁忌证者;5)有脑转移征象者;6)妊娠或哺乳期妇女;7)对本研究用药成分过敏者。
1.5 脱落和剔除标准 1)与本研究纳入和排除标准不符者;2)治疗期间自行停药或换药,影响到疗效评估和治疗安全性判断者;3)病人自行退出临床试验者。1.6 治疗方法 2 组均参考《恶性肿瘤化疗治疗及免疫治疗》[10]接受化疗治疗,具体化疗方案需结合患者个人情况而定,每次化疗间隔2 周,共治疗6 个周期。对照组于化疗开始后第1 d 给予体外高频热疗(珠海和佳HG-200011 体外高频热疗机)治疗,温度控制在42.5℃~43℃,应用频率为13.56 MHz,每次50 ~60 min,每3 d 治疗1 次。观察组在对照组治疗基础上,于化疗开始后第1 d 开始服用八珍汤,处方为人参、白术、茯苓、当归、熟地黄各15 g,川芎、白芍各12 g,甘草9 g。每日1 剂。2 组均观察6 个周期。
1.7 观察指标
1.7.1 中医证候积分 参照《中医病证诊断疗效标准》[9]对2 组患者治疗前后主症(神疲乏力、自汗气短、面色苍白)、次症(头晕目眩、失眠心悸)5 项中医证候症状进行评分,每项内容均有4 个分数等级,即主症3项为无(记0分)、轻度(记2分)、中度(记3分)、重度(记4 分),次症2 项为无(记0 分)、轻度(记1 分)、中度(记2 分)、重度(记3 分)。
1.7.2 免疫功能指标 采集2组治疗前后空腹静脉血,使用流式细胞仪检测CD3+、CD4+、CD8+、CD4+/CD8+水平。
1.7.3 生活质量 参照癌症患者生活质量核心问卷(EORTCQLQ-C30)评价2组治疗前后生活质量评分,量表有社会功能、认知功能、情绪功能、躯体功能和角色功能5 个维度,每个维度分值均0 ~100 分,分值越高,则生活质量越优。
1.7.4 无进展生存期与总生存期 治疗结束后对2 组患者进行随访,随访时间为治疗后1 年内每隔6 周随访1 次,1 年后每隔12 周随访1 次,直至最后一名患者出组,记录2 组患者无进展生存期及总生存期,无进展生存期是指从首次化疗开始到疾病第1 次出现进展或者死亡的时间。
1.7.5 不良反应 参照NCI-CTC AE 4.0 中不良反应标准[11],统计2 组骨髓抑制、消化道副反应、血液毒性、神经毒性以及手足部位皮肤反应发生情况。
1.7.6 临床疗效 参照RECIST 实体瘤[12]评价2 组患者临床疗效。完全缓解:无肿瘤病灶,疗效能维持超过4 周;部分缓解:肿瘤病灶之最大垂直径×最大径缩小超出50%,疗效能维持超过4 周;稳定:肿瘤病灶之最大垂直径×最大径缩小不足50%,但未发现新病灶;进展:肿瘤病灶之最大垂直径×最大径增加超出1/4。完全缓解+部分缓解+稳定=临床总获益。
1.8 统计学方法 使用统计软件SPSS 25.0 进行统计学分析。所有计量资料均采用均数±标准差(±s)表示。计量资料符合正态分布及方差齐性者采用t检验,数据分布若不符合正态分布者则采用秩和检验,计数资料采用χ2检验。所有检验结果以P<0.05 为有统计学意义。
2 结果
2.1 2 组中医证候积分比较 见表1。
表1 2 组中医证候积分比较(± s,n = 50) 分
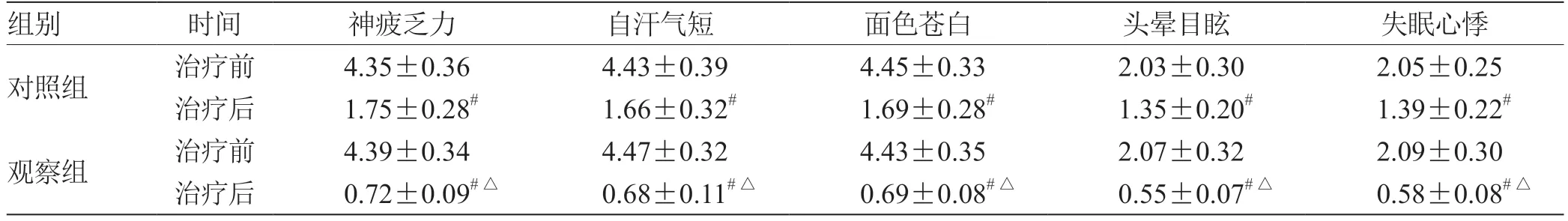
表1 2 组中医证候积分比较(± s,n = 50) 分
注:与治疗前比较,# P <0.05;与对照组比较,△P <0.05
组别 时间 神疲乏力 自汗气短 面色苍白 头晕目眩 失眠心悸对照组 治疗前 4.35±0.36 4.43±0.39 4.45±0.33 2.03±0.30 2.05±0.25治疗后 1.75±0.28# 1.66±0.32# 1.69±0.28# 1.35±0.20# 1.39±0.22#观察组 治疗前 4.39±0.34 4.47±0.32 4.43±0.35 2.07±0.32 2.09±0.30治疗后 0.72±0.09#△ 0.68±0.11#△ 0.69±0.08#△ 0.55±0.07#△ 0.58±0.08#△
2.2 2 组免疫功能指标比较 见表2。
表2 2 组免疫功能指标比较(± s,n = 50)

表2 2 组免疫功能指标比较(± s,n = 50)
注:与治疗前比较,# P <0.05;与对照组比较,△P <0.05
组别 时间 CD3+/% CD4+/% CD8+/% CD4+/CD8+对照组 治疗前 51.26±3.45 31.67±4.38 31.62±3.42 1.18±0.22治疗后 57.48±3.63# 36.16±4.52# 27.68±3.40# 1.52±0.30#观察组 治疗前 51.33±3.48 31.70±4.62 32.03±3.51 1.17±0.24治疗后 65.89±3.62#△ 47.89±5.65#△ 22.58±3.44#△ 1.83±0.23#△
2.3 2 组生活质量评分比较 见表3。
表3 2 组生活质量评分比较(± s,n = 50) 分
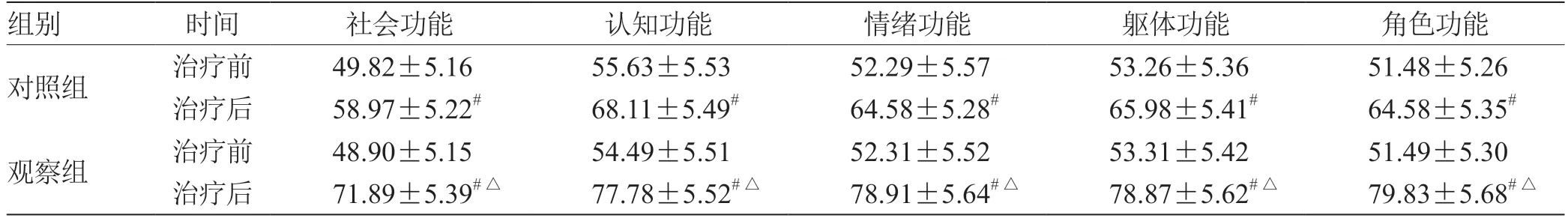
表3 2 组生活质量评分比较(± s,n = 50) 分
注:与治疗前比较,# P <0.05;与对照组比较,△P <0.05
认知功能 情绪功能 躯体功能 角色功能组别 时间 社会功能对照组 治疗前 49.82±5.16 55.63±5.53 52.29±5.57 53.26±5.36 51.48±5.26治疗后 58.97±5.22# 68.11±5.49# 64.58±5.28# 65.98±5.41# 64.58±5.35#观察组 治疗前 48.90±5.15 54.49±5.51 52.31±5.52 53.31±5.42 51.49±5.30治疗后 71.89±5.39#△ 77.78±5.52#△ 78.91±5.64#△ 78.87±5.62#△ 79.83±5.68#△
2.4 2 组无进展生存期与总生存期比较 见表4。
表4 2 组无进展生存期和总生存期比较(± s,n = 50)月

表4 2 组无进展生存期和总生存期比较(± s,n = 50)月
注:与对照组比较,# P <0.05
对照组 4.22±0.63 10.13±0.93观察组 5.95±0.70# 14.29±1.05#
2.5 2 组不良反应发生情况比较 见表5。

表5 2 组不良反应发生情况比较(n = 50) 例
2.6 2 组临床疗效比较 见表6。

表6 2 组临床疗效比较(n = 50) 例
3 讨论
到目前为止恶性肿瘤的发病与治疗仍属于全球性组别 无进展生存期 总生存期的重大难题,据最新调查报告显示,西方欧美国家及亚洲部分发达国家恶性肿瘤病死率虽稍有降低,但恶性肿瘤疾病的发生率并未出现显著降低趋势[13-14]。在中低收入国家和地区,受卫生保健系统不完善和生活方式不健康等因素的影响,恶性肿瘤疾病尤其是结直肠癌和乳腺癌的发病率呈现逐年升高的趋势[15]。而在国内,恶性肿瘤疾病仍然是导致我国居民死亡的首要病因,尤其肝癌、肺癌最为常见,且年龄在30 岁以上的癌症患者病死率明显高于30 岁以下患者[16]。化疗作为临床治疗恶性肿瘤疾病的主要方法之一,其杀伤肿瘤细胞的能力非常强,见效也较迅速,但化疗药物不良反应也较多,主要有骨髓抑制、消化道副反应、肝肾功能损伤等,常常导致化疗无法顺利进行,严重影响患者下一步治疗,甚至会引起病情反复发作和加重。并且伴随抗肿瘤化疗药物的不断出现,其药物不良反应种类也在不断增加,而大多数抗化疗药物不良反应的西药疗效却十分有限。体外高频热疗属于物理疗法的一种,其治疗恶性肿瘤机理主要是对体腔深部进行局部加热,能够达到杀伤肿瘤细胞、调节免疫、提高化疗敏感度以及避免正常细胞遭受损失的功效[17-18]。但单独应用体外高频疗法治疗取得的疗效较有限,靶向治疗作用较多,仍具有一定的局限性。
中医认为正气存内,邪不可干,正气亏虚,气血不足是肿瘤疾病发生的内因,肿瘤形成后继续耗损气血,正气日渐亏虚,从而导致肿瘤得不到有效控制,病情持续恶化,甚至向远处扩散和转移。化疗、放疗、手术等西医治疗措施属“攻伐之法”,会进一步加重正气亏虚。恶性肿瘤疾病化疗后引起的不良反应归属中医学中“虚劳”范畴,中医认为长期使用化疗药物,其毒性会损伤脾胃,导致气血生化乏源,形成气血两虚的中医证候。本研究以气血两虚证候为根据,以益气健脾、活血养血为治则,选择八珍汤对抗化疗引起的不良反应,八珍汤由四君子汤合四物汤组成,有益气补血之功效,能够显著提高人体抵抗力。处方中人参补脾益肺、生津养血,能大补元气;白术为补虚要药,甘补渗利,有健脾益气、燥湿利水之功;茯苓性平,归脾经,有健脾宁心之功;白术与茯苓配伍,能增强健脾渗利之功;当归活血补血,为血中之要药;熟地黄滋阴养血;川芎活血行气、祛风止痛;白芍柔肝养血;甘草补气健脾、缓急止痛,并有调和诸药之功。诸药配合,共收气血双补之功。现代药理学研究表明,人参对提高人体免疫功能具有明显作用,同时还有保护肝脏功能、抗肿瘤、抗炎、抗溃疡、抗应激的作用[19];白术具有抗肿瘤、抗炎性反应、保肝、调节免疫系统及调节免疫代谢的作用[20];茯苓具有增强机体免疫功能、镇静、保肝、抗肿瘤、抗炎、保护胃肠功能的作用[21];当归具有镇痛、抗炎、抗氧化、抗肿瘤、保肝、增强机体免疫功能的作用[22];川芎具有镇痛、抗肿瘤、抗炎、细胞保护的作用[23];白芍具有增强免疫功能、镇痛、保肝、抗炎的作用[24]。另外,根据研究证实,八珍汤能够改善骨髓抑制状态,刺激骨髓细胞增殖,促进白细胞、红细胞等细胞集落生成,促进外周血恢复[25],能够拮抗减轻化疗后消化道毒性,拮抗化疗后肝肾毒性、骨髓毒性,效果良好[26]。
体外高频热疗主要是借助热量达到破坏及杀死癌细胞的目的,一般情况下,正常组织和肿瘤组织对高热的敏感性存在差异,正常组织对温度的安全界值是45℃,局部可长时间耐受42℃~43℃高热,而肿瘤细胞在42℃以上就能很快被灭活。因此通过体外高频治疗的高热可有效抑制肿瘤细胞DNA、RNA 的合成,破坏癌细胞骨架,诱导癌细胞死亡。同时,高热还能促进化疗药物吸收,减少化疗药物给机体带来的不良反应。在化疗基础上配合八珍汤与体外高频治疗可发挥明显互补增敏作用,降低单纯化疗的不良反应,提高远期生存率。本研究结果显示,观察组治疗后各项中医证候积分、免疫功能指标、生活质量评分改善情况均明显优于对照组,化疗药物不良反应发生率低于对照组,而无进展生存期与总生存期以及治疗总获益率均高于对照组。证实八珍汤与体外高频治疗联合应用于肿瘤患者化疗的不良反应的治疗,具有明显的增效减毒作用,能够减轻化疗药物不良反应,调节机体免疫功能,增强机体的抗病能力,改善患者的机体状况,从而抑制肿瘤细胞的生长。

