氨基醇改性GO/CNTs复合气凝胶的制备及对盐湖卤水硼的吸附
崔香梅,潘彤彤,罗清龙,边富璇,叶秀深
(1.青海大学,青海西宁 810016;2.中国科学院青海盐湖研究所,青海西宁 810008;3.中国科学院盐湖资源综合高效利用重点实验室,青海西宁 810008;4.青海省盐湖资源化学重点实验室,青海西宁 810008)
硼及其化合物在众多民生和高科技领域具有广泛应用[1]。但同时,硼的超量使用或泄漏会严重危害人体健康、污染土壤、破坏植被,因此对硼的分离意义重大[2]。硼资源主要分为固体硼资源和液体硼资源。在盐湖卤水、地层卤水和油田卤水中,硼与Na+、K+、Mg2+、Ca2+、Cl-、SO42-和Li+等多种有价组分共存,从中提取硼能有效提高卤水资源利用率和缓解硼资源短缺问题。目前,从卤水中分离提取硼的方法主要有酸化法、沉淀法、分级结晶法、离子交换法、溶剂萃取法和吸附法等[3-4]。这些方法各有优势和不足,其中吸附法适用于低浓度硼的分离,具有选择性高、分离效果好、操作简单、无污染、吸附剂可循环利用等优点[5]。吸附分离硼主要依据多元醇功能基团与硼氧离子的化学络合作用。一般认为,碱性稀溶液中硼sp3杂化,以B(OH)4-形式与多元醇功能基团之间形成稳定四面体结构而达到高效分离硼的目的。前期研究表明[6],硼的吸附也可以采用体系中H+浓度,即溶液的pH 来解释。硼吸附剂从一开始的天然吸附剂到目前的新型高分子材料经历了长期的发展,根据使用材料的类型不同,可分为无机吸附剂、有机吸附剂和天然吸附剂3类。其中,活性炭、葡甲胺或葡萄糖等多元醇功能化的有机二氧化硅、功能化的苯乙烯或甲基丙烯酸缩水甘油酯等单体聚合的共聚物、金属有机框架材料[7]、多元醇功能化的有机共价材料等,都展现出良好的硼吸附容量和循环寿命。大部分硼吸附剂仍然在原料安全性、成本、合成工艺等方面存在问题,所以,对新型硼吸附剂的研发仍具有重要意义。
氧化石墨烯(GO)表面含有大量含氧官能团,具有比表面积较大和亲水性较好的性质,可与其他材料复合使其获得更好的相容性和更多新特征,从而提高复合材料的适用性和利用率。碳纳米管(CNTs)具有较大的特征表面、趋于完美的中空或镂空结构及有助于有效分离分子的高质量密度等优异性能,在吸附脱除各种金属及重金属、染料和有机物质方面显现出优越性。
本文以三维网状氧化石墨烯和多壁碳纳米管制备的新型高比表面积气凝胶作为载体,构筑了氨基和表面羟基化的氧化石墨烯/碳纳米管气凝胶硼吸附剂,旨在协同实现增强对硼的吸附作用,从而提升硼的吸附量。
1 实验部分
1.1 实验试剂
氧化石墨烯、碳纳米管;L-抗坏血酸、羧甲基纤维素钠、2-氨基-1,3-丙二醇、N,N-二甲基甲酰胺、硼酸、氯化钾、氯化钠、氯化镁和氯化锂,均为分析纯。
1.2 氧化石墨烯/碳纳米管气凝胶的制备
首先将3 mg/mL 的氧化石墨烯[8]水溶液与碳纳米管[9]水溶液按照7∶3 的体积比例混合(共100 mL),在混合液中加入3 g 的L-抗坏血酸和1 g的羧甲基纤维素钠,超声处理至固体与溶液混合均匀,将混合液倒入水热反应釜中,在95 ℃反应10 h。待反应结束后,冷冻干燥后获得氧化石墨烯/碳纳米管(GO/CNTs)气凝胶。
1.3 氨基醇改性氧化石墨烯/碳纳米管气凝胶硼吸附剂的制备
称取0.3 g氧化石墨烯(GO)加入100 mL去离子水中,再称取碳纳米管(CNTs)0.1286 g加入42.87 mL去离子水,将GO 溶液和CNTs 溶液超声混合均匀。然后加入L-抗坏血酸(0.9 g)和羧甲基纤维素钠(0.03 g),继续超声至混合均匀。称取6 g的2-氨基-1,3-丙二醇与10 mL去离子水搅拌溶解,加入上述混合溶液中搅拌均匀。将混合液倒入水热反应釜中,在100 ℃下反应9 h。待反应结束后冷冻干燥,获得的气凝胶再次放入反应釜中,加入环氧氯丙烷在125oC反应10 h,再次待反应结束后加入N,N-二甲基甲酰胺(DMF),静置15 min 后过滤,将固体用去离子水洗涤5~6次,然后冷冻干燥,得到氨基醇改性的氧化石墨烯/碳纳米管(GO/CNTs)气凝胶硼吸附剂。
1.4 表征方法
在常规测试条件下,对吸附前后的吸附剂采用扫描电镜 (SEM,JSM-5600V)、傅立叶红外分析(FT-IR,Nicolet 6700)、X射线光电能谱(XPS,Fisher Scientific K-Alpha)进行形貌、结构分析表征。用甲亚胺-H分光光度法[10]测定水溶液中的硼。
1.5 吸附-脱附实验
采用静态吸附法研究硼的吸附行为。具体实验条件在相应的实验部分阐述。吸附量和吸附行为研究采用文献[11]报道方法。
分离与脱附:氨基醇改性的氧化石墨烯/碳纳米管气凝胶呈块状,因此分离相对较容易,采用布氏漏斗固液分离后,利用0.1 mol/L 的盐酸溶液脱附,并用去离子水洗涤后,采用0.05 mol/L 的氢氧化钠溶液还原,再次用去离子水洗涤至pH为9左右后进行循环吸附实验。
2 结果与讨论
2.1 表征分析
图1 为氧化石墨烯/碳纳米管气凝胶改性前和改性后的红外光谱图。从图1 可以看出,改性前在3 347 cm-1处的峰归属于石墨烯和碳纳米管表面—OH的伸缩振动,而改性后在3 433 cm-1处的—OH峰强度和宽度加强,说明氨基醇成功嫁接到氧化石墨烯/碳纳米管气凝胶表面。改性前在3 698 cm-1处的峰归属于—NH2的伸缩振动,而改性后消失,说明氨基醇内的氨基与环氧氯丙烷的环氧基发生开环反应,以致改性后氨基峰消失,说明氨基醇改性的氧化石墨烯/碳纳米管气凝胶硼吸附剂已形成。

图1 氧化石墨烯/碳纳米管气凝胶改性前和改性后的红外光谱图Fig.1 FT-IR spectra of graphene oxide/carbon nanotube aerogels before and after modification
图2 为氧化石墨烯/碳纳米管气凝胶改性前后的SEM 照片。在放大相同倍数(100 倍)的情况下,未改性(图2a)吸附剂表面虽有孔洞,但分布不规则、不均匀,而经2-氨基-1,3-丙二醇改性后(图2b)吸附剂表面呈三维网状结构,孔洞分布较为规律,且将其中骨架放大至800 倍后,可清晰看到吸附剂表面凹凸不平,其比表面积增大有利于对硼的吸附。

图2 氧化石墨烯/碳纳米管气凝胶改性前(a)和改性后(b)的SEM照片Fig.2 SEM images of graphene oxide/carbon nanotube aerogel before(a) and after modification(b)
图3 是氨基醇改性的氧化石墨烯/碳纳米管气凝胶硼吸附剂的N2吸附/解吸等温线图和BET 孔径分布曲线图;表1列出了吸附剂的BET比表面积、孔体积、平均孔径。由图3可以看出,吸附等温线在初始阶段(p/p0<0.85)开始上升,为Ⅲ型,接着(p/p0>0.85)与具有滞后环的Ⅳ型一致,说明结构的主要部分是大孔,小部分是介孔。此外,吸附剂吸附等温线在p/p0=0.85 时,属于有磁滞回线的H3 型,说明材料有颗粒或者狭缝状孔隙的特征[12]。

表1 吸附剂的BET比表面积、孔体积和平均孔径Table 1 BET specific surface area,pore volume and average pore size of adsorbent

图3 氨基醇改性硼吸附剂的N2吸/脱附等温线和BJH孔径分布曲线Fig.3 N2 adsorption-desorption isotherm and BJH pore size distribution curve of amino alcohol modified boron adsorbent
图4为GO/CNTs吸附剂吸附硼后的XPS全谱和硼的XPS谱图分析结果。由图4a可知,GO/CNTs 吸附剂吸附硼后检测到C、O、N、Cl和B元素,再结合图4b可知,改性后吸附剂上的多羟基官能团与硼络合形成了化学键,H3BO3、B(OH)4-、B3O(3OH)4-/B3O(3OH)52-与GO/CNTs的多羟基形成的B—O键的B 1s结合能分别为190.1、190.7、191.3 eV[13-14]。以上结果表明氧化石墨烯/碳纳米管(GO/CNTs)气凝胶成功被氨基醇所修饰,且大量—OH 的存在可有效促进硼的快速吸附。
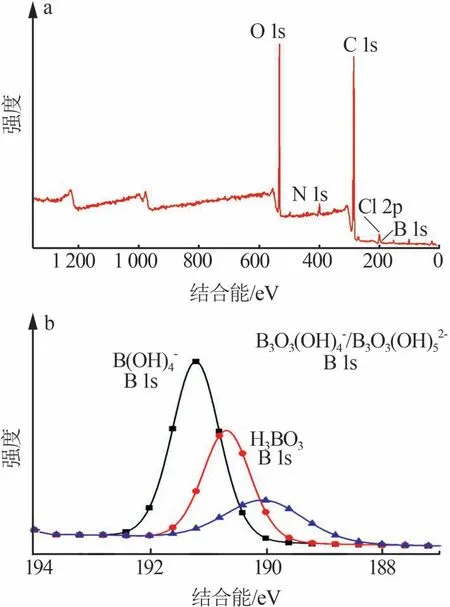
图4 GO/CNTs吸附剂吸附硼后的XPS全谱(a)和硼的XPS谱图(b)Fig.4 XPS full spectrum(a) and boron XPS spectra(b)of GO/CNTs adsorbent after adsorption
2.2 吸附实验
2.2.1 pH影响
水溶液中硼氧配阴离子的形式复杂而多样。大量实验结果表明,在水溶液中主要有6 种形式的硼酸根阴离子[15-16],具体如图5所示。

图5 硼氧配阴离子在溶液中的主要形态[15-16]Fig.5 Main forms of boron-oxygen anions in solution[15-16]
图6 为硼酸根阴离子在水溶液中的形态分布。由图6可知,每种阴离子在不同pH环境中的分布和比例都不同[17]。此外,GO/CNTs 气凝胶吸附剂的正负电性质、质子与去质子平衡受pH影响较大,且pH会影响GO/CNTs 气凝胶吸附剂的吸附性能[18-19],因此研究了GO/CNTs 气凝胶吸附剂在pH=8.0~12.0 的不同硼溶液下的吸附能力。图7 为吸附剂在不同pH 和初始硼浓度溶液下的硼吸附特性。由图7 发现,GO/CNTs 气凝胶吸附剂在pH=10 时对不同初始质量浓度的硼溶液都具有最佳吸附性能,碱性环境有利于吸附反应的进行[20]。硼酸是一种弱酸,当硼溶液呈酸性时,硼主要以H3BO3的形式存在;当溶液为中性时,硼主要以多硼酸盐的形式存在;当溶液为碱性时,硼主要存在形式为B(OH)4-。当pH=7.5~9.5时,H3BO3转化为B(OH)4-和聚阴离子物质[21],此时GO/CNTs 气凝胶吸附剂可吸附的硼阴离子种类增多,吸附性能提高,硼物种与GO/CNTs 气凝胶吸附剂之间的吸附机理如图8所示[22-24];当pH>10时,硼基本全部转化为B(OH)4-,表明GO/CNTs 气凝胶吸附剂与带负电荷的B(OH)4-之间的静电排斥作用增强,削弱了吸附作用,导致吸附性能下降[25]。
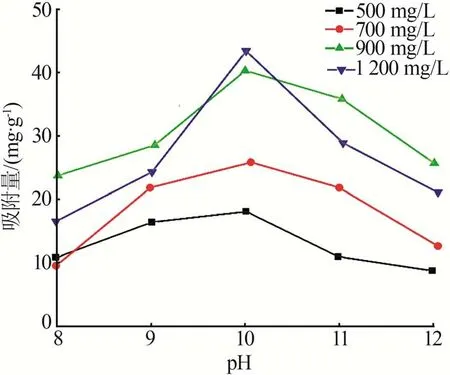
图7 吸附剂在不同pH溶液下的硼吸附特性Fig.7 Boron adsorption characteristics of adsorbents in different pH solutions

图8 硼酸盐阴离子物种与多元醇吸附剂之间的络合方式[22-24]Fig.8 Complexation mode between borate anion species and polyols adsorption[22-24]
2.2.2 初始浓度和温度对硼吸附的影响
分别配制初始质量浓度为400、500、600、700、800、900、1 000、1 100、1 200 mg/L 的硼溶液,调节上述溶液的pH为10±0.1。分别量取50 mL pH为10的不同浓度硼酸溶液,并加入(0.3±0.05) g 的吸附剂,放入恒温振荡器中在25 ℃振荡1 h 后进行吸附实验。图9为不同初始硼浓度和温度对硼吸附性能的影响。由图9a可知,随着初始硼浓度的不断增大硼的吸附量不断增加,直至硼初始质量浓度为1 200 mg/L时,吸附量基本达到最大(43.42 mg/g)。此后随着硼浓度继续增大硼的吸附量无明显变化。此外,25、30、35、40、45、55 ℃时氨基醇改性的GO/CNTs气凝胶硼吸附剂对硼的吸附情况如图9b所示。由图9b可知,随着温度升高硼的吸附量呈现先增加后减小的趋势,当温度为35 ℃时,氨基醇改性的GO/CNTs 气凝胶吸附剂的硼吸附性能最佳(46.73 mg/g)。表2 总结了文献中报道的硼吸附性能数据,对比后发现本研究制备的氨基醇改性GO/CNTs 气凝胶硼吸附剂的性能优于大多数吸附剂。这是因为GO/CNTs 气凝胶吸附剂为三维网状结构且表面富含羟基,经过氨基醇改性后大量的多元醇被负载,使得GO/CNTs复合气凝胶与多元醇协同实现了硼的高效吸附。此外,氨基带正电、硼阴离子带负电,负载大量氨基醇后使得硼阴离子在静电作用下不断地与多元醇络合,三者协同达到硼的高效吸附。
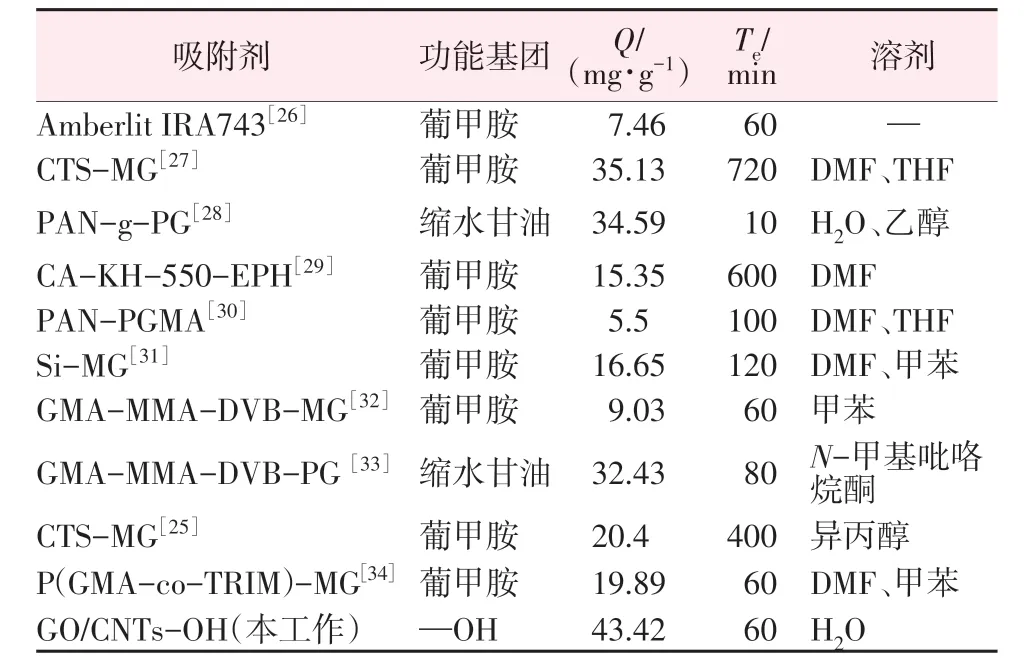
表2 本文吸附剂与文献报道的吸附剂对比Table 2 Comparison of adsorbents with those reported in literatures

图9 硼初始质量浓度(a)和温度(b)对硼吸附性能的影响Fig.9 Effect of initial boron mass concentration(a) and temperature(b) on boron adsorption
2.2.3 吸附时间对硼吸附性能的影响
量取50 mL 质量浓度为700 mg/L、pH 为10±0.1的硼酸溶液,加入(0.3±0.05) g 的氨基醇改性的GO/CNTs气凝胶吸附剂,放入恒温振荡器中,在温度为25 ℃下振荡10~240 min,进行吸附实验,结果如图10所示。由图10可知,硼的吸附量随时间延长不断增加,至240 min时吸附量基本达到最大。这是由于反应过程中硼迅速与吸附剂表面的吸附位点结合,吸附量逐渐升高,120 min后吸附基本达到饱和,其吸附量也不再发生明显变化。利用准一阶和准二阶动力学模型模拟和分析吸附剂的吸附过程,拟合数据列在表3 中。结合图10 和表3 可知,硼在吸附剂上的吸附行为更符合准二阶动力学模型,属于硼与吸附剂多羟基之间的化学络合作用,实验值与计算值基本保持一致。
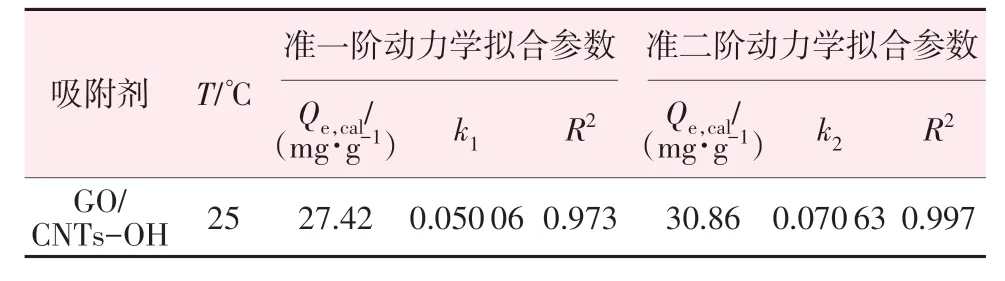
表3 硼吸附的动力学参数Table 3 Kinetic parameters of boron adsorption

图10 接触时间对硼吸附性能的影响Fig.10 Effect of contact time on boron adsorption
2.3 实际卤水吸附、循环和离子干扰影响因素评价
表4 为西台吉乃尔盐湖卤水组成,图11 为吸附剂在无机盐溶液干扰下的硼吸附性能及其在实际卤水中的循环使用性能。用氨基醇改性的GO/CNTs气凝胶吸附剂直接吸附西台吉乃尔盐湖某卤水中的硼,1 h 达到吸附平衡且吸附量为10.89 mg/g。在硼(1 050 mg/L)和锂(1 270 mg/L)共存的溶液中,分别加入1 000 mg/L 的NaCl、MgCl2和KCl 后测定吸附剂的硼吸附性能(见图11a),发现KCl对于该吸附剂吸附硼的影响较大。此外,为了验证吸附剂的循环使用寿命,对吸附剂进行酸脱附-碱还原后循环使用,如图11b 所示,经5 次吸附-脱附循环后吸附容量降低到8.10 mg/g,这可能是由于氨基醇改性的GO/CNTs气凝胶在酸碱和高浓盐卤水作用下结构容易坍塌,亦或在酸碱作用下功能基团脱落,导致吸附容量降低[35]。

表4 西台吉乃尔盐湖卤水组成Table 4 Composition of West Taijinar salt lake brinemg/L

图11 吸附剂在无机盐溶液干扰下的硼吸附性能(a)及其在实际卤水中的循环使用性能(b)Fig.11 Boron adsorption performance of adsorbent under interference of inorganic salt in solution(a) and its recycling performance in actual brine(b)
3 结论
1)本文采用水热法以2-氨基-1,3-丙二醇、碳纳米管、氧化石墨烯、L-抗坏血酸、羧甲基纤维素钠为原料制备了氨基醇改性的GO/CNTs 气凝胶吸附剂,该凝胶吸附剂具有多孔、高比表面积的特征。
2)氨基醇改性的GO/CNTs 气凝胶吸附剂具有丰富的多元醇基团的多孔结构,在碱性条件下吸附性能较好,pH=10、C0=1 200 mg/L时对硼最大平衡吸附量达43.42 mg/g,吸附过程符合准二阶动力学模型,吸附剂在单一溶液中具有良好的硼吸附性能和较强的抗干扰离子的性能,并在实际卤水中展现出一定的硼吸附特性。由于氨基醇改性的碳基(氧化石墨烯和碳纳米管)凝胶吸附剂的溶损、脱落现象,该吸附剂在实际卤水中的应用工艺有待进一步深入探索。

