MOFs 仿生酶传感器构筑及对肌氨酸的高灵敏检测
吴玮轩,杨欣,赵钟兴
(广西大学 化学化工学院,广西南宁 530004)
前列腺癌作为一种常见的恶性肿瘤严重危害人体的健康,其早期的诊断技术以筛查重要的肿瘤标志物为主[1-3]。目前最常用的前列腺肿瘤标志物为前列腺特异性抗原(PSA)和肌氨酸(Sar),PSA 并非前列腺癌的特异性抗原,以PSA 作为标志物对前列腺癌的检测常常出现假阴性和假阳性的情况[4-7]。近年来对Sar 的研究发现,Sar 在血液和尿液中的浓度与前列腺癌关系密切,是更理想的前列腺肿瘤标志物,如何快速、灵敏、低成本检测Sar 的浓度对前列腺癌的早期诊断至关重要[8]。
金属-有机框架材料(Metal-Organic Frameworks,MOFs)是由金属离子或金属簇与有机配体,通过配位键自组装形成的,具有独特孔道结构的多孔结晶材料[9]。由于其独特的孔结构、良好的稳定性以及特殊的催化位点,MOFs 材料在纳米酶传感器方面获得广泛关注[10-12]。设计新型MOFs 纳米酶传感器并探究其实际应用仍是当下研究的热点。ZHAO 等[13]利用铁基金属有机框架(NH2-MIL88B(Fe),NM88B)作为过氧化氢酶纳米酶,将H2O2催化生成·OH,进而将3,3’,5,5’-四甲基联苯胺(TMB)氧化为蓝色的TMBox。当通过NM88B 对多巴胺分子(DA)进行检测时,DA 消耗·OH 从而抑制氧化反应,导致蓝色的TMBox 消失,并且DA 还可以通过电子转移的方式将NM88B 的蓝色荧光猝灭。因此,可以利用NM88B比色和荧光双模式检测DA,在实际样品检测中也具有较好的检测效果,表明该MOFs 纳米酶具有良好的实际应用价值。YANG 等[14]将钴基金属有机框架(ZIF-67)作为人工纳米酶平台电沉积到阿霉素硼纳米片(BNSs-DOX)上,制备得到UOx@MOF/BNSs-DOX 纳米电化学传感器,用于尿酸(UA)的酶促和电化学检测,纳米酶的高效负载使UA 检测下限可达0.025 μmol/L。因此,构筑具有良好催化活性的纳米酶,并将其应用于生物传感器是一个有实际价值的研究方向。
本论文基于Sar 的酶级联反应,提出复合仿生酶级联的策略,设计出NH2-MIL88B(Fe)/ 核黄素(NM88B/Rf)电化学传感器以促进催化H2O2的产生,并将级联信号放大(从H2O2到·OH),来实现对Sar的高灵敏检测。
1 材料与方法
1.1 试剂与仪器
核黄素(Rf)、肌氨酸、六水合氯化铁、2-氨基对苯二甲酸、氢氧化钠,分析纯,上海麦克林生化科技有限公司;N,N-二甲基甲酰胺(DMF)、丙酮,分析纯,天津市科密欧化学试剂有限公司;磷酸二氢钠、磷酸氢二钠,分析纯,上海阿拉丁生化科技有限公司;无水乙醇,分析纯,四川西陇科学股份有限公司;甲基蓝(MB),98.5%,广东光华科技有限公司。
ME204E 型电子天平,梅特勒-托利多仪器(上海)有限公司;DHG-9076A 型电热恒温鼓风干燥箱,上海精宏实验设备有限公司;DZF-6051 型真空干燥箱,上海齐欣科学仪器有限公司;1702742S型超声波清洗机,南京先欧仪器制造有限公司;01301T08913 型超薄磁力搅拌器,上海泰坦科技股份有限公司;PHS-3C 型pH 计,上海雷磁仪器有限公司;SU8020 型高分辨场发射扫描电镜,日本日立公司;SMATLAB3KW 型X-射线衍射仪,日本理学株式会社;TU-1901 型紫外-可见分光光度计,深圳市亿鑫仪器设备有限公司;PARSTAT 4000+型电化学工作站,美国阿美特克集团公司。
1.2 NM88B 的制备
分别称量270 mg(1 mmol)FeCl3·6H2O 和181 mg(1 mmol)2-氨基对苯二甲酸于反应釜中,加入5 mL 的DMF,400 r/min 搅拌30 min;再加入0.4 mL氢氧化钠溶液(2 mol/L),400 r/min 搅拌30 min;使用真空干燥箱在100 ℃下干燥12 h 可得到深褐色固体粉末状材料。
1.3 改性电极的制备
在改性电极之前,使用0.30 μm 氧化铝粉末抛光玻碳电极(GCE,d=5 mm),再使用蒸馏水洗涤GCE,洗涤后的GCE 放置在室温下干燥。在改性电极时,将1.5 mg 的样品NM88B 分散在1 mL 超纯水中,于室温下40 kHz 水浴超声处理5 min 后形成均匀悬浮液,再将20 μL 的悬浮液滴涂在GCE 上并在红外线灯的照射下干燥,得到改性电极NM88B/GCE。
1.4 肌氨酸传感器的制备
将改性电极NM88B/GCE 放入1 100 mL 的核黄素水溶液中(1 mmol/L),在电化学工作站的STEP 模式下设置-0.6 V 电压,时间90 s 的条件下电沉积,再将电极取出,使用超纯水清洗电极表面1 次。室温干燥后即得NM88B/Rf/GCE。
1.5 NM88B 结构表征
扫描电子显微镜(SEM):将微量NM88B 固定于样品台上,在10 kV 电压下放大50 倍图像即可观察NM88B 的形貌。
X 射线晶体衍射(XRD):将2 mg NM88B 压制于显微镜载片上,于室温下进行测量。
1.6 NM88B 电化学表征
实验采用三电极体系。循环伏安法(CV)的扫描电位范围为-0.4 ~0.6 V,扫描速度为50 mV。电化学阻抗谱(EIS)扫描频率为0.1 ~105 Hz;实验温度为室温。
1.7 NM88B 的类酶催化
分 别 将20 μL 的NM88B(1 mg/mL)、TMB(0.5 mmol/L)与不同浓度H2O2底物(0.4 mmol/L、0.8 mmol/L、1.2 mmol/L、1.6 mmol/L、2.4 mmol/L 和2.8 mmol/L)进行稳态动力学实验;保持NM88B 添加量(20 μL,1 mg/mL)和H2O2浓度(30 mmol/L)不变,改变TMB底物浓度(0.4 mmol/L、0.8 mmol/L、1.2 mmol/L、1.6 mmol/L、2.4 mmol/L 和2.8 mmol/L)进行稳态动力学实验。动力学数据可根据Michaelis-Menten 方程计算,见式(1):
式中,Km为米氏常数,mmol/L;Vmax为酶被底物饱和时的反应速度,μmol/(L·min);S为底物浓度,mmol/L;V为反应速率,μmol/(L·min)。
1.8 传感器对Sar 的定量检测
在PBS 缓冲液pH=7.5、NM88B 滴涂量为1.5 mg/mL、Rf 电沉积时间为90 s 的条件下进行Sar 的定量检测实验。加入500 μmol/L MB 参与级联反应的催化中间体时,在-0.28 V 时出现明显增加的电信号,因此采用信号增强的方式分析Sar 的浓度。
1.9 传感器的选择性和时间稳定性
传感器选择性:将100 μmol/L 的丝氨酸(Ser)、葡萄糖(Glu)、赖氨酸(Lys)、半胱氨酸(Cys)、氯化钾(KCl)和氯化钠(NaCl)分别加入含有MB 的溶液中进行抗干扰检测,其余实验条件及步骤与Sar 定量检测相同。
传感器时间稳定性:同时制备3 个相同的NM88B/Rf/GCE 传感器,分别在-4 ℃下储存1 d 和7 d,在包含1.0 μmol/L Sar 的0.1 mol/L PBS 缓冲液(pH=6.5)中进行实验。
2 结果与分析
2.1 NM88B 的结构表征
从图1(b)中可看到,通过溶剂热法所制备的NM88B 材料颗粒大小和尺寸较均匀,平均尺寸约为500 nm,晶体结构规整,表面光滑,呈现出纺锤形结构,与文献报道一致[15]。图1(a)为溶剂热法合成NM88B 的XRD 谱图,在2θ=9.2°、10.3°、13.1°、16.7°、18.5°、20.7°和29.5°出现衍射峰,分别对应(002)、(101)、(102)、(103)、(200)、(202) 和(302)晶面。衍射峰与晶体学信息文件(CCDC No. 647646)中建立的NM88B 结构模拟谱图一致,说明NM88B 材料成功制备。

图1 NM88B 的结构表征结果
2.2 电化学表征
图2 为在含有0.1 mmol/L KCl 的5 mmol/L [Fe(CN)6]3-/[Fe(CN)6]4-溶液下的CV 和EIS 曲线。从图2(a)可知,裸电极具有较大的峰值电位分离(∆EP=321.8 mV),对[Fe(CN)6]3-/4-探针具有较小的电流响应(Ipa=108.5 μA,Ipc=-121.3 μA);而NM88B/GCE 的响应电流明显高于裸电极(Ipa=238.1 μA,Ipc=-256.7 μA),峰值电位明显减小(∆EP=133.2 mV),这主要是由于在电极上滴涂了大比表面积的NM88B,增大了电极的表面积,促进了电极的电子转移。相比于NM88B/GCE,NM88B/Rf/GCE 传感器的电位峰分离几乎不变(∆EP=135.9 mV),而其响应电流显著减小(Ipca=158.6 μA,Ipc=-177.2 μA),这说明由电沉积将电子传递能力较弱的Rf 引入MOFs 骨架中,NM88B 孔道被部分阻塞导致氧化还原峰电流降低。
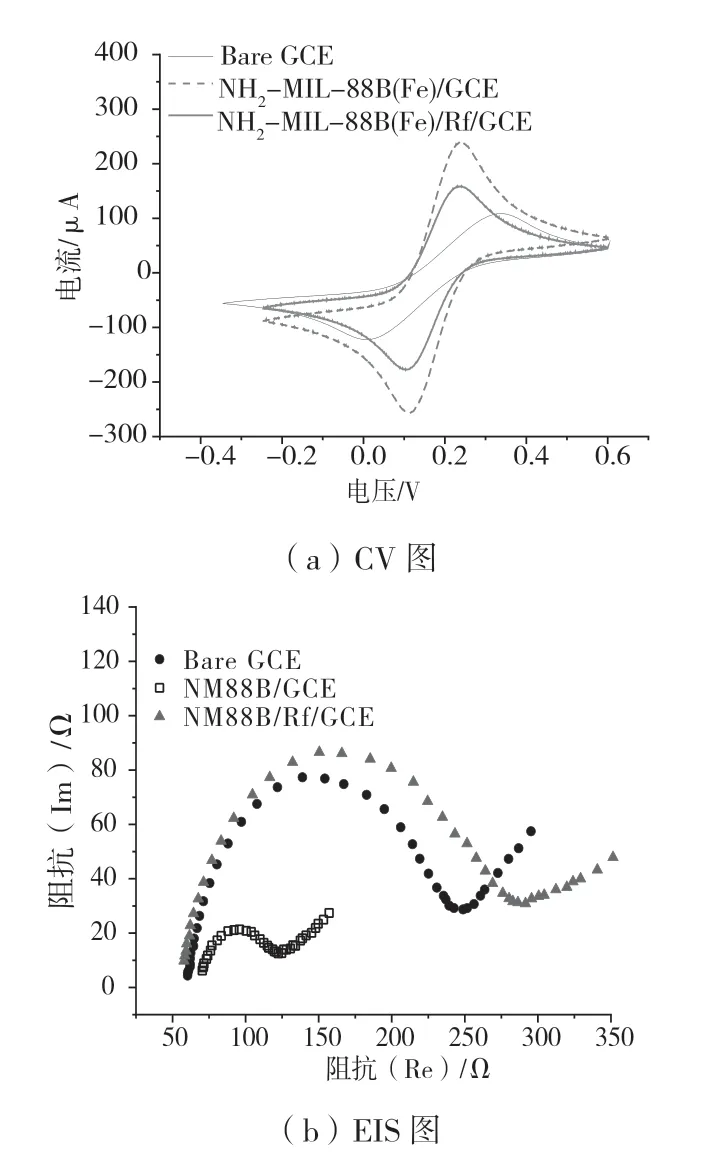
图2 裸电极、NM88B/GCE 以及NM88B/Rf/GCE 的电化学表征
图2(b)为1.0 ~100.0 kHz 的开路电位条件下测量所得EIS 谱,通过Zview 软件对所得数据进行拟合,得到其阻抗参数。NM88B/GCE 和NM88B/Rf/GCE电荷转移电阻(Rct)分别为169.5 Ω 和174.1 Ω,与NM88B/Rf/GCE 的Rct 相比,NM88B/Rf/GCE 的转移电阻较大,这是因为在原材料上电沉积了电子传递能力较弱的Rf,这也侧面说明了Rf 的成功负载。此外,EIS 拟合所得数据和CV 测试图结果一致,再次说明了NM88B 的成功制备和Rf 的成功负载。
2.3 NM88B 的类酶催化
通过测定反应的表观稳态动力学参数,进一步分析了NM88B 的类过氧化物酶活性,通过改变H2O2或TMB 的浓度,得出Michaelis-Menten 方程,并通过该方程斜率和截距计算出最大反应速度(Vmax)和米氏常数(Km)。已知,Km和Vmax是量化酶催化能力的两个关键参数,其中Km是酶对底物的亲和力,Km值越小,酶对底物的亲和力越高。从图3 可知,H2O2为底物的Km值为1.02 mmol/L,以TMB 为底物的Km值为1.11 mmol/L。相较于类似实验报道的辣根过氧化物酶(HRP)的Km值(H2O2和TMB 的Km分别为2.61 mmol/L 和0.53 mmol/L)[16],NM88B 以H2O2为底物的Km低于HRP,而以TMB 为底物的Km高于HRP,这说明NM88B 对H2O2的亲和力大于HRP,对TMB 的亲和力小于HRP。这是因为HRP 的活性中心只有一个Fe 离子,而NM88B 有多个Fe 离子,且材料的介孔结构有利于H2O2与Fe 离子的反应,同时也表明NM88B 具有良好的类过氧化氢酶催化活性。

图3 NM88B 模拟类过氧化氢酶稳态动力学实验
2.4 NM88B/Rf/GCE 传感器对Sar 的定量检测
如图4 所示,·OH 的氧化峰电流随着Sar 的浓度增加而增加,并在1 nmol/L ~10 mmol/L 的范围内呈线性关系,线性方程为Ipa=3.18lgCSar+25.85(R2=0.999),检出限(S/N=3)为0.43 nmol/L。从这些结果可以看出,NM88B/Rf/GCR 传感器在MB 的存在下对Sar 的检测具有高灵敏度和选择性,其主要原因是NM88B 的结构有助于Rf 催化Sar 生成的H2O2立刻被NM88B 催化氧化成·OH,使酶级联效应高效地发生。此外,和其他报道相比(表1),NM88B/Rf/GCR 传感器对Sar 具有较低的检出限和较宽的检测范围。

表1 与不同修饰电极对Sar 的电化学检测比较
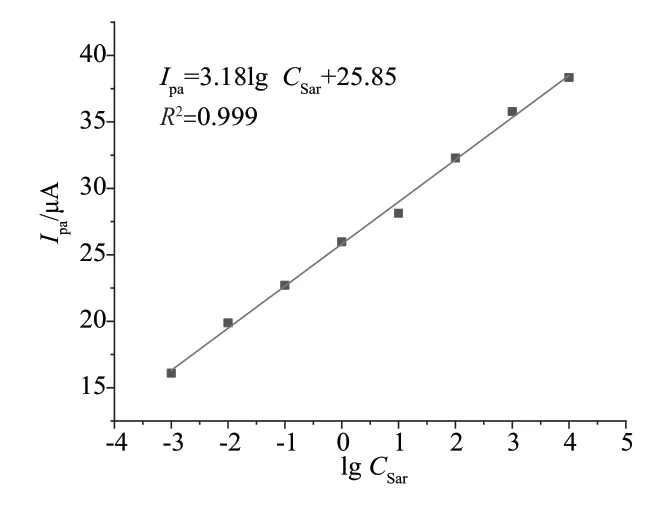
图4 Sar 检测标准曲线
2.5 NM88B/Rf/GCE 传感器的选择性和时间稳定性
为了探究NM88B/Rf/GCE 对Sar 检测的抗干扰能力,研究了几种Sar 类似物存在下的DPV 曲线。如图5所示,首先进行空白样品(Blank)的测试,再加入其他干扰物不能引起氧化峰电流的显著增加,其与空白值的相对误差在±8%之间,说明NM88B/Rf/GCE 传感器表现出优异的抗干扰性。

图5 NM88B/Rf/GCE 传感器的选择性
为了探究传感器的时间稳定性,对依次保存0 d、1 d 和7 d 的电极进行测试,三次实验的电流响应值分别为27.68 μA、27.61 μA 和26.68μA,NM88B/Rf/GCE 传感器对Sar 的响应没有明显下降,Sar 的电流响应值仍然保留在初始值的96.4%,表明NM88B/Rf/GCE 具有良好的稳定性。
3 结论
本文通过溶剂热法合成具有高比表面积、开放的活性金属位点以及类过氧化物酶活性的NM88B材料,并将其与成本低、低毒性、稳定性好的具有类肌氨酸氧化酶活性的Rf 通过氢键作用相结合,制备了能对前列腺癌标记物Sar 高灵敏检测的电化学传感器,并在检测体系中加入能够被·OH 氧化的MB 来增强电化学响应电流,结论如下:
通过溶剂热法合成NH2-MIL88B(Fe),其SEM 和XRD图均与文献报道一致,说明了合成方法的可行性。由稳态动力学分析发现NM88B 具有类过氧化物酶活性,并且能将Rf 催化氧化Sar 生成的H2O2分解成·OH对MB 进行氧化,因此它可以作为电化学传感器运用于Sar 的检测。最后通过电化学工作站的CV、DPV技术对NM88B/Rf/GCE 进行电化学检测,Sar 的检测范围为1 nmol/L~10 mmol/L,其检出限为0.42 nmol/L。除此之外,在抗干扰性实验中发现其他干扰物对传感器的检测影响相对误差均小于±8%,-4 ℃保存一周后其电流响应值仍然保留在初始值的96.4%,说明了NM88B/Rf/GCE 传感器稳定性良好。

