达芬奇机器人手术治疗肺癌的效果观察
董晓瑜 邵兵
肺癌是目前世界上发病率与死亡率最高的恶性肿瘤, 首选治疗方法为手术切除, 其中包括开胸与微创手术对肺叶进行切除[1,2]。随着胸腔镜技术的普及与发展, 肺癌根治术首选术式已逐渐发展为胸腔镜微创手术, 而且其安全性与有效性得到广泛认可[3,4]。达芬奇机器人手术系统是将多种高科技手段集于一身, 手术医生可操纵机器进行手术, 是目前应用较为广泛且成熟的技术。2002 年达芬奇机器人首次应用于肺部手术, 随后应用于肺癌根治术中。本次研究通过选取本院102 例肺癌患者进行观察, 为临床提供参考依据, 现报告如下。
1 资料与方法
1.1 一般资料 选取本院于2017 年4 月~2020 年12 月间收治的102 例肺癌患者进行研究, 根据手术方式不同分为机器人组和腔镜组, 每组51 例。两组患者一般资料比较差异无统计学意义(P>0.05), 具有可比性。见表1。
表1 两组患者一般资料比较(n, ±s)

表1 两组患者一般资料比较(n, ±s)
注:两组比较, P>0.05
组别例数性别年龄(岁)肿瘤类型男女腺癌鳞癌机器人组51272451.73±5.29483腔镜组51282351.37±5.51474 χ2/t0.0390.3370.153 P>0.05>0.05>0.05
1.2 纳入及排除标准 纳入标准:患者均经CT、实验室及病理确诊为肺癌;患者均在术前完善临床资料;此次研究均获得患者及家属同意并签署知情同意书。排除标准:存在其他脏器转移者;患有严重的肝肾功能性疾病者。
1.3 方法 机器人组患者行达芬奇机器人手术治疗,患者全身麻醉后取健侧卧位, 双肢屈曲抱枕状折刀位。机器人系统包含1 个镜头臂和2 个操作臂, 手术切口应用“8857”的方式, 即腋后线第8 肋间为入镜孔, 腋前线前第5 肋间与肩胛线8 肋间为操作孔, 腋中线第7肋间为辅助口。术者应用达芬奇机器人手臂首先将下肺韧带游离, 根据患者自身的发育情况选择单项式手术途径或解剖式, 摘取相关淋巴结和病变的肺组织, 术后留置1~2 根胸腔引流管。
腔镜组患者行胸腔镜手术治疗, 患者全身麻醉后取健侧卧位, 双肢屈曲抱枕状折刀位。在腋中线第7~8肋间作1.5 cm 切口作为观察口, 腋前线第3~4 肋间作3~4 cm 切口作为主操作孔, 腋后线第6~7 肋间作2 cm切口作为次操作孔, 对支气管及肺血管进行处理, 将病变肺叶及相关淋巴结切除, 术后留置引流管。
两组患者术后均安置在监护病房进行观察, 待病情稳定后转出, 患者麻醉苏醒且体征平稳时嘱患者取半卧位以便于引流。术后对患者的呼吸情况加以关注,配合患者主动咳嗽排痰, 给予雾化吸入, 预防肺内感染。术后指导患者进行康复训练, 吹气球训练3 次/d,5 min/次;缩唇呼吸:以鼻吸气, 缩唇缓慢呼气, 2 次/d,10 min/次;手术侧肢体做爬墙运动3 次/d, 10 min/次。
1.4 观察指标 比较两组患者手术指标及术后住院时间, 手术指标包括术中失血量、手术时间、术中淋巴结清扫数量。
1.5 统计学方法 采用SPSS21.0 统计学软件对数据进行处理。计量资料以均数±标准差(±s)表示,采用t 检验;计数资料以率(%)表示, 采用χ2检验。P<0.05 表示差异有统计学意义。
2 结果
机器人组患者术中失血量明显少于腔镜组, 术中淋巴结清扫数量明显多于腔镜组, 差异具有统计学意义(P<0.05);两组患者手术时间以及术后住院时间比较差异无统计学意义(P>0.05)。见表2。
表2 两组患者手术指标及术后住院时间比较( ±s)
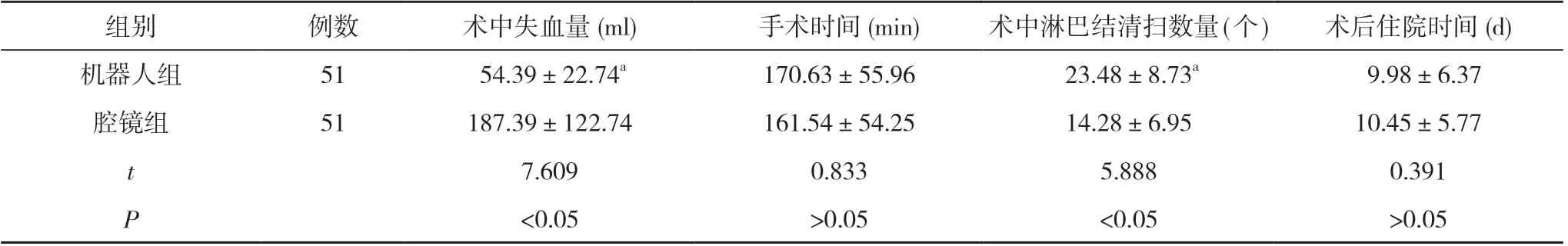
表2 两组患者手术指标及术后住院时间比较( ±s)
注:与腔镜组比较, aP<0.05
组别例数术中失血量(ml)手术时间(min)术中淋巴结清扫数量(个)术后住院时间(d)机器人组51 54.39±22.74a170.63±55.96 23.48±8.73a 9.98±6.37腔镜组51187.39±122.74161.54±54.2514.28±6.9510.45±5.77 t 7.6090.8335.8880.391 P<0.05>0.05<0.05>0.05
3 讨论
据报道肺癌患者预后较差, 在我国肺癌患者5 年生存率为6%~32%[5]。随着医疗检查手段的不断进步,低剂量螺旋CT 广泛应用于肺癌筛查中, 使得肺癌的检出率明显提高, 从而达到早发现早治疗的目的。目前外科手术治疗是肺癌患者的首选方案, 现今微创技术的进步以及手术器械的改进, 胸腔镜手术技术多种样式应用在国内外取得了长足的进步[6]。国内的一些相关资料报导, 与开胸手术比较, 胸腔镜手术显著降低了肺炎、肾衰竭、持续性肺组织漏气及房性心律失常等术后并发症的发生率。但胸腔镜手术还存在一些有待解决的问题, 如空间深度感觉, 操作医生缺乏纵深视觉感受, 特别是在某些深部组织中, 这给手术增加了一定风险;器械操作方向与术者直觉相反, 这就需要术者通过长时间大量的练习才能达到熟练水平;由于手术器械没有活动关节且无法排除操作者手的震颤, 增大了对于狭小空间行深部组织缝扎、止血、打结、吻合及分离等操作难度。随着计算机图文技术、电脑全真模拟仿真技术、机械自动化以及三维成像技术等工程技术的进步, 达芬奇机器人手术系统的研发及应用, 使机械臂取代了外科医生的手臂。
Melfi 等[7]于2002 年报道了首例达芬奇机器人行肺癌根治术后, 通过多年大量临床验证与研究, 达芬奇机器人行肺癌根治术得到了临床的广泛认可。由于达芬奇机器人手术系统成像系统特殊, 可为术者提供3D手术视野, 控制手柄和图像方向一致, 手眼协调性类似于传统开胸手术;不仅无需助手扶镜, 术者还可自行控制镜头, 操作医生不仅可坐在控制台旁, 且无需执行无菌操作规范, 同时不影响医生对复杂手术的操作;仿真手腕7 个自由度突破人手5 个自由度的活动局限,而且完全避免人手震颤, 从而使在狭小空间行精细操作以及行深部组织缝合打结时更加灵活安全。
通过本次研究发现, 两组患者手术时间以及术后住院时间比较差异无统计学意义(P>0.05)。但有研究显示[8,9]机器人组手术时间较长, 这与术者在学习达芬奇机器人初期操作不是很熟练有关, 另外术前机械臂系统的组装也需要消耗一定的时间。本次研究还对术中失血量进行对比发现, 机器人组患者术中失血量明显少于腔镜组, 差异有统计学意义(P<0.05), 这说明由于达芬奇机器人手术系统具有较高的灵活性与精准性, 在手术过程中明显减小了对血管等重要组织的损伤。淋巴结清扫对于肺癌的治疗、判断预后、明确分期以及对后续治疗至关重要, 同时对延长患者生存时间起到重要作用[10-12]。本次研究结果提示, 机器人组术中淋巴结清扫数量明显多于腔镜组, 差异有统计学意义(P<0.05), 说明达芬奇机器人手术可更有效清扫淋巴结, 提高患者的生存率。
综上所述, 达芬奇机器人手术治疗肺癌具有安全、有效等优势, 且对淋巴结清扫更彻底, 在今后的临床应用中值得广泛推广。

