[Zn(PCPA)2(IMZ)2]配合物的合成、晶体结构及性质研究
沈 红,李 波,李勇辉
(宜宾职业技术学院新能源电池学院,四川 宜宾 644000)
配位化合物因特殊的结构,以及在催化、分离、气体吸附、磁性、荧光等方面的应用,成为了化学、材料学、物理学等领域的研究热点[1]。其中,芳香羧酸类配体因其结构的刚性与化学性质的稳定性,被广泛用作桥连配体,以构筑高热稳定性的无机-有机杂化材料[2]。在配合物的合成过程中,将有机羧酸和咪唑类配体作为混合配体用于构筑配合物时,因同时集中了2 种配体的优势,合成出来的产物其性质研究也比较广泛[3]。
金属锌是重要的生命元素,具有抗菌和抗过滤性病原体的作用[4]。具有d10构型的过渡金属(如Ag+、Cu2+或Zn2+)与含氮类配体通过自组装形成的金属有机骨架配合物,能提高配体化合物的稳定性,并能使d10类金属配合物具有良好的各类性能[5]。锌配合物通常具有良好的荧光性质,且锌与芳香羧酸配体配位后,能提高配体的荧光强度和灵敏度[6]。
本研究以锌原子为中心原子,以对氯苯乙酸和咪唑为有机配体,采用溶剂挥发法合成了配合物Zn(PCPA)2(IMZ)2,并对其结构和性质进行了表征,实验数据可为后期作为功能性材料使用提供参考。
1 实验部分
1.1 主要仪器与试剂
Bruker APEX-Ⅲ D8 VENTURE X 射线单晶衍射仪,Hitachi F-4600 型荧光光谱仪,TGA Q500 型热重分析仪,X 射线衍射仪,DHG 型鼓风干燥箱,Nicoletiz10 傅里叶变换显微红外光谱仪,UV2700型紫外分光光度计,SHZ-D 型水循环真空泵,DF-101S 集热式磁力搅拌水浴锅。
对氯苯乙酸、咪唑、氯化锌(均为分析纯)。
1.2 配合物的合成
称取0.8g(0.02mol)NaOH 固体于烧杯中,加10mL 水溶解,将3.4g(0.02mol)对氯苯乙酸溶于50mL 甲醇中,加入配好的氢氧化钠溶液,调节pH至5~6,加入咪唑1.4 g(0.02 mol),完全溶解后,另取氯化锌1.3g(0.01 mol)溶于10mL 水中。在搅拌情况下,缓慢滴加上述溶液,出现沉淀后继续搅拌5h,静置过夜。过滤,滤液在室温条件下自然挥发,8d 后得到适合于单晶分析的白色块状结晶。过滤,用甲醇淋洗,干燥后收集产品,产品收率为56.3%。
1.3 晶体结构测试
选取单晶尺寸为0.08 mm×0.10 mm×0.18 mm的产品,在Bruker Smart AXS CCD 单晶衍射仪上,用石墨单色化的MoKα 射线(λ=0.071073 nm),在1.92°≤θ≤28.35°范围,100 K 温度下,采用ω-scan 技术收集衍射数据。所有衍射数据的还原和结构解析工作使用晶体学软件SHELXT-2014 和SHELXL-2014 完成。所有非氢原子坐标用直接法解出,然后采用全矩阵最小二乘法进行修正。氢原子坐标通过Fourier 法和理论加氢确定[7]。
配合物最后的残差因子R1=0.1249,wR2=0.1757,配合物的主要晶体学数据见表1,主要的键长和键角见表2,氢键数据见表3。
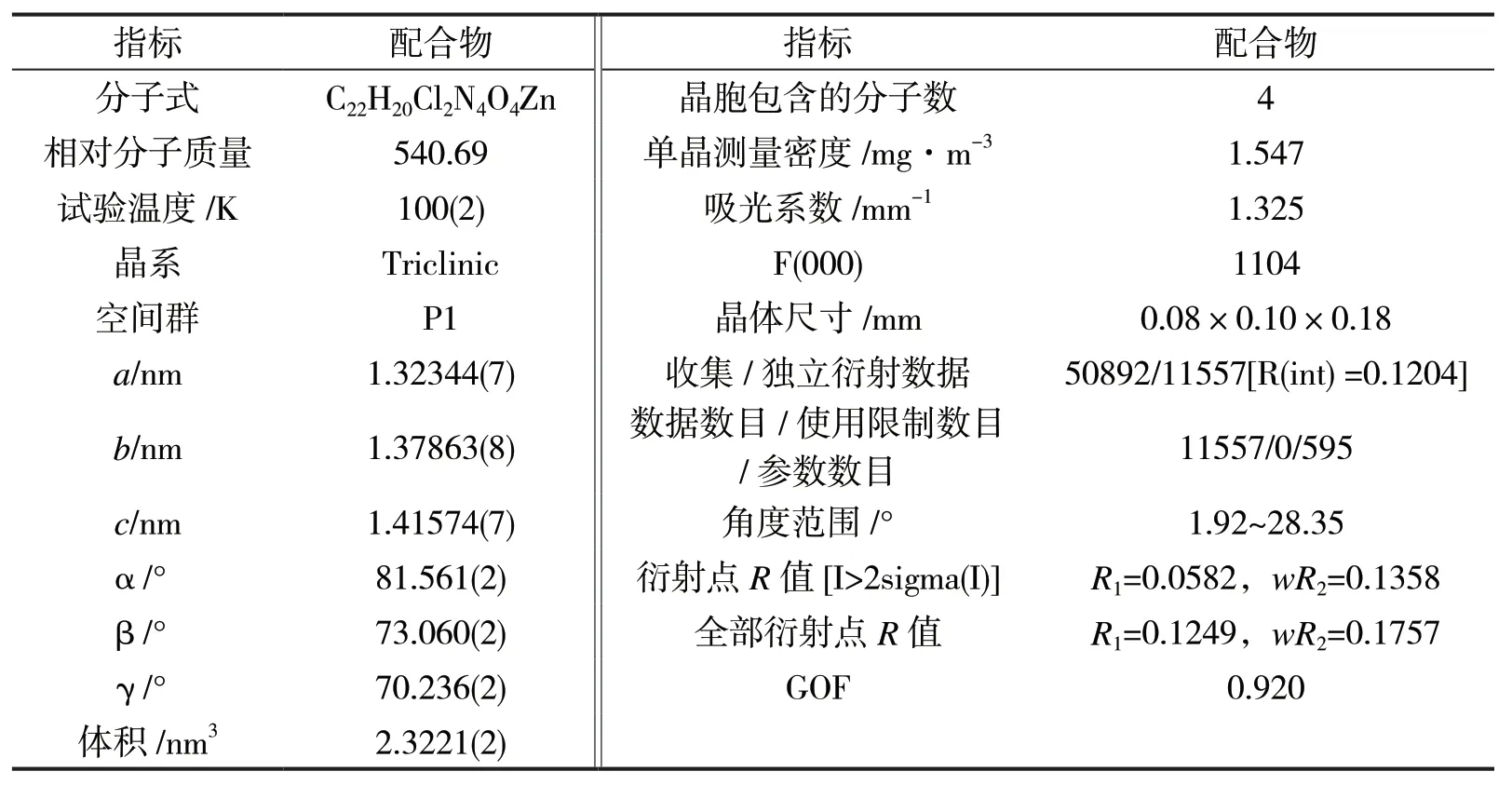
表1 配合物的晶体学数据Table 1 Crystal data of the complex

表2 配合物的主要键长和键角Table 2 Selected bond lengths and bond angles of the complex

表3 配合物的氢键键长和键角Table 3 Hydrogen bond lengths and bond angles of the complex
2 结果与讨论
2.1 晶体结构分析
从图1 和表2 可以看到,锌离子是四配位,与报道的锌离子配合物类似。配合物中Zn1-O1、Zn1-O3、Zn1-N5、Zn1-N7 的键长,分别是0.1956(2)nm、0.1951(3)nm、0.2006(3)nm、0.1988(3)nm,这些都在常见的Zn-O、Zn-N 键的键长范围内,均属于正常的配位键[8]。
从图2 可以看到,配合物中存在N-H···O 氢键,相邻的结构单元间,第1 个配合物中的对氯苯乙酸配体羧基上的O 原子,与第2 个配合物中咪唑配体上的N 形成了N-H···O 氢键。其中,N6···O6 的键长为0.2727nm,键角为155.5°;N8···O8 的键长为0.2749nm,键角为164.5°;N2···O4 的键长为0.2729 nm,键角为149.4°;N4···O2 的键长为0.2761 nm,键角为163.5°。具体的氢键数据见表3。

图2 配合物的氢键图Fig.2 Diagram of hydrogen bonds of complex
2.2 配合物的红外光谱图分析
用傅里叶变换红外光谱研究了配合物的化学结构,结果见图3。3151cm-1的吸收峰是咪唑环的N-H 振动吸收峰,1449 cm-1、1495 cm-1、1581 cm-1的特征振动峰对应的是羧基。1072 cm-1、1146 cm-1、1265 cm-1的特征峰,可归结为C-N 的伸缩振动,859cm-1~810 cm-1是C-H 键的弯曲振动峰,分析结果与晶体结构的分析结果一致。

图3 配合物的红外光图谱Fig.3 IR spectra of complex
2.3 X 射线粉末衍射分析
图4 为室温下配合物的粉末衍射测试结果。实验测定的粉末衍射图谱,与Mercury 软件基于晶体结构模拟得到的衍射峰角度基本吻合,证明配合物为纯相。
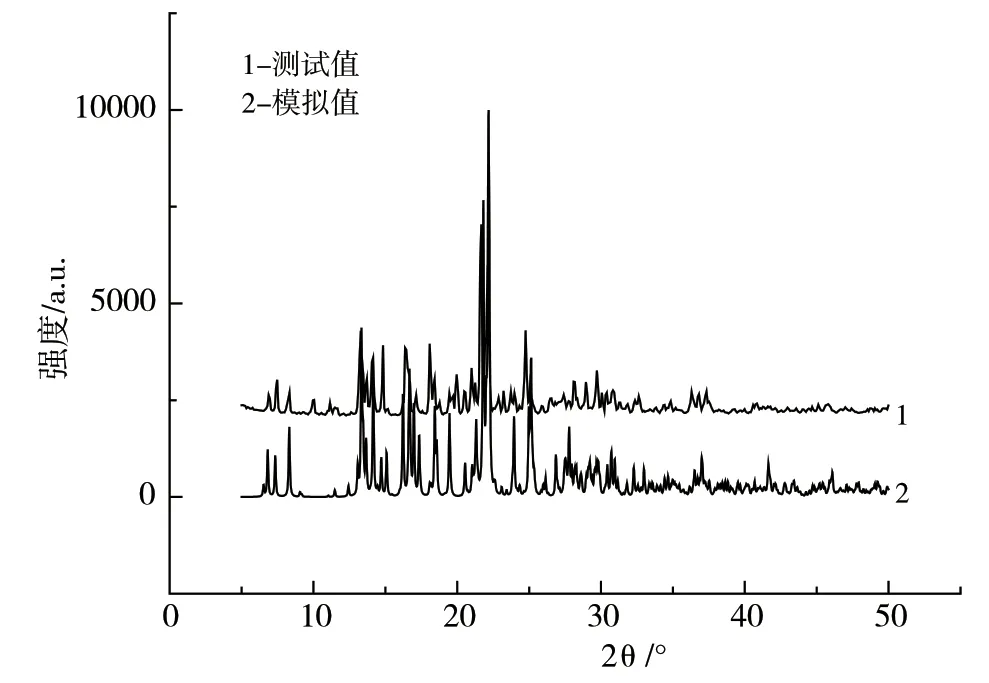
图4 配合物的PXRD 图谱Fig.4 PXRD patterns of complex
2.4 配合物的热重分析
测试温度为30~900℃,空气氛围,升温速率为15℃·min-1,配合物的TG 曲线见图5。该化合物主要分4 步失重:第1 步从247℃至344℃,失重率为40.93%;第2 步失重位于387~423℃之间,失重率为16.28%(2 步失重共为57.21%,对应对氯苯乙酸配体的分解,但保留了Zn 原子所需的氧,理论失重为56.67%);第3 步失重位于521~581℃之间,失重率为8.99%;第4 步失重位于622~676℃之间,失重率为19.01%(2 步共失重28%,对应咪唑配体的分解,理论失重为25.2%),最终残留14.08%,与ZnO 的15.05%相符,表明该配合物在室温下稳定。

图5 配合物的热重曲线Fig.5 TGA curves of complex
2.5 配合物的荧光光谱分析
图6 是对氯苯乙酸配体和配合物的发射光谱。从图6 可以看到,配合物的最大激发峰在381nm,最大发射峰在466nm,相比对氯苯乙酸配体,强度有很大增强。产生这一现象的原因,可能是形成的配合物使得配体的刚性增强。配合物大约红移了116nm,原因可能是锌离子d10电子构型非常稳定,难以被氧化和还原,红移是配体与金属中心的电子跃迁造成的[9-10]。

图6 对氯苯乙酸配体和配合物的发射光谱Fig.6 Emission spectra of p-chlorophenylacetic acid ligand and complex
3 结论
本文采用溶剂挥发法,选择Zn(Ⅱ)作为中心离子,与对氯苯乙酸、咪唑合成了配合物。采用X射线单晶衍射仪测定了金属有机配合物的结构。热重分析结果表明,配合物具有较好的热稳定性。配合物的荧光测试表现出由配体内部的电子跃迁产生的荧光性能。

