氮掺杂碳包覆rGO-纳米硅的制备及电化学性能
周惠, 朱帅波, 王际童, 乔文明, 余子舰, 张寅旭
氮掺杂碳包覆rGO-纳米硅的制备及电化学性能
周惠1, 朱帅波1, 王际童1, 乔文明1, 余子舰2, 张寅旭2
(1. 华东理工大学化学工程联合国家重点实验室, 上海 200237;2. 合盛硅业(鄯善)有限公司, 吐鲁番 838200)
通过静电自组装法, 将自带负电的石墨烯与用正电荷修饰过的纳米硅进行自组装, 再利用多巴胺的黏接特性对复合材料进行氮掺杂碳包覆得到复合材料Si/rGO@CN. 通过改变多巴胺的浓度和聚合时间, 研究了不同厚度的氮掺杂碳层对复合材料电化学性能的影响. 结果显示, 当氮掺杂碳的含量(质量分数)为23.6%时, 复合材料表现出优异的电化学性能. 在0.2 A/g电流密度下循环200次后容量为943.4 mA·h/g; 在1.0 A/g电流密度下的长循环性能测试中, 发现其经300次循环后容量仍然保持在753.8 mA·h/g. 氮掺杂碳层的均匀连续包覆不仅可以避免硅与电解液的直接接触, 还可以缓冲硅纳米材料在脱嵌锂时产生的体积膨胀, 维持材料结构的稳定性, 而石墨烯的存在提高了复合材料的导电性.
锂离子电池; 负极材料; 硅碳复合; 纳米硅; 碳包覆
在众多可充电电池中, 锂离子电池(LIBs)提供了迄今为止最高的能量密度以及合理的长循环寿命, 因此备受青睐. 然而, 随着电动汽车行业的快速发展, 对高性能锂离子电池的需求也与日俱增. 石墨材料自20世纪末首次引入以来, 已经达到其理论容量(372 mA·h/g)[1]. 因此, 需要寻找比石墨容量高得多的新阳极来实现能量密度方面的突破. 在众多替代石墨的候选者中, 硅由于其高达3579 mA·h/g的理论比容量(在室温下以Li15Si4的形式存在)和相对较低的放电电位(约0.5 V. Li/Li+)而被广泛关注[2,3]. 然而, 非导电硅和锂离子之间的电化学反应伴随着剧烈的体积膨胀(约300%)和颗粒粉化, 致使活性材料与集流体直接的电接触消失, 电池容量快速衰减, 而且新裸露在电解液中的硅的表面会重新形成不稳定的固体电解质界面(SEI)膜, 即在电解液与电极表面之间形成的一层薄膜, 导致电解液耗损[4~9]. 为了解决这些与硅相关的问题, 大量的研究已经投入到硅基复合材料的合理设计中, 其中, 硅颗粒尺寸的大小对电池性能有较大影响, 纳米级硅在嵌锂过程中发生体积膨胀所产生的应力明显减小, 这使得电池结构保持完整, 从而增加电池的充放电次数. 此外, 随着硅纳米粒子粒径的减小, 其特殊性质会逐渐显现出来, 较小的硅纳米粒子具有更高的比表面积, 可以减少锂离子的扩散距离和时间, 增强电极的倍率性能. 因此, 将纳米硅与碳材料(如石墨烯、 石墨炔[10~13]等)复合来缓解硅材料的体积效应, 保证 SEI 膜的完整性, 是一种有效的改善电极容量、 提高首次库仑效率的方法[14~18]. Lu等[15]在纳米硅表面原位形成金属有机框架, 随后通过与蔗糖和氧化石墨烯的混合物进行溶剂热反应在硅颗粒的表面沉积第二层碳. 所得复合材料在0.2 A/g的电流密度下循环240次后容量保持在1182 mA·h/g, 并且在1 A/g的大电流密度下进行450次的长循环后容量保持在484 mA·h/g. Su等[17]通过喷雾干燥法和镁热还原法制备了硅/碳复合材料(M-pSi@C). 碳层的保护不仅可以缓解硅的体积膨胀, 还可以提高电极的导电性. 该材料在1 A/g的电流密度下循环250次后容量保持在1702 mA·h/g.
在形成硅基复合材料的众多导电碳质平台中, 石墨烯由于其机械性能优异、 比表面积大以及离子/电子的电导速率优异出而被广泛用来增强硅的循环稳定性[19]. 在制备硅-石墨烯复合材料的众多方法中, 静电自组装是一种有吸引力的策略, 通过静电自组装可以使得硅纳米颗粒均匀分散在复合材料中. 此外, 氮掺杂碳层的包覆可以有效地改善复合材料的导电性, 并且有利于材料表面稳定的SEI膜的形成, 多巴胺因其厚度可控且均匀性及连续性好而在众多氮掺杂碳中脱颖而出.
基于此, 本文采用静电自组装方法以及后续的多巴胺自聚合、 高温碳化制备了一系列的氮掺杂碳包覆硅/石墨烯复合材料(Si/rGO@CN), 并且探讨了氮掺杂碳层的厚度对复合材料电化学性能的影响.
1 实验部分
1.1 试剂与仪器
纳米硅(50 nm, 高纯), 上海水田科技有限公司; 氧化石墨烯, 中国科学院山西煤炭化学研究所;-甲基-2-吡咯烷酮(纯度98%)和十六烷基三甲基溴化铵(CTAB, 分析纯), 上海麦克林生化科技股份有限公司; 盐酸(质量分数37%)和多巴胺盐酸盐, 分析纯, 国药集团化学试剂有限公司; 金属锂片, 天津中能有限公司; 导电炭黑(Super C), 艾览(上海)化工科技有限公司; 聚偏氟乙烯(PVDF, HSV900), 法国阿科玛公司; 硅碳负极电解液(LX-025), 苏州多多化学科技有限公司; 去离子水(电导率 0.5 μS/cm).
Quadrasorb SI型康塔吸附仪, 美国康塔仪器公司; Land CT2001A 型蓝电电池测试系统, 武汉市蓝电电子股份有限公司; IM-6e型交流阻抗分析仪, 美国Gamry电化学仪器公司; Arbin BT 2000型电化学工作站, 美国Arbin Instrument公司; Sigma 300型扫描电子显微镜(SEM), 德国ZEISS公司; Talos F200X G2型透射电子显微镜(TEM), 美国 FEI公司; D/max 2550型X射线衍射仪(XRD), 日本理学株式会社; STAR型热重分析仪(TG), 瑞士 Mettler公司; K-Alpha型X射线光电子能谱分析仪(XPS), 美国Thermo Scientific公司; LabRAM HR Evolution型拉曼光谱分析仪(Raman), 日本 Horiba公司.
1.2 实验过程
1.2.1硅/石墨烯复合材料的制备将CTAB接枝到硅纳米颗粒(Si NPs)的表面, 制备了CTAB修饰的Si NPs. 称取0.4 g Si NPs(直径为20~60 nm), 在超声波的作用下, 将它们分散于40 mL去离子水中. 之后加入0.25 g CTAB并且超声分散1 h, 最后用去离子水重复洗涤3次以除去过量的CTAB, 得到被CTAB修饰后的Si NPs(Si-CTAB). 将一定量的氧化石墨烯原液在去离子水中稀释, 超声分散30 min, 然后在轻度搅拌下将Si-CTAB溶液(将上述Si-CTAB超声分散在40 mL去离子水中)和氧化石墨烯溶液均匀混合. Si-CTAB表面所带的正电荷和GO薄片所带的负电荷之间会产生静电作用使得两者自组装, 并且马上形成硅/氧化石墨烯(Si/GO)聚集体而在溶液中析出.
1.2.2氮掺杂碳包覆的硅/石墨烯复合材料的制备为了制备具有不同氮掺杂碳包覆量的纳米硅和石墨烯的复合材料. 首先, 将100 mg Si/GO样品分散于50 mL 2 mg/mL多巴胺的Tris溶液(pH=8.7)中, 并放置30 min, 之后搅拌混合溶液24 h. 将反应所得物质经过多次去离子水离心洗涤后, 置于烘箱(80 ℃)中干燥12 h, 除去样品中的水分, 最终将烘干后的样品置于氮气气氛中, 并在800 ℃下进行2 h的碳化处理, 即获得氮掺杂碳包覆的纳米硅和rGO(Si/rGO@CN-2)复合材料. 与此同时, 通过调整多巴胺的浓度和聚合时间制备了另外两组样品: 当多巴胺的浓度为2 mg/mL, 聚合时间为12 h时, 得到 Si/rGO@CN-1复合材料; 当多巴胺的浓度为4 mg/mL, 聚合时间为24 h时, 得到Si/rGO@CN-3复合材料.
1.2.3测试电极制备为了测试材料的电化学性能, 按活性物质/乙炔黑/PVDF质量比8∶1∶1称取样品, 并且加入一定量的-甲基-2-吡咯烷酮, 持续搅拌8 h以上, 直至浆料均匀, 并涂布在铜箔表面上, 得到厚度为90~120 µm的薄膜. 之后将其放入真空烘箱中, 在50 ℃下干燥10 h, 以除去极片中的溶剂. 将涂覆有活性材料的铜箔切成直径为12 mm的圆形极片.
在工作电压为5 MPa下将负极极片进一步压实, 从而使得活性材料与铜箔之间的结合更为紧实, 以避免活性材料的脱落, 之后再次放入80 ℃真空烘箱中干燥12 h. 半电池的组装工作在氩气手套箱内完成, 需按照严格的步骤进行组装, 即正极壳-正极-电解液-隔膜-电解液-负极-负极壳(其中, 半电池的正极为实验中所制备的极片, 负极为金属锂片). 将组装完成的电池在室温下放置10 h, 以确保极片 和隔膜被电解液充分润湿, 随后, 将进行一系列的电化学测试. 其中, 恒电流充放电测试(GCD)在蓝电电池测试系统上进行, 其电位范围为0.01~1.5 V; 循环伏安测试(CV)在电化学工作站上进行;电化学阻抗测试(EIS)在交流阻抗分析仪上进行, 正弦激励电压为5.0 mV, 扫描频率范围为0.01Hz~100 kHz.
2 结果与讨论
2.1 样品的结构与形貌表征
Scheme 1为Si/rGO@CN复合材料的制备流程图. 首先, 利用CTAB来修饰Si NPs, Si NPs由于暴露在空气中, 在其表面会形成一层带负电荷的氧化硅; CTAB表面存在氨基而带正电荷, 常被用来作为阳离子表面活性剂软模板, 因此, 可以通过带负电荷的氧化硅与带正电荷的CTAB之间的静电相互作用对纳米硅进行表面改性得到Si-CTAB. GO表面由于酚羟基和羧酸的电离而带负电荷, 基于此, CTAB修饰后的Si NPs和GO之间通过静电自组装成功制备了Si/rGO[20]. 之后, 通过聚合反应, 用聚多巴胺(PDA)对Si/rGO进行包覆得到Si/rGO@PDA, 前驱体在800 ℃氮气气氛下进行2 h的碳化处理后得到 Si/rGO@CN复合材料. 多巴胺广泛来源于蛋白, 其具有强黏附作用, 可以在各种材料表面沉积, 这是由于其表面所存在的胺基易于与其它基团之间形成牢固且持久的共价键; 而且, 由于邻苯二酚基团的存在, PDA具有独特的耐湿附着力, 这意味着即使在电池内部的液态电解液环境下, PDA也可以很好地附着在材料表面. 与无氮碳相比, PDA衍生碳中较多的原位氮的存在有效提高了材料的电化学性能. PDA层的厚度可以通过改变多巴胺的浓度以及聚合时间进行调控[21].
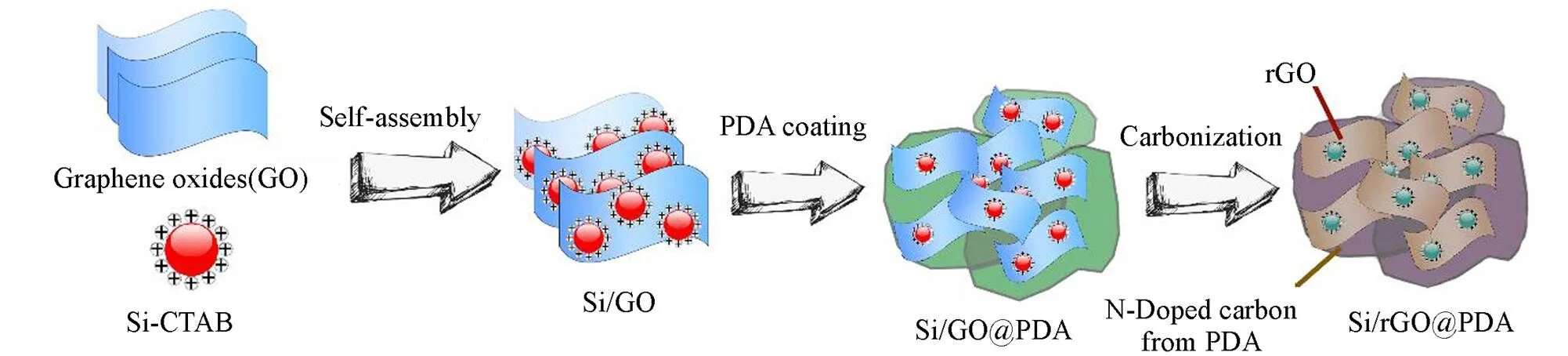
Scheme 1Preparation flowchart of the synthesis process of Si/rGO@CN composites
复合材料的微观结构和形貌可以通过SEM来观察, 如图1所示. 图1(A)和(B)为纳米硅和石墨烯静电自组装后得到的复合材料Si/rGO的SEM照片, 可以观察到, 纳米硅均匀分布在褶皱的石墨烯片层结构之间, 石墨烯的加入有效避免了纳米硅的团聚. 图1(C)和(D)为复合材料Si/rGO@CN的SEM照片, 可见, 包覆多巴胺后, 材料的表面变光滑了, 并且纳米硅的数量相比于Si/rGO[图1(B)]明显减少, 这是由于纳米硅和石墨烯被包覆于碳层之下, 没有直接裸露在材料表面.

Fig.1 SEM images of Si/rGO(A, B) and Si/rGO@CN⁃2(C, D)
复合材料的微观结构通过TEM进一步进行分析. 从图2(A)和(B)可见, 通过静电自组装法显著降低了Si NPs的团聚, Si NPs较为均匀地分布在石墨烯片层之间, 另外, 从图2(C)可见, 纳米硅表面存在一层连续且厚度均匀的无定形氮掺杂碳. 复合材料表面的碳层一方面可以减少纳米硅在电解液中的暴露, 另一方面可以促进材料表面稳定SEI膜的形成, 从而在很大程度上提高了材料的电化学性能.

Fig.2 TEM images of Si/rGO@CN⁃2
图3为复合材料的XRD谱图, 可见, Si/rGO在2=27°左右有一个微弱的衍射峰, 对应于石墨烯的衍射峰, 且此衍射峰随着碳包覆层厚度的增加而减弱. Si/rGO, Si/rGO@CN-1, Si/rGO@CN-2和Si/rGO@CN-3位于228.4°, 47.3°, 56.1°, 69.1°和76.4°处的5个衍射峰, 分别对应于硅晶体的(111), (220), (311), (400)和(331)晶面[22], 结果表明, 硅的结构并没有因为与石墨烯进行静电自组装、 多巴胺涂层和热处理而破坏. 此外, 随着外层碳包覆厚度的增加, 衍射峰的强度逐渐降低. 并且在所有的样品中均未观察到与碳所对应的明显的峰, 这表明复合材料的外层碳涂层为无定型形态. XRD所得结果也表明, 在由纳米硅、 石墨烯和多巴胺热解碳组成的复合材料中未检测到其它杂质相.
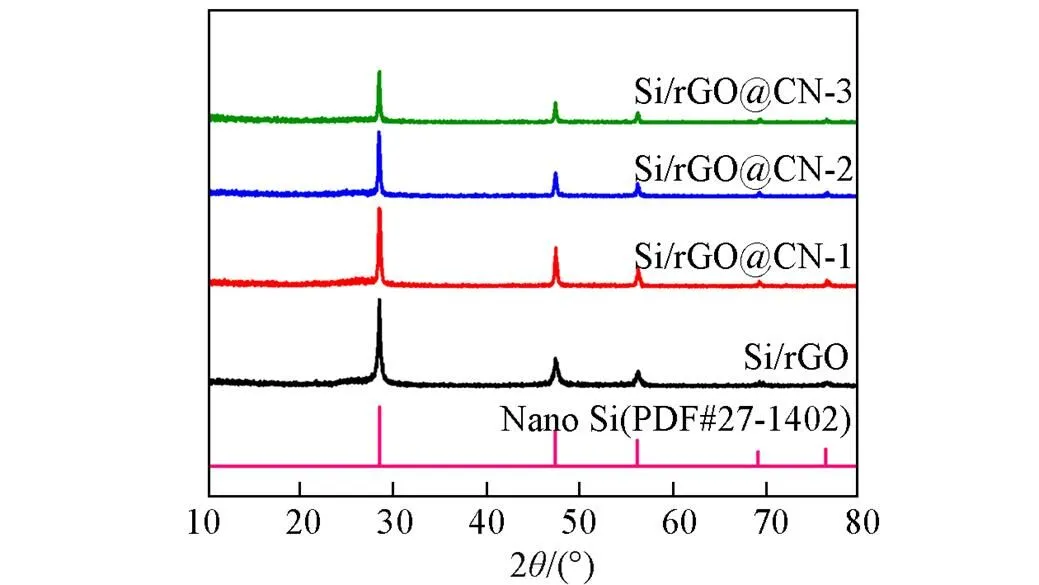
Fig.3 XRD patterns of Si/rGO, Si/rGO@CN⁃1,Si/rGO@CN⁃2 and Si/rGO@CN⁃3 composites
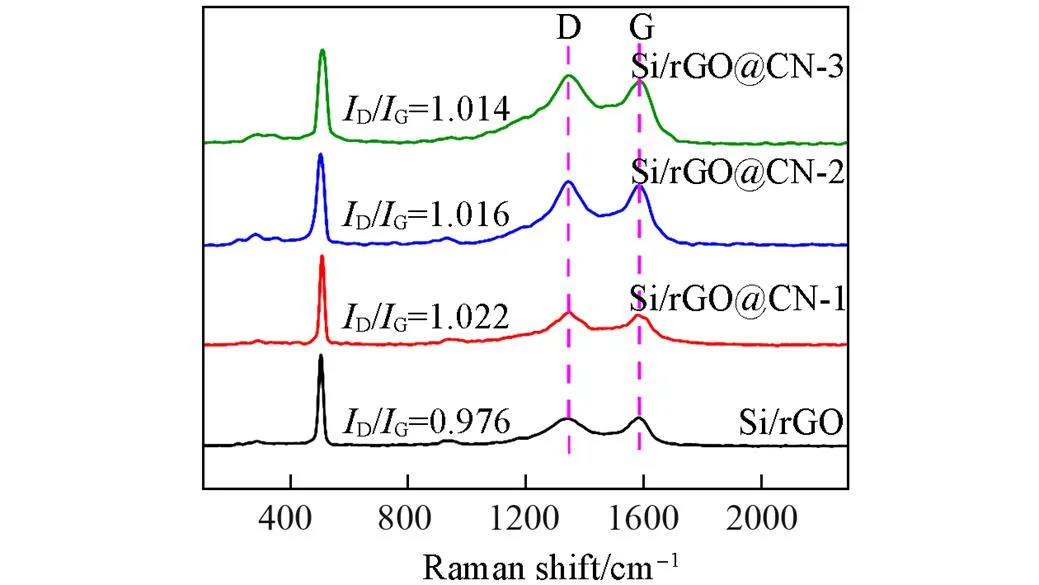
Fig.4 Raman spectra of Si/rGO, Si/rGO@ CN⁃1, Si/rGO@CN⁃2 and Si/rGO@ CN⁃3
通过拉曼光谱对复合材料进行分析来确定复合材料表面碳层的存在, 结果如图4所示. 可以观察到, 位于1344 cm-1处代表材料的无定形状态或缺陷结构的D带, 以及1587 cm-1处代表材料的石墨化状态或晶体结构的G带. D带的强度通常与材料中的无定形碳含量和缺陷结构数量有关, G带的强度通常与材料中的石墨结构数量有关, 它们是表征材料结构和形貌的两个重要参数, 复合材料的石墨化程度可以通过测量D带和G带的峰值强度比(D/G)值进行推断,D/G值较大说明石墨化程度较低[23]. 与 Si/rGO相比, 碳涂层后的样品的D带和G带峰值强度均有所增加. 而且与Si/rGO的D/G值(0.976)相比较而言, 在包覆了外层氮掺杂碳后, Si/rGO@CN-1, Si/rGO@CN-2和Si/rGO@CN-3的D/G值分别增加到1.022, 1.016和1.014, 这也说明了复合材料中无定形碳的存在, 其存在为材料引入更多的表面空位和晶格缺陷, 由于这些缺陷的存在, 能够增加材料的电化学反应表面积, 为反应提供更多的活性位点, 促进电荷传输和物质扩散. 此外, 缺陷还能够调节材料的晶格结构和电子结构, 改变其能带结构和电子亲和力等特性, 从而进一步提高其电化学性能. 而随着外层碳包覆层厚度的增加,D/G值有所减少, 这说明适宜的包覆层厚度有利于电化学性能的提高.
复合材料的硅含量可以通过热重分析得到(图5). 图中的数据经计算可以得出Si/rGO, Si/rGO@CN-1, Si/rGO@CN-2和Si/rGO@CN-3中的碳含量分别为32.4%, 50.2%, 56.0%和63.1%, 所以复合材料中硅含量分别为67.6%, 49.8%, 44.0%和36.9%. 因为复合材料中的碳含量包括石墨烯和外层碳, 其中石墨烯含量约为32.4%, 通过计算可以得到Si/rGO@CN-1, Si/rGO@CN-2和Si/rGO@CN-3的外层多巴胺热解碳的含量分别约为17.8%, 23.6%和30.7%, 这也说明了多巴胺的包覆厚度随多巴胺浓度以及反应时间的增加而增加. 热重分析进一步证明了样品Si/rGO@CN-(=1, 2, 3)中石墨烯、 无定形碳的存在.
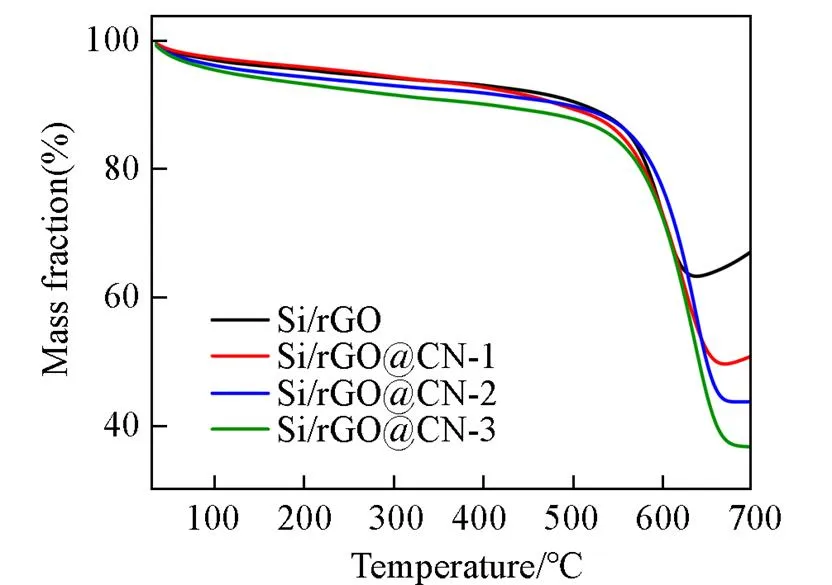
Fig.5 TGA curves of Si/rGO, Si/rGO@CN⁃1,Si/rGO@CN⁃2 and Si/rGO@CN⁃3 composites
Si/rGO, Si/rGO@CN-1, Si/rGO@CN-2和Si/rGO@CN-3的氮气吸附-脱附等温线如图6(A)所示, Si/rGO的等温线呈现中孔材料的等温线形态, 意味着有许多中孔结构存在于Si/rGO复合材料中. 复合材料的比表面积、 孔容、 孔径分布由BET法和BJH法计算得到, 如表1和图6(B)所示. 由图6(B)可见, 材料的孔径大都分布在3~50 nm之间, 这些孔既有相互叠加的氧化石墨烯片层之间的孔, 还有外层氮掺杂碳内部的孔. 与没有外层碳包覆的Si/rGO相比, 包覆后的复合材料的比表面积有所减少, 这就致使在电池的充放电过程中, 复合材料在电解液中的裸露面积减小, 随后消耗的锂离子也减少, 这也说明了在包覆后, Si/rGO@CN-复合材料的电化学性能得到了提高. 随着包覆层厚度的增加, 复合材料的孔径的变化并不明显, 说明了碳材料在纳米硅和石墨烯表面均匀包覆. BET分析结果表明, 适宜的孔隙结构为锂离子的传输提供了便捷的扩散以及转移途径, 且有利于增加电解液的浸润速率, 也使得反应过程中纳米硅的体积膨胀得到了缓解.
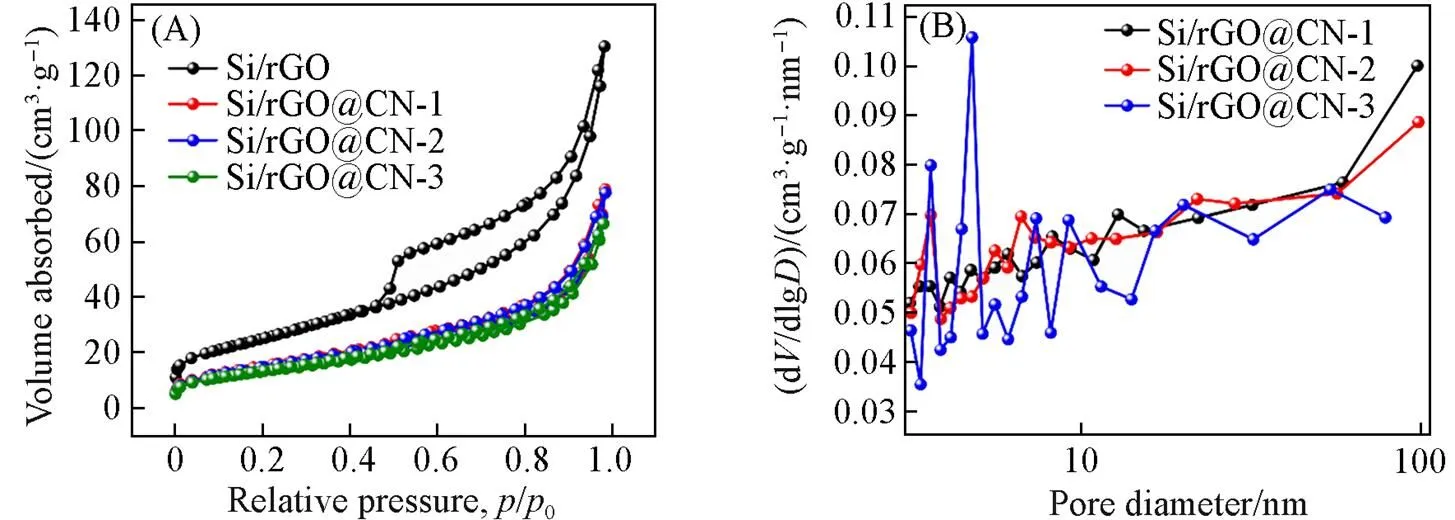
Fig.6 N2 adsorption⁃desorption isotherm curves(A) and BJH pore size distributions of Si/rGO@CN⁃1, Si/rGO@CN⁃2 and Si/rGO@CN⁃3(B)
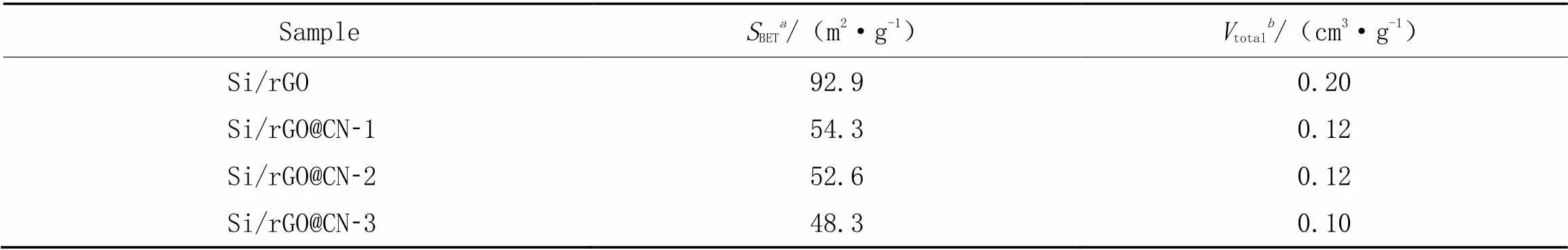
Table 1 Pore parameters of Si/rGO, Si/rGO@CN-1, Si/rGO@CN-2 and Si/rGO@CN-3
.BET: specific surface area;.total: total pore volume(/0=0.98).
使用XPS测试进一步探索了复合材料的表面元素组成和化学键态. 图7(A)为复合材料Si/rGO, Si/rGO@CN-1, Si/rGO@CN-2和Si/rGO@CN-3的XPS全谱图, 可见除了Si/rGO为4个峰以外, 其它复合材料都为5个峰(Si/rGO由于外层没有多巴胺衍生碳层的包覆, 故没有出现氮峰), 图7(B)为图7(A)中的Si/rGO@CN-2的放大图, 可以发现, 这5个峰分别对应C1s, O1s, N1s, Si2s和Si2p, 这证明了复合材料中C, O, N和Si元素的存在. 图7(C)为C1s的高分辨拟合XPS谱图, 283.7和284.7 eV左右的峰分别对应多巴胺碳层衍生的C—C键、 C=N键, 这证明了多巴胺碳层成功涂覆在了复合材料上. 石墨烯的 C—O键和O=C—O键的峰出现在288.0 eV处. N1s的XPS谱图可以分峰拟合为位于397.1, 399.9和402.5 eV处分别对应于氮掺杂碳层中的吡啶氮、 吡咯氮和石墨氮的3个峰[图7(D)]. 碳层中氮的掺杂提高了电极的电导率和电化学活性. 同时, 氮掺杂引入了更多的缺陷结构, 加快了Li+在复合界面中的运输. O1s的XPS谱图出现分别位于531.5, 532.8, 533.5和533.6 eV处的4个峰, 对应于C=O键、 羧基、 Si—O键和醚基[图7(E)]. Si2p的XPS谱图包含分别为位于104.5, 104.0, 103.5, 103.0和99.4 eV处的分别对应Si4+, Si3+, Si2+, Si+和Si的5个峰[图7(F)]. 其中Si的中间价态(Si3+, Si2+, Si+)对应于SiO, Si4+对应于SiO2, 这可能是由于硅纳米颗粒暴露在空气中不可避免地氧化以及在热处理下被GO氧化. 不同价态的Si由于具有不同的电子结构和能带特性、 不同的晶格结构和离子扩散能力以及可能对电解液中的溶质和溶剂发生不同的表面反应, 因此Si的混合价态对材料的电子传导性、 离子传输性以及表面反应性都有一定的影响.
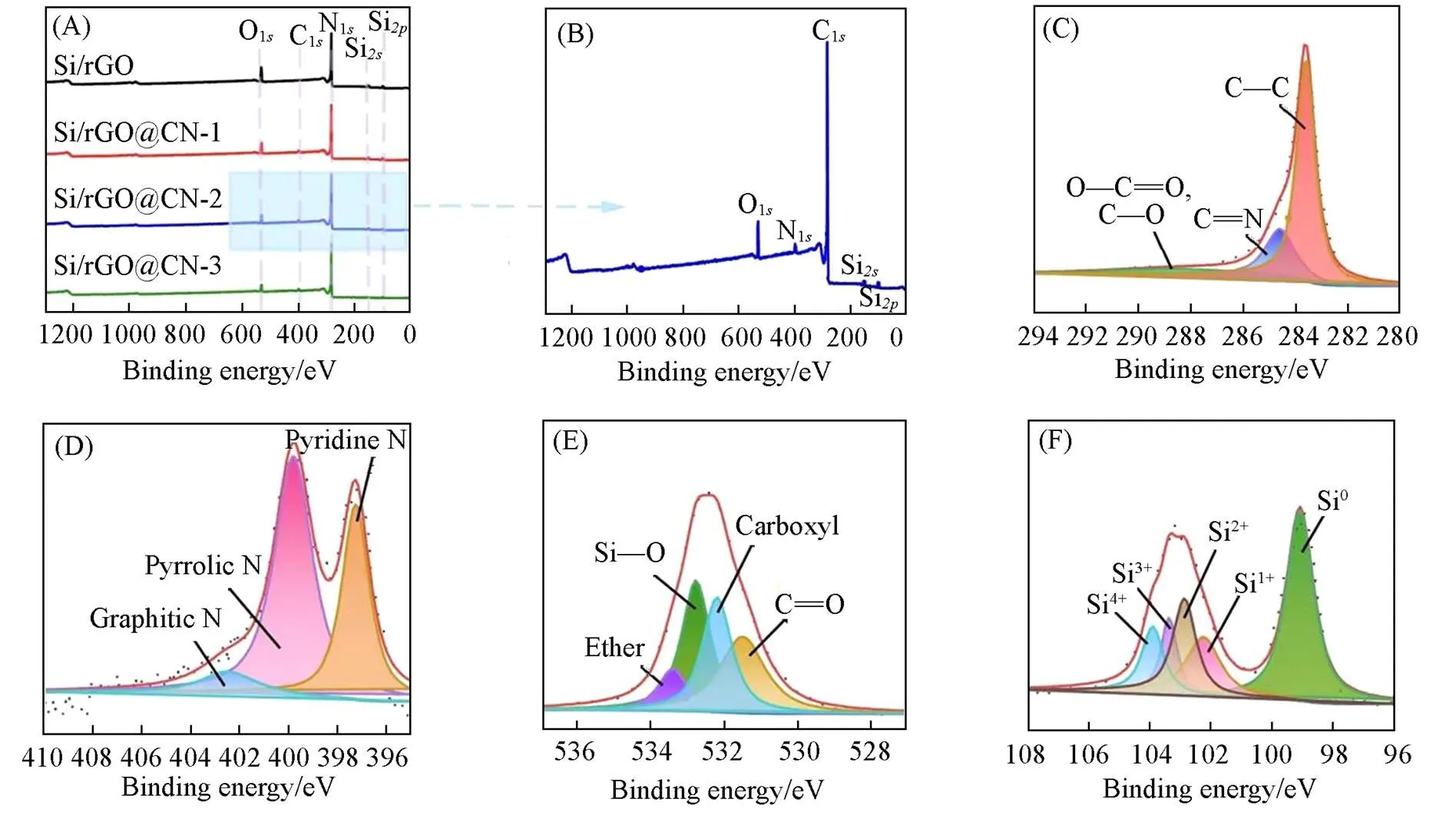
Fig.7 XPS full spectra of Si/rGO, Si/rGO@CN⁃1, Si/rGO@CN⁃2 and Si/rGO@CN⁃3(A) and Si/rGO@ CN⁃2(B), high⁃resolution peak⁃fitting plots of C1s(C), N1s(D), O1s(E) and Si2p(F) of Si/rGO@CN⁃2
2.2 Si/rGO@CN的电化学性能
图8(A)和(B)分别展示了复合材料Si/rGO, Si/rGO@CN-1, Si/rGO@CN-2和Si/rGO@CN-3在电压范围为0~2 V、 扫描速率为0.1 mV/s时初始5次的CV曲线. 可见, 在第一次循环中, 出现了一个还原峰, 其位置在1.5~2.0 V范围内. 这一还原峰对应于少量电解液的分解, 之后在0.75 V附近出现了一个还原宽峰, 对应于SEI膜的形成, 在随后的循环中, 此处的峰消失, 表明SEI膜已经形成并且稳定, 该SEI膜可以保护材料表面, 提高样品的循环稳定性. 在0.2 V附近出现的还原峰是由于锂与硅发生合金化反应形成LiSi. 在0.35和0.52 V附近的氧化峰则对应于Li+从LiSi合金中脱除, 以及形成无定形硅的过程. 随着CV扫描次数的增加, 位于0.2 V附近的还原峰和位于0.35, 0.52 V附近的氧化峰的强度明显增加, 表明复合材料中的活性物质被不断激活, 复合材料的电化学活性不断增强. 复合材料在之后几次的CV扫描时, Si/rGO@CN-2的曲线重合度明显高于其它3个样品, 这说明了Si/rGO@CN-2具有更加优异的可逆性, 在循环过程中更加稳定. 这一结果表明, 合适的碳涂层和石墨烯的引入可以有效地改善硅在反应过程中容易发生体积膨胀从而导致循环性能差的问题.
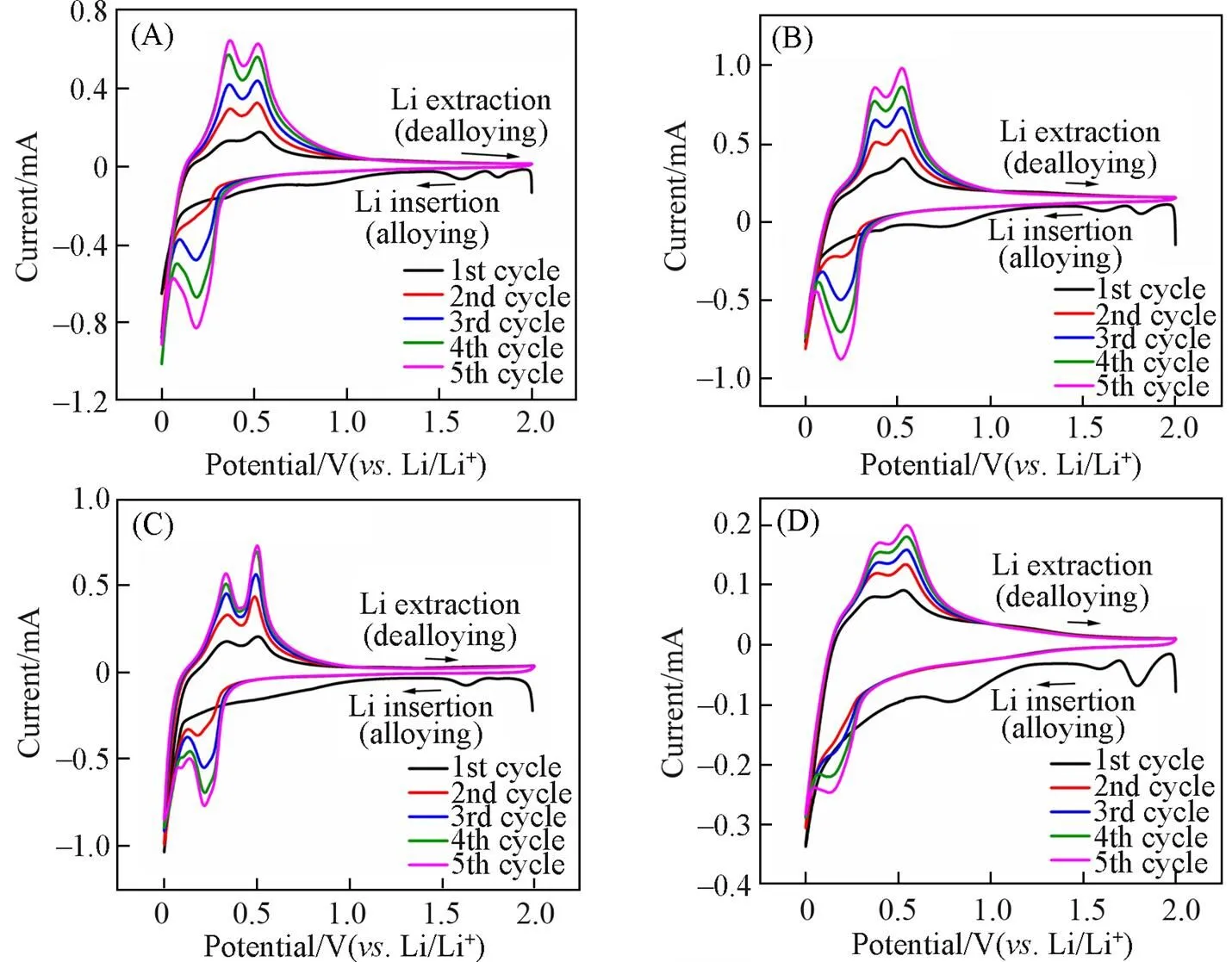
Fig.8 CV curves of Si/rGO(A), Si/rGO@CN⁃1(B), Si/rGO@CN⁃2(C) and Si/rGO@CN⁃3(D) electrodes
图9(A)~(C)分别为复合材料 Si/rGO@CN-1, Si/rGO@CN-2和Si/rGO@CN-3在0.2 A/g电流密度条件下的恒电流充放电曲线. 通过分析曲线可见, Si/rGO@CN-1, Si/rGO@CN-2和Si/rGO@CN-3的首次充/放电比容量分别为1504.5/2202.4, 1398.3/2006.6和1209.5/1821.2 mA·h/g; 再计算它们对应的首次库仑效率(ICE)分别为68.31%, 69.64%和66.41%; 随着碳包覆层厚度的增加, 首次充放电容量有所降低, 这是由于活性物质纳米硅含量的减少, 导致复合材料的理论容量降低. 复合材料的ICE普遍不高, 这主要是由于在首次充放电时电解液与电极材料发生反应形成SEI膜, 并消耗大量的Li+, 从而导致电池容量不可逆的损失. 但是根据数据可以发现, 相对于Si/rGO@CN-1而言, Si/rGO@CN-2的ICE稍有提高, 这可能是由于Si/rGO@CN-1的外层碳涂覆量较少, 导致碳层过薄或不完整, 以至于首次消耗的Li+增多从而导致容量的不可逆损失, 但是当碳包覆层加厚时, Si/rGO@CN-3的ICE较Si/rGO@CN-2却有所降低, 这是由于随着包覆量的增加, Li+脱嵌过程中的阻力也增加, 从而消耗了更多的Li+. 根据复合材料的恒电流充放电曲线可见, 合适的碳层厚度可以增加Li+的传输通道、 加快电池反应、 提高电池的库仑效率. 接下来对Si/rGO@CN-2电极的充放电曲线进行分析. Si/rGO@CN-2的初次放电曲线存在一个位于0.8 V左右较短的电压平台, 这与 SEI膜的形成过程相对应, 在0~0.2 V附近存在一个很长的较低的电压平台, 这是由于Li+与结晶硅之间的合金化反应形成了LiSi. 初次充电曲线的平台出现在0.5 V左右, 对应于Li+从LiSi合金相中析出和形成无定形硅的过程.

Fig.9 Charge/discharge profiles of Si/rGO@CN⁃1(A), Si/rGO@CN⁃2(B) and Si/rGO@CN⁃3(C)
图10(A)为复合材料在0.2 A/g电流密度下充放电200次的循环曲线. 可见, Si/rGO@CN-1, Si/rGO@CN-2和Si/rGO@CN-3的初始放电比容量分别为2202.4, 2006.9和1821.2 mA·h/g, 在充放电循环200次后, 放电比容量分别为280.7, 943.4和447.3 mA·h/g, 对应的容量保持率分别为12.7%, 47.0%和24.6%. 其中, Si/rGO@CN-2在循环过程中容量保持率更高, 表现出更好的电化学性能. 由此可以看出, 适宜厚度的碳包覆层明显提高了电化学性能, Si/rGO@CN-1由于表面碳层太薄, 以至于在循环充放电时, 硅的体积会发生较大的变化, 很快破坏了其表面原本的SEI膜, 纳米硅重新暴露于电解液中, 在其表面会形成新的SEI膜, 消耗更多的Li+, 导致电池较差的循环性能. 而对于Si/rGO@CN-3, 由于其碳包覆层过厚, 纳米硅在复合材料中的含量减少, 从而复合材料的理论容量减少. 图10(B)为在不同电流密度下对电池进行充放电得到的倍率性能图. 可见, Si/rGO@CN-2在0.1, 0.2, 0.5, 1.0和2.0 A/g的电流密度下, 分别呈现出1852, 1396.5, 1182.3, 896.8和775.2 mA·h/g的放电比容量, 虽然其比容量低于Si/rGO@CN-1, 但是其容量衰减要明显小于Si/rGO@CN-1, 且当电流密度回到初始的 0.2 A/g时, Si/rGO@CN-2的容量也会回至1407 mA·h/g, 且在之后的循环过程中, 与Si/rGO@CN-1和 Si/rGO@CN-3相比也更为稳定, 表现出了更加优异的倍率性能. 这主要得益于适宜厚度的碳包覆层有利于Li+的储存、 提高材料的电导率以及促进稳定的SEI膜的形成.
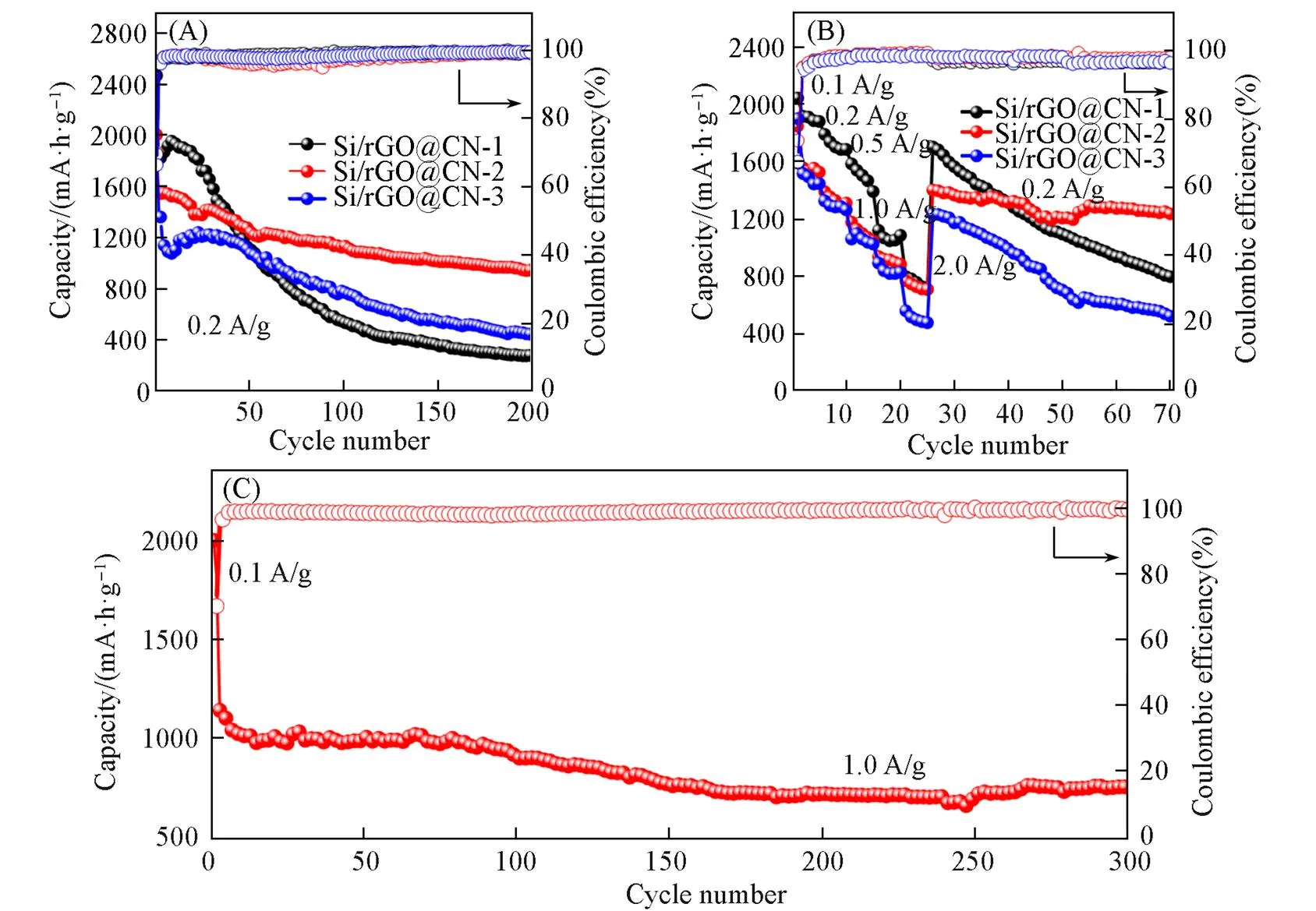
Fig.10 Cycling performance(A), rate performance(B) of Si/rGO@CN⁃1, Si/rGO@CN⁃2, Si/rGO@CN⁃3 and long⁃term cycling performance of Si/rGO@CN⁃2(C)
通常, 通过测试电池的长循环性能来判断复合材料的实际应用价值. 复合材料在1.0 A/g的电流密度下的长循环测试结果如图10(C)所示(在0.1 A/g的电流密度下活化2次), 在经过300次的循环充放电后, 其容量还有753.8 mA·h/g, 呈现出了优越的电化学稳定性. 这主要可以归功于: (1) 外层氮掺杂碳包覆层可以为充放电过程中硅所发生的剧烈体积效应提供缓冲空间; (2) 石墨烯基体其自身所具有的高导电率以及大比表面积对电解液的快速润湿以及锂离子的快速转移有益.
使用EIS进一步了解复合材料的电化学性能与阻抗之间的关系. 图11为复合材料Si/rGO@CN-1, Si/rGO@CN-2和Si/rGO@CN-3的交流阻抗谱图. 阻抗谱图由半圆(高频区)和直线(低频区)构成. 插图为其等效电路, 存在s,ct, CPE和04个变量, 其中,s为高频区半圆与水平轴的交点, 代表Li+通过隔膜和电解液的电阻, 从图11可见, Si/rGO@CN-1, Si/rGO@CN-2和Si/rGO@CN-3的EIS曲线与水平轴的交点都趋近于0, 这意味着Li+在溶液中的迁移电阻可以忽略不计.ct可以反映电荷转移电阻, 可以通过高频区半圆的曲率来判断其阻值大小, 曲率越大, 电阻越小. 从图11可以看出, Si/rGO@CN-2的ct最小, 这是因为外层氮掺杂碳的包覆对电荷在电极中的扩散有益, 但随着碳层的加厚, 复合材料的电荷转移电阻有所增加. CPE表示电极中的双电层电容.0表示Warburg阻抗, 即Li+扩散电阻, 可以通过低频区直线的斜率来加以判断, 斜率越大,0越小, 从图11可以观察到, Si/rGO@CN-3的Li+扩散电阻要大于Si/rGO@CN-2, 这可能是由于过厚的碳层包覆使得Li+的扩散途径减少, 从而增大了Li+的扩散阻力. 然而, 当Si/rGO的表面碳层过薄时, 正如Si/rGO@CN-2, 其Li+扩散电阻也有所增大, 这说明适宜的氮掺杂碳涂层提高了复合材料整体的导电性. Si/rGO@CN-1, Si/rGO@CN-2和Si/rGO@CN-3的等效电路拟合值如表2所示, 其中, CPE需要用dl和两个参数描述,0需要用-,-,-3个参数描述. 以上结果表明, 适宜厚度的碳涂层和还原氧化石墨烯的存在有利于提高电极材料的离子和电子传输速率, 从而使电导率最高的Si/rGO@CN-2复合材料表现出最佳的电化学性能.

Table 2 Fitting values of equivalent circuits of Si/rGO@CN-1, Si/rGO@CN-2 and Si/rGO@CN-3
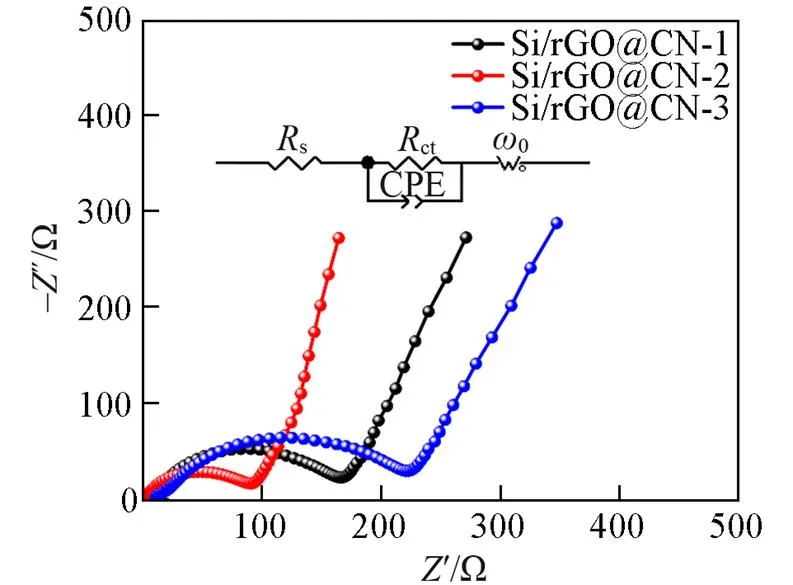
Fig.11 Nyquist plots curves of Si/rGO@CN⁃1, Si/rGO@CN⁃2 and Si/rGO@CN⁃3
Inset: equivalent circuit diagram.
3 结 论
利用静电自组装法以及多巴胺的高黏接性制备了包覆有外层氮掺杂碳的Si/rGO@CN复合材料, 并且探究了外层包覆碳的厚度对复合材料电化学性能的影响. 通过对纳米硅进行改性得到Si-CTAB, 将其与石墨烯进行静电自组装得到Si/GO, 利用多巴胺的黏接特性制备出氮掺杂碳包覆层的Si/rGO@CN复合材料, 通过改变多巴胺的浓度以及自聚合的时间合成了具有不同厚度的氮掺杂碳层包覆的复合材料. 石墨烯和多巴胺碳层的加入缓解了硅的体积变化, 减少了硅和电解质的直接接触, 提高了材料的电化学性能. 当碳层太厚时, 锂离子扩散到硅表面的途径减少, 路径变长, 甚至无法与大部分硅进行电化学反应; 当碳层太薄或涂覆不完整时, 复合材料在第一次充放电时消耗大量的锂离子, 致使电池容量发生不可逆衰减, 而且在后来的循环过程中, 过薄的碳层也无法起到抑制硅体积膨胀的作用, 从而使得复合材料在循环过程中容量快速衰减. 因此, 适宜厚度的碳层有利于提高复合材料的电导率、 提高离子和电子的迁移速率、 降低运输时的阻力、 抑制硅体积的膨胀, 从而使得复合材料在循环充放电过程中表现出更加优异的电化学性能. 在电化学性能的检测中, Si/rGO@CN-2表现出了最佳的电化学性能. 在电流密度为0.2 A/g下循环充放电200次后容量为943.4 mA·h/g; 在1.0 A/g电流密度下测试电池长循环性能时, 循环300次后容量仍然保持在753.8 mA·h/g. 研究结果表明, 制备的Si/rGO@CN复合材料是锂离子电池负极材料的一个潜在候选者.
[1] Li P., Zhao G. Q., Zheng X. B., Xu X., Yao C., Sun W., Dou S. X.,, 2018,422446
[2] Megahed S., Scrosati B.,, 1994,(1/2), 79—104
[3] Wang Q. Y., Zhu M., Chen G. R., Dudko N., Li Y., Liu H., Shi L., Wu G., Zhang D.,, 2022,(16), 2109658
[4] Ryu J. H., Kim J. W., Sung Y. E., Oh S. M.,, 2004,(10), A306—A309
[5] Li P. H., Miao C., Yi D., Wei Y., Chen T., Wu W.,, 2023,, 16855—16863
[6] Feng K., Li M., Liu W., Kashkooli A. G., Xiao X., Cai M., Chen Z.,, 2018,(8), 1702737
[7] Leung K., Soto F., Hankins K., Balbuena P. B., Harrison K. L.,, 2016,(12), 6302—6313
[8] Liu X. H., Wang J. W., Huang S., Fan F., Huang X., Liu Y., Krylyuk S., Yoo J., Dayeh S. A., Davydov A. V., Mao S. X., Picraux S. T., Zhang S., Li J., Zhu T., Huang J. Y.,, 2012,(11), 749—756
[9] Trill J., Tao C., Winter M., Passerini S., Eckert H.,, 2011,(2), 349—356
[10] Zheng Z. Q., He F., Xue Y. R., Li Y. L.,, 2022,(1), 92—98
[11] Luan X. Y., Xue Y. R.,, 2021,(6), 1268—1274
[12] Luan X. Y., Qi L., Zheng Z. Q., Gao Y. Q., Xue Y. R., Li Y. L.,, 2023,(8), e202215968
[13] Fang Y., Liu Y. X., Qi L., Xue Y. R., Li Y. L.,, 2022,, 2681—2709
[14] Zhang M., Li J., Sun C. W., Wang Z., Li Y., Zhang D.,2022167687
[15] Lu Y. H., Ye Z. T., Zhao Y. T., Li Q., He M., Bai C., Wang X., Han Y., Wan X., Zhang S., Ma Y., Chen Y.,, 2022,, 962—971
[16] Zhang Z. H., Ying H. J., Huang P. F., Zhang S., Zhang Z., Yang T. T., Han W. Q.,, 2022,(3), 138785
[17] Su H. P., Li X. R., Liu C. W., Shang Y., Liu H.,, 2022,(1), 138394
[18] An W. L., He P., Che Z. Z., Xiao C., Guo E., Pang C., He X., Ren J., Yuan G., Du N., Yang D., Peng D. L., Zhang Q.,, 2022,(8), 10308—10318
[19] Brownson D. A. C., Kampouris D. K., Banks C. E.,, 2011,(11), 4873—4885
[20] Wang F. F., Lin S., Lu X. S., Hong R., Liu H.,, 2022,139708
[21] Liang J., Xiao C., Chen X., Gao R., Ding S.,, 2016,(21), 215403
[22] Hu Y., Demir⁃Cakan R., Titirici M., Mueller J. O., Schloegl R., Antonietti M., Maier J.,, 2008,(9), 1645—1649
[23] Zhang J., Zhang L., Xue P., Zhang L., Zhang X., Hao W., Tian J., Shen M., Zheng H.,, 2015,(15), 7810—7821
Construction and Electrochemical Properties of Si/rGO@CN as Anode Materials for High-performance Lithium-ion Batteries
ZHOUHui1, ZHUShuaibo1, WANGJitong1, QIAOWenming1*, YUZijian2, ZHANGYinxu2
(,,200237,;(),838200,)
In this paper, the self-charged graphene and the nano-silicon modified with positive charge were self- assembled by electrostatic self-assembly method, and then the dopamine bonding characteristics was used to nitrogen-doped carbon coating of the composite material to obtain Si/rGO@CN composites, and the effect of different thicknesses of nitrogen-doped carbon layers on the electrochemical performance of the composite materials was studied by changing the concentration and polymerization time of dopamine. The electrochemical results showed that when the content of nitrogen-doped carbon was 23.6%(mass fraction), the composite showed excellent electro- chemical performance. The capacity of the composite was 943.4 mA·h/g after 200 cycles at a current density of 0.2 A/g, and its capacity remained at 753.8 mA·h/g after 300 cycles in the long cycle performance test at a current density of 1.0 A/g. The uniform continuous coating of the nitrogen-doped carbon layer can not only avoid the direct contact between silicon and electrolyte, but also buffer the volume expansion generated by silicon nanomaterials during lithium intercalation and maintain the stability of the material structure. The presence of graphene improves the conductivity of composite materials.
Lithium-ion battery; Anode material; Silicon-carbon composite; Nanosilicon; Carbon coating
2023-08-01
乔文明, 男, 博士, 教授, 主要从事储能材料研究. E-mail: qiaowm@ecust.edu.cn
国家自然科学基金(批准号: 22178107, U21A2060, 22178116, 21978097)和新疆维吾尔自治区重点项目(批准号: 2022B01030)资助.
O646
A
10.7503/cjcu20230354
2023-09-13.
Supported by the National Natural Science Foundation of China(Nos.22178107, U21A2060, 22178116, 21978097) and the Xinjiang Uygur Autonomous Region Key Research and Development Program, China(No.2022B01030).
(Ed.: Y, K, S)