高效价抗-D 抗体导致新生儿RhD 抗原遮蔽的处理方法及输血策略
骆园园 沈雨青 苏奶助 龚君顺 符虹 卢春敬 郑艳玲
RhD 血型不合导致的新生儿溶血症(hemolytic disease of newborn,HDN)通常发生在第二胎及以后,一般病情严重,很容易导致胎儿出现黄疸、贫血、水肿、肝脾肿大,甚至死胎或新生儿死亡等,如治疗不及时,病死率极高[1]。然而由于血液成分复杂多变,其中的纤维蛋白、药物或相关抗体都可能干扰检测结果[2-3],因此如何准确鉴定血型和快速有效地确诊致病抗体类型对患儿的临床救治尤为关键。我们在工作中遇到了1 例抗-D 效价高达2 048 的孕妇,新生儿出生后发生重度HDN 并出现RhD 抗原遮蔽现象,导致常规RhD 抗原检测方法所得结果为阴性,通过酸放散试验和血型基因检测确诊患儿血型,及时配型换血使其成功获救,现报告如下。
1 资料与方法
1.1 一般资料 患儿为女性,出生6 h 后因皮肤黄染进行黄疸相关检测,总胆红素(total bilirubin,TBil)382.89 μmol/L。母亲血型为RhD 阴性,有妊娠史,无输血史。因患儿外院初检ABO 和RhD 同血型而出现其他病情无法解释的速发高胆红素血症而送检至本院。本研究已通过本院伦理委员会审批(审批号:KY-2023-088-K01)。
1.2 仪器与试剂 THZ-82 恒温震荡水浴箱(常州国华仪器有限公司),KA-2200 细胞洗涤离心机(久保田中国投资有限公司),孵育器及离心机(北京斑珀斯技贸有限责任公司),Lab-Aid 824s 全自动核酸检测仪(厦门致善生物科技股份有限公司),IH1000全自动血型检测仪(伯乐生命医学产品上海有限公司)。单克隆抗-A、抗-B(批号:20201016)、抗-D(批号:20201810)、抗-E(批号:20203201)、抗-e(批号:20203301)、抗-C(批号:20203001)、抗-c(批号:20203101)、多特异性抗-IgG、C3d(批号:20201016)、抗体筛选细胞(批号:20217014)均由上海血液医药有限责任公司提供;抗体鉴定谱细胞(荷兰三昆试剂有限公司,批号8000452946),ABO/Rh 正反定型血型定型试剂卡(达亚美有限责任公司,批号50093.91.16),微柱凝胶卡(北京斑珀斯技贸有限责任公司,批号:21072.01),血液基因组DNA 提取试剂(厦门致善生物科技股份有限公司,批号:21060901),Rh 血型分型检测卡(江苏力博医药生物技术股份有限公司,批号:202102014),红细胞放散液(珠海贝索生物技术有限公司,批号:20201014),人类红细胞RhD 基因分型试剂盒(天津秀鹏基因科技有限公司,批号:K210525002),BX1020 抗IgG1、抗vgG3 抗人球蛋白检测卡(长春博迅生物技术有限责任公司)。
1.3 血清学检测
1.3.1 血型鉴定、新生儿溶血病检测、抗体鉴定及抗体效价检测 ABO 血型鉴定、Rh 血型鉴定、Rh血型分型、直接抗球蛋白试验、新生儿溶血病、抗体筛选与鉴定、抗体效价检测中使用的盐水试管法、聚凝胺法、抗人球蛋白法均参照输血科(血库)临床技术操作规范操作[4]。不同品牌的凝胶卡及酸放散试剂使用方法参考试剂说明书。
1.3.2 患儿红细胞热放散处理 配制浓度为1%的患儿红细胞,用37 ℃生理盐水洗涤3 次后,于56 ℃水浴箱中热放散10 min,取出后再用37 ℃生理盐水洗涤3 次,配制浓度为3%的红细胞与IgM 抗-D 试剂,采用盐水试管法检测RhD 抗原。
1.3.3 患儿红细胞酸放散处理 酸放散试剂使用步骤参见试剂说明书。酸放散处理后的红细胞配制成3%浓度,用37 ℃生理盐水洗涤至少8 次,以洗涤液由淡红色转为清亮为节点,再配制成3%~5%红细胞后,采用IgM 抗-D 试剂和盐水试管法检测红细胞RhD 抗原。
1.4 血型基因的分子生物学鉴定 采用全自动核酸检测仪提取DNA,送检天津秀鹏生物有限公司,采用跨越断裂点聚合酶链反应(gap-polymerase chain reaction,GAP-PCR)分析RhD 基因盒子,再进一步采用基因测序方法检测血型,具体检测方法及步骤参见文献[5-6]。
1.5 抗体IgG 分型检测 样本送检长春博迅生物技术有限责任公司,具体检测步骤参见文献[7]。
2 结果
2.1 患儿RhD 抗原血清学鉴定 采用酸放散试验处理红细胞后,结果为RhD 抗原阳性(2+)。见表1。
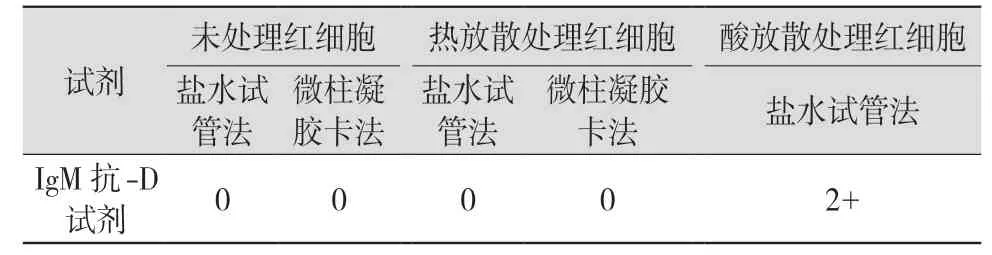
表1 不同方式处理红细胞后与抗-D 试剂反应结果
2.2 分子生物学鉴定 患儿的RhD 血型基因为RhD+/RhD-杂合型(阳性)。
2.3 血型鉴定结果 母亲和患儿的血型鉴定结果分别为O、dccee 和O、DccEe。
2.4 抗体鉴定 将母亲和患儿的血浆及放散液分别与抗体鉴定谱细胞进行反应,结果显示母亲和患儿血清中均存在抗-D,反应格局见表2。

表2 母亲与患儿抗体鉴定表
2.5 抗体效价结果 母亲及患儿IgG 抗-D 效价测定结果均为2 048。
2.6 致病抗体IgG 分型 母亲和患儿体内存在高效价IgG1 和低效价IgG3 抗体。
2.7 患儿换血及输血前后血红蛋白(hemoglobin,Hb)和TBil 水平变化 患儿出生6 h 内Hb 仅为82 g/L,TBil 为382.89 μmol/L。使用3 U 去白细胞悬浮红细胞(O 型,Rh 血型为dccee)和200 mL 血浆,于24 h内进行换血治疗。3 h 后复查TBil 降为221.5 μmol/L,Hb 升至129 g/L,指标明显改善,与其他文献报道一致[8]。持续进行光照和药物治疗,换血48 h 后,复查Hb 为132 g/L。每日监测经皮胆红素,1 周后患儿体征平稳,已出院。
3 讨论
HDN 的发病率和严重程度除了与母亲IgG 抗体效价呈正相关,也与致病抗体IgG 类型相关[9-11],一般认为Rh 血型不合抗体效价在16 时具有临床意义,需在孕期密切监测胎儿相关指标的变化[12]。IgG 抗体是唯一能通过胎盘的抗体,胎盘上含有新生儿Fc 受体(FcRn),IgG 可选择性地与FcRn 结合,从而转运到胎儿的血液循环中[13]。根据r 链抗原性差异,IgG 抗体可分为4 个亚型,在血浆中的浓度由高至低依次为IgG1>IgG2>IgG3>IgG4[14]。Rh系统的血型抗体以IgG1 和IgG3 为主,而IgG1、IgG3较易通过胎盘,并具有细胞毒作用,可以促使巨噬细胞接触和吞噬红细胞,并促使K 淋巴细胞、单核细胞破坏红细胞,因此由其引起的HDN 发展迅速,溶血程度严重,病死率高[15-16]。临床应积极对产前孕妇体内的IgG1、IgG3 水平进行动态监测,为进一步保障RhD 抗原阴性孕产妇生育和再次生育质量与输血安全,在《RhD 阴性孕产妇血液安全管理专家共识》[17]中,制定详细的孕期抗-D Ig 使用指南,减少RhD 阴性妇女由于怀孕、输血和有创诊疗导致的抗-D 抗体产生,降低孕产妇与围产儿死亡率。
本病例中,母亲体内的抗-D 效价高达2 048,考虑与其多次妊娠相关。母亲为非厦门本地产妇,在初次妊娠时未能注射抗-D Ig 进行有效保护。腹中胎儿能存活至分娩,可能与胎盘的屏障作用、胎儿红细胞抗原强弱以及母体人类白细胞抗原(human leucocyte antigen,HLA)抗体等因素有关。孕期胎儿体内的胆红素可经胎盘进入母体,由母亲肝脏处理后排出。当胎儿娩出后,新生儿产生的胆红素无法通过母体排出,而新生儿本身不成熟的肝脏缺少结合酶,导致其体内未结合胆红素升高,引起黄疸[18]。也有可能是因为患儿母亲多次妊娠后,体内产生的抗HLA 抗体封闭了胎儿巨噬细胞的FcRn,阻止了胎儿致敏红细胞被破坏[7]。胎儿分娩后,失去了母源性HLA 抗体的保护,因此在出生6 h 后TBil 水平急速升至382.89 μmol/L,Hb 降为82 g/L。患儿血型鉴定采用盐水法、试管法、血型卡检测RhD 抗原均为阴性,鉴于其高胆红素血症的临床表现、直接抗人球蛋白试验强阳性,结合母亲及其血浆抗-D 效价为2 048,考虑疑似出现RhD 抗原“遮蔽现象”,即新生儿D抗原阳性红细胞完全被抗-D 抗体封闭,导致红细胞上没有D 位点与血清试剂反应,从而呈现假阴性结果[2]。本研究采用热放散处理患儿红细胞后进行RhD 抗原检测,结果却仍为阴性,考虑是由于该患儿红细胞上高效价IgG 型抗-D 抗体数量多,结合力强所致。因患儿病情危急,遂采取酸放散试剂对患儿红细胞进行洗脱,检测结果为RhD 抗原阳性(2+)。在随后的血型基因检测中也证实该试验结果的准确性。根据患儿、母亲的血型和血站的血库情况急诊换血时,可直接选用O、dccee 红细胞和血浆进行操作。
综上所述,RhD 阴性孕产妇应及早纳入高危妊娠管理系统,在孕期建立完备的产检资料,将Rh 分型鉴定纳入必检项目,并持续定期监测Rh 抗体效价。有文献指出常规检测Rh 血型的必要性[19],有条件的孕产妇应根据《RhD 阴性孕产妇血液安全管理专家共识》[17]进行抗D Ig 的预防注射。随着我国“三孩政策”的放开,RhD 阴性女性的妊娠概率将明显增高,医院在此类特殊孕产妇及新生儿的规范管理能力和实验室检测水平方面亟需加强。实验室应根据母婴就诊状况,及时选用合适的试剂和检测方法,快速正确地鉴定血型,为临床救治争取时间。有条件的实验室可根据2021 年发布的《胎儿新生儿溶血病实验室检测专家共识》[20]进行检测方法的指导,通过血型基因检测、孕母出血情况监测、IgG 亚型检测、母亲外周血非侵入性胎儿血型基因检测(cff-DNA)等方法来验证新生儿血型,预测胎儿血型,分析HDN 的严重程度,制定个性化的诊疗方法,减少胎儿HDN 的发病率,从而提高HDN 新生儿的救治率。
利益冲突所有作者均声明不存在利益冲突

