双镜联合治疗胆囊结石合并肝外胆管结石患者疗效及安全性分析*
古乾权,陈 杰,邓 开
胆石症是临床常见的多发性胆道疾病,发病率随人口老龄化和生活方式改变而不断升高,其中胆囊结石(gallbladder stones,GS)合并肝外胆管结石(extrahepatic bile duct stones,EBDS)占10%~15%[1, 2]。GS合并EBDS具有个体差异大、病情复杂、易复发等特点。若治疗不及时,易导致梗阻性黄疸、胆源性胰腺炎等疾病,增加不良预后风险[3]。手术是现阶段临床治疗GS合并EBDS的主要手段,在手术治疗过程中需处理胆囊结石和解除胆总管梗阻,手术操作较为复杂[4]。因此,临床需选择合适的术式治疗GS合并EBDS患者,以减轻手术损伤、提高结石清除率。既往临床多采用传统开腹手术治疗GS合并EBDS患者,但手术易损害胆管系统功能,存在较多的并发症,不利于术后恢复[5]。随着微创理念发展和内镜技术的完善,胆道镜和腹腔镜等内镜治疗广泛应用于GS合并EBDS的治疗,双镜联合治疗能有效清除结石、减少并发症,具有创伤小、精确度高和安全性高等特点[6, 7]。本研究观察了采用双镜联合治疗GS合并EBDS患者的效果和安全性,为临床治疗提供参考经验。
1 资料与方法
1.1 一般资料 2020年1月~2022年12月我院收治的GS合并EBDS患者76例,男性46例,女性30例;年龄为37~67岁,平均年龄为(51.6±6.9)岁。符合《实用肝胆外科学》[8]中关于GS合并EBDS的诊断标准,经超声、CT或MRI等影像学检查确诊,结石数量为(3.6±0.7)个,胆囊结石直径为(8.9±2.4) mm,肝外胆管结石直径为(9.0±2.8)mm,胆总管内径为(10.1±1.4)mm。排除标准:急性胆囊炎、重度萎缩性胆囊炎、急性化脓性胆管炎、急性重症胆管炎、胆道畸形或狭窄、胆囊恶性肿瘤;有肝胆系统手术史或腹部重大手术史;存在脑、肾、心、肺等脏器严重疾病;存在造血、凝血、认知和视听功能损伤;存在手术禁忌证;腹腔严重粘连。将患者分为观察组和对照组,分别采用双镜联合治疗或传统开腹手术治疗,两组基线资料比较无显著性差异(P>0.05)。本研究经我院医学伦理委员会批准,患者及其家属签署知情同意书。
1.2 手术方法 在对照组,行传统开腹手术。全身麻醉、气管插管。经胆道造影,确定结石位置。于患者上腹正中处作一切口,进腹后使用取石钳取出结石。经胆道镜或胆道造影检查,确认取尽结石。留置腹腔和胆总管引流管;在观察组,采用双镜联合治疗,先行内镜下逆行胰胆管造影术(ERCP):采用静脉麻醉,置入十二指肠镜后行乳头括约肌切开术,用小切刀于乳头隆起部位切开乳头,使切线位于乳头11点方向,切开深度不超过隆起部位的1/3,经造影确认结石位置。对于直径<15 mm的结石,采用取石网篮或气囊取出或拖出,对于直径≥15 mm的结石,使用碎石机或碎石网篮碎石再取出结石。经胆道镜检查或胆道造影确认无结石残留。对发现的残留结石,则冲洗胆管,常规留置鼻胆管。在术后5 d,采用腹腔镜胆囊切除术(LC)治疗:全身麻醉和气管插管,保持头高脚低体位,于脐下常规构建气腹,保持腹腔压力为13 mmHg。以右侧腋前线肋缘和右锁骨中线上切口为辅助操作孔和观察孔,充分暴露胆囊动脉和胆囊管,使用可吸收生物夹结扎胆囊动脉、离断,切除胆囊。撤出器械,缝合切口。术后,常规给予两组预防感染、对症处理。
1.3 指标检测 使用Beckman Coulter公司生产的AU680型全自动生化分析仪检测血生化指标;采用ELISA法检测血清白细胞介素-6(IL-6)、C反应蛋白(CRP)、皮质醇(Cor)和肿瘤坏死因子-α(TNF-α,上海酶联生物);使用Bechman Coulter公司生产的LH750型全自动血球分析仪检测血常规。
1.4 疼痛程度评估 采用视觉模拟评分法(VAS)评估疼痛程度。VAS评分为0~10分,分值越高,疼痛感越强烈[9]。

2 结果
2.1 两组围术期指标比较 两组结石清除率均为100.0%,但观察组手术时间、术中出血量和术后3 d VAS评分显著短于或少于对照组(P<0.05,表1)。
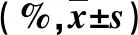
表1 两组围术期指标比较
2.2 两组肝功能指标比较 在术后7 d,观察组血清AST和ALT水平显著低于对照组(P<0.05,表2)。
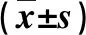
表2 两组肝功能指标比较
2.3 两组血清应激指标比较 在术后7 d,观察组血清TNF-α、IL-6、CRP和Cor水平及外周血WBC计数显著低于对照组(P<0.05,表3)。
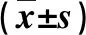
表3 两组血清应激指标比较
2.4 两组并发症发生率比较 术后,观察组并发症发生率显著低于对照组(P<0.05,表4)。

表4 两组并发症发生率(%)比较
3 讨论
GS合并EBDS是临床常见的急腹症,以右上腹疼痛、持续胀痛或胆绞痛等表现为主,可累及胰腺、肝脏等多个脏器,影响患者生命安全[10, 11]。虽然传统开腹手术能清除结石,但患者术后疼痛感相对强烈,且存在较多的并发症,易延长恢复时间[12, 13]。近年来,微创治疗理念不断发展,利用内镜微创手术治疗GS合并EBDS逐渐成为临床的重要选择[14, 15]。相较于传统开腹手术,内镜下微创手术具有创伤小、术后恢复快等特点。ERCP联合LC是临床常用的双镜治疗方法。ERCP能显示胆管病变,明确胆管走行和结石分布,治疗损伤胆总管的机会小[16, 17]。
本研究两组结石清除率无显著性差异,提示双镜联合治疗与传统开腹手术治疗的疗效相当,均能有效清除胆结石。但进一步研究显示,观察组手术时间、术后3 d VAS评分和术中出血量显著短于或少于对照组,提示双镜联合治疗能改善GS合并EBDS患者围术期指标,减轻术后疼痛。国内研究发现,双镜联合治疗能缩短手术操作时间,降低术中操作对机体的影响,减轻医源性损伤,有利于术后恢复[18]。传统开腹手术治疗的创口较大,术中出血量明显增加,手术创伤较大,会严重影响胆管系统功能,增加术后发生并发症的风险,导致恢复缓慢。相较于传统开腹手术,双镜联合治疗通过内镜能明确胆管狭窄部位和胆管结石分布情况,从而确定手术范围,避免术中切开胆管,有利于快速完成手术,且对腹腔的干扰较少,有利于缓解术后疼痛。双镜联合治疗的创伤较小,不会对胃肠道蠕动节律造成严重的影响,有利于降低术后肠内容物淤积风险,促进肠道功能恢复。
国内外研究发现,双镜联合治疗创伤远低于传统开腹手术治疗,能有效减轻术中操作对肝功能的损伤[19, 20]。本研究术后7 d观察组血清AST和ALT水平显著低于对照组,表明双镜联合治疗能改善GS合并EBDS患者肝功能。双镜联合治疗能准确发现和取出结石,避免传统开腹手术中反复钳夹结石可能所致的胆管损伤,通过高效取石能缓解胆汁外流引起的水电解质紊乱,减少代谢产物损伤肝组织,有利于保护肝功能。临床研究显示,手术操作属于应激源,GS合并EBDS患者在双镜联合治疗或传统开腹手术治疗后,术中刺激及疼痛会促进大量促炎因子的释放,引起机体应激反应[21, 22]。本研究发现,在术后7 d,观察组血清IL-6、CRP、Cor、TNF-α和外周血WBC计数显著低于对照组,表明双镜联合治疗诱发的应激反应相对较轻。双镜联合治疗的创伤程度较轻,能避免大量炎性因子释放所致的炎症反应,从而减轻应激损伤对机体的影响。为探寻双镜联合治疗的安全性,本研究对比分析术后并发症发现观察组显著低于对照组,提示双镜联合治疗能降低EBDS患者术后并发症发生风险,具有较高的安全性。双镜联合治疗无需留置T形管,保证了胆管的完整性,有利于降低胆道出血、急性胰腺炎和感染风险[23]。
综上所述,在GS合并EBDS患者,采用双镜联合治疗能改善围术期指标,加快术后恢复,改善肝功能,缓解应激反应,减少并发症,安全性较高。本研究尚存在一些不足,比如系单中心研究,样本量相对偏少,可能存在选择偏倚。由于胆石症患者可能存在高脂血症、高血压和糖尿病的基础疾病,对手术治疗提出了很高的要求,这些都需要认真控制和处理。

