无机化学课程思政探索
——以“缓冲溶液”为例
畅炳蔚,秦建芳,姜秀平,秦英恋,郭晶琳
(运城学院,山西运城 044000)
教育部《高等学校课程思政建设指导纲要》[1]中指出:全面推进课程思政建设是落实立德树人根本任务的战略举措,是全面提高人才培养质量的重要任务。理学、工学类专业课程,要在课程教学中把马克思主义立场观点方法的教育与科学精神的培养结合起来,提高学生正确认识问题、分析问题和解决问题的能力。
无机化学课程是化学、化学工程与工艺、材料化学、生命科学、药学等专业必修的一门专业基础课。通过本课程的学习,使学生了解无机化学的研究对象和发展趋势;掌握化学基本概念、化学反应原理、物质结构基础及元素化学等内容;培养学生具备综合运用所学知识独立完成化学实验和化学计算的能力,以及分析问题和解决问题的能力,为学生学习后续课程以及今后在化学及其相关领域从事工作打下良好的基础。
“缓冲溶液”是无机化学课程中很重要的一节内容,在生命科学、自然界、科学研究、工业生产、医药等领域中都有着广泛应用[2-4]。然而,目前大多数老师采取的教学方法是结合PPT 讲授,学生参与度低,上课注意力容易分散,很难达到提高学生的学习能力、分析问题和解决问题能力的课程目标。本文设计了以学生为中心的缓冲溶液教学方案,采用了案例教学法、问题驱动法、讨论法、实验法、任务驱动法等教学方式,充分调动学生的主观能动性,将价值塑造、知识传授和能力培养三者融为一体,落实立德树人根本任务。为广大教师践行无机化学课程思政提供参考。
1 学情分析
无机化学课程的教学对象是大学一年级学生,学生在高中时已经对弱电解质的电离平衡有一定认识。在学习本节内容前,学生已经学习了一元弱酸、多元弱酸的解离平衡,会根据平衡常数计算平衡时溶液中各离子的浓度,溶液pH 值,为缓冲溶液的学习打下基础。笔者所在高校使用教材为宋天佑主编的《无机化学(第四版)》[5],授课对象是一所省属普通本科院校化学专业大一学生。学生学习的主观能动性一般,往往需要教师下达任务驱动学生学习。此外,学生的计算能力比较薄弱,上课专注度一般。鉴于此,本文设计了以学生为中心的教学方案,将“缓冲溶液”知识点与案例充分融合,驱动学生结合案例自主探究出缓冲溶液的组成、原理及其pH 的计算。通过实验论证,提高学生独立思考、举一反三、解决问题的能力。通过“人体酸碱体质”、海绵城市等案例挖掘缓冲溶液中的课程思政元素。
2 教学目标
2.1 价值塑造
(1)通过探究人体血液缓冲体系,培养学生崇尚科学,善于思考的科学态度;
(2)通过辨析“人体酸碱体质”,培养学生辨证唯物主义科学的世界观;
(3)通过讨论海绵城市的缓冲作用,使学生认识到人类要合理开发大自然,用科技手段平衡人类发展与生态环境的关系;
(4)通过讨论辅导员在调节学生矛盾中的缓冲作用,培养学生解决问题的能力,遇到困难学会寻求辅导员、外界的帮助。
2.2 知识传授
(1)掌握缓冲溶液的定义、组成、作用机制;
(2)会计算缓冲溶液的pH 值;
(3)掌握缓冲溶液的配制方法,能根据反应条件选择合适的缓冲溶液;
(4)会运用缓冲溶液的作用机制,解释生产生活中的缓冲作用。
2.3 能力培养
(1)将酸碱平衡知识应用到缓冲溶液pH 计算中,提升学生知识迁移能力;
(2)带领学生推导出弱酸-弱酸盐缓冲溶液pH计算公式后,让学生独立推导出弱碱-弱碱盐缓冲溶液pH 计算公式,提升学生独立思考,举一反三的能力;
(3)通过实验验证缓冲溶液的作用机制,培养学生实验论证的能力;
(4)结合缓冲溶液在生产生活中的案例,培养学生知识应用,学以致用的能力。
3 教学内容设计
3.1 缓冲溶液的定义——案例法导入
【导入】人体各个部位pH 值保持在一定范围,比如正常人体血液pH 维持在7.35~7.45 之间[6-7]。而我们日常所吃的食物pH 各异,详见表1。但是不论我们摄入酸性较强的可乐,还是偏碱性的鸡蛋,或是喝了大量水后,人体各部位pH并不会有明显变化。像血液这种“能抵抗少量强酸、强碱和大量水的稀释而保持体系pH 基本不变的溶液”称为缓冲溶液。

表1 常见食物的pH
通过列举人体血液的缓冲作用,导入缓冲溶液的定义,激发学生的学习兴趣。
3.2 缓冲溶液的作用机制——问题驱动式教学
【教师提出问题】血液是如何控制pH 在如此小的波动范围内呢?
【教师引导】在血液中存在4 种缓冲对:①碳酸盐缓冲体系(NaHCO3/H2CO3);②血红蛋白缓冲体系(Hbb/KHb;HbbO2/KHbO2);③血浆蛋白缓冲体系(HPr/NaPr);④磷酸氢盐缓冲体系(Na2HPO4/NaH2PO4;K2HPO4/KH2PO4)[8]。其 中NaHCO3/H2CO3起主导作用。
【教师提出问题】以NaHCO3/H2CO3缓冲体系为例,当血液中酸性物质增多时会发生什么?
【学生分析问题】HCO3-会结合H+生成H2CO3,从而保持血液中H+浓度基本不变,血液pH 不变。同理,当血液中碱性物质产生或增多时,H2CO3与OH-反应生成HCO3-,从而维持血液pH 基本恒定。
【教师】当摄入酸性物质时,体内产生的H2CO3会分解出CO2从肺部排出;当摄入碱性物质后,产生的HCO3-则会从肾脏排出,如图1所示。

图1 血液的缓冲机制[9]
【讨论】缓冲溶液的作用机制是什么?
【学生分析问题】通过缓冲对之间的质子转移,消耗外加的少量的H+和OH-,从而维持缓冲溶液pH 值基本不变。
3.3 缓冲溶液的组成——讨论式教学
【讨论】缓冲溶液是由什么组成的?请以血液缓冲体系为例进行分析。
【学生分析问题】血液中碳酸盐缓冲体系(NaHCO3/H2CO3)是由弱酸-弱酸盐构成的,磷酸氢盐缓冲体系(Na2HPO4/NaH2PO4)是由多元酸盐及其次级酸盐构成。
【教师提出问题】那么弱碱-弱碱盐可以构成缓冲溶液吗?
【学生分析问题】在NH3-NH4Cl 体系中加入少量酸,NH3可以和H+结合生成NH4+;加入少量碱后,NH4Cl 会和OH-反应生成NH3·H2O,不会引起溶液pH 明显变化,因此弱碱-弱碱盐也可以构成缓冲溶液。
【归纳总结】缓冲溶液的三种组成方式:弱酸-弱酸盐、弱碱-弱碱盐、多元酸盐及其次级酸盐。
相较于传统的讲授法,讨论式教学法不仅活跃了课堂气氛,充分调动了学生的主观能动性,学生对于“缓冲溶液组成”这一知识点的理解和认识也更加深入。
3.4 缓冲溶液pH 的计算——任务驱动式教学
【教师】以弱酸-弱酸盐缓冲溶液HAc-NaAc 为例,引导学生找出其中的平衡关系,推理出弱酸-弱酸盐缓冲溶液pH 的计算公式pH=
【教师下达任务】请同学们以NH3-NH4Cl 缓冲溶液为例,自主推导出弱碱-弱碱盐缓冲溶液pH 的计算公式。
【学生解决问题】学生找出NH3-NH4Cl 缓冲溶液的平衡关系:NH3+H+⇌NH4+;NH4++OH-⇌NH3·H2O。最终推导出弱碱-弱碱盐缓冲溶液pH 的计算公式:pOH=
学生自主推导出缓冲溶液pH 的计算公式,相比于讲授法,学生主观能动性大幅提高,有效避免学生对这两个公式的混淆,清楚各公式的适用条件。
【练习】缓冲溶液中有1 mol/L HAc 和1 mol/L NaAc,试计算:
(1)缓冲溶液的pH;
(2)将1 mL 1 mol/L HCl 加入100 mL 该缓冲溶液引起的pH 变化;
(3)将100 mL 1 mol/L HCl 加入100 mL 该缓冲溶液引起的pH 变化;
【学生解决问题】经计算得,(1)缓冲溶液的pH为4.74;(2)缓冲溶液pH 变为4.73,pH 变化仅0.01;(3)缓冲溶液pH 变为2.37,pH 下降了2.37。
学生通过对比练习(2)(3),发现(2)在缓冲溶液中加入少量强酸时其pH 基本不变,而(3)在缓冲溶液中加入大量强酸后pH 有较大变化,失去缓冲作用。因此缓冲溶液抵抗强酸、强碱的能力是有限度的。进而提出缓冲容量及缓冲溶液pH 范围的概念。
【讨论】缓冲容量跟什么有关系?请同学结合表2、表3 进行分析。

表2 HAc-NaAc 缓冲对总浓度与缓冲能力的关系
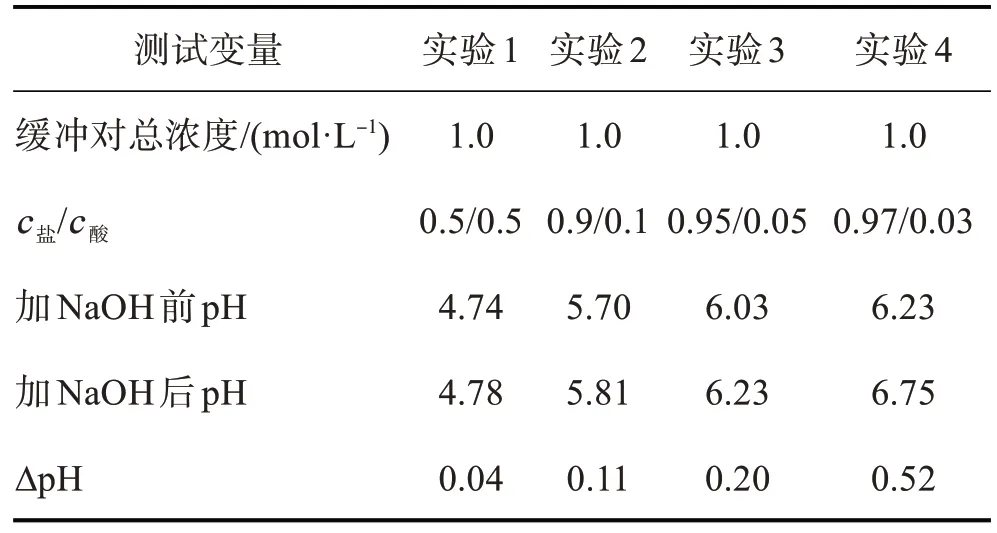
表3 HAc-NaAc 缓冲对浓度比与缓冲能力的关系
【学生分析问题】由表2 数据可得,缓冲对浓度越大,缓冲容量越大;由表3 数据可得,缓冲对浓度比值越接近,缓冲容量越大。
【教师】当c盐=c酸,缓冲对浓度较大时,缓冲容量较大。但一旦加入过多的强酸或强碱时,缓冲对将被大量消耗,抗酸抗碱能力也随之减弱甚至消失。缓冲溶液都有最佳的缓冲范围,理论上最佳pH 缓冲范围在pKaΘ±1 区间,实际应用中因缓冲对不同略有变化。
3.5 缓冲溶液的性质探究实验——实验教学
(1)分别向100 mL 蒸馏水和100 mL HAc-NaAc 缓冲溶液(HAc 和NaAc 浓度均为1 mol/L)中加入1 mL 1 mol/L HCl 溶液,观察溶液pH 的变化。
(2)向上述蒸馏水和HAc-NaAc 缓冲溶液中分别加入1 mL 1 mol/L NaOH 溶液,观察溶液pH 的变化。
(3)取10 mL 1 mol/L HCl 溶液和10 mL HAc-NaAc缓冲溶液,分别加水稀释至100 mL,观察溶液pH的变化。
在该实验教学中实验(1)和(2)探究了酸碱对缓冲溶液pH 的影响,实验(3)探究了稀释对缓冲溶液pH 的影响。
结果与讨论中,学生不仅要记录实验观察到溶液pH 的实际变化值,还需要通过缓冲溶液pH的计算公式,求解出溶液pH 的理论变化值。通过对比pH 的理论值和实际值,学生发现两者十分相近,进一步验证了缓冲溶液pH 的计算公式。
通过实验和计算让学生深切感受到缓冲溶液的作用机制,同时加深了学生对缓冲溶液pH 计算知识点的掌握,锻炼了学生的实践应用能力、计算能力和实验技能。
3.6 缓冲溶液的配制——任务驱动式教学
【教师】在化工生产,医药领域经常需要控制反应pH 在一定范围内,那么如何选择和配制合适的缓冲溶液呢?①缓冲溶液中弱酸或弱碱的p和p应尽量接近于反应所需pH。②通过调整弱酸-弱酸盐c酸/c盐或弱碱弱碱盐c碱/c盐比值,使缓冲溶液的缓冲范围与反应pH 范围相吻合。
【案例】栲胶脱硫工艺是一种脱除H2S 气体的湿法脱硫工艺,是我国目前在煤化工气体净化领域使用效果最好的脱硫方法之一[10]。脱硫液的pH值是影响整个脱硫工艺最重要的因素。pH 过低,H2S 去除率较低;pH 过高,平衡时HS-的转化率降低。脱硫液的pH 值需控制在9.00~9.20 之间。
【教师下达任务】请你从以下缓冲对(HAc-NaAc:pKaΘ=4.75、NaH2PO4-Na2HPO4:pKaΘ=7.21、NH4Cl-NH3·H2O:pKaΘ=9.25、NaHCO3-H2CO3:pKaΘ=10.25)中选择一组你认为最适合栲胶脱硫工艺的缓冲对,并设计配制该缓冲溶液的方案。
【学生解决问题】缓冲对的pKaΘ值应尽量接近所要求的pH 值,因此表4 中NH4Cl-NH3·H2O 缓冲对更符合要求,再根据亨德森-哈塞尔巴尔赫方程,设计出配制NH4Cl-NH3·H2O 缓冲溶液方案。
通过工业实例探究,让学生独立设计配制缓冲溶液,即加强了学生对知识点的掌握,也将知识付诸于实践,让学生不再觉得“知识无用论”,感受知识与人们生产生活的密切联系。
3.7 思政案例1:辨析人体酸碱体质——讨论式教学
【讨论】“有人说人体有酸性体质,碱性体质,并通过保健品、食疗等方式可以使酸性体质变为碱性体质。你认为这有科学依据吗?请说明原因。”
【学生】人体血液中存在以NaHCO3/H2CO3为主的缓冲体系,适量摄入碱性食物或保健品后,由于血液缓冲体系的存在,正常人血液pH 依旧维持在7.35~7.45,因此酸碱体质是不可信的。
【教师】网络上一些公众号、视频号经常发布关于人体酸碱质的内容,误导了很多群众。请同学们将血液缓冲体系的知识科普给家人朋友,帮助身边人分辨网络上关于酸碱体质的谬论。
3.8 思政案例2:海绵城市——讨论式教学
【教师】2021 年7 月发生在河南的特大暴雨令很多人终身难忘,当地很多人民的房屋、车辆被洪水淹没,群众被困家中,河南省紧急转移安置147.08 万人。这次灾害虽为极端天气引发,但集中暴露出许多问题,请同学们讨论分析。
【学生1】城市防雨系统比较薄弱,无法应对特大暴雨。
【学生2】市政府应急管理能力有待加强。在遇到特大暴雨时,没能第一时间进行有效的处置。
【教师】同学们从城市建设和政府管理方面都找到了问题。这次暴雨给我们也带来了深厚的教训:随着城市化发展,越来越多的土地变成水泥路面、盖上了高楼大厦,但与此同时土壤的防雨防汛能力大大下降,而地下管网容纳能力又不足,因此在面临这种特大暴雨时,整个城市的防雨防汛系统被击溃。
【教师】有什么措施可以提高城市的防雨防汛能力?
【学生3】增加城市绿化面积,在居民区周围修建公园,人工湖。
【学生4】扩容城市地下管网,增强排水能力。
【教师】是的,这些措施正是目前政府构建“海绵城市”的主要举措。除了上述同学提到的,政府将一些园区、居住区的道路改为透水混凝土,在部分居民区构建绿色屋顶。这些雨水通过排水沟、雨水链等方式进行贮蓄或下渗。政府也在积极地构建蓄水模块,如雨水花园、生态滞留池、渗透池、人工湿地等。
在雨水比较多的夏季,雨水通过土壤的渗透被净化后储存在蓄水模块中,城市的积水、汛情也大大减少。在枯水季节,蓄水模块中的水又可以涵养植被,也可处理后用于生产生活中。海绵城市通过储存或排放雨水,来保护城市抵抗过涝或过旱的天气,起到缓冲作用。
3.9 思政案例3:辅导员在调节学生矛盾中的缓冲作用——讨论式教学
【教师】进入大学后,同学们都过上了寄宿生活。在集体生活中同学们难免会发生一些摩擦,大家是如何化解矛盾的呢?
【学生1】让时间来化解矛盾,一般过两天大家就重归于好了。
【学生2】舍友帮忙调解,解开误会。
【学生3】有时因性格不合产生的矛盾,互不理睬就好了。
【教师】小的矛盾大家互吐心声,大部分能够内部解决。但是当遇到大的矛盾无法调和时,大家就要寻求辅导员,老师的帮助了。2013 年,复旦大学医学院研究生林森浩因琐事对室友黄洋怀恨在心,将剧毒化学品二甲基亚硝胺注入饮水机,导致黄洋死亡。林森浩与黄洋的矛盾早在2011 年就已产生,但是两人都没有寻求外界的帮助,随着长期矛盾的累积才发生了如此悲剧。近年来,国家越来越重视高校辅导员队伍的建设。辅导员更加年轻化,更好地与学生沟通、大家生活中有什么困难都可以向辅导员提出,辅导员会耐心地帮助大家解决问题,调解矛盾,作同学生活中的缓冲剂。在复旦投毒案事件中,倘若这两位同学及时找辅导员或老师调解,相信不会发生这样的悲剧。
3.10 课后作业:缓冲溶液思维导图及其应用——任务驱动式教学
课尾帮助学生回顾本节所学知识:缓冲溶液的定义、原理、缓冲溶液pH 的计算、缓冲容量、缓冲范围、缓冲溶液的配制等。
【作业1】完成缓冲溶液思维导图,培养学生养成及时梳理知识的良好习惯,巩固课堂内容。
【作业2】请同学挖掘缓冲作用在生产生活中案例,包括在生命科学、自然界、科学研究、工业生产、医药等领域的应用。以小组为单位,进行课堂汇报。
4 教学反思
(1)课堂导入引入人体血液缓冲体系,激发学生的好奇心和求知欲,有效提高上课注意力和学习效果。
(2)通过问题驱动式教学方法,学生逐步探究出缓冲溶液的组成,作用机制,pH 的计算,锻炼了学生自主学习,分析问题和解决问题的能力,体现了“以学生为中心”的教学理念。
(3)化学是一门实验性的学科,结合实验验证缓冲溶液作用机制,加深了学生对知识点的理解与记忆,提升了学生的动手能力及科学探究能力。
(4)将例题与工业实例结合,培养学生理论联系实际的能力。
(5)通过辨析“人体酸碱质”,不仅巩固了知识,还提高了学生知识应用、辩证思维能力。
(6)通过讨论海绵城市的缓冲作用,使学生认识到要合理开发大自然,保护土壤的蓄水作用,用科技手段平衡人类发展与生态环境的关系,与大自然和谐共处。
(7)通过讨论辅导员在调节学生矛盾中的缓冲作用,使学生认识到当遇到自身无法调和的矛盾时,要积极寻求辅导员和老师的帮助。
(8)学生通过寻找生产生活中缓冲溶液案例并说明其中缓冲作用机制,提升了学生查阅文献资料的能力及自学能力,也加强了知识的理解与运用。
——以大安古河道试验区“古河妈妈”粳米为例

