顶空气相色谱和顶空气相色谱-质谱法测定20种中药材中磷化铝的残留量
王月玲,戚鹏飞,吴福祥,邵长春,徐雪梅*,杨金草(1.兰州市食品药品检验检测研究院,兰州 70050;2.国家市场监管重点实验室(食品中农药兽药残留监控),兰州 70050;.甘南藏族自治州药品检验检测中心,甘肃 合作 747000)
磷化铝是国内外粮食贮藏中普遍使用的高效杀虫剂,遇水或酸可产生磷化氢气体,该气体是杀虫的有效成分,其穿透性强,易挥散,且对霉菌也有抑制作用[1]。近年来,药材市场上广泛采用磷化铝熏蒸来代替硫磺熏蒸药材应用于中药材贮存[2-4],经过磷化铝熏蒸处理的中药材可防虫5~6个月[5]。本课题组前期市场调研发现,市场上普遍存在磷化铝熏蒸中药材的情况,尤其是从每年的春季惊蛰至秋季寒露期间,熏蒸尤为普遍,在甘肃省地产大宗中药材中,以党参熏蒸最甚,黄芪、当归次之。
然而熏蒸产生的磷化氢属于剧毒易燃气体,在熏蒸过程中如处理不当会造成较为严重的后果,一般会引起以神经系统、呼吸系统损害为主的全身性疾病[6],严重的会导致心、肝、肾等重要器官衰竭等[7-8]。熏蒸后磷化氢气体还容易残留在药材中,其安全性尚缺乏系统的研究。目前,中药材中尚无直接检测磷化铝的方法,磷化氢的检测方法也较匮乏和落后,主要有钼蓝比色法、滴定法、离子色谱法等[9-11],这些方法的前处理操作均较复杂,方法稳定性差,灵敏度较低,专属性不强,易造成假阳性结果[12],并且需要较大的取样量。近年来,顶空气相色谱法广泛应用于食品[13-14]、药品[15-17]、化妆品[18]等样品中挥发性和半挥发性有机物的分析,也应用于烟草、水果等基质中磷化氢的检测[19-22],相比传统磷化氢检测方法,该法具有前处理简单、灵敏度高的优势,但目前该方法对中药材中磷化铝残留方面的研究十分有限[23-24]。因此,本试验选择甘肃省市售中药材、中药饮片中易生虫的品种(其中包括部分甘肃省地产中药材品种)党参、大黄、黄芪、桔梗、枸杞子、款冬花、当归、杏仁、泽泻、白芷、土鳖虫、柏子仁、皂角、肉苁蓉、桑白皮、天花粉、防己、瓜蒌、酸枣仁、板蓝根作为研究对象,采用顶空气相色谱(HSGC)和顶空气相色谱-质谱(HSGCMS)法建立此20种中药材、中药饮片中磷化铝残留量的检测方法,并通过对样品中磷化铝的残留量进行风险评估,为科学评价中药材的安全性提供数据参考,为中药材市场监管提供技术支撑。
1 材料
1.1 仪器
岛津GC-2010 Plus气相色谱仪(日本岛津),配置火焰光度检测器(FPD)和顶空进样系统(DANI HSS 86.50 Plus);安捷伦7890B-7000D(GS-MS)气相色谱-质谱联用仪,配置安捷伦7697A顶空进样器,Agilent HP-PLOT/Q-PT毛细管柱(30 m×0.53 mm,40 μm)(美国安捷伦);MettlerToledo ME403型电子天平(瑞士梅特勒-托利多公司);Milli-Q超纯水仪(美国Millipore公司);Vortexer 涡旋混匀仪(上海嘉鹏科技有限公司);10、1000、5000 μL鲁尔头阀门型气体密封针(上海玻利鸽有限公司);带密封翻盖橡胶塞的600 mL玻璃瓶(徐州荣昌玻璃制品有限公司);20 mL顶空钳口样品瓶及其PTFE硅胶垫瓶盖(安捷伦);封口均质袋(比克曼生物科技有限公司)。
1.2 试药
56%磷化铝(济南天邦化工有限公司);硫酸(纯度:98%,分析纯,重庆川东化工有限公司);纯化水(Milli-Q 超纯水仪自制);其余试剂均为分析纯。
中药材、中药饮片在甘肃兰州、定西及安徽亳州药材市场购买,共20个品种252批次,具体信息见表 1,样品均经兰州市食品药品检验检测研究院戚鹏飞主管药师鉴定为正品。
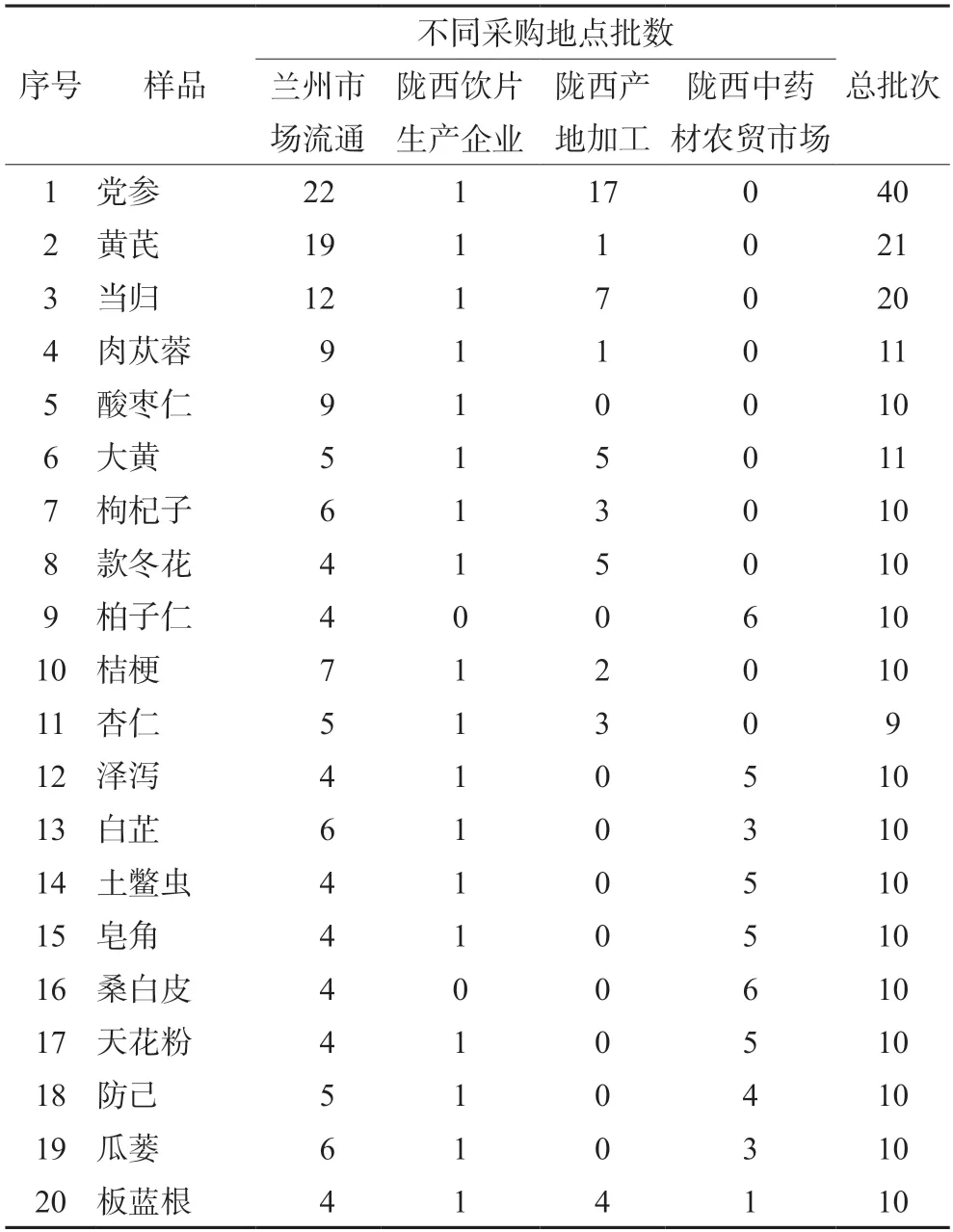
表1 样品收集信息表Tab 1 Sample collection information table
2 方法与结果
2.1 定量分析
2.1.1 气相色谱法分离条件 岛津GC-2010 Plus气相色谱仪配置火焰光度检测器、磷滤光片、Agilent HP-PLOT/Q-PT毛细管柱(30 m×0.53 mm,40 μm);检测器温度250℃;升温程序为初始50℃保持10 min,升至200℃保持2 min;进样口温度220℃,分流进样,分流比10∶1;载气:高纯氮30 mL·min-1,氢气 62.5 mL·min-1,空气90 mL·min-1,柱流量 2 mL·min-1。顶空进样器条件:气相循环时间20 min,顶空瓶平衡温度50℃,平衡时间10 min,采用振荡模式。
2.1.2 标准曲线 磷化氢标准贮备气体的制备:取磷化铝片1片,称重为3.232 g,置于600 mL玻璃瓶中,加水10 mL,迅速盖紧翻盖橡胶塞密封,室温下静置2 d[25],作为磷化氢标准贮备气体。用气体密封针吸取标准贮备气5.0 mL,注入另一600 mL密封玻璃瓶中,轻轻晃动使混合均匀,作为磷化氢标准原气。用气体密封针吸取标准原气1.0 mL,注入另一600 mL密封玻璃瓶中,轻轻晃动使混合均匀,作为磷化氢标准气体。
磷化氢标准贮备气的含量标定:参照SN/T4395—2015中的标定方法[26],在一个可密封的50 mL试剂瓶中,预先加入10 mL95%的乙醇和20 mL1.5%的氯化汞溶液,吸取5.0 mL磷化氢标准贮备气注射到此瓶中,充分振摇后,把瓶口倒置约30 s 使其反应完全,用甲基红作指示剂,用氢氧化钠滴定液(0.05 mol·L-1)滴定至黄色终点(或电位滴定仪滴定),根据消耗的氢氧化钠滴定液的体积计算出磷化氢标准贮备气体的含量。标定数据见表2。
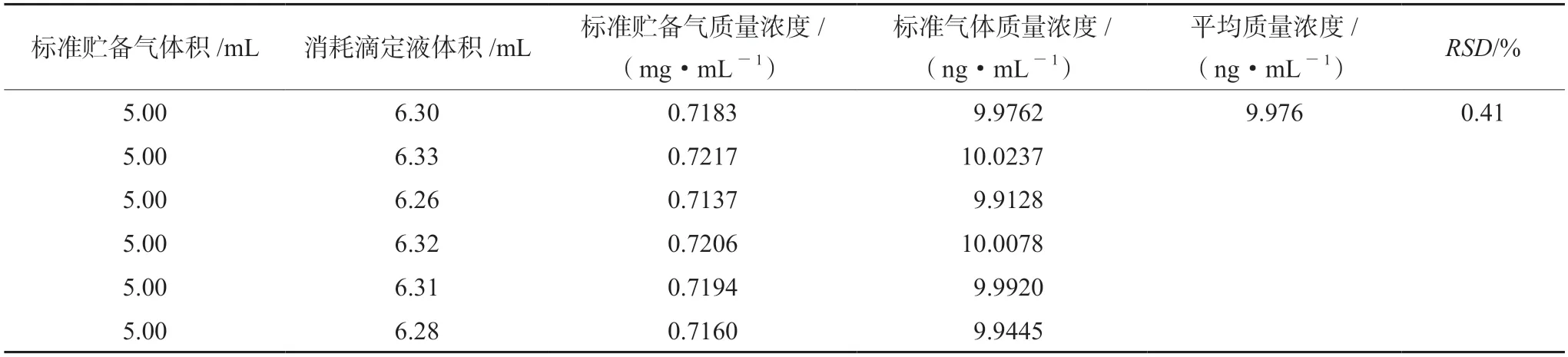
表2 磷化氢标准贮备气及标准气体含量Tab 2 Content of standard reserve gas and standard gas of phosphine
标准溶液的制备:分别吸取标准气体0、100、200、500、1000、2000、3000和5000 μL(分别约相当于磷化氢0、0.9976、1.9952、4.9880、9.9760、19.9520、29.9280和49.8800 ng)注入预先加有5.0 mL5%硫酸的20 mL顶空瓶中,涡旋10 s,即得系列对照品溶液。
2.1.3 供试品溶液的制备 取供试品粉碎,混匀,精密称取1 g,置20 mL顶空瓶中,加入5.0 mL 5%硫酸溶液,迅速压盖封口,涡旋10 s,即得。
2.1.4 精密度试验 用气密针吸取标准磷化氢气体3000 μL(约相当于磷化氢30 ng),注入预先加有5.0 mL 5%硫酸的20 mL顶空进样瓶中,平行6份,涡旋10 s,进样测定,测得磷化氢峰面积RSD为1.3%,表明仪器精密度良好。
2.1.5 线性关系考察 精密吸取“2.1.2”项下系列对照品溶液,注入气相色谱仪测定。以磷化氢质量(ng)为横坐标(X),峰面积为纵坐标(Y)进行回归,得方程为Y=2.496×105X-2.540×105(r=0.9966),结果表明磷化氢在1~50 ng内与峰面积呈良好的线性关系。
2.1.6 专属性 将未经磷化铝熏制的白芷样品作为阴性样品,经过熏制的白芷样品作为阳性样品,分别取磷化氢标准气体、阴性样品、阳性样品各适量,按“2.1.3”项下方法制备成溶液,注入气相色谱仪,记录色谱图。结果表明:阴性样品溶液色谱图中未出现与对照品保留时间一致的色谱峰,阳性样品溶液色谱图中色谱峰保留时间与对照品一致,且无杂质峰干扰。色谱图见图1。

图1 不同溶液的气相色谱图Fig 1 Gas chromatograms of different solutions
2.1.7 检测限与定量限测定 将标准气体逐步稀释,根据磷化氢色谱峰信噪比为S/N≈10,计算该方法的定量限为0.9976 μg·kg-1;S/N≈3时计算该方法检测限为0.0665 μg·kg-1。
2.1.8 加样回收试验 取白芷样品粉末,称取约0.5 g,置20 mL顶空瓶中,加入5.0 mL5%硫酸溶液,迅速压盖封口,分别加入200、300、500µL的磷化氢标准气体,每个质量浓度平行3份,涡旋10 s,进样测定,计算加样回收率。结果显示,低、中、高浓度平均加样回收率分别为88.9%(RSD=6.2%)、84.8%(RSD=1.5%)、82.3%(RSD=2.1%)。
2.1.9 稳定性试验 取经磷化铝熏制的白芷样品,按“2.1.3”项下方法制备成供试品溶液,分别于0、2、4、6、8、10、12、18、24 h进样测定,测得磷化氢峰面积RSD为1.3%,表明溶液在10 h内基本稳定。
2.1.10 重复性试验 取经磷化铝熏制的白芷样品,按“2.1.3”项下方法制备6 份供试品溶液,进样测定,结果磷化氢平均含量为0.056 mg·kg-1,RSD为3.8%。
2.2 定性分析
2.2.1 气相色谱-质谱条件 安捷伦7890B-7000D(GS-MS)气相色谱-质谱联用仪,配置安捷伦7697A顶空进样器、Agilent HP-PLOT/Q-PT毛细管柱(30 m×0.53 mm,40 μm);色谱柱升温程序:50℃保持5 min,以50℃·min-1速率升温至200℃,保持2 min;进样口温度:200℃;传输线温度:200℃;载气:氦气;进样方式:分流进样,分流比:10∶1;电子轰击能量:70 eV;离子源温度:200℃;倍增器电压:自动调谐值;柱流量:1.0 mL·min-1;质量扫描范围:19~80 amu;扫描方式:离子监测扫描SIM,检测离子:m/z31、33、34。
顶空进样器条件:加热箱温度50℃,定量环温度95℃,传输线温度105℃,气相循环时间20 min,进样瓶加热平衡时间10 min,加压时间0.2 min,定量环充满时间0.2 min,定量环平衡时间0.2 min,进样时间1.0 min。
2.2.2 对照品溶液的制备 用气体密封针吸取标准贮备气0.2 mL,注入预先加有5.0 mL5%硫酸的20 mL顶空瓶中,涡旋10 s,即得系列对照品溶液。
2.2.3 供试品溶液的制备 同“2.1.3”项下供试品溶液的制备方法。
2.2.4 检测限的测定 将标准气体逐步稀释,直到磷化氢色谱峰信噪比为S/N≈3时,计算出该方法的检测限为0.0023 μg·g-1。
2.3 样品的测定和检测结果判定
将检出磷化铝的阳性样品按“2.2.1”项下方法进样测定。
定量分析采用外标法计算磷化氢含量,为保证检测结果的可靠性,平行测定2份,并计算相对偏差。如果平行样相对偏差≤20%,则认为定量数据可靠,其含量按2份检材的平均值计算。如果平行样相对偏差>20%,则认为定量数据不可靠,应重新检验。样品中磷化铝残留量检测数据见表3。

表3 中药材、中药饮片样品中磷化铝残留量检测数据Tab 3 Aluminum phosphide residues in samples of Chinese medicinal materials and Chinese herbal slices
定性分析中,m/z选择31、33、34作为监测离子,34的响应值相对比较高,因此选择34作为特征离子丰度比参考离子。在相同条件下进行样品测定时,样品中磷化氢的色谱峰保留时间与标准溶液一致,且在扣除背景后的样品质谱图中,磷化氢的质谱特征离子与标准溶液一致,特征离子丰度比与浓度接近的标准溶液相比,相对偏差不超过表4规定的范围,空白样品无干扰,则可判断检材样品中检出磷化氢。

表4 特征离子丰度比的最大允许相对偏差范围Tab 4 Maximum allowable relative deviation of characteristic ion abundance ratio
检测数据显示,20种中药材、中药饮片均有不同程度的磷化铝残留检出。其中,土鳖虫中的检出率最高,达到100%;黄芪、款冬花、党参、瓜蒌、防己、肉苁蓉、当归、桑白皮、杏仁次之,检出率达50% 以上,天花粉、白芷等淀粉含量高的样品检出率较低。
基于残留量数据分析可见,残留量最高的是当归,最大达到0.4623 mg·kg-1;黄芪次之,最大残留量为0.0774 mg·kg-1;土鳖虫、桔梗、杏仁较低。由此可见,中药材部分品种中磷化铝残留量高于中国食品安全国家标准GB 2763—2021食品中农药最大残留量国家限量标准中规定中谷物、油料和油脂、蔬菜中磷化铝残留量限度0.05 mg·kg-1,也高于欧洲议会和理事会规定的国际粮食限量标准(0.01 mg·kg-1)及国际食品法典委员会针对干制蔬菜、干制水果、香料等中磷化氢残留量的限量标准(0.01 mg·kg-1)。
3 讨论
3.1 试验方法设计
试验采用气相色谱法-火焰光度检测器(GSFPD-P)定量、气相色谱-质谱法(GS-MS)定性的设计,主要是由于GS-FPD-P对含磷化合物有高选择性、高灵敏度,而磷化铝残留量是一个痕量检测,因此选择GS-FPD-P定量更为适宜。然而中药材种类繁多,成分复杂,GS-FPD-P在定性方面会受其他一些含磷挥发性成分的干扰,因此,选择GS-MS对阳性样品进一步确认。
3.2 磷化铝标准气体的含量标定
参照SN/T 4395—2015对磷化铝标准气体含量进行标定,用甲基红作指示剂,溶液颜色由橙色变为黄色。在实际操作中,由于橙色与黄色颜色比较接近,目测观察颜色突跃有一定困难,影响终点判定,因此建议采用电位滴定法。
3.3 色谱柱的考察
在气相色谱分析中,为达到理想的分离效果,考察了4种色谱柱,分别是安捷伦HP-5气相色谱柱(30 m×0.32 mm,0.25 μm)、HP-PLOT/Q-PT 色谱柱(30 m×0.53 mm,40 μm)、DB-1701色谱柱(30 m×030 m×0.32 mm,0.25 μm)和岛津Rtx-624色谱柱(30 m×0.25 mm,1.40 μm)。结果发现,除HP-PLOT/Q-PT柱外,其他3种色谱柱对磷化氢均无保留,出峰时间均在3 min以内,且峰形存在不同程度的分叉;HP-PLOT/Q-PT柱出峰时间约在8 min左右,峰形光滑对称,理论板数高,满足分析方法需求。
3.4 影响稳定性因素
在稳定性试验中,溶液在10 h内浓度基本稳定,10 h后逐渐减小,分析原因可能是由于磷化氢化学性质活泼,能与氧气发生反应所致。在检测中建议供试品溶液在10 h内进样。
4 结论
本试验建立了HSGC和HSGCMS法测定20种中药材中磷化铝残留量的方法,该方法操作简便,灵敏度高,专属性好,适用于中药材、中药饮片中残留的磷化铝的检测。

