基于UPLC-Q-TOF-MS技术的脉络宁注射液酯提废渣大孔树脂富集液的化学成分鉴定和含量测定
鲁正熹,姚静远,印敏,李林蔚,何晓东,刘群,李剑,陈雨*(.江苏卫生健康职业学院,南京 009;.江苏省中国科学院植物研究所/江苏省中药材生态种植与高值化利用工程研究中心,南京 00;.南京金陵药业股份有限公司,南京 0009;.河南金陵金银花药业有限公司,河南 新乡 500)
脉络宁注射液,为黄棕色至红棕色的澄清液体,由金银花、山银花、牛膝、玄参、石斛等组成,有清热养阴、活血化瘀的功效,临床上用于治疗血栓闭塞性脉管炎[1]、急性缺血性脑血管病[2]、急性脑梗死[3]、静脉血栓形成[4]、动脉硬化性闭塞症[5]、脑血栓形成及后遗症[6]。有研究表明,脉络宁注射液在一定程度上对治疗急性缺血性卒中[7]、腰椎间盘突出症[8]、非酒精性脂肪肝[9]、急性肺损伤[10],喉头水肿[11]等也有效。
脉络宁注射液采用水煎煮提取药效物质,经乙醇沉淀、乙酸乙酯萃取、浓缩等精制而得[12],导致在生产过程中产生了大量废渣。中药废渣的处理一直是我国医药行业和环境行业所关注的问题,通常采用填埋、焚烧、固定区域堆放等措施处理,但会对周围的水质、土壤和空气造成严重的污染,影响环境质量,且耗费大量资金[13],因此对中药废渣的资源再利用极其重要。到目前为止,有关脉络宁注射液废渣的资源再利用,主要是对水提和醇沉物的研究[12,14-16]。乙酸乙酯萃取后的母液废渣,为生产脉络宁注射液过程中的废弃物之一,如不进行资源化再次利用,不仅造成浪费,而且作为废渣排放还会造成二次污染。本研究运用超高效液相-四极杆串联飞行时间质谱技术(ultraperformance liquid chromatography quadrupole time-of-flight mass spectrometry,UPLC-Q-TOF-MS)对脉络宁注射液酯提废渣化学成分进行鉴定,并对其中的酚酸类成分(绿原酸、异绿原酸A和异绿原酸C)和三萜皂苷类成分(灰毡毛忍冬皂苷甲和灰毡毛忍冬皂苷乙)进行定量分析,以期为脉络宁注射液酯提废渣资源再利用提供科学参考,从而为后续中药渣的回收利用和环境保护奠定基础。
1 材料
1.1 仪器
Agilent 1260 UPLC-DAD-6530 ESI-Q-TOF-MS液质联用仪(美国Agilent公司);KQ-400KDE型数控超声波清洗器(昆山市超声仪器有限公司);JY/YP型电子天平(上海良平仪器仪表有限公司);SPING-S5i超纯水仪(南京妙之仪电子科技有限公司);OSB-2200型旋转蒸发仪(日本EYELA公司);Q-TOF Quantitative Analysis定量软件;Molecular Structure Correlator结构鉴定软件。
1.2 试药
甲醇(色谱纯,美国TEDIA公司);无水乙醇(分析纯,国药集团化学试剂有限公司);甲酸(色谱纯,美国ROE SCIENTIFIC INC公司);蒸馏水(屈臣氏);ASD-7大孔吸附树脂(郑州和成新材料科技有限公司);硅胶(青岛海洋化工厂);绿原酸(批号:0753-9607)、异绿原酸A(批号:111782-201807)、异绿原酸C(批号:111894-202104)(中国食品药品检定研究院);灰毡毛忍冬皂苷甲、灰毡毛忍冬皂苷乙来自本课题组分离,所有对照品纯度均大于95%。
本研究所用脉络宁注射液酯提废渣来自金陵药业股份有限公司,共8个批次,分别为20210228、20210301、20210302、20210303、20210312、201210313、20210314、20210315。
2 方法与结果
2.1 溶液的制备
2.1.1 供试品溶液的制备 称取一定质量的脉络宁注射液酯提废渣,废渣-水为1∶10稀释,稀释液经ASD-7大孔树脂柱梯度洗脱,洗脱剂为0%、10%、90%、100%乙醇水溶液,取90%乙醇水溶液洗脱部位500 μL,氮吹至干,1 mL甲醇溶解,甲醇稀释10倍,过0.45 μm微孔滤膜,即得。其中90%乙醇水溶液部位大孔树脂得率为43.31%~60.77%,8批脉络宁注射液酯提浸膏过大孔树脂后90%乙醇水溶液部分干燥质量分别为11.5、12.0、12.1、12.4、18.5、17.9、22.4、28.5 mg。
2.1.2 对照品储备溶液的制备 精密称定绿原酸、异绿原酸A、异绿原酸C、灰毡毛忍冬皂苷甲和灰毡毛忍冬皂苷乙,制成33.33、16.67、33.33、16.67、66.67 µg·mL-1的对照品储备溶液,冷藏备用。
2.2 色谱条件
色谱柱Agilent Poroshell 120 SB-AQ C18(3.0 mm×100 mm,2.7 μm);柱温0~20 min,20℃;20~75 min,40℃;流动相为0.1%甲酸水溶液(A)-甲醇(B),梯度洗脱(0~20 min,20%~25%B;20~25 min,25%~35%B;25~40 min,35%~50%B;40~75 min,50%~70%B);流速为0.3 mL·min-1;进样量为5 μL。
2.3 质谱条件
采用ESI离子源,离子化模式为负离子模式,毛细管电压为3.5 kV,干燥气温度350℃,裂解电压为:酚酸、黄酮和环烯醚萜90 V,三萜皂苷210 V,碰撞能量为195 V,雾化气体为N2,离子扫描范围为m/z100~1700,雾化气压力50 psi,干燥气流速10.0 L·min-1,Skimmer电压65 V。
2.4 UPLC-Q-TOF-MS定量方法学考察
2.4.1 专属性试验 精密吸取混合对照品溶液和供试品溶液适量,进样分析,各成分出峰位置无干扰组分,表明本法专属性良好,符合液质定量分析要求,典型色谱图见图1。
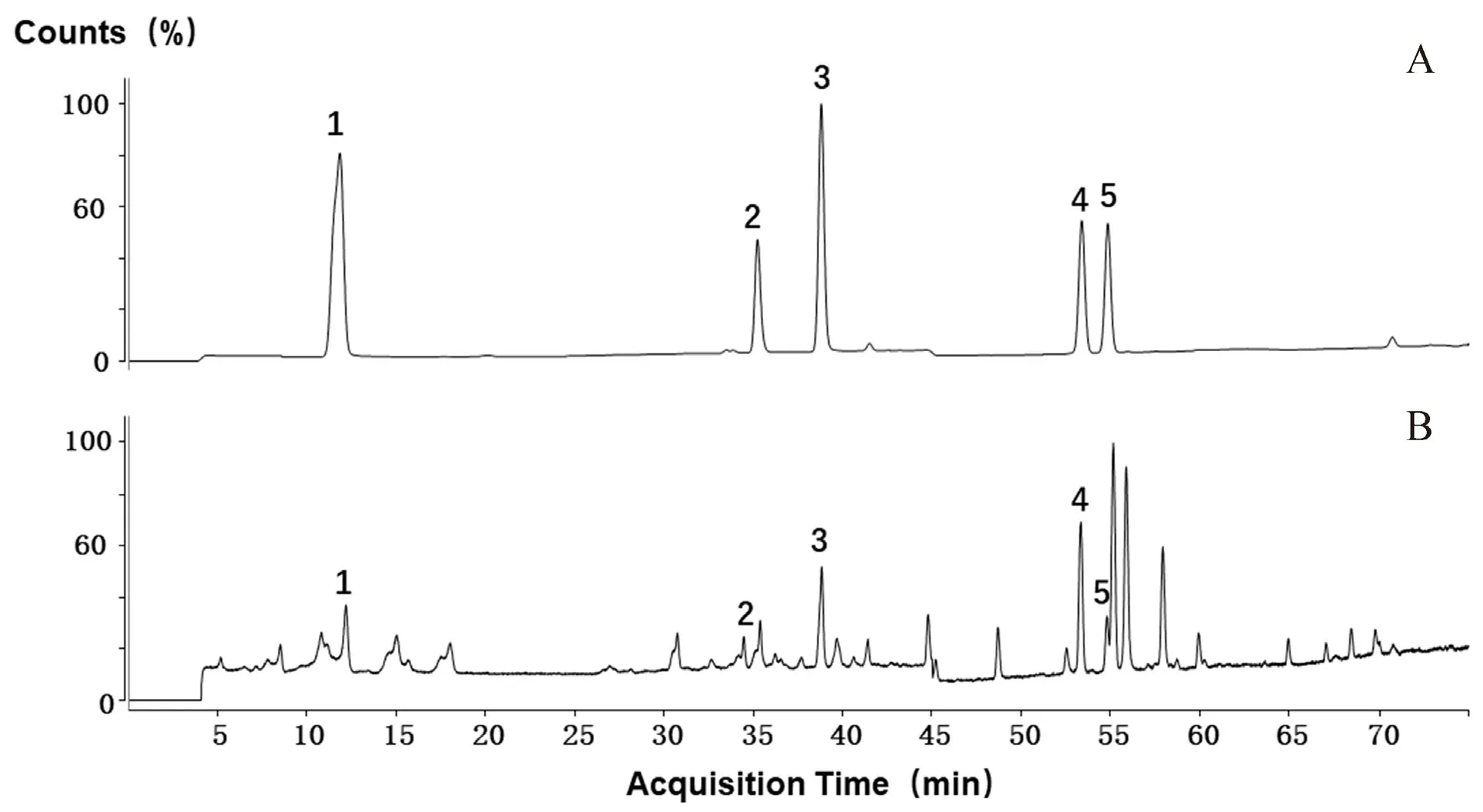
图1 混合对照品(A)和脉络宁注射液酯提废渣(B)UPLC-Q-TOF-MS图Fig 1 UPLC-Q-TOF-MS of mixed control(A)and Mailuoning injection ester extraction residue(B)
2.4.2 线性关系、检测限和定量限 分别精密吸取对照品储备液适量于5 mL具塞棕色量瓶中,以甲醇逐步稀释配成系列混合对照品溶液,进样测定峰面积,以峰面积(Y)对对照品质量浓度(X)进行线性回归,计算5种分析物的回归方程,结果见表1。

表1 5种分析物的线性范围、回归方程、相关系数、检测限和定量限Tab 1 Linear ranges,calibration curves,coefficients,limit of quantitation and detection of 5 analytes
2.4.3 精密度试验 取供试品溶液,连续进样6次,分别计算5种分析物峰面积的RSD,结果峰面积的日内精密度RSD在2.3%~4.5%,表明仪器精密度良好。
2.4.4 稳定性试验 取供试品溶液,分别于0、4、8、12、24 h进样分析,分别计算5种分析物峰面积的RSD,结果峰面积的RSD分别在0.60%~4.6%,表明测定成分在24 h内稳定性良好。
2.4.5 重复性试验 取平行制备的6份供试品溶液(批号:20210303),进样测定峰面积,计算得绿原酸、异绿原酸A、异绿原酸C、灰毡毛忍冬皂苷甲和灰毡毛忍冬皂苷乙的质量分数分别为10.98、3.92、8.06、36.90、3.87 mg·g-1,峰面积的RSD分别为0.80%、1.7%、1.6%、0.60%、1.0%,表明方法重复性良好。
2.4.6 加样回收试验 取已知含量的脉络宁注射液酯提废渣处理液9份(批号:20210314),分别加入低、中、高3个浓度的混合对照品溶液,进行含量测定,计算得5个成分的加样回收率为95.38%~103.06%,RSD为0.76%~1.8%,表明本方法准确性良好。
2.5 UPLC-Q-TOF-MS定性分析脉络宁注射液酯提废渣
经过色谱条件优化,供试品溶液在负离子模式下的色谱图得到了良好的分离效果及离子化效率,其TIC图见图2。

图2 负离子模式下的脉络宁注射液酯提废渣TIC图Fig 2 Total ion chromatogram of Mailuoning injection ester extract ion residues at the negative ion mode
样品经UPLC-Q-TOF-MS进行一级及二级质谱采集,获得提取液中各色谱峰的保留时间、准分子离子峰及MS/MS碎片离子的精确相对分子质量信息。若目标成分与其对照品(无对照品的与参考文献数据比对[17-18])的保留时间、准分子离子峰和二级特征离子吻合,以及Agilent定性软件推断碎片离子破碎规律,据此鉴定色谱峰。推断出脉络宁注射液酯提废渣中42个化合物的结构,包括9个酚酸类化合物、9个黄酮类化合物、10个环烯醚萜类化合物、8个三萜皂苷类成分化合物、5个苯丙素类化合物和1个联苄类化合物,结果见表2。

续表2
2.6 各类化合物结构解析规律
2.6.1 酚酸类化合物的结构鉴定 本文从脉络宁注射液酯提废渣中鉴定了9个绿原酸类化合物。通过MS1图谱确定化合物5的准分子离子峰为m/z353.0866 [M-H]-,预测分子式为C16H18O9。MS2图谱中主要的碎片离子为m/z191.0551、179.0321、173.0448、161.0225、127.0384、93.0327,分别计算其元素组成为C7H11O6-、C9H7O4-、C7H9O5-、、C6H7O3-和C6H5O-。绿原酸准分子离子峰m/z353.0866脱去一分子咖啡酰基形成m/z191.0511或者脱去一分子奎宁酰基形成m/z179.0321,m/z179.0321再脱去一分子H2O形成m/z161.0225,m/z191.0511再脱去一分子H2O形成m/z173.0448,再脱去一分子HCOOH形成m/z127.0384或者脱去两分子H2O和一分子CO2形成m/z93.0327,与对照品比对后推断为绿原酸。其 MS2质谱和具体的质谱裂解行为见图3。

图3 绿原酸的二级质谱图和质谱裂解途径推断Fig 3 MS/MS spectra and MS fragmentation pathway deduction of chlorogenic acid
双取代酚酸类化合物,通过MS1图谱确定化合物13的准分子离子峰为m/z515.1165 [MH]-,预测分子式为C25H24O12。MS2图谱中主要的碎片离子为m/z353.0827、335.0734、191.0540、179.0323、173.0427、135.0426,分别计算其元素组成为C16H17O9-、C16H15O8-、C7H11O6-、、C7H9O5-、C8H7O2-。其中碎片离子m/z353.0827是由准分子离子峰m/z515.1165脱去一分子咖啡酰基(C9H6O3)形成,m/z335.0734是由碎片离子m/z353.0827脱去一分子H2O形成,m/z191.0540是由碎片离子m/z353.0827脱去一分子咖啡酰基(C9H6O3)形成的奎宁酸负离子,m/z179.0323是碎片离子m/z353.0827脱去一分子奎宁酰基(C7H10O5)形成的咖啡酸负离子,m/z173.0448是m/z191.0540脱去一分子H2O形成,m/z135.0426是由碎片离子m/z179.0323脱去一分子CO2形成,与对照品比对后推断为异绿原酸A。其MS2质谱和具体的质谱裂解行为见图4。
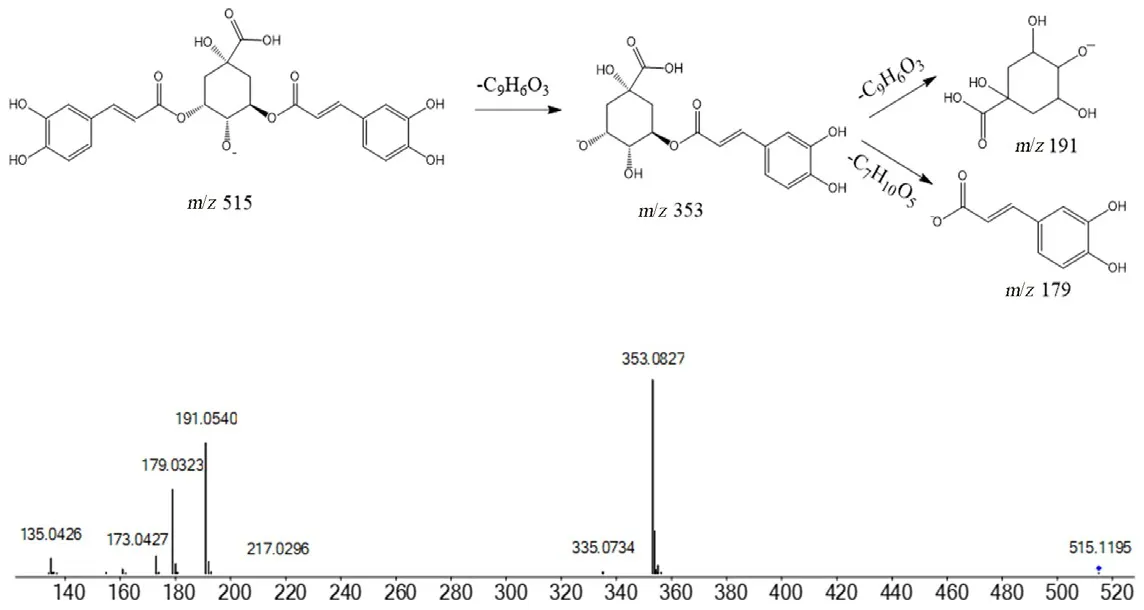
图4 异绿原酸A的二级质谱图和质谱裂解途径推断Fig 4 MS/MS spectra and MS fragmentation pathway deduction of isochlorogenic acid A
2.6.2 黄酮类化合物的结构鉴定 本文从脉络宁注射液酯提废渣中鉴定了9个黄酮类化合物。通过MS1图谱确定化合物19的准分子离子峰为m/z447.0908 [M-H]-,预测分子式为C21H20O11。MS2图谱中,主要的碎片离子为m/z285.0381,是由木犀草苷的准分子离子峰447.0908脱去一分子葡萄糖(C6H10O5)形成。与对照品比对后推断为木犀草苷。其MS2质谱和具体的质谱裂解行为见图5。
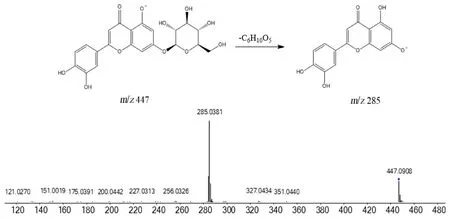
图5 木犀草苷的二级质谱图和质谱裂解途径推断Fig 5 MS/MS spectra and MS fragmentation pathway deduction of cynaroside
2.6.3 环烯醚萜苷类化合物的结构鉴定 本文从脉络宁注射液酯提废渣中鉴定了10个环烯醚萜苷类化合物。通过MS1图谱确定化合物8的准分子离子峰为m/z403.1249 [M-H]-,预测分子式为C17H24O11。MS2图谱中主要的碎片离子为m/z371.0926、223.0582、179.0660、165.0534、121.0270,分别计算其元素组成为C16H19O10-、C11H11O5-、C6H11O6-、C9H12O3-、C7H10O2-,其中碎片离子m/z371.0926是由准分子离子峰m/z403.1249脱去一分子CH3OH形成,碎片离子m/z223.0582是由准分子离子峰m/z403.1249脱去一分子葡萄糖(C6H12O6)形成,碎片离子m/z179.0660是脱去一分子葡萄糖形成的碎片离子,碎片离子m/z165.0534是由碎片离子m/z223.0582脱去COOCH2形成,碎片离子m/z165.0534脱去一分子CO2形成碎片离子m/z121.0270。与对照品比对后推断为断氧化马钱子苷。其MS2质谱和具体的质谱裂解行为见图6。

图6 断氧化马钱子苷的二级质谱图和质谱裂解途径推断Fig 6 MS/MS spectra and MS fragmentation pathway deduction of secoxyloganin
2.6.4 三萜皂苷类化合物的结构鉴定 本文从脉络宁注射液酯提废渣中鉴定了8个三萜皂苷类化合物。通过MS1图谱确定化合物35的准分子离子峰为m/z1397.6427 [M-H]-,预测分子式为C65H106O32。MS2图谱中主要的碎片离子为m/z1073.5338、911.4834,分别计算其元素组成为C53H85O22-、C47H75O17-,其中相对丰度最高的碎片离子m/z1073.5338是由准分子离子峰m/z1397.6427脱去两分子葡萄糖(C12H20O10)形成,m/z1073.5338脱去一分子鼠李糖形成碎片离子m/z911.4834。与对照品比对后推断为灰毡毛忍冬皂苷乙。其MS2质谱和具体的质谱裂解行为见图7。

图7 灰毡毛忍冬皂苷乙的二级质谱图和质谱裂解途径推断Fig 7 MS/MS spectra and MS fragmentation pathway deduction of macranthoidin B
2.6.5 苯丙素类化合物的结构鉴定 本文从脉络宁注射液酯提废渣中鉴定了5个苯丙素类化合物。通过MS1图谱确定化合物23的准分子离子峰为m/z783.2668 [M-H]-。MS2图谱中主要的碎片离子为m/z607.2151、461.1614、329.1203、175.0393,分别计算其元素组成为C26H39O16-、C20H29O12-、C15H21O8-、C10H7O3-。其中碎片离子m/z607.2151是分子离子峰脱去阿魏酰基(C10H8O3)所形成,m/z607.2151 脱去一分子鼠李糖基(C6H10O4)形成碎片离子m/z461.1614,碎片离子m/z329.1203是碎片离子m/z461.1614脱去C5H8O4形成,碎片离子m/z175.0393是碎片离子m/z329.1203脱去C5H14O5形成,其MS2质谱和具体的质谱裂解行为见图8。
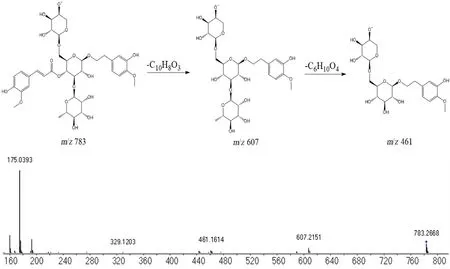
图8 安格洛苷C的二级质谱图和质谱裂解途径推断Fig 8 MS/MS spectra and MS fragmentation pathway deduction of angoroside C
2.6.6 联苄类化合物的结构鉴定 本文从脉络宁注射液酯提废渣中鉴定了1个联苄类化合物。通过MS1图谱确定化合物34的准分子离子峰为m/z303.1239 [M-H]-。MS2图谱中主要的碎片离子为m/z221.1564,分别计算其元素组成为C13H17O3-。其中碎片离子m/z221.1564是碎片离子m/z303.1239脱去C4H3O2形成,其MS2质谱和具体的质谱裂解行为见图9。
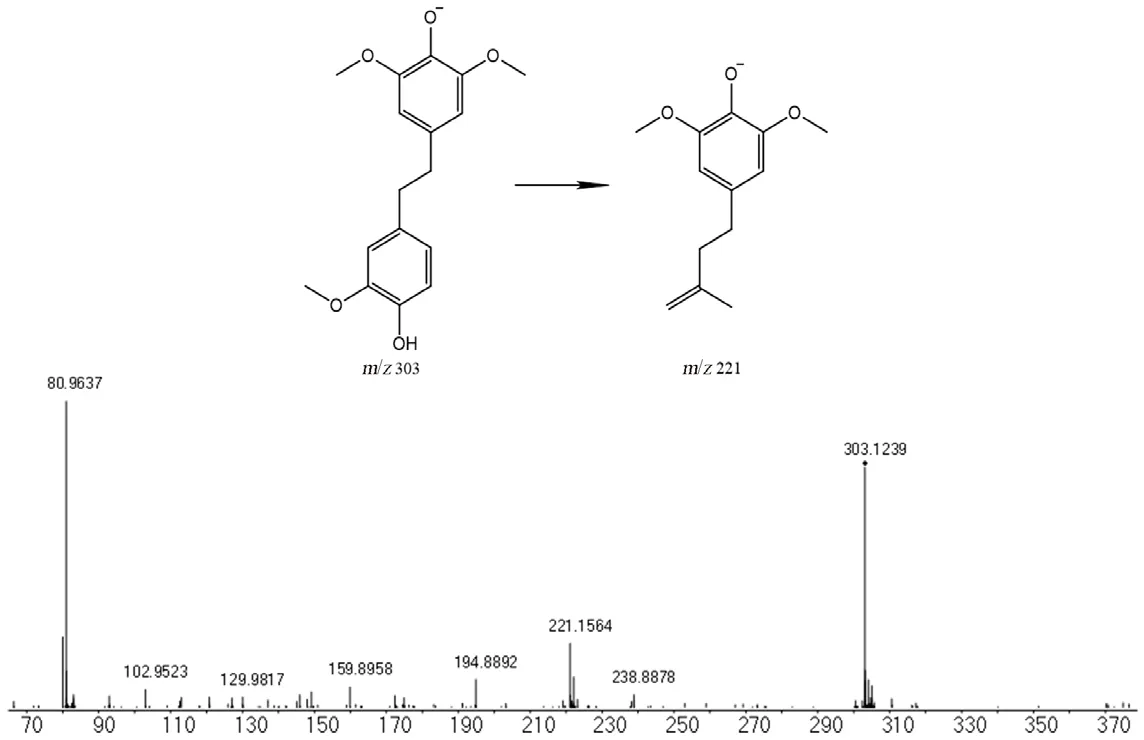
图9 杓唇石斛素的二级质谱图和质谱裂解途径推断Fig 9 MS/MS spectra and MS fragmentation pathway deduction of moscatilin
2.7 样品含量测定
取8批脉络宁注射液酯提废渣制备供试品溶液,对8 批脉络宁注射液酯提废渣大孔树脂富集液的5种有效成分进行含量测定,结果见表3。
3 讨论
本试验对大孔树脂富集(0%→10%→100%乙醇水溶液洗脱)脉络宁注射液酯提废渣化学成分的程度进行了考察,洗脱剂分别为0%→10%→50%→100%乙醇水溶液;0%→ 20%→50%→100%乙醇水溶液和0%→ 10%→ 60%/70%/80%/90%乙醇水溶液;经液相色谱结果分析,结果发现洗脱剂为0%→10%→90%乙醇水溶液梯度洗脱时,90%乙醇部位主要化学成分富集程度最大。
由脉络宁注射液酯提废渣鉴定结果表明,其中环烯醚萜苷类成分最多,推测脉络宁酯提废渣中可能含有较多的金银花和山银花原药材成分;含量测定结果显示,脉络宁注射液酯提废渣大孔树脂富集液中三萜皂苷类成分(灰毡毛忍冬皂苷甲和灰毡毛忍冬皂苷乙)的含量最高,其次为酚酸类成分(绿原酸、异绿原酸A、异绿原酸C),表明废渣中含有丰富的原药材活性成分,尤其是酚酸类和三萜皂苷类成分含量较高。
以往的中药废弃物的主要用途是作为有机肥料[19]、微生物发酵产物[20]、燃料和饲料添加剂,以及开发高附加值的资源产品[21]。该研究采用ASD-7大孔树脂柱富集方法和UHPLC-Q-TOFMS技术建立了脉络宁注射液酯提废渣大孔树脂富集液中化学成分的鉴定以及5种有效成分的含量测定方法,通过液相色谱的分离和质谱的检测,推断了脉络宁注射液酯提废渣的主要化学成分组成,并对其中酚酸类和三萜皂苷类成分进行含量测定,结果明确了多种中药材活性成分在废渣中的含量,首次实现了脉络宁注射液酯提废渣化学成分的鉴定和有效成分的含量测定,为脉络宁注射液酯提废渣后续再利用提供了科学依据。

