氨基化CdSe/ZnS量子点对克百威的高灵敏荧光测定*
崔 婧,耿春辉
(衡水市综合检验检测中心,河北 衡水 053000)
克百威,又名呋喃丹,是氨基甲酸酯类农药的一类,是一种广谱高效杀虫剂,广泛用于蔬菜、农作物的杀虫防虫中[1-2]。但是克百威可与亚硝酸盐反应生成有潜在致癌、致畸、致突变作用的亚硝胺;与胆碱酯酶结合后不可逆,因此毒性高。残留在蔬菜和农作物上的克百威进入人体可经消化道、呼吸道和皮肤被人吸收,吸收后主要分布于肝、肾、脂肪和肌肉中,会造成神经毒性,易产生流涎、流泪、瞳孔缩小等反应,严重的会出现血压下降、意识不清等症状。长期食用克百威超标的食品会对人体造成巨大的危害。另外,克百威在土壤中的半衰期为30~60天,不易降解,迁移性较大,易造成环境污染[3-5]。
针对克百威的检测方法主要有高效液相色谱法[6]、气相色谱法[7]、液相色谱—串联质谱法[8]、气相色谱—质谱法[9]、酶抑制法[10]等,这些方法具有检测限低、准确性好等优点,但存在因前期处理烦琐、所使用的仪器昂贵、需专人操作等特点,使快速简便的检测受到一定的限制。因此建立灵敏、简便、低成本的环境水体中氨基甲酸酯类农药残留快速检测方法对环境监测领域意义重大。
荧光光谱技术具有灵敏度高、操作简便、快速等优势,在有毒有害物质的检测中得到了广泛关注和应用[11-12]。荧光强度不仅受荧光物质的种类、结构的影响,还受溶剂种类、溶液酸碱度、离子等因素的影响。量子点是一种高效的荧光物质,因其尺寸可调,具有独特的光学和电学性能,受到研究人员的热捧。CdSe量子点具有高的能带宽,是一种成熟的半导体量子点,因其具有一定的毒性,在其表面覆盖高能带宽的ZnS壳层,形成核壳式结构,可有效降低毒性,改善量子点的发光效率和稳定性[13-14]。通常情况下,溶液中的量子点在保存时会聚集沉淀或被氧化使其荧光性能降低。因此对其进行一定的修饰有助于保持量子点原有的荧光效率。
荧光物质的分子结构包含正电荷取代基,如-OH、-NH2以及-OCH3等会改善荧光强度、溶解性及稳定性[15]。荧光强度的大小一定程度上取决于给电子取代基团的位置和数量,其数量愈多,发射的荧光更强。本文首先制备氨基修饰的CdSe/ZnS量子点,使其溶于水,以其为荧光探针,通过测试克百威对其荧光响应的影响实现对克百威的高灵敏检测。
1 实 验
1.1 仪器与试剂
AB5500超高效液相色谱-三重四极杆质谱仪、F-7000荧光光谱仪,日立;Talos F200X200kV场发射透射电子显微镜,赛默飞;烘箱,杭州标盾;超纯水仪,Millipore;圆周振荡器,IKA VORTEX 1;DK-S28恒温水浴锅,上海精宏;涡旋振荡器,IKA;离心机,上海安亭等。
克百威(99%,AR)、硒粉(99%,AR)、乙酸镉二水合物(99%,AR)、油酸钠,上海阿拉丁生化科技股份有限公司;巯基乙酰胺(98%,AR)、乙酸锌(98%,AR)、氢氧化钠(96%,AR)、无水磷酸二氢钠(99%,AR)、无水磷酸氢二钠(99%,AR),乙腈,无水硫酸镁(98%,AR)、氯化钠(99.8%,AR)、柠檬酸钠二水合物(99%,AR)、柠檬酸二钠盐倍半水合物(99%,AR),中国医药集团有限公司。所有试剂均为购买后直接使用。
实验所用水均为超纯水(电阻率为18.2 MΩ·cm)。
1.2 实验步骤
1.2.1 氨基化CdSe/ZnS量子点的制备
首先将1 mM乙酸镉二水合物、1.2 g油酸钠分散于10 mL乙醇,再将2 mL油酸、1 mmol硒粉加入到20 mL水中,将上述乙醇分散液和水分散液混合均匀,N2保护下于40 ℃加热2 h后转移至100 mL反应釜中,180 ℃下反应3 h,得到CdSe量子点。在N2氛围下向CdSe量子点溶液交替滴加1 mmol乙酸锌和1 mmol硫代乙酰胺溶液,同时剧烈搅拌,在100 ℃下反应2 h,离心并用水洗涤三次后于80 ℃真空烘箱中干燥,制得氨基修饰的CdSe/ZnS核壳结构量子点。将量子点重新分散于水中,得到1.0 mg/mL的量子点溶液,冷藏备用。
1.2.2 氨基化CdSe/ZnS量子点的表征
利用场发射透射电子显微镜对所制得的量子点进行尺寸、形貌分析。采用荧光光谱仪对所制备的量子点进行荧光响应分析。
1.2.3 溶液的配制
配制系列浓度(0.01、0.02、0.05、0.1、0.2、0.5、1.0 mg/mL)的量子点溶液用于荧光响应的确定。
配制含1.0 mol/L氢氧化钠溶液、1.0 mol/L盐酸溶液、1.0 mol/L磷酸氢二钠和磷酸二氢钠(PBS)缓冲液,备用。
配制系列浓度的克百威溶液。
1.2.4 测定条件
荧光光谱测定条件为:激发和发射的狭缝宽度:5 nm,PMT电压:500 V,扫描速率:1 200 nm/min,响应时值:0.002 s。
液相色谱-质谱联用测试条件(参照GB 23200.121-2021标准):
液相色谱:C18,2.1 mm(内径),长度100 mm,粒径1.8 μm,或相当者;流动相:A相为甲酸铵-甲酸水溶液(4∶4∶2),B相甲酸铵-甲酸甲醇溶液(4∶4∶3),梯度洗脱;流速:0.3 mL/min。
质谱测试条件:离子源类型:电喷雾离子源;扫描方式:正离子和氟负离子同时扫描;电喷雾电压:正离子5 500 V,负离子-4 500 V;离子源温度:350 ℃;雾化气:0.345 MPa;辅助加热气:0.345 MPa。
1.2.5 样品前处理
荧光分析:称取10 g蔬菜搅碎置于50 mL离心管中,加入10 mL超纯水,振荡1 min后8 000 r/min离心5 min,吸取上清液,向下层沉淀物再加入10 mL超纯水振荡后离心,重复以上操作三次,将上清液并入一个离心管中,备用。
液相色谱-质谱联用(LC-MS):依照GB 23200.121-2021标准,称取10 g蔬菜试样于50 mL离心管,加入10 mL乙腈,剧烈振荡1 min,加入4 g无水硫酸镁、1 g氯化钠、1 g柠檬酸钠二水合物、 0.5 g柠檬酸二钠盐倍半水合物,剧烈振荡1 min后4 200 r/min离心5 min。吸取上清液至内含除水剂和净化材料的塑料离心管中,4 200 r/min离心5 min,吸取上清液过0.45 μm微孔滤膜,待测。
2 结果与讨论
2.1 氨基化CdSe/ZnS量子点的表征
利用透射电镜对所制备的量子点进行表征,如图1(A)所示,所制备的量子点为核-壳式量子点,尺寸为15~40 nm。
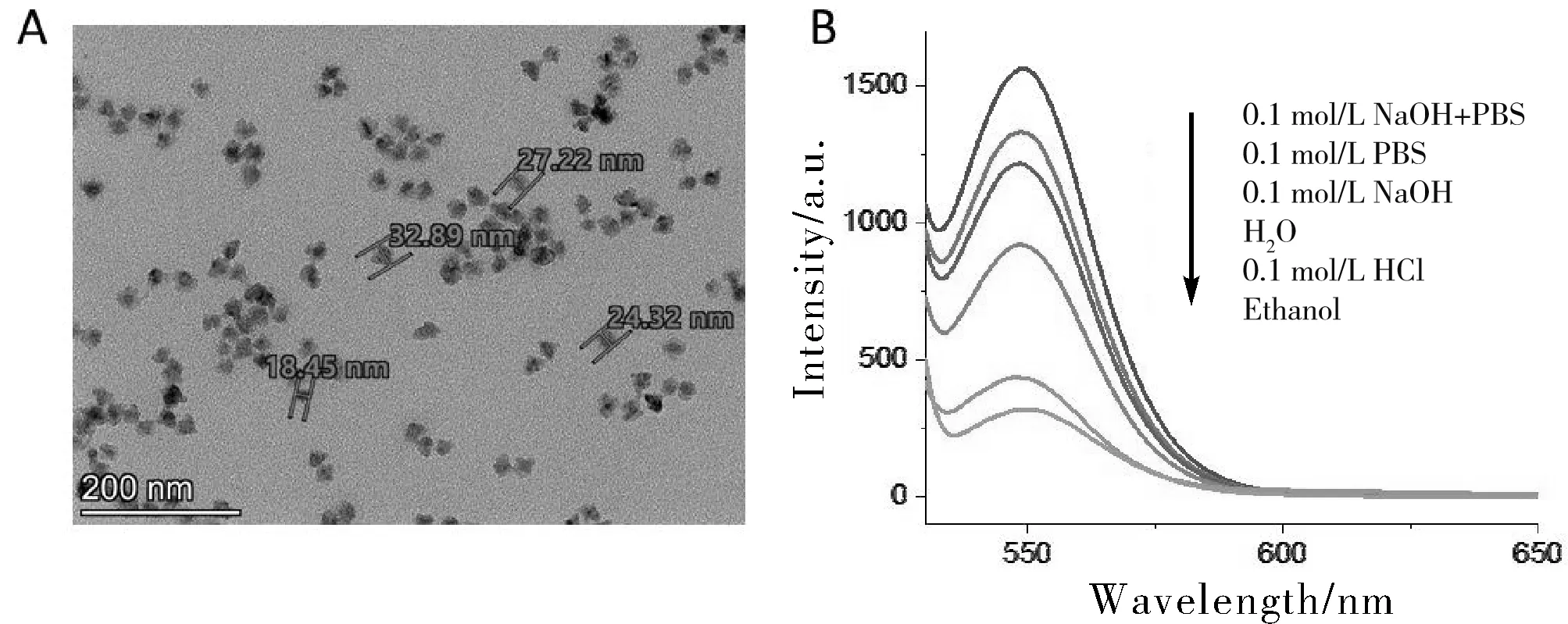
图1 0.1 mg/mL氨基化CdSe/ZnS量子点透射电镜图(A)和不同溶剂(水,0.1 mol/L氢氧化钠,0.1 mol/L盐酸,0.1 mol/L磷酸盐缓冲溶液,乙醇)中的荧光响应图(B)
采用荧光光谱仪对所制备的量子点进行荧光响应分析,最大激发波长为260 nm,最大发射波长为543 nm。
2.2 氨基化CdSe/ZnS量子点荧光测试的溶剂选择
为测试溶剂对量子点的荧光响应影响,将量子点溶于不同的溶剂(水、0.1 mol/氢氧化钠溶液、0.1 mol/L盐酸溶液、0.1 mol/L磷酸盐缓冲溶液、含0.1 mol/L氢氧化钠的磷酸盐缓冲溶液,乙醇)中,氨基化CdSe/ZnS量子点的荧光信号呈现明显的差异,如图2(B)所示,在碱性溶液和磷酸盐缓冲溶液中荧光相应较高,在盐酸溶液和乙醇中的响应最低。

图2 0.1 mg/mL氨基化CdSe/ZnS量子点在不同浓度(0.01 mol/L,0.02 mol/L,0.05 mol/L,0.1 mol/L,0.2 mol/L,0.5 mol/L,1.0 mol/L)的NaOH和PBS溶液中的荧光响应(A);10.0 mg/L克百威和0.1 mg/mL氨基化CdSe/ZnS量子点的荧光响应(B)

图3 克百威对氨基化CdSe/ZnS量子点的荧光淬灭时间
为确定氨基化CdSe/ZnS量子点的最佳溶剂及浓度,选取氢氧化钠溶液和PBS缓冲液作为溶剂进行进一步的荧光响应探索,以0.01、0.02、0.05、0.1、0.2、0.5、1.0 mol/L的氢氧化钠溶液和0.01、0.05、0.1、0.2、0.5、1.0 mol/L的PBS溶液分别作为氨基化CdSe/ZnS量子点的溶剂,并测定其荧光响应。如图2(A)所示,0.1 mol/L氢氧化钠溶液和0.1 mol/L的PBS溶液作为溶剂时量子点的荧光响应最大。因此本实验将以含有0.1 mol/L氢氧化钠溶液和0.1 mol/L的PBS混合溶液作为荧光测定的最佳溶剂。
2.2 氨基化CdSe/ZnS量子点对克百威的荧光测定
为探索克百威分子对量子点的影响,以含有0.1 mol/L氢氧化钠溶液和0.1 mol/L的PBS混合溶液为溶剂,配制10.0 mg/L的克百威溶液(溶液1)、0.1 mg/mL氨基化CdSe/ZnS量子点溶液(溶液2)、含有10.0 mg/L的克百威及0.1 mg/mL氨基化CdSe/ZnS量子点的混合溶液(溶液3),并进行荧光测定。结果如图2(B)所示,溶液1几乎没有荧光响应,溶液2具有较高的荧光响应,而溶液3响应降低,因此,可以推断克百威分子的加入对氨基化CdSe/ZnS量子点的荧光具有猝灭作用。
2.3 氨基化CdSe/ZnS量子点对克百威的荧光测定条件的选择
为探索克百威对量子点的荧光猝灭效果,以0.1 mg/mL氨基化CdSe/ZnS量子点为荧光探针,以10.0 mg/L的克百威为猝灭剂,测试以上溶液放置0 min,2 min,5 min,10 min,15 min,20 min后的荧光响应,结果发现10 min基本为最佳反应时间。
2.4 标准曲线及检出限
配制系列浓度的克百威(0,0.1,0.2,0.5,1.0,2.0,5.0,10.0,20.0,50.0,100.0 μg/L)及0.1 mg/mL氨基化CdSe/ZnS量子点混合标准工作溶液各10 mL,室温下静止10 min,分别取300 μL于石英比色皿中进行荧光测定。结果如图4显示,在0.1~100.0 μg/L的范围内荧光强度与克百威浓度的对数呈线性关系,线性方程为I=-340.8 lgC+21 720.0,相关系数为R2=0.99,检出限为0.06 μg/L(S/N=3)。

图4 氨基化CdSe/ZnS量子点对克百威荧光测定线性关系图
2.5 实际样品检测
对市售菠菜样品进行测定,未发现含有克百威残留。因此,为验证所构建的方法的适用性,对波菜样品进行加标:每9.9 mL前处理后的样品水溶液中加入100 μL的1.0 mg/mL,将该溶液稀释使其含有的克百威浓度大约0.5,5.0,20.0 μg/L,以量子点为探针进行荧光检测。结果如表1所示,加标后的菠菜样品溶液通过以荧光测定,回收率在91.6%~100.1%之间。
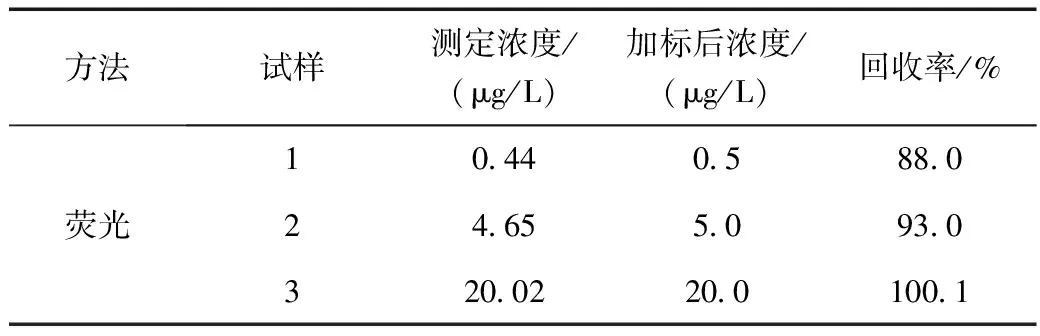
表1 NH2-CdSe/ZnS QDs 荧光法和LC-MS法测定波菜中克百威的浓度
2.6 LC-MS检测
LC-MS是针对克百威等农药残留的常用检测方法之一,此方法检测的保留时间为3.73 min(图5),定量限为10.0 μg/L。
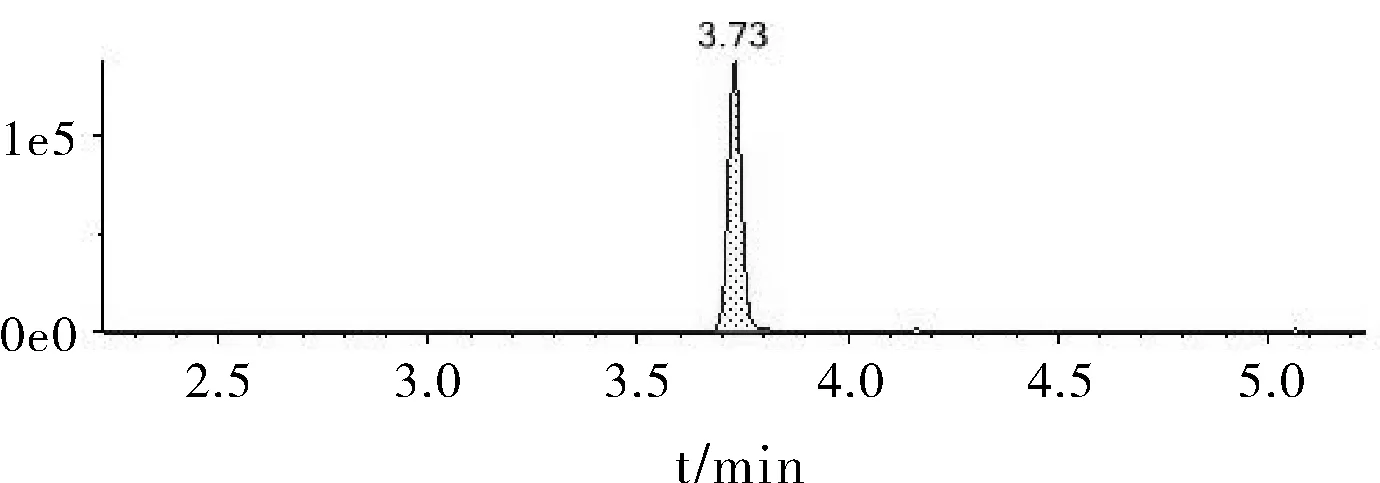
图5 LC-MS检测克百威的谱图
3 结 论
首先制备了一种氨基化的CdSe/ZnS量子点,并通过透射电镜进行了形貌表征。荧光测试发现该量子点在543 nm处有最大发射。将该量子点用于克百威的测定,结果显示克百威对其荧光信号有猝灭作用。在最佳条件下(0.1 mol/L氢氧化钠和PBS溶液为溶剂,10分钟为猝灭时间),量子点的荧光强度随着克百威浓度的增大而降低,与其对数值呈线性关系。该方法的准确性可以与常规的LC-MS方法媲美,具有更低的检测限。实验对蔬菜样品加标后进行测试,回收率较高,结果令人满意。

