超声造影下以实时连续微血管叠合方法重建乳腺肿瘤血管
徐冰荷,曾 琪,韦立丽,梁子轩 ,黄 真,韦长元,杨伟萍*
(1.广西医科大学肿瘤医学院,广西 南宁 530000;2.广西医科大学附属肿瘤医院超声科,3.乳腺外科,广西 南宁 530000)
乳腺恶性肿瘤血管丰富程度及超微血管构筑均与良性肿瘤存在显著差异[1-3]。CDFI、超声造影(contrast-enhanced ultrasound, CEUS)、超微血管成像(superb microvascular imaging, SMI)及微血管成像(micro flow imaging, MFI)等均可用于观察肿瘤血管,但对于观察立体血管构筑存在一定局限性。本研究观察CEUS下以实时连续微血管叠合方法重建乳腺肿瘤血管的价值。
1 资料与方法
1.1 研究对象 回顾性分析2019年1月—2022年12月广西医科大学附属肿瘤医院545例乳腺肿瘤患者,均为女性,年龄13~85岁,平均(49.7±11.6)岁;共555个乳腺肿瘤,包括恶性409个、良性146个(表1)。纳入标准:①超声检查前未接受乳腺肿瘤穿刺活检及手术、放射、化学治疗等相关治疗;②CEUS后经肿瘤穿刺活检或手术病理明确诊断;③于CEUS下以实时连续微血管叠合检查完整扫描乳腺肿瘤,且数据完整。本研究经院医学伦理委员会批准(LW2023091)。
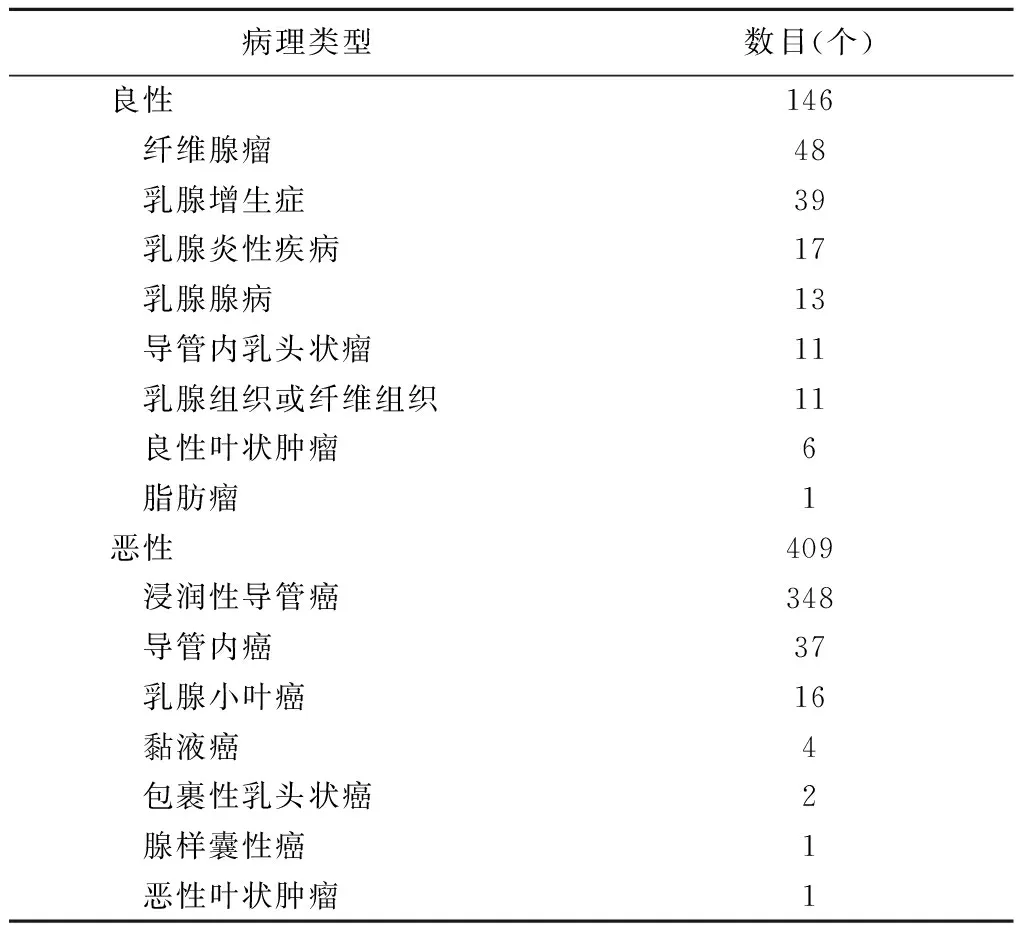
表1 545例共555个乳腺肿瘤病理类型
1.2 仪器与方法 采用Toshiba Aplio 500彩色多普勒超声诊断仪、频率5~14 MHz线阵探头,设置机械指数为0.04。嘱患者仰卧,先以常规超声扫查双侧乳腺;于CEUS模式下选取肿瘤血流较丰富切面或最大切面,切换为常规对比谐波成像(contrast harmonic imaging, CHI),经肘静脉团注声维诺(Bracco)4.8 ml及0.9%氯化钠注射液5 ml,于注入开始1 min后行血管重建同时录制视频:于CHI模式下依次启动SMI、MFI,即CHI+SMI+MFI,于肿瘤一侧开始依次缓慢扫查整个肿瘤,并以实时连续叠合肿瘤内微血管方法重建肿瘤血管,包括供血动脉及肿瘤内血管,同时观察肿瘤血管特征,即有无穿入血管、血流分级、血管主干与分支关系、血管走行及超微血管构筑等。
1.3 图像分析 由2名具有5年以上乳腺CEUS诊断经验的超声科医师分别观察肿瘤血管特征。穿入血管指自肿瘤边缘延伸至肿瘤内部并先于肿瘤实质增强的血管。参考Alder半定量血流分级法[4]进行血流分级:0级为病灶内未见血流;Ⅰ级为少量血流,病灶内可见1~2个点状或短棒状血流信号;Ⅱ级为中量血流,病灶内可见3~4个点状血流或1条长度接近/超过肿瘤半径的血管;Ⅲ级为丰富血流,可见5个及以上点状血流或2条较长血管;以0~Ⅰ级为不丰富型,Ⅱ~Ⅲ级为丰富型。评估血管主干与分支的关系:以目测法观察穿入血管与其分支血管形成的夹角,(90±5)°为直角,否则为非直角。血管走行:观察血管在肿瘤内的走向,以多支血管向肿瘤内任意一点汇聚为“有中心”,否则为“无中心”。超微血管构筑:参考文献[1],将肿瘤内部超微血管构筑分为无血管型(肿瘤内未探及血管)、线型(肿瘤内可见1~2条线样血流信号)、树枝型(肿瘤内可见粗细均匀的血管发出分支,形似树枝)、残根型(肿瘤内血管扭曲无序,周边增粗扭曲的血管不超过2条)或蟹足型(肿瘤内血管扭曲无序,周边增粗扭曲的血管大于2条或呈细小毛刺状);以残根型或蟹足型为恶性、其余为良性征象。
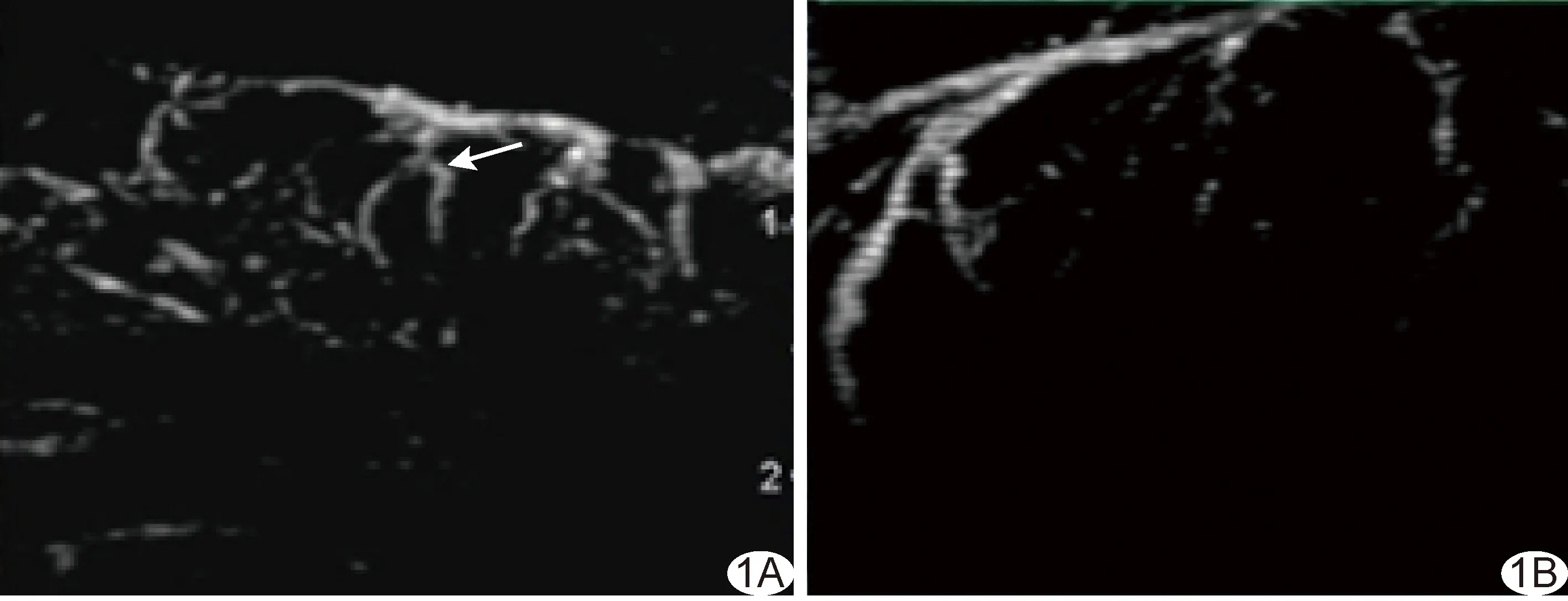
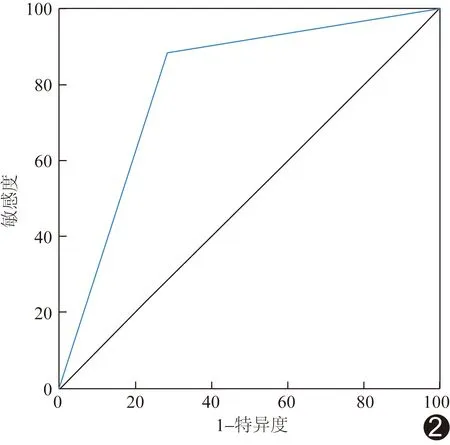
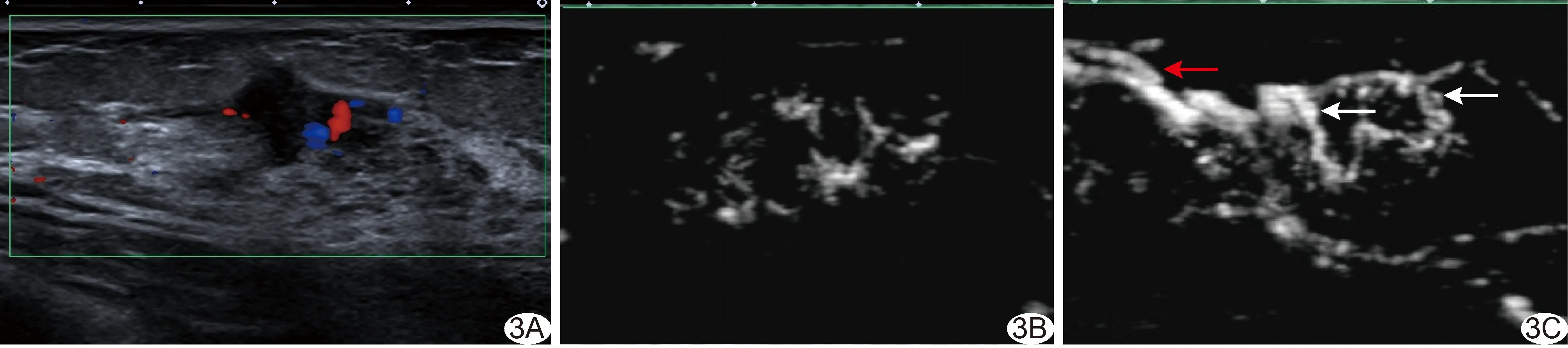
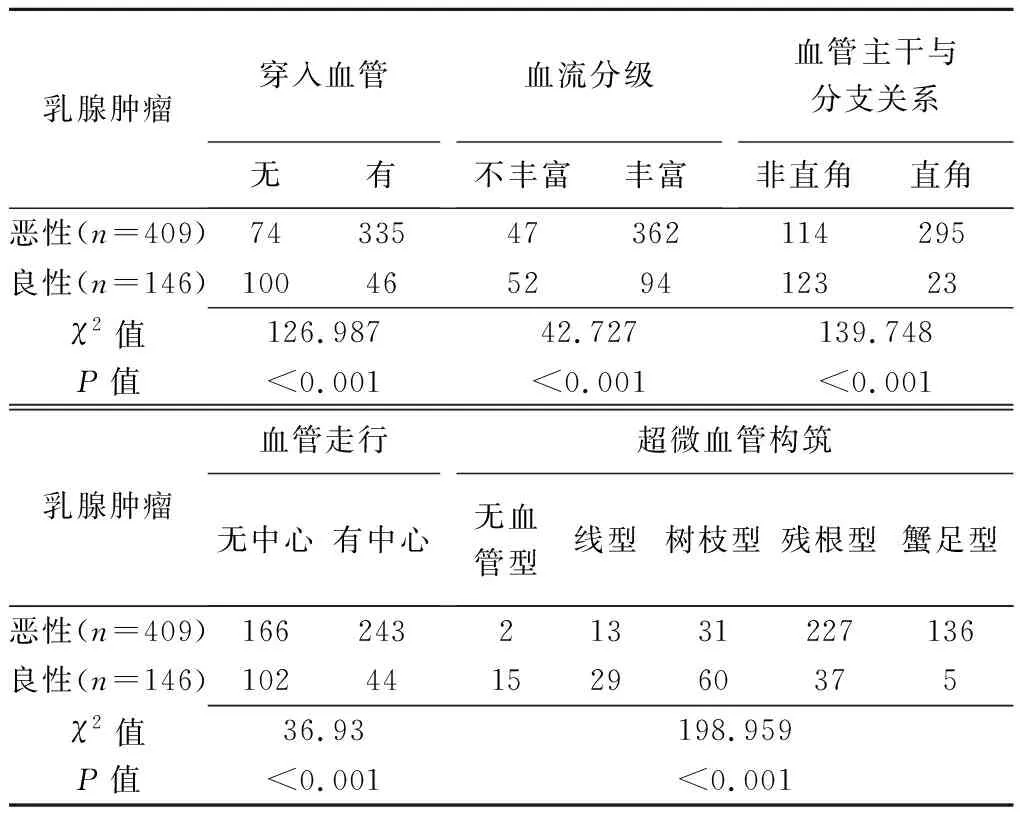
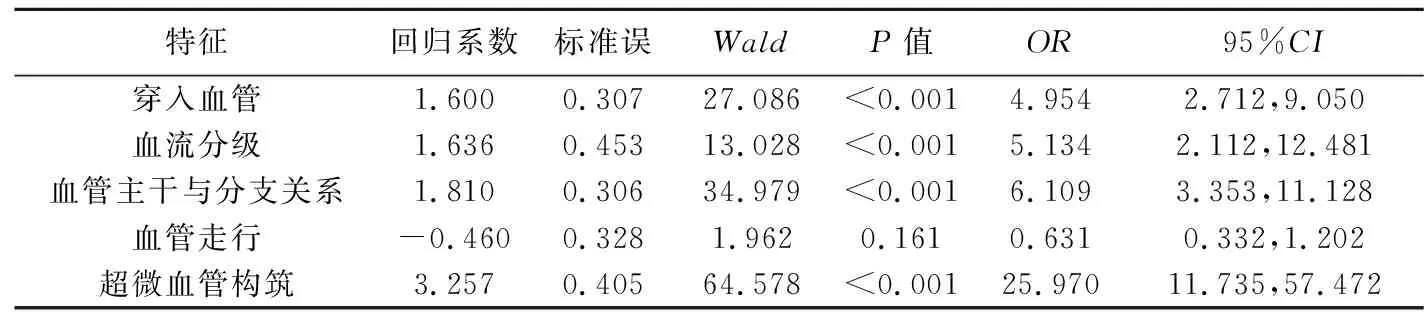
1.4 统计学分析 采用SPSS 26.0统计分析软件。以χ2检验或Fisher精确概率法比较计数资料。对乳腺肿瘤血管特征行单因素及多因素logistic回归分析,筛选恶性肿瘤的独立危险因素(P<0.001)。采用Medcale 20.022绘制受试者工作特征(receiver operating characteristic, ROC)曲线,计算曲线下面积(area under the curve, AUC),评估超微血管构筑判断肿瘤性质的价值。以Kappa检验评估观察者间一致性:Kappa≥0.75为一致性好,0.40 2.1 超声所见 555个乳腺肿瘤中,381个(381/555,68.65%)超声可见穿入血管,包括良性46个、恶性肿瘤335个。乳腺恶性肿瘤中,血流分级丰富、血管主干与分支呈直角及血管走行有中心者占比分别为88.51%(362/409)、72.13%(295/409)及59.41%(243/409),良性肿瘤中占比分别为64.38%(94/146)、15.75%(23/146)及30.14%(44/146)。 肿瘤内超微血管构筑显示405个恶性肿瘤(病理结果为363个恶性、42个良性)和150个良性肿瘤(病理结果为46个恶性、104个良性),见图1;其鉴别乳腺良、恶性肿瘤的敏感度、特异度、准确率及AUC分别为88.75%、71.23%、84.14%及0.80,见图2。 图1 CEUS下微血管叠合重建乳腺肿瘤血管图 A.患者女,53岁,左侧乳腺浸润性导管癌,穿入血管位于肿瘤外并向肿瘤内部发出丰富分支并与血管主干呈直角(箭),超微血管构筑为蟹足型; B.患者女,34岁,右侧乳腺增生,穿入血管环绕于肿瘤周边,向肿瘤内部发出的分支较少且与血管主干夹角为非直角,超微血管构筑为树枝型 图2 超微血管构筑鉴别乳腺良、恶性肿瘤的ROC曲线 2.2 单因素及多因素分析 乳腺良、恶性肿瘤之间,穿入血管、血流分级、血管主干与分支的关系、血管走行及超微血管构筑差异均有统计学意义(P均<0.001),见表2及图3;其中,穿入血管、血流分级、血管主干与分支关系及超微血管构筑为乳腺恶性肿瘤的独立危险因素(P均<0.001),见表3。 图3 患者女,52岁,左侧乳腺浸润性导管癌 A.CDFI示肿瘤内Ⅱ级血流信号; B.CHI+SMI+MFI下肿瘤血供较丰富,断面成像示肿瘤血管粗细不均、分布不规则; C.CEUS下微血管叠合血管重建图示肿瘤穿入血管(红箭)紧贴肿瘤边缘,可见多支新生分支血管与血管主干形成直角(白箭),血管走行有中心,超微血管构筑为残根型 表2 555个乳腺肿瘤血管超声特征(个) 表3 乳腺恶性肿瘤独立危险因素的多因素分析 2.3 一致性分析 观察者间观察肿瘤血管各项特征结果的一致性均好(Kappa均>0.75,P均<0.001)。 新生肿瘤血管是乳腺肿瘤的重要病理特征。超声观察乳腺肿瘤血管特征多限于肿瘤内部超微血管构筑,仅能反映肿瘤新生血管状态。本研究联合超声血流成像技术及实时连续微血管叠合立体重建乳腺肿瘤血管,观察供血动脉与肿瘤的关系及其血管分布特征。 乳腺良、恶性肿瘤之间穿入血管分布存在明显差异,动脉供血方式亦明显不同[5]。本研究共于555个乳腺肿瘤中检出381条穿入血管,占比为68.65%,与刁雪红等[6]的结果相近,提示利用本研究方法可较好地显示乳腺肿瘤穿入血管。既往研究[1-2]显示,乳腺肿瘤超微血管构筑对鉴别其良、恶性具有较佳效能。本研究以CEUS下实时连续微血管叠合血管重建方法获得的超微血管构筑分型用于鉴别乳腺良、恶性肿瘤的敏感度、特异度、准确率及AUC分别为88.75%、71.23%、84.14%及0.80。 SMI可提高对低速血流信号的检出率,CHI能通过对比增强更敏感地显示肿瘤内部微血管,MFI则可根据叠加微泡运动轨迹实时反映造影剂在肿瘤内的动态分布过程、进而清晰显示肿瘤内及其周边血管走行及分布;CHI+SMI+MFI三者联合可更准确地反映乳腺肿瘤血管形态学特征[7]。本研究在CHI+SMI+MFI基础上录制连续扫查整个乳腺肿瘤的视频,对造影剂在肿瘤内的运动轨迹进行依次叠加,以快速、简便地重建乳腺肿瘤内、外血管,获取肿瘤血管立体分布构筑。乳腺良、恶性肿瘤之间,血管数目及形态特征存在差异[8-9]。有学者[10-11]提出,相比乳腺良性肿瘤,恶性肿瘤内部血管粗细更不均、分布更不规则。本研究血管重建图显示,乳腺恶性肿瘤呈现穿入血管数目多、走行扭曲,呈多分支、多直角、有中心等特点,且单因素及多因素分析显示穿入血管、血流分级、血管主干与分支的关系及超微血管构筑均为乳腺恶性肿瘤的独立危险因素。上述结果表明,本研究血管重建方法可在直观显示肿瘤内部超微血管构筑的同时较好地描述肿瘤穿入血管与分支分布特点,以弥补传统二维超声仅能显示某一切面血管形态的局限性。 综上所述,CEUS下实时连续微血管叠合方法可用于乳腺肿瘤血管重建并具有较好临床应用前景。但本研究良、恶性肿瘤样本量相差较大,且未与其他血流成像技术进行对比,有待进一步研究。2 结果
3 讨论

