分类释疑近5年高考试题情境中的“催化剂”
陈丽娟 刘 帅 郭依婷
(广东东莞市万江中学)
催化剂在众多化学化工领域中扮演着至关重要的角色.2021年诺贝尔化学奖被授予“不对称有机催化”领域,催化剂情境下的高考试题成为热点,近3年全国高考试卷多道试题中涉及催化剂相关知识.高考试题既考查催化剂必备知识,又考查基于深度理解解决真实情境下的综合性问题的能力.本文通过整理近5年催化剂情境下的高考试题,以4类题型重构对催化剂的系统认识,以提高催化剂专题的复习效率.
1 题型分类释疑
1.1 催化机理循环(流程图)
近5年高考试卷中多次考查了催化循环(如图1)或流程图(如图2),主要设问包括判断反应物、生成物、催化剂、中间体、化学键断裂与生成、化合价升降、化学反应方程式是否合理等.解决此类问题的关键在于深度理解每一步反应的断键和成键机理以及电子转移的方向和数目等.

图1

图2
例1(2023年湖南卷)N2H4是一种强还原性的高能物质,在航天、能源等领域有广泛应用.我国科学家合成的某Ru(Ⅱ)催化剂(用[L-Ru—NH3]+表示)能高效电催化氧化NH3合成N2H4,其反应机理如图1所示.下列说法错误的是( ).
A.Ru(Ⅱ)被氧化至Ru(Ⅲ)后,配体NH3失去质子能力增强
B.M 中Ru的化合价为+3
C.该过程有非极性键的形成
D.该过程的总反应式:
例2(2023年全国新课标卷)“肼合成酶”以其中的Fe2+配合物为催化中心,可将NH2OH 与NH3转化为肼(NH2NH2),其反应历程如图2 所示.下列说法错误的是( ).
A.NH2OH、NH3和H2O 均为极性分子
B.反应涉及N—H、N—O 键断裂和N—N 键生成
C.催化中心的Fe2+被氧化为Fe3+,后又被还原为Fe2+
D.将 NH2OH替换为 ND2OD,反应可得ND2ND2
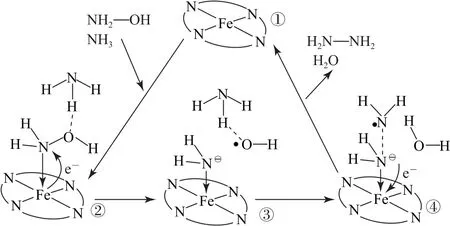
图3
由图3可知,反应①→②过程中NH2OH 中的氮原子与催化中心Fe2+形成配位键后,催化中心Fe2+失去电子被氧化成Fe3+;反应②→③过程中,NH2OH 中的氮原子得到电子形成—1价离子,N—O键均裂形成自由基;羟基自由基与氨气发生自由基反应(N—H 键断裂),生成H2O;反应③→④过程中,氮负离子与氨基自由基形成N—N 键,同时将电子转移至催化中心,Fe3+被还原为Fe2+,选项B和C 说法正确.理解断键机理,若将NH2OH 替换为ND2OD,·NH2将取代·OD,最终生成ND2NH2和HDO,选项D 说法错误.答案为D.
1.2 催化实验数据表/图
近5年高考试卷中多次考查了真实情境中的实验数据或现象分析.催化剂问题必备知识包括催化剂具有选择性,能通过降低该反应的活化能,加快反应速率,提高转化率及相关产物的比例;催化剂不能改变平衡转化率.试题综合可逆反应的平衡移动、转化率、平衡转化率等相关问题,通过深度理解化学反应原理,解决应用性或创新性问题.
例3(2023年1月浙江卷,节选)“碳达峰”“碳中和”是我国社会发展重大战略之一,CH4还原CO2是实现“双碳”经济的有效途径之一,相关的主要反应有
Ⅰ:CO2(g)+CH4(g)⇌2CO(g)+2H2(g)ΔH1=+247kJ·mol—1,K1.
Ⅱ:CO2(g)+H2(g)⇌CO(g)+H2O(g)ΔH2=+41kJ·mol—1,K2.
CH4还原能力(R)可衡量CO2转化效率,R=Δn(CO2)/Δn(CH4)(同一时段内CO2与CH4的物质的量变化量之比).催化剂X 可提高R值,另一时段内CH4的转化率和R值随温度变化情况如表1所示.
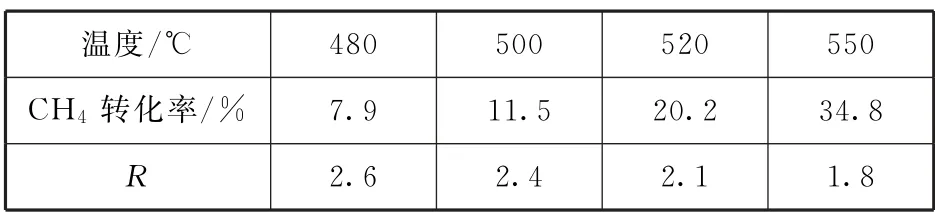
表1
下列说法不正确的是_________(填字母).
A.R值提高是由于催化剂X 选择性地提高反应Ⅱ的速率
B.温度越低,含氢产物中H2O 占比越高
C.温度升高,CH4的转化率增加,CO2的转化率降低,R值减小
D.改变催化剂提高CH4的转化率,R值不一定增大
利用催化剂选择性加快反应Ⅱ的速率,使同一时段内ΔnⅡ(CO2)>ΔnⅠ(CO2),可以提高R值,选项A 说法正确.由表1可知,在一定范围内降低温度,反应Ⅰ和Ⅱ的速率均降低,因此CH4转化率降低;R值增大是由于降温使反应Ⅰ速率降低得更多,同一时段内ΔnⅡ(CO2)>ΔnⅠ(CO2),即含氢产物中H2O 占比高,选项B说法正确.同理,因为反应Ⅰ和Ⅱ都是吸热反应,所以在一定范围内温度升高,反应Ⅰ和Ⅱ的速率均提高,CH4和CO2转化率均提高;R值减小是由于升温使反应Ⅰ速率提高得更多,同一时段内ΔnⅡ(CO2)<ΔnⅠ(CO2),选项C说法不正确.若改变催化剂提高CH4转化率,即催化剂选择性提高反应Ⅰ的速率,则同一时段内ΔnⅡ(CO2)<ΔnⅠ(CO2),R值减小,选项D 说法正确.答案为C.
1.3 能量—反应进程图
近5年高考试卷中多次考查了能量—反应进程图(历程图).催化剂问题必备知识包括催化剂能降低活化能,加快反应速率,使反应更容易进行;催化剂能改变反应路径,催化进程分步进行,但不影响始末状态的相对能量.理解活化能、反应历程、基元反应、决速步骤、竞争反应等概念成为解决问题的关键.
例4(2021 年河北卷,节选)在电解质水溶液中,3种不同催化剂(a、b、c)上CO2电还原为CO 的反应进程中(H+被还原为H2的反应可同时发生),相对能量变化如图4、图5所示.由此判断,CO2电还原为CO 从易到难的顺序为_________(用a、b、c字母排序).

图4 CO2 电还原为CO

图5 H+电还原为H2
1.4 催化表面微观机理图
近5年高考试卷中多次考查了催化反应微观机理图,主要考查学生宏观辨识与微观探析的化学素养,准确获取微观图例信息的能力;通过理解催化剂吸附原理,利用电负性描述断键机理,判断催化中心元素化合价变化等.
例5(2022年辽宁卷,节选)工业合成氨是人类科学技术的一项重大突破,目前已有三位科学家因其获得诺贝尔奖,其反应为
针对反应速率与平衡产率的矛盾,我国科学家提出了解决方案:双温—双控—双催化剂.使用Fe-TiO2—xHy双催化剂,通过光辐射产生温差(如体系温度为495℃时,Fe的温度为547℃,而TiO2—xHy的温度为415 ℃),如图6所示.
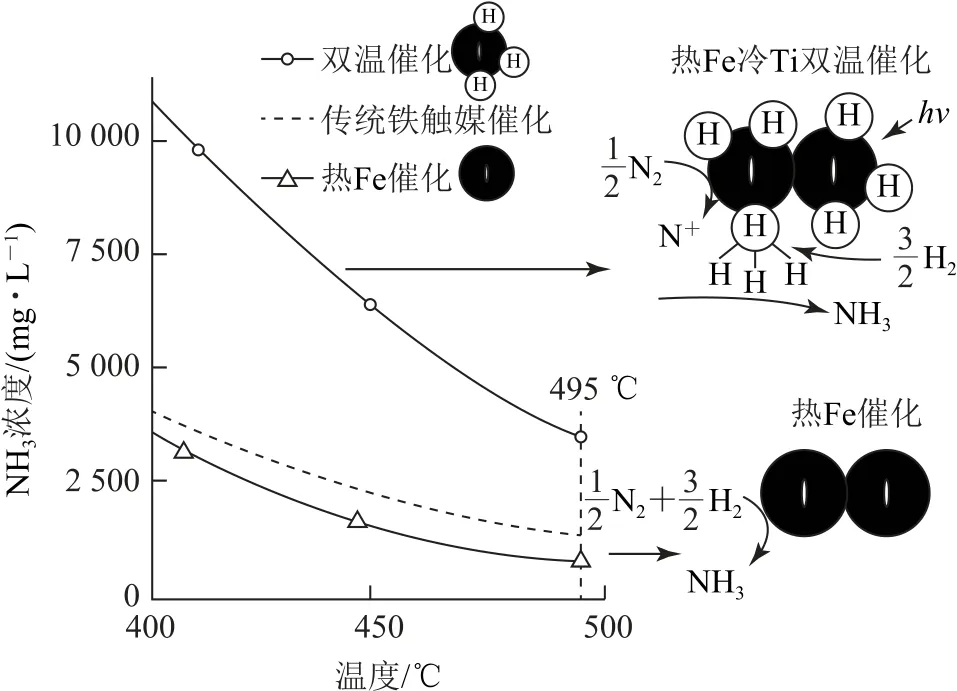
图6
下列说法正确的是( ).
A.氨气在“冷Ti”表面生成,有利于提高氨的平衡产率
B.N≡N 在“热Fe”表面断裂,有利于提高合成氨反应速率
C.“热Fe”高于体系温度,有利于提高氨的平衡产率
D.“冷Ti”低于体系温度,有利于提高合成氨反应速率
2 催化剂专题备考策略
教材简要介绍了催化剂的概念、催化剂的活性、催化反应的选择性以及其改变活化能、改变反应速率、不影响平衡移动的结论.然而,催化剂相关高考试题多嵌于真实情境中,体现了高考试题的综合性、应用性和创新性要求.教学实践中发现,部分学生具有较强的教材知识再现能力,但由于缺乏学科理解的评析能力,故对于真实问题情境下的迁移性问题常感到无所适从.因此,相互兼顾、协调统一新授课与复习课的关系是高中化学专题备考的基本策略.高一和高二适度拓展催化剂陈述性知识,减少“口诀套用”的机械训练.多维度表征化学相关名词、原理或问题的来龙去脉,可以帮助学生形成认识化学新世界的大概念视角.新授课适度增加基于预测的认识过程,帮助学生从更多维度理解概念,让学生能有机会调用必备知识,迁移至真实情境,评价科学问题,有利于大脑“实现最佳学习”.
重整概念、深化理解的主题式高考试题分类释疑是专题备考的基本策略.分类释疑应注重总结同类问题中的必备知识,体会不同类问题中的关键能力,显化需要迁移的知识内容、试题的表现形式和答题的基本模式,体会高考评价体系背景下的考查内容和要求.掌握催化剂相关问题的来龙去脉,才能调用“旧知识”,迁移“真情境”,不怕“新题型”.
(完)

