增容剂马来酸酐接枝聚丙烯接枝率的酸碱反滴定法测定误差分析
李 朝,贾元山
(1. 西安工业大学材料与化工学院,西安 710021;2. 西安新思路橡塑材料有限公司,西安 710025)
0 前言
聚丙烯(PP)是综合性能优异的通用塑料,易于纺丝、注射和挤出成型加工成编织、零件、管和薄膜等制品。近几年国内聚丙烯的生产、应用增长迅速[1-3]。为扩大PP的应用领域,增容剂PP-g-MAH常用于增加PP的极性,以改善PP与极性聚合物相容性、与无机物和金属的粘接性、PP的染色印刷性及润湿性[4-6]。PP-g-MAH的接枝率是其改性性能的重要指标,因此,接枝率测定是PP-g-MAH研究和制备过程中的一个重要环节。
PP-g-MAH 接枝率测定最常用的是酸碱滴定法和红外分光光度法[7-19],因酸碱滴定法简便易行,在实验及实际生产中较多采用,但酸碱滴定测定有较大的误差,再现性差[20]。为提高酸碱滴定法的测定精度,研究人员对测定方法、样品取样量、标准滴定碱溶液浓度、有机溶剂种类、指示剂、滴定温度等参数对测定结果的影响进行了研究[15,21-23],但未见对PP-g-MAH 酸碱反滴定法测定接枝率进行误差分析的报道。
本文以误差传递公式为基础,建立酸碱反滴定法测定接枝率的误差模型,分析样品取样量、HCl-异丙醇滴定溶液浓度和PP-g-MAH 接枝马来酸酐含量等因素对接枝率测定误差的影响。以熔融法制备PP-g-MAH,酸碱反滴定法测定样品的接枝率,优化测试条件。
1 实验部分
1.1 主要原料
PP,T30S,陕西延长石油(集团)有限责任公司延安石油化工厂;
马来酸酐(MAH)、过氧化苯甲酰(BPO),化学纯,国药集团化学试剂有限公司;
抗氧剂1010,化学纯,成都格雷西亚化学技术有限公司;
二甲苯、异丙醇、氢氧化钾、浓盐酸、无水乙醇、酚酞、溴甲酚绿、甲基红、丙酮、邻苯二甲酸氢钾、无水碳酸钠,分析纯,天津大茂化学试剂厂。
1.2 主要设备及仪器
反应混合压制模,自制;
酸碱滴定管,50 mL,扬州市葵花玻璃仪器厂;
电子天平,FA2004,上海舜宇恒平科学仪器有限公司;
傅立叶变换红外光谱分析仪(FTIR),iS50,美国赛默飞世尔科技公司。
1.3 样品制备
PP-g-MAH 的制备与纯化:将PP 制成薄片,根据PP 薄片质量按比例分别称取MAH、BPO、抗氧剂1010,用丙酮、乙醇配制成溶液;将PP 薄片浸于所制溶液中,溶剂挥发后MAH、BPO 和抗氧剂1010 均匀分散于PP 表面,再将PP 薄片置于反应混合压制模中,加热熔融接枝反应制得接枝物PP-g-MAH[24];
称取3 g 接枝物,于150 mL 二甲苯中加热溶解,再将热溶液立刻倒入未加热的同样体积的丙酮中,通过沉析、过滤以及干燥等处理,以丙酮为溶剂在索氏抽提器将滤饼抽提处理10 h,提取物在120 ℃下进行真空干燥至恒重,冷却得纯化接枝物。
1.4 性能测试与结构表征
FTIR分析:取一定量的纯化接枝物,在190 ℃下压制成厚度为50~100 μm 的薄膜,120 ℃真空干燥24 h,分辨率为4 cm-1,扫描次数为32,扫描范围为4 000~400 cm-1,得到样品的FTIR曲线;
酸碱标准滴定溶液的配制和标定:KOH-乙醇标准滴定溶液的配制,根据GB/T 601—2016,用KOH 和无水乙醇配制浓度为0.01、0.04、0.07、0.10 mol/L 的KOH-乙醇溶液,使用酚酞指示液,以邻苯二甲酸氢钾为基准试剂标定KOH-乙醇标准溶液;
HCl-异丙醇标准滴定溶液的配制,根据GB/T 601—2016,用浓盐酸和异丙醇配制浓度为0.01、 0.04、0.07、 0.10 mol/L 的HCl-异丙醇溶液,以溴甲酚绿-甲基红为混合指示剂,无水碳酸钠为基准试剂标定HCl-异丙醇标准溶液;
酸碱反滴定法测定接枝率:分别称取0.20、0.35、0.50、0.65 g 纯化接枝物置于锥形瓶中,加入70 mL 二甲苯,加热回流30 min 使接枝物完全溶解,冷却后用移液管加入过量的KOH-乙醇标准溶液,加热至回流,反应2 h 使接枝的马来酸酐与碱完全反应,溶液冷却至乙醇沸点以下,加3 滴酚酞指示液;在滴定过程中溶液温度不断降低,PP-g-MAH 的沉析现象也随之加重,为减小温度变化对滴定结果的影响,本实验将锥形瓶置于60°C 水浴中,保持滴定过程处于恒温状态;使用与加入的KOH-乙醇溶液浓度相同或接近的HCl-异丙醇溶液,滴定至溶液呈粉红色并保持30 s,即为滴定终点;同时进行空白试验,在锥形瓶中加入70 mL 的二甲苯,再用移液管加入相同体积的KOH-乙醇标准溶液,按相同方法以HCl-异丙醇滴定至终点;接枝率计算公式如式(1)所示:
式中G——PP-g-MAH上接枝的MAH质量百分数,%
c1——盐酸-异丙醇标准滴定溶液浓度,mol/L
c2——氢氧化钾-乙醇标准滴定溶液浓度,mol/L
V0——空白试验消耗盐酸-异丙醇标准滴定溶液体积,L
V1——反滴定消耗盐酸-异丙醇标准滴定溶液体积,L
V2——氢氧化钾-乙醇标准溶液体积,L
m——纯化接枝物样品质量,g
M0——马来酸酐摩尔质量,98.06,g/mol
式(1)等号左边分式中,分子第1 项与第3 项可消去,简化得式(2):
保持相同的测试及操作条件进行3次平行测定,按式(2)计算接枝率,同时计算接枝率的相对标准偏差。
2 酸碱反滴定法测定接枝率误差模型的建立及误差分析
由于酸碱滴定法测定PP-g-MAH 接枝率精度低,因而接枝率的准确度难以保证。为降低总体误差,提高接枝率测定的准确度及精度,研究人员采用红外分光度法,通过定量分析得到PP-g-MAH 接枝率的精确值。首先制备确定MAH含量的基准物质,建立标准工作曲线;再通过待测PP-g-MAH 的红外光谱数据得到接枝率。但MAH熔点较低、易升华,难以与PP混合制备基准物[17,23],因此通常用含酸酐的十二烯基琥珀酸酐、十八烷基琥珀酸酐与PP 或聚马来酸酐均匀混合以建立标准工作曲线[25-26]。与MAH 类似,这2 种物质的熔点与PP 相差较大,混合过程及试样制备过程复杂,酸酐含量准确性难以确定。由上所述,先降低测定接枝率的随机误差提高精度,再减小系统误差提高准确度,是一种可行的方法。
误差传递公式用于分析各参数对测定结果的影响,可优化测试方法,提高测定精度[27-28],本文对酸碱反滴定法测定接枝率的随机误差进行分析。
设式(2)中c1、V1、V0、m等的随机误差相互独立,且均服从正态分布,应用随机误差传递公式[29],接枝率G的标准偏差平方如式(3)所示:
根据式(2)计算G对c1、V0、V1和m的偏微分,并代入式(3)可得式(4):
式中sG、sc1、sV0、sV1、sm分别为G、c1、V0、V1、m的标 准偏差。
由式(4)可看出,影响接枝率测定误差的因素有:HCl-异丙醇的浓度c1、空白体积V0、滴定体积V1及接枝物取样量m及上述4 个因素的标准偏差sc1、sV0、sV1、sm。由于式(1)中含c2、V2的项已抵消,因此KOH-乙醇溶液的浓度c2、加入的过量KOH-乙醇溶液体积V2对接枝率测定误差的影响可不考虑。马来酸酐的摩尔质量M0视为常数,不考虑其影响。
除式(4)中各因素外,还要考虑本文接枝率测定的特点为聚合物在非水溶剂中的滴定。PP 长链分子在溶液中呈现不同构象,其沉析对小分子物质,如KOH、HCl 的包裹效应会影响滴定结果。自由基引发的接枝反应易发生PP 大分子自由基的β-断裂,使PP 分子量降低、分子量分布变化;MAH 自由基发生接枝、歧化终止,因此接枝反应有反应历程随机、产物接枝率低的特点;PP-g-MAH 结构随PP、引发剂、接枝助剂及制备工艺的不同而呈现多种变化[30]。在分析测定误差产生的机制中,应考虑PP 长链分子在溶液中的沉析及PP-g-MAH接枝率低的影响。
2.1 样品取样量对接枝率测定误差的影响
由于(V0-V1)与样品中接枝MAH 含量G是单值函数关系。在确定工艺条件下,所制备接枝物中MAH的含量G为定值,因此将式(2)代入式(4),两边除以G,得接枝率测定相对标准偏差模型(以下简称误差模型)如式(5)所示,式中(sr)G为接枝率相对标准偏差。
取c1为0.1 mol/L、PP-g-MAH 接枝率G为1.0 %(质量分数,下同)时,设sc1、sm为2×10-4,sV0、sV1为2×10-2,代入式(5),可得取样量与接枝率测定误差的关系曲线,如图1所示。可以看出,随取样量增加,接枝率测定误差呈非线性减小,图1曲线显示当样品质量大于0.5 g 时,误差在曲线水平渐近线区间,测定误差趋于稳定。由于PP 的长链结构,取样量过大会导致滴定溶液体系黏度增加,沉析的PP 对KOH 的包裹效应增强,对测定误差影响增大,因此在测定接枝率时,取样量通常的范围为0.2~1.0 g[14-16,21-23,31,32],从图1 局部放大图可以看出,在不考虑PP-g-MAH 包裹效应的影响下,其接枝率测定误差<10 %。
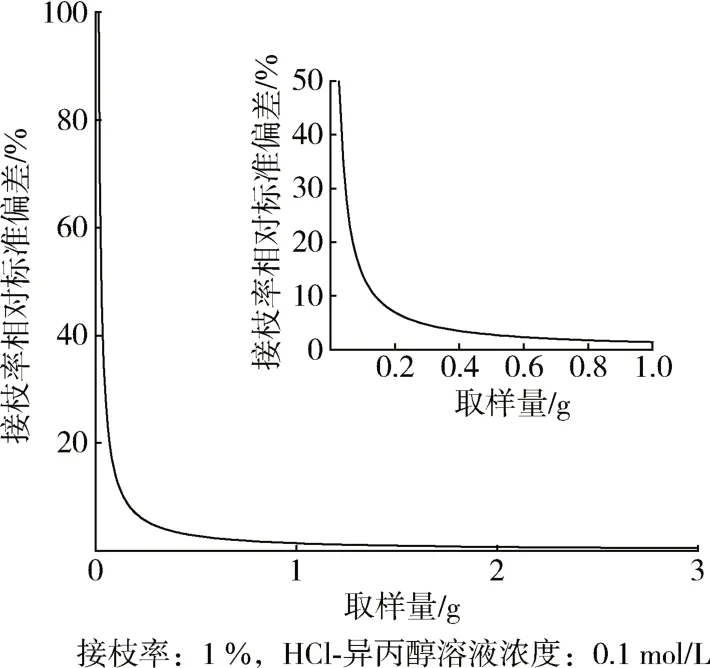
图1 取样量与接枝率相对标准偏差的关系曲线Fig.1 Relationship between sampling amount and relative standard deviation of grafting ratio
2.2 HCl-异丙醇溶液浓度对接枝率测定误差的影响
取PP-g-MAH接枝率G为1.0 %,sc1、sm为2×10-4,sV0、sV1为2×10-2,代入式(5)可得HCl-异丙醇溶液浓度与接枝率测定误差的关系曲线,如图2 所示。随HCl-异丙醇溶液浓度增加,测定误差先减小后增加,总体变化趋势与实验值相符合[23]。图2 局部放大图显示在浓度0.01~0.04 mol/L 区间,测定误差随取样量的增加而减小的幅度较小,误差在最低值范围。当取样量m不变,HCl-异丙醇溶液浓度c1增大,中和过量碱消耗HCl-异丙醇溶液的体积V1量减小,测定误差随之增大。当溶液浓度小于0.01 mol/L 时,因浓度过小产生的误差使得整体测定误差急剧增大。综合实验仪器精度及操作因素,为减小接枝率测定误差,HCl-异丙醇溶液浓度范围取0.01~0.05 mol/L[23,26,33]。
2.3 PP-g-MAH马来酸酐含量对接枝率测定误差的影响
由于原料、制备工艺不同,所制得PP-g-MAH 接枝率的范围在0.8 %~2.9 %[9,12,14,34],因此在分析中G分别取1.0 %、1.5 %、2.0 %、2.5 %,HCl-异丙醇及相应的KOH-乙醇溶液浓度为0.01 mol/L,代入式(5),得到马来酸酐含量对接枝率测定误差影响的曲线,如图3所示,在相同测试条件下,高接枝马来酸酐含量PP-g-MAH 测定误差小于低含量PP-g-MAH 的测定误差。当取样量大于0.2 g 时,不同含量接枝物的测定误差接近并趋于最小值2 %;当取样量小于0.2 g 时,接枝马来酸酐含量对测定误差影响增大。
3 结果与讨论
3.1 接枝物的FTIR分析
纯PP 与PP-g-MAH 的FTIR 曲线如图4 所示,与纯PP 的FTIR 图相比,接枝物在1771 cm-1有弱的C=O 非对称振动吸收峰,在1 717 cm-1有强的C=O对称振动吸收峰,为五元环酸酐分子C=O 的2 个特征振动吸收峰[16],表明PP 分子链上已接枝MAH。由于自由基反应历程不同,MAH 主要在PP 分子链末端、叔碳或仲碳上接枝[图5(a)、(c)、(d)],特征吸收峰为1 792、1 715 cm-1;或MAH以聚合物形式接枝[图5(b)],特征吸收峰为1 784、1 715 cm-1[16,30]。本实验制备的PP-g-MAH 的特征吸收峰分别比纯MAH 的1 850、1 790 cm-1低约76 cm-1,推测是由于接枝MAH分子中2 个羰基C=O 受PP 分子链上甲基诱导效应的影响,使得其特征吸收峰波数降低,已接枝MAH 的结构变为丁二酸酐[32,35],其在PP分子接枝的结构如图5(d)所示。

图4 纯PP与PP-g-MAH的FTIR谱图Fig.4 FTIR of pure PP and PP-g-MAH

图5 自由基反应接枝制备PP-g-MAH可能的结构Fig.5 Possible structure of PP-g-MAH by free radical grafting reaction
3.2 取样量对接枝率测定误差的影响
同批制备的PP-g-MAH 样品进行3 个平行样测定,不同取样量接枝物的接枝率测定结果如图6 所示,随着取样量增加,接枝率测定误差减小并趋于稳定,其变化趋势与误差模型符合。接枝物实验测定误差的范围在30 %附近,较文献中的5 %~20 %[23]高,由误差模型可知,这是由于取样量(0.2~0.65 g)及PP-g-MAH接枝率(~1 %)都较文献值低,因而测定误差高。图6 显示误差的实验测定值较模型值高,这主要是PPg-MAH 对的包裹效应对测定误差产生较大的影响[31]。酸碱反滴定过程中,过量KOH 与PP-g-MAH 在加热回流(~145°C)状态下为均匀溶液,当有机溶液体系逐渐降温至乙醇沸点以下,以进行后续的HCl-异丙醇溶液滴定时,PP-g-MAH 溶解性降低而在二甲苯中析出沉析,如图7所示,PP-g-MAH长分子链的热运动减弱,以缠绕线团状将KOH包裹,滴定过程中不能被HCl-异丙醇中和,因而使测定值偏高[21]。虽然聚合物对小分子物质包裹的影响未在误差模型中考虑,但取样量对接枝率测定误差影响的分析仍不失一般性。
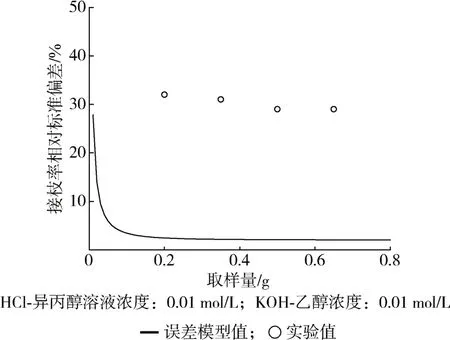
图6 不同取样量下接枝率的相对标准偏差Fig.6 Relative standard deviation of grafting ratio under different sampling amounts

图7 PP-g-MAH在二甲苯中的溶解与析出及对KOH包裹示意图Fig.7 Dissolution and precipitation of PP-g-MAH in xylene and schematic diagram of encapsulation for KOH by PP-g-MAH
3.3 HCl-异丙醇溶液浓度对测定误差的影响
0.2 g 接枝物分别溶于不同浓度KOH-乙醇溶液,反应后再用与碱溶液相应浓度的HCl-异丙醇溶液进行反滴定分析,测定结果如图8 所示。可以看出,测定误差随HCl-异丙醇溶液浓度增加而增加,实验测定误差的范围在32 %~60 %之间,最低值小于40 %[20]。测定误差的实验值较模型值高,主要与PP-g-MAH 在二甲苯溶液中沉析后对KOH 的包裹效应有关。在取样量、温度一定时,滴定测试过程中,有机溶液体系中PPg-MAH 由高温溶解状态转为低温絮状团聚状态,接枝物沉析的体积一定,其所包裹的KOH 体积一定,当KOH-乙醇标准溶液浓度增大,沉降物中被包裹而不能扩散到溶液中的KOH越多,如图9所示。反滴定时,由于被包裹的KOH不能与HCl发生中和反应,滴定HCl-异丙醇溶液的体积小,因HCl-异丙醇溶液滴定体积小造成误差使接枝率测定误差增大[29]。
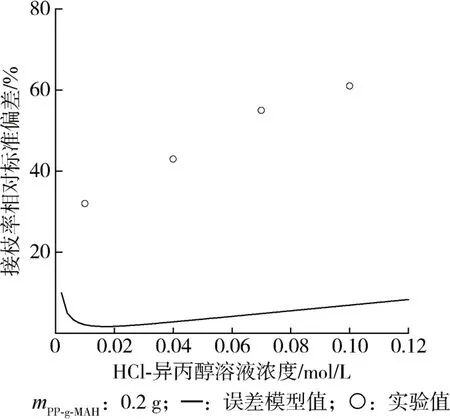
图8 不同HCl-异丙醇溶液浓度下接枝率相对标准偏差Fig.8 Relative standard deviation of grafting ratio under different concentrations of HCl-isopropanol solution
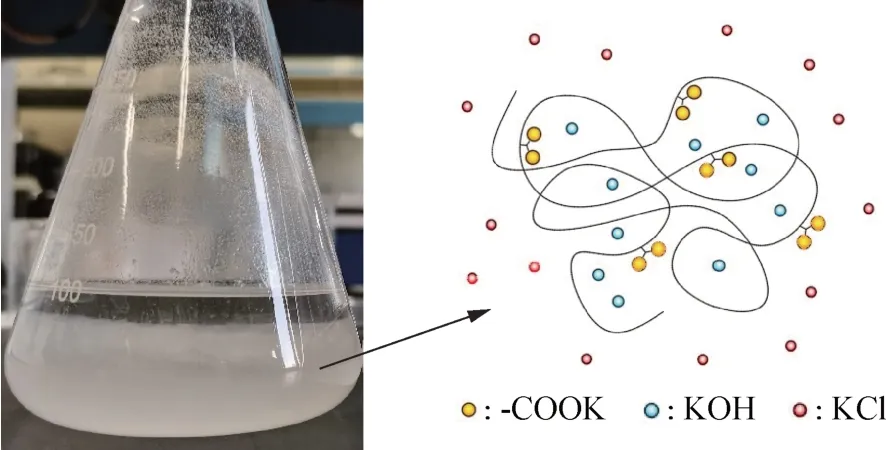
图9 滴定后PP-g-MAH在二甲苯溶液沉降及对KOH包裹示意图Fig.9 Schematic diagram of entrapment of KOH by PP-g-MAH precipitation after titration
3.4 接枝马来酸酐含量对接枝率测定误差的影响
以2个不同比例分别制备PP-g-MAH,在取样量为0.2 g,HCl-异丙醇和KOH-乙醇溶液浓度为0.01 mol/L条件下,测定接枝率平均值分别为0.6 %、1.1 %,以PP-g-MAH低和PP-g-MAH高表示,计算标准偏差,结果如图10所示。由于酸碱滴定测得的是马来酸酐含量的绝对值,因此接枝率平均值可看作PP-g-MAH 接枝马来酸酐的含量。图10 显示2 个测定结果的标准偏差接近,但PP-g-MAH高的相对标准偏差远低于PP-g-MAH低的相对标准偏差。从误差模型计算比较,如图3(b)所示,在相同测定参数条件下,当接枝物的接枝率从1.0 %增加到2.5 %时,其测定接枝率相对标准偏差降低了4.7 %。实验结果及误差模型表明接枝物中马来酸酐含量低也是接枝率测定误差大、再现性差的原因。

图10 不同马来酸酐含量PP-g-MAH接枝率测定结果Fig.10 Determination results of PP-g-MAH grafting ratio with different maleic anhydride content
从以上误差模型及实验结果的分析可知,酸碱反滴定测定中接枝物对KOH 的包裹效应是产生误差的主要原因。为减小包裹效应的影响,接枝物的取样量应尽可能减小,并且当接枝物结构稳定、酸碱反滴定测定参数及测定操作条件稳定并为最优时,接枝率的误差可减小至最低值。在现有制备工艺条件下,由于自由基熔融接枝反应的特点,PP-g-MAH 接枝率通常在1 %左右,通过提高接枝率以减小测定误差较难实现,因此,优化接枝制备工艺,使接枝产物的结构组成稳定,对减小测定误差也能起到辅助作用。
4 结论
(1)PP-g-MAH 在有机溶液中的沉析及对KOH 的包裹效应,是接枝率测定误差大、再现性差的主要原因,接枝物马来酸酐含量低是产生测定误差原因之一;
(2)在现有PP-g-MAH 制备工艺条件下,接枝率通常在1 %~2 %,为减小包裹效应的影响,取样量为0.2 g、HCl-异丙醇及KOH-乙醇标准溶液浓度为0.01~0.05 mol/L是最优实验测试条件;
(3)实验测定误差随测试条件变化的趋势与误差模型预测相符,所建误差模型可用于减小接枝率测定误差。

