邻苯二甲酸氢钾低电导率标准溶液均匀性和稳定性
王金珍 陈青华 林粦芳 / 莆田市计量所
0 引言
电导率是评价和监控水体质量的一个重要物理量。化工、食品、医药和电子等行业对水质都有较高的要求。例如,在发电厂,需要将锅炉水和给水的电导率严格控制在低水平范围内,避免因高温高压产生的蒸汽引起设备腐蚀和结垢[1];在分析实验室,高效液相色谱、气相色谱和电感耦合等多种离子质谱分析测试手段均要求使用一级水质,即水质的电导率不超过0.1 μS/cm,电阻率大于18.0 MΩ·cm。由此可见,电导率的高低直接影响企业产品质量,准确测量溶液电导率值就显得尤为重要[2]。
电导率仪是测量水溶液或非水溶液电导率的测量仪器,广泛应用于锅炉水、环境监测、地表水盐度等测量。为准确测量溶液电导率值,需要选择合适的电导率标准物质校准电导率仪。目前,我国常用的电导率标准物质主要有111.31 mS/cm、12.85 mS/cm、1408 μS/cm、146.5 μS/cm 和84 μS/cm 5 种[3],中国计量科学研究院生产的50 μS/cm(GBW13122,U=0.5%,k=2)和19 μS/cm(GBW13122,U=1.2%,k=2),两者不确定度均超过JJG 376—2007《电导率仪》检定规程的要求,即检定中使用的标准溶液参考值的相对不确定度应小于或等于0.25%(k=2)[4]。该标准溶液仅能够满足电导率仪常用量程20 ~20 000 μS/cm 的校准,对于量程段在0.1 ~10 μS/cm的低电导率标准溶液尚处于空缺状态,无法校验电导率仪的低量程段,导致各行业用水质量得不到保证[5]。因此,为满足我国对低量程电导率仪的日常校准和核验需求,开展低电导率标准物质的研究具有重要意义。
低电导率标准溶液是不稳定的,一旦暴露于空气中便会吸收空气中的二氧化碳并电离产生氢离子、碳酸根离子和碳酸氢根离子,使溶液电导率增大,量值和稳定性均发生改变[6]。酸性溶液可以有效抑制碳酸的电离,从而降低二氧化碳的溶解[7-9]。在前期的研究中选择硫酸氢钠、磷酸二氢钠、邻苯二甲酸氢钾三种常见的酸式盐为研究对象,通过监测三种低电导率酸式盐溶液电导率值的变化,发现邻苯二甲酸氢钾低电导率标准溶液暴露于空气1 h,电导率值变化小于0.1 μS/cm,表现出良好的稳定性[10]。本文按照JJF 1343—2022《标准物质的定值及均匀性、稳定性评估》的相关要求,对候选的邻苯二甲酸低电导率标准溶液样品进行了均匀性检验和稳定性考察,通过方差分析法(F检验法)检验样品瓶间均匀性,t检验法检验样品瓶内均匀性,并对邻苯二甲酸氢钾低电导率标准溶液跟踪监测6 个月,电导率值无显著性变化,稳定性良好,样品的均匀性和稳定性满足标准物质研制的要求。低电导率标准溶液的研制,有助于电导率仪低量程段的校准与核验,同时也为我国行业用水质量提供计量保障。
1 实验部分
1.1 主要仪器与试剂
S230 型精密电导率仪(0.5 级)、inlab® 741 电导电极(0. 105 cm-1,Mettler Toledo 公司);AL204 型电子天平(最大秤量210 g,特种准确度级,MettlerToledo 公司);精密恒温水浴槽(均匀性不超过±0.10 ℃,波动度不大于0.10 ℃),玻璃汞温度计(0 ~50 ℃,分度值0.1 ℃)。
邻苯二甲酸氢钾标准物质(GBW06106,99.994%±0.008%,中国计量科学研究院),Mili-Q 超纯水(18 MΩ·cm),电解质电导率水溶液标准物质(GBW13121,19.90 μS/cm,中国计量科学研究院)。
1.2 环境条件
恒温恒湿间,温度:20 ℃,湿度60%RH。
1.3 标准溶液的配制
1.3.1 试剂预处理
在配制溶液之前,应将试剂放在称量瓶中,在110 ℃下干燥2 h,取出放在有硅胶干燥剂的保干器中,冷却至室温,再用精密电子天平进行称量。
1.3.2 邻苯二甲酸氢钾低电导率溶液的配制
称取0.041 0 g 干燥后的邻苯二甲酸氢钾粉末,用超纯水溶解,移入2 000 mL 的容量瓶中并定容,得到0.001 mol/L 的邻苯二甲酸氢钾溶液,测得电导率约为16 μS/cm(20 ℃),继续将溶液稀释4 倍,得到邻苯二甲酸氢钾低电导率溶液。
1.4 测量装置
实验采用的电导率测量装置如图1 所示。
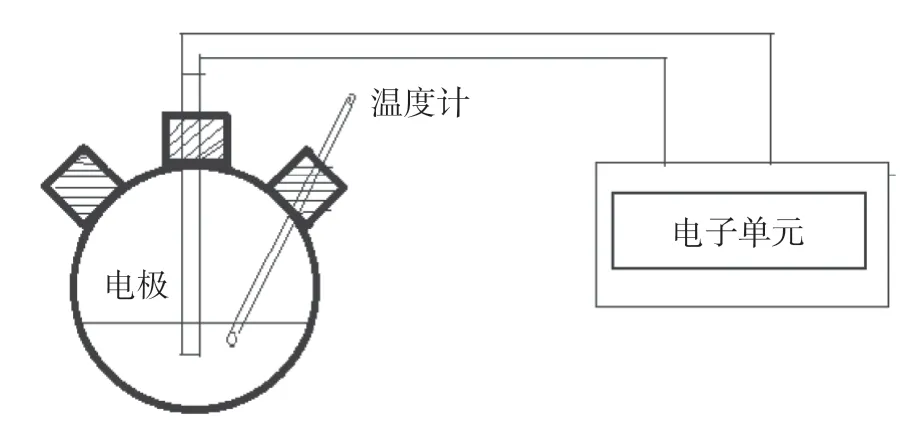
图1 电导率测量装置
在测量过程中应做好该测量装置的密封处理,可以在防止溶液挥发的同时,降低空气中二氧化碳的渗入,有助于提高溶液测量的稳定性。
1.4.1 电导电极常数的标定
将电解质电导率水溶液标准物质(GBW13121,19.90 μS/cm)恒温至25 ℃,将电导率仪电极常数Kcell·R调节为0.105 cm-1,温度系数设定为不补偿。测量标准物质的电导率κM,并按照式(1)计算电极常数Kcell。
式中:Kcell—— 电导电极常数,cm-1;
κs—— 标准溶液在25 ℃下的电导率值,μS/cm;
κM—— 电导率仪测量标准溶液的示值,μS/cm
在25 ℃,对电极常数进行3 次重复标定,按式(1)计算得到电极常数Kcell,分别为0.103 852 cm-1、0.104 059 cm-1、0.103 749 cm-1,取平均值,得到电极常数为0.103 887 cm-1。
1.4.2 低电导率标准溶液的测量
用邻苯二甲酸氢钾低电导率溶液冲洗电导池、温度计和测量杯2 ~3 次,往测量装置中加入电导率标准溶液并密封,放入恒温槽进行恒温,待溶液的温度稳定在水浴温度后,用标定好的电导率仪测量溶液电导率值。
1.5 均匀性检验
将配制好的低电导率溶液分装编号,每瓶约100 mL,共70 瓶,随机选择11 个样本(瓶),进行瓶内及瓶间均匀性检验。首先取出其中1 瓶,在该瓶的上、中、下部分取出3 个子样进行瓶内均匀性检测,每个子样重复测定3 次,并采用t检验法评价瓶内均匀性,按式(2)计算t值。对抽样余下的10 瓶溶液分别测定电导率值,每瓶测定3 次,取平均值,用于瓶内实验的该瓶溶液取瓶中位置的电导率值参与瓶间均匀性计算,11 瓶溶液的测量数据见表2。本文采用方差分析法(F检验法)评价低电导率溶液的瓶间均匀性,组间方差和Q1与组内方差和Q2按式(3)和式(4)计算。
t检验法:
—— 第二组电导率平均值,μS/cm;
S1—— 第一组电导率标准偏差,μS/cm;
S2—— 第二组电导率标准偏差,μS/cm;
n1—— 第一组电导率测量次数;
n2—— 第二组电导率测量次数
自由度v=n1+n2- 2
F检验法:
式(3)(4)中:—— 第i个样品电导率平均值,μS/cm;
—— 样品电导率的总平均值,μS/cm;
xij—— 第i个样品第j次的电导率测量值,μS/cm;
ni—— 第i个样品电导率的测量次数,μS/cm;
m—— 样品个数按式(5)和式(6)计算分布函数的自由度(v1,v2);按式(7)计算统计量F:
1.6 稳定性考察
低电导率标准溶液配制以后,装于聚乙烯容器内低温保存。与均匀性检验方法相同,随机选取12瓶样品,每隔1 周测量溶液电导率值,共测量23 周,记录溶液电导率随时间的变化。根据统计学理论,若溶液稳定性良好,测量结果应满足式(8)。
式中:xi—— 第i次测定值,μS/cm;
——n次测定值的平均值,μS/cm;
S—— 测量方法的标准偏差,μS/cm;
ta(n-1)——显著性水平a,自由度n- 1 的t检验临界值
2 结果与讨论
2.1 低电导率标准溶液的定值
随机取5 瓶制备好的邻苯二甲酸氢钾低电导率溶液,并按照本文1.4.2 介绍的方法进行测量,每瓶溶液重复测量10 次,测量数据见表1。
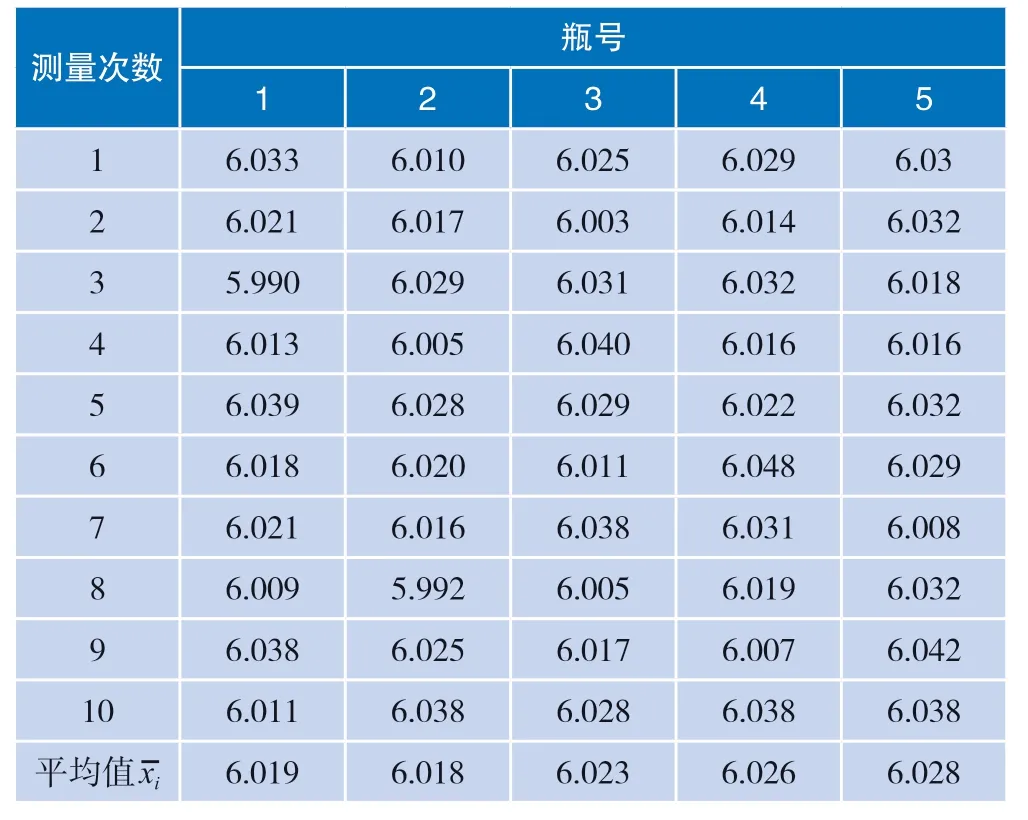
表1 标准溶液在25 ℃时电导率测量数据单位:μS·cm-1
在25 ℃下,邻苯二甲酸氢钾低电导率溶液的标准值为各组平均值的平均值,即:
2.2 均匀性检验结果
瓶内和瓶间均匀性测量结果分别列于表2 和表3,将均匀性检测结果列于表4。由表3 可知,瓶上部和瓶中部,瓶上部和瓶下部的t值小于临界值t0.05(4),说明这三部分电导率平均值之间无显著差异,可认为该样品瓶上部、瓶中部和瓶下部三部分溶液是均匀的。同时,通过瓶间均匀性检验统计结果可知F小于F0.05(10,22),说明这11 瓶低电导率溶液瓶间的测量列无显著性差异,即各瓶之间溶液是均匀的。因此,在95%的置信概率下,可以根据以上结果判定该溶液是均匀的。

表2 邻苯二甲酸氢钾低电导率溶液的瓶内均匀性检验测量数据
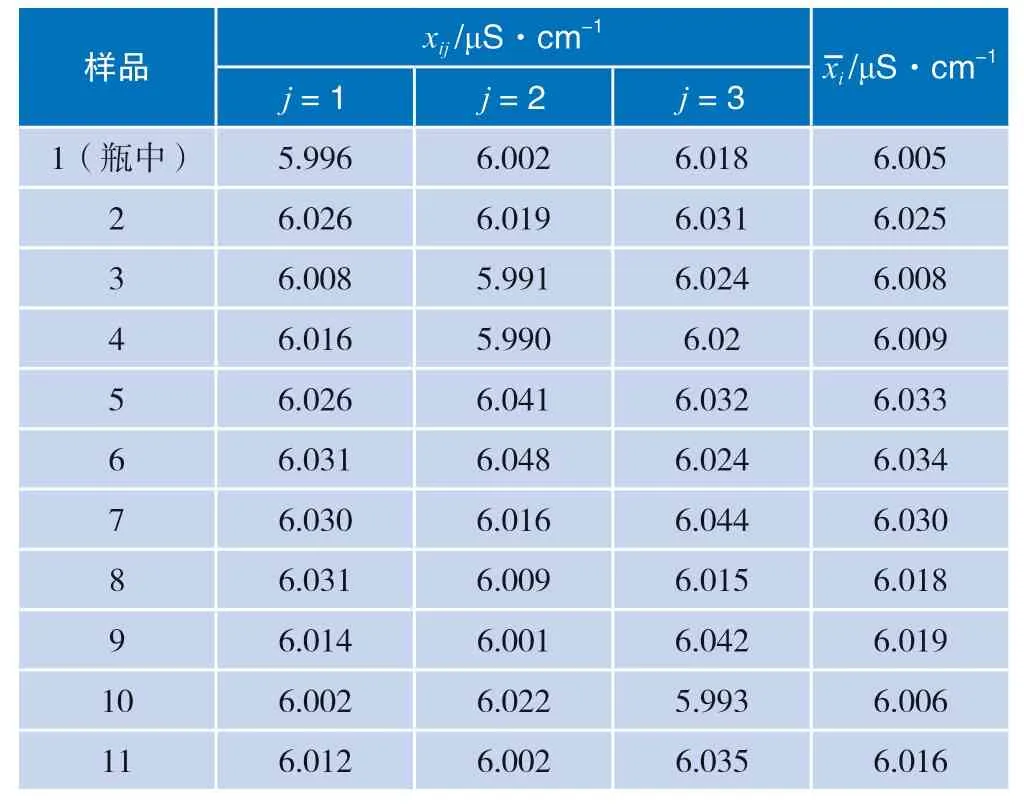
表3 邻苯二甲酸氢钾低电导率溶液瓶间均匀性检验测量数据
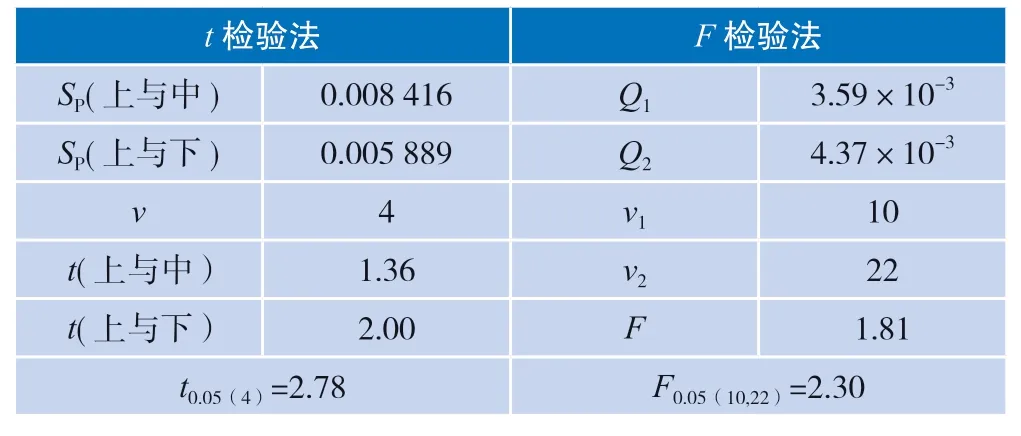
表4 溶液均匀性检验结果
2.3 稳定性考察结果
本文跟踪检测23 周的邻苯二甲酸氢钾低电导率溶液稳定性试验数据,约6 个月。由表5 的测量数据计算可得平均值= 6.022 μS/cm,标准偏差S=0.023 μS/cm,由a= 0.05,样品容量n= 12,查t检验临界值分布表得t0.05(11)= 2.201,则t0.05(11)·S= 0.051。监测期内测定值与平均值的差符合式(8), 可以认为在监测周期内溶液电导率值无显著性变化,稳定性良好。同时,由图2 稳定性曲线看出, 稳定性曲线无明显上升或下降趋势,因此,可以判定邻苯二甲酸氢钾低电导率的稳定贮存期应在23 周以上。

表5 邻苯二甲酸氢钾低电导率溶液的稳定性试验数据

图2 低电导率标准溶液稳定性曲线
3 结语
研制邻苯二甲酸氢钾低电导率标准物质,电导率平均值为6.02 μS/cm,本文采用方差分析法进行瓶间均匀性检验,t检验法进行瓶内均匀性检验,结果表明该标准溶液是均匀的;同时,经稳定性考察试验,在监测周期内溶液电导率值无显著性变化,稳定性曲线无明显上升或下降趋势,稳定性良好,贮存期在23 周以上。

